Аммиак
(нитрид водорода) — химическое соединение азота и водорода с формулой NH3, при нормальных условиях — бесцветный газ с резким характерным запахом.
Плотность аммиака почти вдвое меньше, чем у воздуха, ПДКр.з. 20 мг/м3 — IV класс опасности (малоопасные вещества) по ГОСТ 12.1.007. Растворимость NH3 в воде чрезвычайно велика — около 1200 объёмов (при 0 °C) или 700 объёмов (при 20 °C) в объёме воды. В холодильной технике носит название R717, где R — Refrigerant (хладагент), 7 — тип хладагента (неорганическое соединение), 17 — молекулярная масса.
Аммиак относится к числу важнейших продуктов химической промышленности, ежегодное его мировое производство превышает 180 млн тонн.
Молекула аммиака имеет форму треугольной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота участвуют в образовании полярных ковалентных связей с 1s-электронами трёх атомов водорода (связи N − H), четвёртая пара внешних электронов является неподелённой, она может образовать ковалентную связь по донорно-акцепторному механизму с ионом водорода, образуя ион аммония NH4+. Несвязывающее двухэлектронное облако строго ориентировано в пространстве, поэтому молекула аммиака обладает высокой полярностью, что приводит к его хорошей растворимости в воде.
В жидком аммиаке молекулы связаны между собой водородными связями. Сравнение физических свойств жидкого аммиака с водой показывает, что аммиак имеет более низкие температуры кипения (tкип −33,35 °C) и плавления (tпл −77,70 °C), а также меньшие плотность, вязкость (в 7 раз меньше вязкости воды), проводимость (почти не проводит электрический ток) и диэлектрическую проницаемость. Это в некоторой степени объясняется тем, что прочность водородных связей в жидком аммиаке существенно ниже, чем у воды; а также тем, что в молекуле аммиака имеется лишь одна пара неподелённых электронов, в отличие от двух пар в молекуле воды, что не даёт возможность образовывать разветвлённую сеть водородных связей между несколькими молекулами. Аммиак легко переходит в бесцветную жидкость с плотностью 681,4 кг/м³, сильно преломляющую свет. Подобно воде, жидкий аммиак сильно ассоциирован, главным образом за счёт образования водородных связей. Жидкий аммиак — хороший растворитель для очень большого числа органических, а также для многих неорганических соединений. Твёрдый аммиак — кубические кристаллы.
Содержание
- 1 Химические свойства
- 2 История
- 3 Происхождение названия
- 4 Жидкий аммиак
- 5 Комплексообразование
- 6 Биологическая роль
- 7 Физиологическое действие
- 8 Применение
- 9 Получение 9.1 Расходные нормы на тонну аммиака
Химические свойства
- Благодаря наличию неподелённой электронной пары во многих реакциях аммиак выступает как основание Бренстеда или комплексообразователь (не следует путать понятия «нуклеофил» и «основание Бренстеда». Нуклеофильность определяется сродством к положительно заряженной частице. Основание имеет сродство к протону. Понятие «основание» является частным случаем понятия «нуклеофил»). Так, он присоединяет протон, образуя ион аммония:
NH3 + H+ ⟶ NH4+.
- Водный раствор аммиака («нашатырный спирт») имеет слабощелочную реакцию из-за протекания процесса:
NH3 + H2O ⟶ NH4+ + OH− , Ko=1,8⋅10−5.
- Взаимодействуя с кислотами, даёт соответствующие соли аммония:
NH3 + HNO3 ⟶ NH4NO3.
- Аммиак также является очень слабой кислотой (в 10 000 000 000 раз более слабой, чем вода), способен образовывать с металлами соли — амиды, имиды и нитриды. Соединения, содержащие ионы NH2−, называются амидами, NH2− — имидами, а N3− — нитридами. Амиды щелочных металлов получают, действуя на них аммиаком:
2NH3 + 2K ⟶ 2KNH2 + H2.
Амиды, имиды и нитриды ряда металлов образуются в результате некоторых реакций в среде жидкого аммиака. Нитриды можно получить нагреванием металлов в атмосфере азота.
Амиды металлов являются аналогами гидроксидов. Эта аналогия усиливается тем, что ионы OH− и NH2−, а также молекулы H2O и NH3 изоэлектронны. Амиды являются более сильными основаниями, чем гидроксиды, а следовательно, подвергаются в водных растворах необратимому гидролизу:
NaNH2 + H2O ⟶ NaOH + NH3.
и в спиртах:
KNH2 + C2H5OH ⟶ C2H5OK + NH3.
Подобно водным растворам щелочей, аммиачные растворы амидов хорошо проводят электрический ток, что обусловлено диссоциацией:
KNH2 ⇄ K+ + NH2− .
Фенолфталеин в этих растворах окрашивается в малиновый цвет, при добавлении кислот происходит их нейтрализация. Растворимость амидов изменяется в такой же последовательности, что и растворимость гидроксидов: LiNH2 — нерастворим, NaNH2 — малорастворим, KNH2, RbNH2 и CsNH2 — хорошо растворимы.
- При нагревании аммиак разлагается, проявляет восстановительные свойства. Так, он горит в атмосфере кислорода, образуя воду и азот. Окисление аммиака воздухом на платиновом катализаторе даёт оксиды азота, что используется в промышленности для получения азотной кислоты:
2NH3 →1200—1300∘C N2 + 3H2 (реакция обратима), 4NH3 + 3O2 ⟶ 2N2 + 6H2O (без катализатора, при повышенной температуре), 4NH3 + 5O2 ⟶ 4NO + 6H2O (в присутствии катализатора, при повышенной температуре).
На восстановительной способности NH3 основано применение нашатыря NH4Cl для очистки поверхности металла от оксидов при их пайке:
3CuO + 2NH4Cl ⟶ 3Cu + 3H2O + 2HCl + N2.
Окисляя аммиак гипохлоритом натрия в присутствии желатина, получают гидразин:
2NH3 + NaOCl ⟶ N2H4 + NaCl + H2O.
- Галогены (хлор, йод) образуют с аммиаком опасные взрывчатые вещества — галогениды азота (хлористый азот, иодистый азот).
- С галогеноалканами аммиак вступает в реакцию нуклеофильного присоединения, образуя замещённый ион аммония (способ получения аминов):
NH3 + CH3Cl ⟶ [CH3NH3]Cl (гидрохлорид метиламмония).
- С карбоновыми кислотами, их ангидридами, галогенангидридами, эфирами и другими производными даёт амиды. С альдегидами и кетонами — основания Шиффа, которые возможно восстановить до соответствующих аминов (восстановительное аминирование).
- При 1000 °C аммиак реагирует с углём, образуя синильную кислоту HCN и частично разлагаясь на азот и водород. Также он может реагировать с метаном, образуя ту же самую синильную кислоту:
2CH4 + 2NH3 + 3O2 ⟶ 2HCN + 6H2O,
- NH4OH ⟶ NH3 + H2O.
- C солями меди и с серебром образует комплексные соли-аммиакаты
Cu(NO3)2 + 4NH3 ⟶ [Cu(NH3)4](NO3)2, Cu3(PO4)2 + 12NH3 ⟶ [Cu(NH3)4]3(PO4)2, Cu(CH3COO)2 + 4NH3 ⟶ [Cu(NH3)4](CH3COO)2, AgNO3 + 2NH3 ⟶ [Ag(NH3)2]NO3.
Колонна синтеза аммиака, построенная в 1921 году BASF в Оппау, ныне расположена при университете Карлсруэ.
Последствия отравления
После интоксикации аммиаком человека могут ждать очень серьезные необратимые последствия. В первую очередь страдает центральная нервная система, что влечет за собой целый ряд осложнений:
- Мозг перестает полностью выполнять свои функции и начинает давать сбои, из-за этого снижается интеллект, появляются психические заболевания, амнезия, нервные тики.
- Понижается чувствительность некоторых частей тела.
- Нарушается работа вестибулярного аппарата. Из-за этого человек ощущает постоянное головокружение.
- Органы слуха начинают терять свою работоспособность, что приводит к глухоте.
- При поражении глазных покровов снижается зрение и его острота, в худшем случае пострадавшего ждет слепота.
- Наступление летального исхода. Это зависит от того, насколько концентрация газа в воздухе была высокой и сколько паров аммиака попало в организм.
Знать и соблюдать предписанные меры безопасности — значит оградить себя от риска угрозы собственной жизни или худшей участи — инвалидности, потери слуха или зрения.
История
Аммиак был впервые выделен в чистом виде Дж. Пристли в 1774 году, который назвал его «щелочной воздух» (англ. alkaline air). Через одиннадцать лет, в 1785 году К. Бертолле установил точный химический состав аммиака. С того времени в мире начались исследования по получению аммиака из азота и водорода. Аммиак был очень нужен для синтеза соединений азота, поскольку получение их из чилийской селитры ограничивалось постепенным истощением запасов последней. Проблема уменьшения запасов селитры обострилась к концу XIX века. Только в начале XX века удалось изобрести процесс синтеза аммиака, пригодный для промышленности. Это осуществил Ф. Габер, начавший трудиться над этой задачей в 1904 году и к 1909 году создавший небольшой контактный аппарат, в котором использовал повышенное давление (в соответствии с принципом Ле-Шателье) и катализатор из осмия. 2 июля 1909 года Габер устроил испытания аппарата в присутствии К. Боша и А. Митташа, оба — от Баденского анилинового и содового завода (BASF), и получил аммиак. К. Бош к 1911 году создал крупномасштабную версию аппарата для BASF, а затем был построен и 9 сентября 1913 года вступил в строй первый в мире завод по синтезу аммиака, который был расположен в Оппау (ныне район в черте города Людвигсхафен-на-Рейне) и принадлежал BASF. В 1918 году Ф. Габер стал лауреатом Нобелевской премии по химии «за синтез аммиака из составляющих его элементов». В России и СССР первая партия синтетического аммиака была получена в 1928 году на Чернореченском химическом комбинате.
Способы получения
Аммиак производят при водородном и азотном взаимодействии молекул в промышленности. Техника производства называется процессом Габера. Вся реакция протекает с выбросом тепла и уменьшением объема. Таким образом, реакция проводится при пониженной температуре окружающей среды и повышенном давлении. Равновесие смещается вправо. В этих условиях скорость прохождения реакции маленькая, а при повышении показаний температуры скорость начинает увеличиваться. Для безопасного проведения реакции требуется специальное оборудование, поддерживающее повышенное давление.
Для ускорения получения состояния равновесия используют катализаторные материалы — железо с пористым составом и некоторым процентом добавок.
По всем свойствам процесс получения аммиака происходит при температуре в 500 градусов по Цельсию и при наличии высокого давления, достигающего 350 атмосфер. Процент добычи при соблюдении этих факторов составит 30 процентов. В промышленности процесс зациклен. Происходит охлаждение состава и удаление аммиака, а непрореагировавший азот и водород возвращают для повторного синтеза обратно. Этот способ добычи аммиака в промышленности считается самым экономичным.
В условиях лаборатории аммиак добывают за счет действия щелочей. Химический элемент получают путем нагревания аммония с известью. Для сушки аммиака используют известь с натром.
Благодаря физическим и химическим свойствам аммиака его успешно используют в промышленности, производстве, медицине, химии и многих других областях человеческой деятельности.
Происхождение названия
Аммиак (в европейских языках его название звучит как «аммониак») своим названием обязан оазису Аммона в Северной Африке, расположенному на перекрёстке караванных путей. В жарком климате мочевина (NH2)2CO, содержащаяся в продуктах жизнедеятельности животных, разлагается особенно быстро. Одним из продуктов разложения и является аммиак. По другим сведениям, аммиак получил своё название от древнеегипетского слова амониан
. Так называли людей, поклоняющихся богу Амону. Они во время своих ритуальных обрядов нюхали минерал нашатырь (NH4Cl), который при нагревании испаряет аммиак.
Описание элемента
В жидкой форме аммиака молекулы соединены водородной связью. Температура, вязкость и плотность аммиака по сравнению с водой значительно ниже. Процесс кипения начинается от 33 градусов, а процесс горения или плавления — от 77 градусов по Цельсию. Показатели проводимости и диэлектрической проницаемости аммиака низкие. Следовательно, прочность связей в состоянии жидкости низкая.
Аналогично воде, аммиак в жидком состоянии ассоциирован из-за наличия водородной связи. Переход химического состава в состояние жидкости, не имеющей цвета, с плотностью 681 килограмм на метр кубический, быстрый. Проводимость тока в этом состояние практически отсутствует.
Жидкий аммиак
Жидкий аммиак, хотя и в незначительной степени, диссоциирует на ионы (автопротолиз), в чём проявляется его сходство с водой:
2NH3 ⟶ NH4+ + NH2−.
Константа самоионизации жидкого аммиака при −50 °C составляет примерно 10−33 (моль/л)².
Жидкий аммиак, как и вода, является сильным ионизирующим растворителем, в котором растворяется ряд активных металлов: щелочные, щёлочноземельные, Mg, Al, а также Eu и Yb. В отличие от воды с жидким аммиаком данные металлы не реагируют, а именно растворяются и могут быть выделены в исходном виде при испарении растворителя. Растворимость щелочных металлов в жидком NH3 составляет несколько десятков процентов. В жидком аммиаке NH3 также растворяются некоторые интерметаллиды, содержащие щелочные металлы, например, Na4Pb9.
Разбавленные растворы металлов в жидком аммиаке окрашены в синий цвет, концентрированные растворы имеют металлический блеск и похожи на бронзу. При испарении аммиака щелочные металлы выделяются в чистом виде, а щелочноземельные — в виде комплексов с аммиаком [Э(NH3)6], обладающих металлической проводимостью. При слабом нагревании эти комплексы разлагаются на металл и NH3.
Растворённый в NH3 металл постепенно реагирует с образованием амида:
2Na + 2NH3 ⟶ 2NaNH2 + H2 .
Получающиеся в результате реакции с аммиаком амиды металлов содержат отрицательный ион NH2−, который также образуется при самоионизации аммиака. Таким образом, амиды металлов являются аналогами гидроксидов. Скорость реакции возрастает при переходе от Li к Cs. Реакция значительно ускоряется в присутствии даже небольших примесей H2O.
Металлоаммиачные растворы обладают металлической проводимостью, в них происходит распад атомов металла на положительные ионы и сольватированные электроны, окружённые молекулами NH3. Металлоаммиачные растворы, в которых содержатся свободные электроны, являются сильнейшими восстановителями.
Агрегатные состояния
Аммиак может находиться в разных агрегатных состояниях:
- Он присутствует в виде бесцветного газа с неприятным резким запахом в нормальных условиях.
- Также он очень хорошо может растворяться в воде, поэтому его можно хранить в виде водного раствора с определенной концентрацией. Он сжижается и становится жидкостью в результате давления и сильного охлаждения.
- Аммиак имеет твердое состояние, в котором он предстает бесцветными кубическими кристаллами.
Комплексообразование
Благодаря своим электронодонорным свойствам молекулы NH3 могут входить в качестве лиганда в комплексные соединения. Так, введение избытка аммиака в растворы солей d-металлов приводит к образованию их аминокомплексов:
CuSO4 + 4NH3 ⟶ [Cu(NH3)4]SO4. Ni(NO3)2 + 6NH3 ⟶ [Ni(NH3)6](NO3)2.
Комплексообразование обычно сопровождается изменением окраски раствора. Так, в первой реакции голубой цвет (CuSO4) переходит в тёмно-синий (окраска комплекса), а во второй реакции окраска изменяется из зелёной ( Ni(NO3)2 ) в сине-фиолетовую. Наиболее прочные комплексы с NH3 образуют хром и кобальт в степени окисления +3.
Профилактика при отравлении
Первая помощь в данном случае состоит из нескольких простых действий. Сначала необходимо вынести пострадавшего на свежий воздух, промыть ему лицо и глаза проточной водой. Даже те, кто был не очень хорош в химии, со школы знают: щелочь нейтрализуется кислотой, поэтому ротовую полость и нос нужно обязательно промыть водой с добавлением лимонного сока или уксуса.
Если отравившийся потерял сознание, следует уложить его на бок на случай рвоты, а при остановке пульса и дыхания сделать массаж сердца и искусственное дыхание.
Биологическая роль
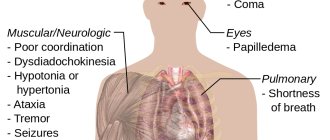
Основные симптомы гипераммониемии (повышения уровня эндогенного аммиака до токсических концентраций).
Аммиак является важным источником азота для живых организмов. Несмотря на высокое содержание свободного азота в атмосфере (более 75 %), очень мало живых существ способны использовать свободный, нейтральный двухатомный азот атмосферы, газ N2. Поэтому для включения азота атмосферы в биологический оборот, в частности в синтез аминокислот и нуклеотидов, необходим процесс, который называется «азотфиксацией». Некоторые растения зависят от доступности аммиака и других нитрогенных соединений, образующихся в почве в результате разложения органических (растительных и животных) остатков. Другие, такие как бобовые, используют преимущества симбиоза с азотфиксирующими бактериями (ризобиями), которые способны синтезировать аммиак из атмосферного азота с помощью ферментов, называемых нитрогеназами. И хотя маловероятно, что когда-либо будут изобретены биомиметические методы, способные конкурировать по производительности с химическими методами производства аммиака из азота, тем не менее, учёные прилагают большие усилия к тому, чтобы как можно лучше понять механизмы биологической фиксации азота. Научный интерес к этой проблеме отчасти мотивируется необычной структурой активного каталитического центра азотфиксирующего фермента (нитрогеназы), которая содержит необычный биметаллический молекулярный ансамбль Fe7MoS9.
Аммиак является также конечным побочным продуктом метаболизма аминокислот, а именно продуктом их дезаминирования, катализируемого такими ферментами, как глутамат-дегидрогеназа. Экскреция аммиака в неизменённом виде является обычным путём детоксикации аммиака у водных существ (рыбы, водные беспозвоночные, отчасти амфибии). У млекопитающих, включая человека, аммиак обычно быстро превращается в мочевину, которая гораздо менее токсична и, в частности, имеет менее щелочную реакцию и меньшую реакционную способность в качестве восстановителя. Мочевина является основным компонентом сухого остатка мочи. Большинство птиц, пресмыкающихся, насекомых, паукообразных, однако, выделяют в качестве основного нитрогенного остатка не мочевину, а мочевую кислоту.
Аммиак также играет важную роль как в нормальной, так и в патологической физиологии животных. Аммиак производится в процессе нормального метаболизма аминокислот, однако весьма токсичен в высоких концентрациях. Печень животных преобразует аммиак в мочевину с помощью серии последовательных реакций, известных как цикл мочевины. Нарушение функции печени, такое, например, какое наблюдается при циррозе печени, может приводить к нарушению способности печени обезвреживать аммиак и образовывать из него мочевину, и, как следствие, к повышению уровня аммиака в крови, состоянию, называемому гипераммониемия. К аналогичному результату — повышению уровня свободного аммиака в крови и развитию гипераммониемии — приводит наличие врождённых генетических дефектов в ферментах цикла мочевины, таких, например, как орнитин-карбамилтрансфераза. К тому же результату может приводить нарушение выделительной функции почек при тяжёлой почечной недостаточности и уремии: вследствие задержки выделения мочевины её уровень в крови возрастает настолько, что «цикл мочевины» начинает работать «в обратную сторону» — избыток мочевины гидролизуется обратно почками в аммиак и углекислый газ, и, как следствие, уровень аммиака в крови возрастает. Гипераммониемия привносит свой вклад в нарушения сознания и развитие сопорозных и коматозных состояний при печёночной энцефалопатии и уремии, а также в развитие неврологических нарушений, часто наблюдаемых у больных с врождёнными дефектами ферментов цикла мочевины или с органическими ацидуриями.
Менее выраженная, однако клинически существенная, гипераммониемия может наблюдаться при любых процессах, при которых наблюдается повышенный катаболизм белков, например, при обширных ожогах, синдроме сдавления или размозжения тканей, обширных гнойно-некротических процессах, гангрене конечностей, сепсисе и т. д., а также при некоторых эндокринных нарушениях, таких, как сахарный диабет, тяжёлый тиреотоксикоз. Особенно высока вероятность возникновения гипераммониемии при этих патологических состояниях в тех случаях, когда патологическое состояние, помимо повышенного катаболизма белков, вызывает также выраженное нарушение детоксицирующей функции печени или выделительной функции почек.
Аммиак важен для поддержания нормального кислотно-щелочного баланса крови. После образования аммиака из глютамина, альфа-кетоглутарат может быть далее расщеплён с образованием двух молекул гидрокарбоната, которые затем могут использоваться как буфер для нейтрализации кислот, поступающих с пищей. Полученный из глютамина аммиак затем выделяется с мочой (как непосредственно, так и в виде мочевины), что, с учётом образования двух молекул бикарбоната из кетоглутарата, приводит в сумме к потере кислот и сдвигу pH крови в щелочную сторону. Кроме того, аммиак может диффундировать через почечные канальцы, соединяться с ионом водорода и экскретироваться совместно с ним ( NH3 + H+ ⟶ NH4+ ), и тем самым ещё больше способствовать выведению кислот из организма.
Аммиак и ионы аммония являются токсическим побочным продуктом метаболизма у животных. У рыб и водных беспозвоночных аммиак выделяется непосредственно в воду. У млекопитающих (включая водных млекопитающих), земноводных и у акул аммиак в цикле мочевины преобразуется в мочевину, поскольку мочевина гораздо менее токсична, менее химически реакционноспособна и может более эффективно «храниться» в организме до момента возможности её выделения. У птиц и пресмыкающихся (рептилий) аммиак, образовавшийся в процессе метаболизма, преобразуется в мочевую кислоту, которая является твёрдым остатком и может быть выделена с минимальными потерями воды.
Симптомы отравления
Ниже перечислен ряд признаков отравления аммиаком:
- Сильный кашель, затруднение дыхания.
- Жжение в глазах, слезоточивость, болевая реакция на яркий свет.
- Жжение в полости рта и носоглотке.
- Головокружение, головная боль.
- Боли в животе, рвота.
- Снижение слухового порога.
- При более серьезном отравлении возможны: потеря сознания, судороги, остановка дыхания, острая сердечная недостаточность. Совокупность нарушений может привести пострадавшего в коматозное состояние.
Физиологическое действие
Аммиак токсичен. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных при ингаляционном поражении вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Аммиак обладает как местным, так и резорбтивным действием.
Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы. Это человек и воспринимает как резкий запах. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог конъюнктивы и роговицы, потерю зрения, приступы кашля, покраснение и зуд кожи. При соприкосновении сжиженного аммиака и его растворов с кожей возникает жжение, возможен химический ожог с пузырями, изъязвлениями. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени. Запах аммиака ощущается при концентрации 37 мг/м³.
Предельно допустимая концентрация в воздухе рабочей зоны производственного помещения (ПДКр.з.) составляет 20 мг/м³. В атмосферном воздухе населённых пунктов и в жилых помещениях среднесуточная концентрация аммиака (ПДКс.с.) не должна превышать 0,04 мг/м³. Максимальная разовая концентрация в атмосфере — 0,2 мг/м³. Таким образом, ощущение запаха аммиака свидетельствует о превышении допустимых норм.
Раздражение зева проявляется при содержании аммиака в воздухе 280 мг/м³, глаз — 490 мг/м³. При действии в очень высоких концентрациях аммиак вызывает поражение кожи: 7—14 г/м³ — эритематозный, 21 г/м³ и более — буллёзный дерматит. Токсический отёк лёгких развивается при воздействии аммиака в течение часа с концентрацией 1,5 г/м³. Кратковременное воздействие аммиака в концентрации 3,5 г/м³ и более быстро приводит к развитию общетоксических эффектов.
В мире максимальная концентрация аммиака в атмосфере (больше 1 мг/м³) наблюдается на Индо-Гангской равнине, в Центральной долине США и в Туркестанской (ранее — Южно-Казахстанской) области Казахстана.
Области применения
Область применения аммиака и аммиачного спирта широка, он используется практически во всех сферах жизнедеятельности человека, начиная от технологических процессов и заканчивая медициной и бытовыми нуждами.
Применение аммиака
Аммиак широко применяется в качестве хладагента в различном бытовом и промышленном оборудовании.
Он является одним из важнейших продуктов, используемых в химической промышленности. В частности, его используют в производстве:
- нашатырного спирта;
- добавок в строительные материалы для использования в морозных условиях;
- полимеров, соды и азотной кислоты;
- удобрений;
- взрывчатых веществ.
Использование аммиачного спирта
Аммиачный спирт применяется в медицине и в быту.
Применение в медицине показано в следующих случаях:
- для возбуждения дыхания при обморочных состояниях: для этого подносят к носу пострадавшего флакон с нашатырным спиртом; флакон надо держать в 5 см от носа, чтобы избежать ожога;
- для стимуляции рвоты при различных видах отравления: 10 капель на стакан воды и дать выпить;
- наружно для местного охлаждения при болях от невралгии или миозитов;
- наружно при зуде от укусов насекомых: сделать раствор из спирта с водой в пропорции 1 часть спирта на 10 частей воды и протереть зудящее место;
- наружно для обработки рук хирурга в качестве антисептика;
- внутрь при отравлении алкоголем: на 1 стакан воды 5 капель спирта. Это позволяет быстро очнуться, собраться с мыслями и адекватно отвечать на вопросы;
- в качестве антисептика для стерилизации игл при отсутствии автоклава или разовых игл;
- для удаления бородавок: неразбавленным спиртом смочить ватный тампон и прижить к бородавке на 5−6 секунд, не дотрагиваясь до здоровой кожи, чтобы избежать ожога;
- в стоматологии в определенной концентрации при обработке полости рта;
- и в других случаях.