ОРВИ, как известно, составляют большинство случаев обращения к врачам в холодное время года, а пандемия новой коронавирусной инфекции только усугубляет ситуацию. Заражение чаще всего происходит воздушно-капельным путем. Вирусы попадают в организм через носоглотку, поэтому ее часто называют «воротами» инфекции. Патогены, рассеянные в окружающей среде, при вдохе воздуха оседают на слизистой оболочке полости носа, и именно там происходит их внедрение в организм, в результате чего могут развиться респираторные заболевания. Вот почему важно не допустить непосредственного контакта вирусов со слизистой и их последующего проникновения в дыхательные пути. Прибегая к противовирусным средствам, которые наносятся непосредственно на слизистую носовых ходов, мы препятствуем их размножению и дальнейшему распространению вируса.
- Как подобрать мазь ребенку
- Механизм передачи ОРВИ
- Простуды в детском возрасте
- Назальные противовирусные для детей
- Приём взрослыми противовирусных в нос (интраназально)
- Виферон Гель
- Виферон мазь
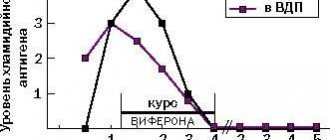
- Схема применения
- Механизм работы иммунитета
Как подобрать противовирусные мази для детей
Многие понимают, что наиболее «выигрышной» тактикой в противостоянии простудным заболеваниям является предотвращение заболевания. Поэтому многие родители задаются вопросом: какая мазь для носа противовирусная для детей будет работать в помощь местному иммунитету? Однако не все средства подходят для Вашего малыша. Дело в том, что большинство препаратов имеют ограничения по возрасту пациента, следует внимательно читать инструкцию и не применять недопустимые лекарства, которые могут нарушить хрупкий баланс иммунной системы малыша или повредить еще не окрепшие органы. В настоящее время количество специфических противовирусных средств, разрешенных к применению в педиатрии, ограничено.
Виферон
Отечественное лекарственное средство виферон представляет собой один из белков иммунной системы человека — рекомбинантный интерферон альфа-2b. Препарат обладает иммуномодулирующим, антипролиферативным (препятствующим клеточному размножению) и противовирусным эффектом. Сфера его применения достаточно обширна: это вирусные и бактериальные инфекции самой разнообразной этиологии и локализации. Инфекционные заболевания чаще других досаждают человеку в течение всего его жизненного пути. Борьба с ними ведется по всем фронтам с использованием самого разнообразного фармакологического «вооружения», самым серьезным из которого справедливо считаются антибиотики и химиопрепараты. Однако зачастую противовирусная и антибактериальная терапия превращается в попытки убить муху отбойным молотком: не секрет, что те же антибиотики, помимо смертоносного воздействия на микроорганизмы, подтачивают защитные силы организма и истощают его иммунные ресурсы. В этой связи в рамках комплексного лечения вирусных и бактериальных инфекций было предложено использовать препараты интерферона. Эти белки из семейства цитокиновых медиаторов являются важным звеном в формировании иммунитета. Видным представителем данной группы лекарственных средств является российский препарат виферон, выпускаемый в трех лекарственных формах: мазь, гель и суппозитории. Комбинация входящих в состав виферона ингредиентов приносит в его копилку ряд дополнительных и отнюдь не лишних фармакологических эффектов. Так, выступающие в роли вспомогательных веществ антиоксиданты — токоферола ацетат и аскорбиновая кислота (последняя присутствует только в суппозиториях) — увеличивают противовирусный потенциал интерферона альфа-2b. При их деятельном участии усиливается иммуномодулирующее действие виферона на T- и B-лимфоциты, возрастает концентрация секреторных иммуноглобулинов (антител) класса А, нормализуется концентрация иммуноглобулина Е, восстанавливается работа внутренней системы интерферона альфа-2b.
Альфа-токоферол и аскорбиновая кислота сами по себе способны подавлять воспаление, стабилизировать клеточные мембраны и восстанавливать поврежденные ткани. Таким образом, виферон позволяет обойтись меньшими дозами антибактериальных и гормональных лекарственных средств, а значит — уменьшить вероятность развития побочных реакций в рамках противовирусной и антибактериальной терапии.
Это, что называется, официальная программа. Теперь — о насущном, а именно: виферон, и это не секрет, является предметом бурных дискуссий в медицинском и околомедицинском мире. Дело в том, что ряд уважаемых специалистов высказывают объективные сомнения в его эффективности, считая его чуть ли не плацебо. Одним из аргументов здесь является его неустойчивость в желудочно-кишечном тракте, куда он попадает, будучи введенным ректально. И единственным способом сохранить препарат в целости является подкожное или внутримышечное введение, а, как известно, таких лекарственных форм виферона производителем не предусмотрено. С другой стороны, в базах данных MEDLINE (крупнейшая мировая база данных медицинской информации, объединяющая около 75% медицинских изданий, выпускаемых на земном шаре) насчитывается более 40 упоминаний виферона. Да, основным предметом исследований все же являлся не отечественный виферон, а его фармакологически активное вещество — интерферон альфа-2. Тем не менее, даже при подобном допущении, виферон уж точно нельзя назвать пустышкой, не имеющей «за душой» ни малейших доказательств своей эффективности. В любом случае, пока ведутся все эти жаркие споры, сам препарат весьма комфортно чувствует себя на аптечных прилавках и абсолютно не жалуется на недостаток внимания со стороны врачей и пациентов.
Пути передачи ОРЗ взрослым и детям
Распространенность ОРВИ связана как со множеством возбудителей, так и с тем, что специфический иммунитет против перенесенных инфекций не сохраняется на продолжительный период времени. Патогены с легкостью передаются в окружающей среде. Необходимость нахождения в общем пространстве с другими людьми (общественный транспорт, детские дошкольные и образовательные учреждения и проч.) увеличивает риск заразиться. В ряде случаев носитель инфекции, даже не подозревая о своей опасности для окружающих, может передавать вирус за несколько суток до манифестации клинических симптомов. Максимальная опасность заражения обычно наступает на 1-3 день от начала заболевания. Минимальная социальная дистанция, о которой часто напоминают во время пандемии коронавируса, составляет 1,5 – 2 метра, однако такое расстояние, к сожалению, не учитывает таких факторов как турбулентность воздуха, скорость с которой частицы вылетают при кашле и чихании.
Простуды в детском возрасте
Дети легко обмениваются инфекцией, контактируя друг с другом. Относительно безопасны лишь первые месяцы жизни, когда ребенок сохраняет пассивный иммунитет, полученный от матери. Младенец находится в некоторой изоляции: контакты часто ограничены членами семьи. К сожалению, нельзя полностью исключить вероятность заражения даже во младенчестве. Среди дошкольников, не достигших пятилетнего возраста, наблюдается наибольшая заболеваемость что, очевидно связано с возрастанием социальных контактов и посещением детских коллективов. «Садовские» дети в течение первого года могут болеть ОРВИ до 10–15 раз, затем частота снижается примерно в два раза, но и в последующие годы остается довольно высокой — 3–5 раз в год. Повторяющиеся простуды могут истощать детский организм, снижать защитные силы, задерживать нормальное развитие, способствуют формированию «тлеющих» очагов инфекции, аллергии, препятствуют проведению профилактических прививок. К специфическим методам профилактики относится вакцинация. Однако вакцина работает в отношении конкретного возбудителя, например, вируса гриппа, а вот против остальных инфекций, которых как известно, насчитывается несколько сотен, – нет. К неспецифическим методам можно отнести закаливание и применение противовирусных по схеме, предложенной вашим педиатром.
Виферон гель для местного и наружного применения 36000 МЕ/г 12 г в Тамбове
Гель, наружно и местно.
В комплексной терапии ОРВИ, включая грипп, длительных и частых ОРВИ, в т.ч. осложненных бактериальной инфекцией
:
полоску геля длиной не более 0,5 см наносят на предварительно подсушенную поверхность слизистой оболочки носа и/или на поверхность небных миндалин 3–5 раз в день при помощи шпателя или ватного тампона/ватной палочки (см. Примечание
). Курс лечения составляет 5 дней, при необходимости курс может быть продлен.
Профилактика ОРВИ, включая грипп
:
в период подъема заболеваемости полоску геля длиной не более 0,5 см наносят на предварительно подсушенную поверхность слизистой оболочки носа и/или на поверхность небных миндалин 2 раза в день в течение 2–4 нед.
В комплексной терапии рецидивирующего стенозирующего ларинготрахеобронхита
:
полоску геля длиной не более 0,5 см наносят на поверхность небных миндалин при помощи шпателя или ватного тампона/ватной палочки в остром периоде заболевания 5 раз в день, в течение 5–7 дней, затем 3 раза в день в течение последующих 3 нед.
Профилактика рецидивирующего стенозирующего ларинготрахеобронхита
:
полоску геля длиной не более 0,5 см наносят на поверхность небных миндалин при помощи шпателя или ватного тампона/ватной палочки 2 раза в день в течение 3–4 нед, курсы повторяют 2 раза в год.
В комплексной терапии острой и хронической рецидивирующей герпетической инфекции (при появлении первых признаков заболевания или в период предвестников):
полоску геля длиной не более 0,5 см наносят при помощи шпателя или ватного тампона/ватной палочки на предварительно подсушенную пораженную поверхность 3–5 раз в день в течение 5–6 дней, при необходимости продолжительность курса увеличивают до исчезновения клинических проявлений.
В комплексной терапии герпетического цервицита
:
1 мл геля наносят ватным тампоном на предварительно очищенную от слизи поверхность шейки матки 2 раза в день в течение 7 дней, при необходимости продолжительность курса может быть увеличена до 14 дней.
Примечание
.
На слизистую оболочку носовой полости гель наносят после очищения носовых проходов, на поверхность небных миндалин — через 30 мин после принятия пищи. При нанесении геля на небные миндалины не прикасаться к миндалинам ватным тампоном, а лишь гелем, гель при этом самостоятельно стекает вниз по поверхности миндалины. При нанесении геля на шейку матки следует предварительно удалить ватным или марлевым тампоном слизь и выделения со сводов влагалища и шейки матки.
При нанесении геля на пораженные участки кожи и слизистых оболочек через 30–40 мин образуется тонкая пленка, на которую вновь наносят препарат. При желании, пленку можно отслоить или смыть водой перед повторным нанесением препарата.
Назальные противовирусные мази как способ защиты детей от простуды
Чаще всего под «простудой» подразумевают нетяжелое заболевание верхних дыхательных путей, которое вызвано вирусной инфекцией. Входными воротами для возбудителей ОРВИ является слизистая оболочка верхних дыхательных путей, где и локализуется воспаление при большинстве ОРВИ. Тяжелое течение ОРВИ с поражением нижних дыхательных путей с развитием бронхита, пневмонии может быть связано со сниженными показателями иммунитета ребенка. Известно, что до 7 лет иммунитет ребенка претерпевает изменения около 4-5 раз. При ОРВИ в острый период как правило применяется этиотропная терапия с использованием противовирусных препаратов как местного, так и общего действия. Роль противовирусных препаратов состоит в том, что они препятствуют репродукции вирусов, способствуют снижению вирусной нагрузки на организм. Кроме того, противовирусная терапия облегчает течение болезни, снижает вероятность развития осложнений и уменьшает опасность инфицирования окружающих больного лицi. Для лечения ОРВИ и гриппа можно применять ВИФЕРОН Мазь у детей старше 1 года. Самым маленьким педиатры рекомендуют ВИФЕРОН Гель, который разрешен с 0 лет.
Также в терапии ОРВИ задействуют противовоспалительные и симптоматические средства для облегчения симптомов. Больным предписывается постельный и питьевой режим, диета, витаминные добавки. А вот антибиотики применяют строго по показаниям и назначению врача.
Эффективность применения мази виферон при реабилитации часто болеющих детей
Система интерферона осуществляет в организме полифункциональное действие в трех основных направлениях: антивирусном, антипролиферативном, иммуномодулирующем. Несовершенство функционирования системы интерферона может явиться причиной повышения чувствительности детей к инфекционным заболеваниям и усугубления тяжести их течения.
Исследования, посвященные становлению системы интерферона в онтогенезе, позволили выявить некоторые связанные с этим возрастные особенности [3]. У новорожденных детей, по сравнению со взрослыми донорами, отмечается значительное снижение способности лейкоцитов к продукции α-интерферона (α-ИФН), а также γ-интерферона (γ-ИФН). При этом чем меньше гестационный возраст новорожденного ребенка, тем в большей степени оказываются снижены эти показатели [1]. У недоношенных новорожденных концентрация эндогенного интерферона в сыворотке крови превышает таковую у доношенных, детей раннего возраста и взрослых. Циркулирующий интерферон рассматривается в настоящее время как «ранний» интерферон, который имеет физиологическую направленность, отражая состояние системы интерферона развивающегося плода [3].
Действие «раннего» интерферона направлено не столько на защиту, сколько на развитие и дифференцировку клеток плода. Установлена взаимосвязь снижения уровня продукции «раннего» интерферона и отклонений от нормы развития плода у беременных женщин [5]. Выявлено также, что патология анте- и перинатального периодов онтогенеза, приводящая к развитию перинатальной гипоксии, фетаплацентарной недостаточности, провоцирует развитие иммунологических нарушений в системе мать–плацента–плод и отклонения в становлении иммунной системы в постнатальном онтогенезе [6].
Задачей данного исследования явилась разработка методов реабилитации часто болеющих детей с использованием мази виферон и анализ их эффективности.
Часто болеющим ребенок считался, если он переносил в течение года 4 и более острых респираторных заболеваний или если его индекс резистентности (РИ) составлял 0,33 и выше [4]:
РИ = (число острых респираторных заболеваний, перенесенных ребенком)/ (число месяцев наблюдений)
В работе использовались клинические методы, исследование интерферонового статуса (сывороточный, α-ИФН, γ-ИФН), по методу, предложенному С. С. Григорян и соавторами (1988), изучение клеточного звена иммунитета. Для выделенных субпопуляций Т-лимфоцитов определялось количество кислой фосфатазы методом азосочетания, по Goldberg и Barka (1978).
Препараты интерферонов характеризуются сочетанием противовирусной, антибактериальной и иммуномодулирующей активности. В последние годы генно-инженерным методом были получены препараты интерферонов нового поколения (реаферон, реальдирон, а также зарубежные — интрон А, роферон А), что позволяет исключить использование в качестве сырья донорскую кровь. Среди них следует выделить отечественный комплексный препарат виферон, в состав которого входят человеческий рекомбинантный интерферон α-2b, мембраностабилизирующие компоненты (витамины Е и С) и основа. Препарат выпускается в двух лекарственных формах: мазь и ректальные суппозитории. Комплексный состав виферона обусловливает ряд новых эффектов: в сочетании с мембраностабилизирующими компонентами противовирусная активность рекомбинантного интерферона α-2b возрастает в 10–14 раз, усиливается его иммуномодулирующее действие на Т- и В-лимфоциты, нормализуется содержание иммуноглобулина Е, усиливается фагоцитоз, отсутствуют побочные эффекты, возникающие при парентеральном введении препаратов интерферона (гриппоподобные явления, сильные головные боли, артралгия, галлюцинации, выпадение волос, диарея). Установлено, что при длительном применении виферона в течение 2 лет не образуются антитела, нейтрализующие антивирусную активность рекомбинантного интерферона α-2b.
Перечисленные свойства виферона, в частности интерфероно- и иммунокорригирующее действие, послужили основанием для его применения при реабилитации данной категории детей. В качестве лекарственной формы применялась мазь виферон, содержащая в 1 г 40 тыс. МЕ интерферона.
Препарат использовался в трех основных направлениях: при проведении курсов иммуно- и интерферонореабилитации; в периоде адаптации к дошкольному учреждению; с профилактической целью в период подъема заболеваемости ОРВИ.
Мазь виферон вводилась интраназально по разработанному нами методу (патент РФ № 2214272 от 20.10.2003) 2 раза в день в суточной дозе 1 г. Первые 2 нед препарат применялся ежедневно, последующие 2–4 нед — 3 раза в неделю. Под наблюдением находились часто болеющие дети, посещающие дошкольные учреждения и воспитывающиеся в доме ребенка. Возраст детей колебался от 3 мес до 5,5 лет. Из них более половины (61,6%) составляли дети раннего возраста. Все часто болеющие дети имели отклонения в анте- и перинатальном периоде развития. Мазь виферон получили 73 ребенка (основная группа). Группу сравнения, в которой дети не получали препарат, а также другие иммуномодулирующие средства, составили 34 ребенка того же возраста, имеющие неблагоприятное течение раннего онтогенеза и страдающие частыми респираторными инфекциями. В обеих группах проводились общеоздоровительные мероприятия (массаж, витаминотерапия, лечебная физкультура и т. д.).
Анализ клинической эффективности мазевой формы виферона показывает его выраженное влияние на заболеваемость детей в периоде адаптации к дошкольному учреждению. Среди детей, получавших виферонореабилитацию, 41% не заболели в первые 3,5 мес после поступления в дошкольное учреждение. В группе сравнения все наблюдавшиеся дети за этот период переболели. Число дней, пропущенных по болезни, в группе получавших виферон оказалась в 2,2 раза ниже, чем в группе сравнения (р < 0,01), а число эпизодов ОРЗ, перенесенных одним ребенком, — почти в 2 раза ниже (р < 0,01).
Одновременно с положительным клиническим эффектом отмечалось улучшение иммунологических показателей. Это выражалось в достоверном (р < 0,01) увеличении хелперной субпопуляции лимфоцитов (38,2 ± 0,45% и 41,73 ± 0,67% соответственно), в уменьшении Т-супрессоров (22,98 ± 0,52% и 21,27 ± 0,62% соответственно, р < 0,05), в нормализации иммунорегуляторного индекса (1,68 ± 0,06 и 1,96 ± 0,09 соответственно, р < 0,01). Достоверных различий в динамике иммунологических показателей у детей группы сравнения за это же время не выявлено (p > 0,05). Последующие наблюдения в течение года показали, что влияние виферонореабилитации, проведенной в периоде адаптации к дошкольному учреждению, на заболеваемость детей постепенно со временем уменьшается. Так, если заболеваемость детей за первые 3,5 мес после приема препарата была в 2 раза ниже, чем в группе сравнения, то за 6 мес она оказалась в 1,5 раза, а за 8 мес — в 1,4 раза ниже, чем в группе детей, не получавших препарат. Это обусловливает необходимость проведения повторных курсов виферонореабилитации у часто болеющих детей, поступивших в дошкольные учреждения, через каждые 3–4 мес до достижения стойкого клинического эффекта.
Виферонореабилитация, наряду со снижением заболеваемости, способствовала облегчению адаптации к дошкольному учреждению и за счет уменьшения эмоционально-поведенческих нарушений. Это связано с более длительным пребыванием детей в коллективе, возможностью осуществления психолого-педагогических воздействий.
Мазь виферон была включена также в комплекс реабилитации часто болеющих детей, которая проводится обычно 2 раза в год. Клинические наблюдения, проведенные в течение года, показали, что виферонореабилитация приводит к снижению заболеваемости респираторными инфекциями в 2,0–1,7–2,1 раза. При этом наиболее выраженный эффект отмечается у детей раннего возраста.
Применение мази виферон способствует достоверному (р < 0,01) увеличению синтеза γ-интерферона у часто болеющих детей как первого года жизни, так и более старшего возраста. Отмечается достоверное снижение циркулирующего «раннего» интерферона у детей второго и третьего года жизни. Если до виферонореабилитации он определялся у 66,67% обследованных, то после ее окончания — у 28,27% часто болеющих детей (р < 0,05). У часто болеющих детей первого года жизни достоверного снижения циркулирующего «раннего» интерферона не происходит (р > 0,05). После курса виферонореабилитации циркуляция его сохраняется у подавляющего большинства (85,71%) детей, что указывает на необходимость более длительного применения препарата у детей данного возраста. Достоверного повышения способности к продукции α-ИФН не выявлялось у всех без исключения обследованных детей (р > 0,05). Можно утверждать, что параллельно с нарастанием синтеза γ-ИФН после курса виферонореабилитации у часто болеющих детей отмечается существенная положительная динамика показателей клеточного иммунитета; нарастает хелперная субпопуляция Т-лимфоцитов (p < 0,01), снижается число Т-супрессоров (p < 0,01), возрастает иммунорегуляторный индекс (p < 0,01). Достоверных изменений в изученных показателях клеточного иммунитета в группе детей, не получавших виферон, за это время не происходило (p > 0,05).
Таким образом, применение мази виферон с целью реабилитации нарушений в системе интерферона у часто болеющих детей с дизонтогенетическими отклонениями в анамнезе оказывает существенное интерферонокорригирующее и иммуномодулирующее действие. Оно проявляется в стимуляции γ-интерфероногенеза, уменьшении циркулирующего «раннего» интерферона, повышении хелперной активности клеточного звена иммунитета, нормализации соотношения субпопуляций Т-лимфоцитов. Клинически данный процесс коррелирует со снижением числа эпизодов респираторных инфекций, повышением резистентности детей, облегчением адаптационного синдрома в период привыкания к дошкольному учреждению.
Курс виферонопрофилактики проводился в весеннее время года с учетом выявленных и описанных нами ранее сезонных ритмов интерфероногенеза. Для сопоставления полученных данных анализировалась заболеваемость респираторными инфекциями за 2 мес до виферонопрофилактики и в течение 2 мес после ее окончания. Изучение клинической эффективности препарата показало ее различие у детей раннего и дошкольного возраста. У детей раннего возраста во время виферонопрофилактики не было случаев заболеваний. В течение последующих 2 мес по сравнению с тем же временным отрезком, предшествующим профилактике, отмечалось снижение заболеваемости ОРВИ в 4 раза по числу случаев и в 6,6 раза по числу дней, пропущенных одним ребенком (р < 0,01). Достоверных различий в заболеваемости детей дошкольного возраста до и после проведения виферонопрофилактики не определялось.
Более выраженная эффективность виферонопрофилактики у детей первых 3 лет жизни может быть обусловлена оптимально подобранной дозой препарата и схемой его введения, пластическими способностями организма детей раннего возраста, и в частности их иммунной системы, обусловливающими высокий иммуномодулирующий эффект.
Исследование интерферонового статуса детей до и после виферонопрофилактики показывает ее положительное влияние на состояние системы интерферона. У обследованных детей отмечается достоверное нарастание продукции γ-ИФН (р < 0,01), уменьшение циркулирующего «раннего» интерферона (р < 0,01). Число детей, у которых выявляется «ранний» интерферон уменьшается в 2,7 раза. В группе сравнения исследования, проведенные в те же сроки, достоверных изменений в показателях интерферонового статуса не выявили (р > 0,05).
Следует отметить отсутствие побочных эффектов, в том числе аллергических реакций, отрицательных изменений лабораторных показателей, при применении мази виферон у всех наблюдавшихся детей.
Таким образом, использование мазевой формы отечественного препарата виферон у часто болеющих детей оказывает интерферонокоррегирующее и иммуномодулирующее действие, способствуя нарастанию продукции γ-ИФН, хелперной субпопуляции Т-лимфоцитов, уменьшению циркулирующего «раннего» интерферона, нормализации иммунорегуляторного индекса, снижению заболеваемости ОРВИ, облегчению адаптации в период привыкания к новым микросоциальным условиям.
По вопросам литературы обращайтесь в редакцию.
З. С. Макарова, доктор медицинских наук, профессор В. А. Доскин, доктор медицинских наук, профессор В. В. Малиновская, доктор биологических наук, профессор РМАПО, ГУ НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН, Москва
Механизм действия иммунитета в носу
Большинство инфекционных агентов проникают в организм с поверхности слизистых оболочек, которые являются первоначальными входными воротами для большинства респираторных вирусов. Для борьбы с инфекциями иммунная система задействует различные механизмы. – Кроме повышения активности со стороны общего системного иммунитета, немаловажную роль в защите от патогенных вирусов играет местный иммунитет. Именно он помогает справиться с теми патогенами, которые осели на поверхности слизистых оболочек носоглотки, и препятствует дальнейшему распространению инфекции внутрь.
Секреторные иммуноглобулины А-типа – особые белковые вещества – они играют основную роль в предупреждении заболевания или в выздоровлении. Специфическая профилактика вирусных инфекций задействует иммунитет слизистых. Присутствующие на них IgA, действие которых направлено на нейтрализацию инфекции, могут происходить из сыворотки крови либо секретироваться клетками подслизистой ткани.
Действенной мерой для защиты верхнего отдела респираторного тракта считается индукция иммуноглобулинов именно в местах репликации вируса – носоглотке. Стимуляция выработки сывороточных белков в высоком титре более эффективна для нижних дыхательных путей.
Усиление активности местного иммунитета играет важную роль в предотвращении инфицирования организма некоторыми вирусами, особенно гриппа. Знание механизма формирования местного иммунитета делают поиск средств, обеспечивающих защиту слизистых оболочек от инфекционных агентов решаемой задачей. Так в начале прошлого века была сформулирована теория местного иммунитета, а впоследствии накоплены данные, свидетельствующие о важной роли факторов местной защиты при ряде вирусных инфекций. С открытием иммуноглобулина А и доказательством его секреции клетками слизистой оболочки началась новая эра в развитии прикладной иммунологии.
В частности, было установлено, что IgA — наиболее важный иммуноглобулин, основная биологическая функция которого состоит в защите слизистых оболочек от инфекционных агентов. Наиболее вероятный механизм нейтрализации вируса IgA заключается в предотвращении связи вируса с клетками-мишенями слизистой, хотя возможны и другие.
Было установлено, что IgA могут не только препятствовать присоединению вируса к клеточным рецепторам, но и подавлять проникновение его в клетку или репликацию. Исследования механизма внутриклеточной нейтрализации вируса, позволяют заключить, что IgA может способствовать не только защите от вирусной инфекции слизистых, но и ее прекращениюii.
Препарат ВИФЕРОН Гель, например, обладает выраженным местным иммуномодулирующим действием и способствует увеличению локально образующихся антител класса секреторных IgA, препятствующих фиксации и размножению патогенных микроорганизмов на слизистых оболочках, что обеспечивает профилактический эффект препарата для профилактики вирусных и других заболеваний.