Причины
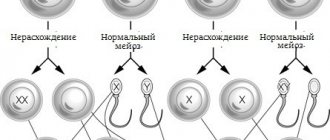
При отсутствии в анамнезе семьи данного заболевания, при абсолютном здоровьем родителей, всё равно есть риск рождения ребенка с данным заболеванием. Науке известно, что клетка человека включает 46 хромосом. В яйцеклетке и сперматозоиде находится по двадцать три хромосомы. Когда они объединяются, то объединяется и количество хромосом. Причины синдрома Эдвардса на сегодняшний день изучены недостаточно.
Исследователи говорят, что вследствие мутаций генов формируется в 18-й паре хромосом одна лишняя. В 2 случаях данной болезни из 100 восемнадцатая хромосома удлиняется, при этом 47-й хромосомы не формируется, а происходит транслокация.
В трех случаях болезни из ста врачи говорят о мозаичной трисомии. Это значит, что лишняя хромосома присутствует только в части клеток организма плода, а не абсолютно во всех. Но по симптомам три описанные варианта болезни сходятся. Только в первом случае течение может быть тяжелым и больше шансов летального исхода.
Трисомия 18 (синдром Эдвардса) является наиболее распространенной аутосомной аномалией среди родившихся живыми детей после синдрома Дауна (трисомия 21). В большинстве случаев трисомия 18 (синдром Эдвардса) является истинной, т.е. ее причиной является нерасхождение хромосом во время мейоза. В небольшом числе случаев (до 10%) трисомия 18 (синдром Эдвардса) является мозаичной (мозаицизм — состояние, при котором в организме присутствуют ткани генетически различных типов, например, нормальные клетки и клетки имеющие три хромосомы), вызванные постзиготным нерасхождением хромосом в анафазе — на ранней стадии развития зародыша (Chen 2004, Forrester 1999, Carothers 1999, Huether 1996, Pradat 1991, Buyse, 1990. Возможна и частичная трисомия. При этом часть хромосомы 18 присоединяется к другой хромосоме. Такой эффект называется «Транслокация», и он может произойти как при созревании гамет, так и после оплодотворения в клетках зародыша. В клетках организма при этом оказываются две гомологичные хромосомы 18 и, дополнительно, часть хромосомы 18, прикрепленная к другой хромосоме. У людей, страдающих частичной трисомией 18, аномалии проявляются слабее, нежели при типичном синдроме Эдвардса. Большинство трисомий 18 обнаруживаются у плодов в середине второго триместра и очень часто такие беременности заканчиваются внутриутробной гибелью плода. (Hook, 1989).
Клинические особенности, связанные с трисомии 18 включают, но не ограничиваются следующими: расстройства центральной нервной системы (голопрозенцефалия, менингомиелоцеле), пороки развития глаз, носа, расщелина губы и / или неба, деформация ушных раковин, деформированные конечностей, полидактилия, а также дефекты сердца, половых органов, и пр.
Прогноз для этого заболевания, как правило, неблагоприятный. Большинство рожденных детей, умирают, в среднем, в течение 2 — 10 дней (Parker, 2003). Тем не менее, есть дети, продолжительность жизни которых достигает года и более (Rasmussen, 2003). Однако, такие дети имеют как физическое, так и психическое отставание в развитии (Parter 2003). Популяционная частота примерно 1:7000.
ЭТИОЛОГИЯ
Причиной истинной трисомии 18 является нерасхождение хромосом при формировании яйцеклетки и сперматозоида, когда одна гамета получает дополнительную 18 хромосому. Нерасхождение может произойти в первом (MI) или втором (MII) мейотического этапе.
В 90-97% случаев дополнительная хромосома 18 имеет материнское происхождение, а отцовское происхождение в 3-10% всех случаев. Среди случаев трисомии 18 материнского происхождения, 31-39% бывают в результате нерасхождения хромосом в фазе MI и 61-69% в результате нерасхождение в фазе MII (Bugge et al., 1998; Nicolaidis and Petersen, 1998; Eggermann et al., 1996; Ramesh and Verma, 1996; Fisher et al., 1995; Jacobs and Hassold, 1995; Fisher et al., 1993; Ya-gang et al., 1993).
ДЕМОГРАФИЯ И РЕПРОДУКТИВНОСТЬ
Риск трисомии 18, как известно, возрастает с увеличением возраста матери (Munne 2004, Naguib 1999, Baty 1994, Buyse 1990, Goldstein 1988, Schreinemachers 1982). Риск трисомии 18 (синдрома Эдвардса) связывают также и с увеличением отцовского возраста, однако, если риск трисомии 18 увеличивается за счет возраста матери, то возрастом отца в таких случаях пренебрегают. (Naguib 1999, Baty 1994). Для женщин старше 45 лет риск родить больного ребёнка составляет 0,7 %.
Раса/этническая принадлежность практически не влияет на риск трисомии 18 (Buyse 1990). Одно исследование показало, что из четырех расовых/этнических групп обследованных (европейцы, дальневосточные азиаты, жители островов тихого океана, филиппинцы), риск трисомии 18 был самым высоким для дальневосточных азиатов и самым низким для жителей островов тихого океана (Forrester, 1999). Тем не менее, эти различия в риске по видимому, связаны с различиями в распределении материнского возраста среди этих расовых / этнических групп.
Географическая область может влиять на риск трисомии 18. В одном исследовании приводятся данные, что риск трисомии 18 выше среди городских жителей (Forrester, 1999). Этот повышенный риск остается после учета возраста матери. Несколько исследований показали, что на распространенность трисомии 18 могут влиять сезонные колебания (Naguib, 1999).
Некоторые исследования показали, что Трисомия 18 (синдром Эдвардса) в последние годы имеет тенденцию к увеличению. Однако, возможно, это связано как с улучшением диагностики анеуплоидий, в т.ч. пренатальной диагностики и диагностики фетусов (Pradat 1991), так и с повышением возраста рожающих женщин.(Gessner 2003, Forrester, 1999).
За последние несколько десятилетий, было установлено, что в сыворотке женщин с плодом с трисомией 18 имеется низкий уровень альфа-фетопротеина, хорионический гонадотропин человека, и эстриол (anick 1993, Greenberg 1992, Doran 1986). Кроме того, при пренатальном ультразвуковом исследовании обнаруживаются различные структурные аномалии часто связаны с трисомией 18 (Abramsky 1993, Vintzileos 1987). Пренатальный скрининг маркеров, УЗИ и окончательный диагноз подтвержденный кариотипированием с помощью таких процедур, как амниоцентез и биопсия хориона, позволяют определить трисомию 18 в период внутриутробного развития.
Пол ребенка влияет на риск трисомии 18. Девочки с трисомией 18 рождаются в 3 раза чаще мальчиков. (Forrester 1999, Naguib 1999, Carothers 1999, Huether 1996, Pradat 1991, Buyse 1990, Goldstein 1988). Одно исследование показало, что соотношение полов изменяется в различных расовых /этнических группах, однако это такие наблюдения сделаны на небольших выборках, что не позволяет говорить о такой связи достоверно.(Huether 1996).
Риск повторения для трисомии 18 составляет, примерно, 1% (Baty 1994, Buyse 1990). Последние исследования показали, что риск трисомии увеличивается у женщин, которые имели трисомии 18 в предыдущих беременностях, независимо от рождения живого ребенка или внутриутробной гибели плода. То есть, даже если беременность самопроизвольно прерывается, риск остается повышенным (Munne 2004). Существует также повышенный риск трисомной беременности у женщин, с низким числом овоцитов (Kline, 2000). Вероятно, это условие связано с наступлением менопаузы.
ОБРАЗ ЖИЗНИ И ФАКТОРЫ ОКРУЖАЮЩЕЙ СРЕДЫ.
Нет достоверных данных, которые подтверждали бы влияние факторов окружающей среды на риск трисомии 18. Тем не менее, различия в распространенности трисомии 18 между популяциями (Forrester 1999, Naguib 1999) позволяют предположить, что экологические факторы могут влиять на риск хромосомных ошибок. В то же время, отсутствует повышенный риск трисомии 18 у людей живущих рядом со свалками твердых отходов или мусоросжигательными заводами (Cordier 2004, Harrison 2003). Наличие хлоридов и нитратов в питьевой воде (Cedergren 2002) , а также пестицидов (Berkowitz 2003) не увеличивают риск этого дефекта. У матерей, чья работа связана с химическими растворителями, также не увеличивает риск трисомии 18 (Wennborg 2005).
Вероятность хромосомных ошибок в настоящее время может увеличиваться из-за вспомогательных репродуктивных технологий (ВРТ). Однако, до конца не ясно, связано ли это с несовершенством лабораторных методов или с генетическими нарушениями у родителей, которые одновременно могут являться и причиной бесплодия. То есть пары, которые не могут забеременеть естественным путем могут быть предрасположены к генетическим ошибкам (Palermo 2000).
Одно исследование показало, что различия в метаболизме фолиевой кислоты у женщин не связаны с мейотическими ошибками приводящими к анеуплоидиям.
Регулярное употребление поливитаминов не связано с уменьшением риска трисомии 18 (Botto 2004).
ГЕНЕТИЧЕСКАЯ ПРЕДРАСПОЛОЖЕННОСТЬ
Иногда, вследствие явления, которое называется сбалансированная транслокация, некоторые люди могут нести генетический материал, принадлежащий хромосоме 18 в другой хромосоме. Поскольку у таких людей нет дополнительного генетического материала они не имеют признаков трисомии 18. Однако, у таких людей есть повышенный риск рождения детей с этим заболеванием. Установить носительство сбалансированной хромосомной транслокации можно при исследовании кариотипа.
В редких случаях один из родителей может быть носителем частичной трисомии 18, которая может передаваться по наследству. Установить носительство частичной трисомии можно с помощью хромосомного микроматричного анализа.
Таким образом, в большинстве случаев синдром Эдвардса является результатом случайных ошибок в делении клетки и мало связан с какими либо факторами окружающей среды или состояния человека.
Литература
- Abramsky L, Chapple J. Room for improvement? Detecting autosomal trisomies without serum screening. Public Health 1993;107:349-354.
- Baty BJ, Blackburn BL, Carey JC. Natural history of trisomy 18 and trisomy 13. I. Growth, physical assessment, medical histories, survival, and recurrence risk. Am J Med Genet 1994;49:175-188.
- Berkowitz GS, Obel J, Deych E, Lapinski R, Godbold J, Liu Z, Landrigan PJ, Wolff MS. Exposure to indoor pesticides during pregnancy in a multiethnic urban cohort. Environmental Health Perspectives 2003;111:1:79-84.
- Botto LD, Mulinare J, Yang Q, Liu Y, Erickson JD. Autosomal trisomy and maternal use of multivitamin supplements. American Journal of Medical Genetics 2004:125A:113-116.
- Buyse ML, editor-in-chief. Birth Defect Encyclopedia . Cambridge, Massachusetts: Blackwell Scientific Publications, 1990.
- Canfield MA, Honein MA, Yuskiv N, Xing J, Mai CT, Collins JS, Devine O, Petrini J, Ramadhani TA, Hobbs CA, Kirby RS. National estimates and race/ethnic-specific variation of selected birth defects in the United States, 1999-2001. Birth Defects Res A Clin Mol Teratol. 2006 Nov;76(11):747-56.
- Canick JA, Saller DN. Maternal serum screening for aneuploidy and open fetal defects. Obstet Gynecol Clin North Am 1993;20:443-454.
- Cardonick E, Iacobucci A. Use of chemotherapy during human pregnancy. The Lancet Oncology 2004;5:283-291.
- Carothers AD, Boyd E, Lowther G, Ellis PM, Couzin DA, Faed MJ, Robb A. Trends in prenatal diagnosis of Down syndrome and other autosomal trisomies in Scotland 1990 and 1994, with associated cytogenetic and epidemiological findings. Genet Epidemiol 1999;16:179-190.
- Cedergren MI, Selbing AJ, Lofman O, Kallen BAJ. Chlorination byproducts and nitrate in drinking water and risk for congenital cardiac defects. Environmental Research Section A 2002;89:124-130.
- Chen M, Yeh GP, Shih JC, Wang BT. Trisomy 13 mosiacism: study of serial cytogentic changes in a case from early pregnancy to infancy. Prenatal Diagnosis 2004;24:137-143.
- Cordier S, Chevrier C, Robert-Gnansia E, Lorente C, Brula P, Hours M. Risk of congenital anomalies in the vicinity of municipal solid waste incinerators. Occup Environ Med 2004;61:8-15.
- Doran TA, Cadesky K, Wong PY, Mastrogiacomo C, Capella T. Maternal serum alpha-fetoprotein and fetal autosomal trisomies. Am J Obstet Gynecol 1986;154:277-281.
- Forrester MB, Merz RD. Trisomies 13 and 18: Prenatal diagnosis and epidemiologic studies in Hawaii, 1986-1997. Genet Test 1999;3:335-340.
- Forrester MB , Merz RD, Yoon PW. Impact of prenatal diagnosis and elective termination on the prevalence of selected birth defects in Hawaii. Am J Epidemiol 1998;148:1206-1211.
- Fried PA. The consequences of marijuana use during pregnancy: a review of the human literature, in Women and Cannabis: Medicine, Science, and Sociology, The Haworth Integrative Healing Press, 2002.
- Gessner BD. Reasons for trisomy 13 and 18 births despite the availability of prenatal diagnosis and pregnancy termination. Early Human Development 2003; 73:53-60.
- Goldstein H, Nielsen KG. Rates and survival of individuals with trisomy 13 and 18. Clin Genet 1988;34:366-372.
- Greenberg F, Schmidt D, Darnule AT, Weyland BR, Rose Esmie, Alpert E. Maternal serum alpha-fetoprotein, beta-human chorionic gonadotropin, and unconjugated estriol levels in midtrimester trisomy 18 pregnancies. Am J Obstet Gynecol 1992;166:1388-1392.
- Harrison RM. Hazardous waste landfill sites and congenital anomalies. Occup Environ Med 2003; 60:79-80.
- Hassold TJ, Burrage LC, Chan ER, Judis LM, Schwartz S, James SJ, Jacobs PA, Thomas NS. Maternal folate polymorphisms and the etiology of human nondisjuntion. American Journal of Human Genetics; 2001:69:434-439.
- Hook EB, Topol BB, Cross PK. The natural history of cytogenetically abnormal fetuses detected at midtrimester amniocentesis that are not terminated electively: New data and estimates of the excess and relative risk of late fetal death associated with 47,+21 and other abnormal karyotypes. Am J Hum Genet 1989;45:855-861.
- Huether CA, Martin LM, Stoppelman SM, D’Souza S, Bishop JK, Torfs CP, Lorey F, May KM, Hanna JS, Baird PA, Kelly JC. Sex ratios in fetuses and liveborn infants with autosomal aneuploidy. Am J Med Genet 1996;63:492-500.
- Jeng W, Wong AW, Ting-A-Kee R, Wells PG Methanmphetamine-enhanced embryonic oxidative DNA damage and neurodevelopmental deficits.Free Radical Biology and Medicine 2005; 39:317-326.
- Kallen B. Use of antihistamine drugs in early pregnancy and delivery outcome. Journal of Maternal-Fetal and Neonatal Medicine 2002;11:146-152.
- Kline J, Kinney A, Levin B, Warburton D. Trisomic pregnancy and earlier age at menopause. American Journal of Human Genetics 2000;67:395-404.
- Kupke KG, Muller U. Parental origin of the extra chromosome in trisomy 18. Am J Hum Genet 1989;45:599-605.
- Munne S, Sandilinas M, Magli C, Gianaroli L, Cohen J, Warburton D. Increased rate of aneuploid embryos in young women with previous aneuploid conceptions. Prenatal Diagnosis 2004; 24: 638-643.
- Naguib KK, Al‑Awadi SA, Moussa MA, Bastaki L, Gouda S, Redha MA, Mustafa F, Tayel SM, Abulhassan SA, Murthy DS. Trisomy 18 in Kuwait. Int J Epidemiol 1999;28:711-716.
- Nothen MM, Eggermann T, Erdmann J, Eiben B, Hofmann D, Propping P, Schwanitz G. Retrospective study of the parental origin of the extra chromosome in trisomy 18 (Edwards syndrome). Hum Genet 1993;92:347-349.
- Palermo GD, Neri QV, Hariprashad JJ, Davis OK, Veeck LL, Rosenwaks Z. ICSI and its outcome. Seminars in Reproductive Medicine 2000; 18:2: 161-169.
- Parker MJ, Budd JLS, Draper ES, Young ID. Trisomy 13 and trisomy 18 in a defined population: epidemiological, genetic, and prenatal observations. Prenatal Diagnosis 2003;23:856-860.
- Park-Wyllie L, Mazzotta P, Pastuszak A, Moretti ME, Beique L, Hunnisett L, Friesen MH, Jacobson S, Kasapinovic S, Chang D, Diav-Citrin O, Chitayat D, Nulman I, Einarson TR, Koren G. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology 2000;62:385-392.
- Pradat P. Is trisomy 18 increasing in Sweden? An analysis of the syndrome during a ten-year period and a comparison with a French registry. Hereditas 1991;114:97-102.
- Ramesh KH, Verma RS. Parental origin of the extra chromosome 18 in Edwards syndrome. Ann Genet 1996;39:110-112.
- Rasmussen SA, Wong LYC, Yang Q, May KM, Friedman JM. Population based analysis of mortality in trisomy 13 and trisomy 18. Pediatrics 2003;111:777-784.
- Schreinemachers DM, Cross PK, Hook EB. Rates of 47,+21, 47,+18, 47,+13 and other chromosome abnormalities in about 20,000 prenatal studies compared with estimated rates in live births. Hum Genet 1982;61:318-324.
- Sorensen HT, Czeizel AE, Rockenbauer M, Steffensen FH, Olsen J. The risk of limb deficiencies and other congenital abnormalities in children exposed to calcium channel blockers. Acta Obst Gynecol Scand 2001;80:397-401.
- Vintzileos AM, Campbell WA, Nochimson DJ, Weinbaum PJ. Antenatal evaluation and management of ultrasonically detected fetal anomalies. Obstet Gynecol 1987;69:640-660.
- Wennborg H, Magnusson LL, Bonde JP, Olsen J. Congenital malformations related to maternal exposure to specific agents in biomedical research laboratories. JOEM 2005; 47:1:11-19.
- Vrijheid M, Dolk H, Stone D, Abramsky L, Alberman E, Scott JES. Socioeconomic inequalities in the risk of congenital anomaly. Arch Dis Child 2000; 82:349-352.
- Ya-gang X, Robinson WP, Spiegel R, Binkert F, Ruefenacht U, Schinzel AA. Parental origin of the supernumerary chromosome in trisomy 18. Clin Genet 1993;44:57-61.
Частота
В 60 случаях мутаций из 100 дети с рассматриваемым синдромом погибают внутри живота матери, потому что из пороки несовместимы с жизнью. Но выживаемость детей с синдромом Эдвардса достаточно высокая (чуть ниже, чем у плодов с трисомией 21). На 3-8 тысяч младенцев один рождается в рассматриваемым диагнозом.
Врачи говорят, что среди младенцев женского пола болезнь встречается в три раза чаще, чем среди мальчиков. Большой риск родить ребенка с данными отклонениями у рожениц, которым более 30 лет. На проятжении первых 12 месяцев жизни умирает около 90 детей из 100 с таким диагнозом. Мальчики живут в среднем от 2 до 3 месяцев, а девочки около 10 месяцев. Шансы, что ребенок с синдромом Эдвардса сможет дожить до взрослых лет, мизерные. Осложнения пороков развития становятся причинами смерти детей:
- кишечная непроходимость
- сердечно–сосудистая недостаточность
- пневмония
- удушье
Профилактика
Говоря о профилактике заболевания, следует отметить, что риск его развития у будущего ребенка существует всегда. Но все же он повышается у родителей в возрасте после 40 лет.
Поэтому беременной очень важно выполнять все предписания наблюдающего ее гинеколога и проходить процедуру антенатального скрининга для своевременного выявления патологий.
Если у одного из супругов отмечается неблагоприятный семейный анамнез, то на этапе планирования беременности стоит обязательно посетить специалиста-генетика и следовать всем его советам.
Симптомы
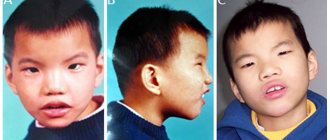
Проявления болезни делят на несколько групп. В первую причисляют те, что характеризуют внешний вид больного человека:
- вес тела при рождении составляет примерно 2кг 100 грамм или 2 кг 200 грамм
- ненормально развитая нижняя или верхняя челюсть
- голова маленькая по отношению ко всему телу
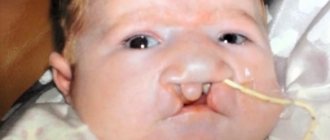
- расщелина верхней губы и/или твердого неба
- неправильный прикус и неправильная форма лица ребенка
- стопа-качалка
- косолапость от рождения
- перепонки на пальцах ног или полное слияние пальцев
- уши низко посажены
- пальцы кисти сжаты, наблюдается неровное их расположение в кулачке
- ротовая щель меньше, чем должна быть
Вторая группа симптомов болезни касается нервно-психической сферы, моторики и функции органов больного ребенка:
- пупочная или паховая грыжа
- врожденные пороки сердца, включая открытый артериальный проток, дефект межжелудочковой перегородки и т.п.
- сглаживание или атрофия мозговых извилин
- недоразвитость мозжечка, мозолистого тела
- умственная отсталость
- задержка нервно–психического развития ребенка
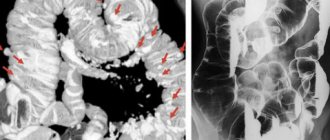
- нарушение локации кишечника
- меккелев дивертикул
- атрезия пищевода или заднего прохода
- нарушение глотательного и сосательного рефлекса
- ГЭРБ
- удвоение мочеточников
- подковообразная или сегментированная почка
- недоразвитость яичников у девочек
- гипертрофированный клитор у младенцев женского пола
- гипоспадия у младенцев мужского пола
- крипторхизм у больных мальчиков
- атрофия мышц
- сколиоз
- косоглазие
Диета
Диета при планировании беременности
- Эффективность: нет данных
- Сроки: 3-5 месяцев до планируемой беременности
- Стоимость продуктов: 1800-2000 руб. в неделю
Детям с такой патологией требуется специальное питание. В тяжелых случаях, при отсутствии глотательного и сосательного рефлексов, проводится питание через зонд.
Будущим мамам до и после зачатия нужно питаться правильно, не потребляя вредных продуктов и спиртного.
Диагностика
О генетических патологиях чаще всего можно узнать, пока женщина еще вынашивает ребенка. Это касается и трисомий. Скрининг беременности проводят с 11-й по 13-ю неделю. Женщина сдает анализы крови (биохимию), проводится УЗИ. Также диагностика заключается в определении каротипа эмбриона, если женщина находится в группе риска (отягощенный семейный анамнез, инфекционные болезни в первом триместре и т. д.).
В скрининге первого семестра определяют, сколько в крови хорионического гормона человека и плазменного протеина А ассоциированного с беременностью. Потом учитывают возраст беременной, чтобы узнать, с каким риском у нее может родиться ребенок с трисомией 18.
Если женщину отнесли в группу риска, чуть позже делают биопсию плода, чтобы точно знать, родится ли ребенок с отклонениями, или здоровый. С 8 до 12 неделю берется анализ ворсин хориона. С 14 по 18-ю неделю проводится изучение вод, окружающих плод. После 20-й недели могут сделать кордоцентез. Процедура подразумевает, что возьмут крови из пуповины (в процессе применяется ультразвук для контроля взятия материала).
В материале обнаруживают количество хромосом. В этом помогает метод КФ–ПЦР. При условии непрохождения беременной генетического скрининга на поздник сроках гестации делают предварительную диагностику генетической мутации методом ультразвукового исследования. Во втором и третьем триместре есть признаки, которые говорят о том, что ребенок с большой вероятностью родится с трисомией:
- заячья губа
- низко расположенные уши плода
- микроцефалия
- волчья пасть
- пороки опорно–двигательного аппарата
- пороки развития мочеполовой системы
- пороки сердца и сосудов
Как пройти тест Prenetix?
Чтобы пройти тест Prenetix, необходимо сделать заявку на исследование и сдать кровь. Забор крови на исследование можно произвести в любом регионе страны – в специализированных медицинских учреждениях или лабораториях, имеющих договор с ЦГРМ Genetico. Далее материал будет отправлен на анализ в московскую лабораторию Genetico. Через 12 дней вы сможете получить результат.
Для получения более подробной информации и записи на анализ свяжитесь с нашими специалистами по указанным телефонным номерам или через онлайн-форму на сайте.
Диагностика после рождения
Синдром Эдвардса у новорожденных обнаруживают по таким признакам:
- небольшой вес новорожденного
- микроцефалия
- волчья пасть или заячья губа
- поперечная ладонная борозда
- неразвитая на пальцах дистальная сгибательная складка
- дистальное расположение осевого трирадиуса и увеличение гребневого счета на ладони
- дуги на подушечках пальцев рук
Но эти признаки еще не говорят о том, что у ребенка именно синдром Эдвардса. Диагноз нуждается в подтверждении. Для этого применяют выше упомянутый метод КФ-полиплазменной цепной реакции, чтобы определить каропин новорожденного. УЗИ показывает кисты сосудистых сплетений у младенца.
Факторы риска
Основными факторами риска являются возраст (особо значимо для синдрома Дауна), а также воздействие радиации, некоторых тяжелых металлов. Следует учитывать, что даже без факторов риска плод может иметь патологию.
Как видно из графика, зависимость величины риска от возраста наиболее значима для синдрома Дауна, и менее значима для двух других трисомий.
Диагностика на УЗИ до рождения
Выявляются такие косвенные признаки заболевания, начиная с двенадцатой недели гестации:
- 1, а не 2 пуповинных артерии
- косточки носа на УЗИ не визуализируются
- грыжа брюшной полости
- низкая ЧСС
- кисты сосудистых сплетений
Кисты не опасны для младенца, на 26-й недели гестации они ликвидируются. Но такие кисты говорят о том, что у ребенка генетическая аномалия развития. Это может быть и рассматриваемый в данной статье синдром. Кисты находят у трети больных с данным диагнозом. Если на УЗИ врач видит кисты, то следующим этапом пренатальной диагностики является консультация генетика.
Классификация
Полная трисомия – если целая дополнительная хромосома появилась на этапе одной клетки, то набор хромосом нарушается в каждой клетке плода. При такой форме у ребенка наблюдаются многочисленные пороки развития, несовместимые с жизнью. Это наиболее тяжелый вариант болезни.
Частичная трисомия – диагностируется, если лишняя хромосома появляется не на самых ранних этапах развития плода. В таком случае нарушение генетического набора отмечается не во всех клетках, и часть из них останутся здоровыми.
Лечение синдрома Эдвардса
Цель терапии: скорректировать опасные для жизни ребенка пороки развития. Но стоит помнить, что у ребенка могут быть серьезные нарушения, и он вряд ли доживет до 12-месячного возраста. Если обнаружена пневмония, то младенцу вводят лекарства от воспаления и антибиотики. Если обнаружено, что у малыша нет сосательного и глотательного рефлекса, то его кормят с помощью зонда. При обнаружении у больного атрезии анала или кишечника нужно восстановить проход пищи.
Если врач видит, что течение синдрома Эдвардса благоприятное, то нужно сделать операцию, чтобы устранить пупочную грыжу, паховую грыжу, сердечные пороки, волчью пасть. Некоторые симптомы можно убрать приемом лекарств. Например, если у младенца запоры, ему понадобятся определенные слабительные лекарства. При скоплении газов в кишечнике назначаются препараты из ряда «пеногасителей».
Дети, у которых выявлена рассматриваемая трисомия, имеют риск таких болезней:
- мочеполовые инфекции
- синуситы и фронтиты
- гипертензия артериальная
- апноэ
- гипертензия легочная
- воспаление легких
- рак почки
- средний отит
Важно вовремя найти у младенца эти болезни и правильно их пролечить. Прогноз в большинстве случаев болезни неблагоприятный. Как уже отмечалось, ребенок имеет крайне низкие шансы дожить до полового созревания. Если ребенок и выживает, ему нужен неусыпный уход и контроль, потому что его мозг не будет достаточно развит. Некоторые больные могут без помощи посторонних кушать, а также улыбаются и приобретают минимальные навыки.
Патогенез
Трисомия 18 – это генетическая патология. В каждой человеческой клетке содержится 46 хромосом – это нормальные показатели. Во время оплодотворения по 23 хромосомы женских и мужских половых клеток соединяются и дают в сумме именно такое количество хромосом. Иногда по неизвестным причинам происходят генетические мутации, и в результате появляется лишняя 47 хромосома, дополнительная в 18 паре. Лишняя хромосома у гамет появляется вследствие нерасхождения хромосом при мейотическом делении. В большинстве случаев – в 95% — именно лишняя хромосома становится причиной развития болезни Эдвардса. Но иногда – примерно в 2% случаев – сумма хромосом остается нормальной, но при этом 18 хромосома аномально удлиняется, что приводит к развитию врожденной патологии. Еще в 3% случаев отмечается мозаичная трисомия, при которой дополнительная хромосома присутствует не во всех клетках организма, а только в какой-то его части. Все три формы синдрома протекают по одному типу. Но все же более тяжелое течение отмечается при первой форме болезни.