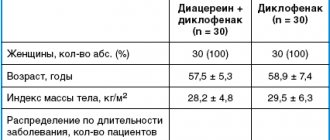
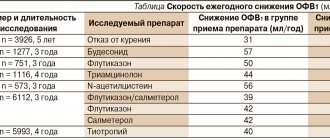
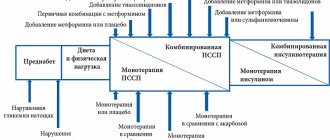
Крапивница — одно из самых распространенных заболеваний кожи, характеризующихся возникновением кожной сыпи, первичным элементом которой является волдырь.
По данным эпидемиологических исследований, крапивница наблюдается хотя бы однократно на протяжении жизни у 15—25% населения, причем у 25% из них отмечается хроническое течение заболевания. По данным разных авторов [1—4], 75—95% больных имеют хроническую идиопатическую крапивницу (ХИК). Хроническая крапивница распространена больше у взрослых, чем у детей, и существенно чаще встречается у женщин. Обычно дебют заболевания приходится на третье—четвертое десятилетия жизни.
Пациенты предъявляют жалобы на пониженное настроение, ухудшение сна и эмоциональный дискомфорт, который частично связан с ограничением социальной активности. Несмотря на то что высыпания являются преходящими, более половины пациентов отмечают связанные с заболеванием проблемы в повседневной жизни.
Клинически уртикарные высыпания сопровождаются зудом, бледнеют при надавливании и представляют собой ограниченный отек сосочкового слоя дермы. Высыпания при крапивнице могут иметь любую локализацию, включая волосистую часть головы, ладони и подошвы. В области головы и шеи число тучных клеток кожи на единицу площади повышено по сравнению с другими участками кожи, поэтому крапивница и зуд этой локализации характеризуются большей интенсивностью [5—10].
Своевременно начатая адекватная терапия имеет большое значение для уменьшения симптомов хронической крапивницы и улучшения качества жизни пациентов [11—15].
В основе патогенеза крапивницы лежит выделение в большом количестве в окружающие ткани и кровь основного медиатора тучных клеток гистамина. Гистамин синтезируется из гистидина в тучных клетках и хранится в везикулах, называемых гранулами. Кроме тучных клеток, гистамин выделяют и другие клетки — базофилы, гистаминергические нервные клетки, однако именно тучным клеткам принадлежит ключевое значение в выделении упомянутого биологически активного вещества.
Очевидно, что исследования фармацевтических компаний были направлены на поиск препаратов, способных блокировать влияние гистамина на организм. В 1942 г. в терапии аллергических заболеваний началась новая эра: было синтезировано первое антигистаминное лекарственное средство. Важность этого открытия трудно переоценить, в пользу чего свидетельствует тот факт, что в 1957 г. за синтез и изучение свойств антигистаминных препаратов Даниэль Бове (Daniel Bovet) получил Нобелевскую премию. Базисной терапией как острых, так и хронических крапивниц являются антигистаминные препараты. В связи с этим блокаторы Н1-гистаминовых рецепторов считаются средством первой линии в лечении острой и хронической крапивницы. Эти препараты являются обратимыми агонистами H1-рецепторов и уменьшают аллергические реакции, опосредованные гистамином [16—20].
Антигистаминные лекарственные средства I поколения (хлоропирамин, дифенгидрамин, клемастин, ципрогептадин, прометазин, фенкарол, гидроксизин) позволили сделать существенный шаг вперед в терапии аллергии, однако при этом обладали фармакологическими особенностями, ограничивающими возможность их применения при широком спектре заболеваний, особенно при хроническом аллергозе, требующем длительного лечения. Их отличала кратковременность терапевтического действия, что требовало многократного приема препарата в течение суток. Неполное связывание с Н1-гистаминовыми рецепторами (около 30%) определяло относительно высокие терапевтические дозы лекарственных средств. Благодаря их свойствам препараты I поколения применяют для достижения быстрого эффекта: они назначаются в остром периоде аллергической реакции как в качестве монотерапии, так и в комбинации с представителями других поколений антигистаминных лекарственных средств. Препараты этой группы незаменимы при острых аллергических реакциях, таких как крапивница, отек Квинке, медикаментозная аллергия, анафилактический шок и т. д. Они оказывают выраженное антигистаминное и антихолинергическое действие [21—25].
Однако при длительной противоаллергической терапии у таких средств недостатков больше, чем преимуществ. Это и послужило причиной появления во второй половине ХХ века антигистаминных препаратов II поколения (терфенадин, астемизол, акривастин, диметенден, лоратадин, левокабаксин, азеластин). Их отличало высокое сродство с Н1-рецепторами, быстрое начало действия и достаточная его продолжительность. Высокая избирательность препаратов обеспечивает отсутствие блокады других видов рецепторов, что минимизирует побочные эффекты при применении. Низкая степень или даже полное отсутствие проходимости гематоэнцефалического барьера определяют отсутствие седативного эффекта и зависимости его проявления от употребления алкоголя. Убедительным аргументом в пользу длительной терапии препаратами этой группы является и отсутствие привыкания.
Главной целью лечения больных хронической крапивницей независимо от этиологического фактора является контроль клинических проявлений и субъективных симптомов. В значительной степени они опосредованы гистамином. В соответствии с клиническими рекомендациями II международной конференции по крапивнице препаратами базисной терапии являются селективные блокаторы Н1-рецепторов. Преимуществами этих препаратов являются не только выраженное влияние на основные симптомы заболевания и хорошая переносимость, но и наличие у них противовоспалительных свойств. Высказано предположение, что при резистентной к терапии хронической крапивнице является допустимым увеличение дозы антигистаминных средств этой группы до 4 раз по сравнению с рекомендуемыми схемами, хотя безопасность и эффективность подобного выбора должны быть дополнительно подтверждены в клинических исследованиях.
Одним из современных блокаторов Н1-рецепторов второго поколения является биластин
— препарат, разрешенный к применению для лечения крапивницы, а также аллергического ринита.
Цель исследования — установить эффективность Никсара
современного блокатора гистаминовых рецепторов 1-го типа биластина у больных хронической идиопатической крапивницей.
Материал и методы
На базе клинико-диагностического ФГБОУ ВО СибГМУ Минздрава Р.Ф. с 2021 по 2021 г. был обследован 51 пациент с диагнозом «L50.1. Хроническая идиопатическая крапивница» в возрасте от 21 года до 53 лет (среднее 36,4±3,4 года), в том числе 36 (71%) мужчин и 15 (29%) женщин. Длительность заболевания составляла от нескольких месяцев до 12 лет (в среднем по группе 4,2±1,6 года). У всех пациентов отмечалось часто рецидивирующее течение крапивницы (более 4 обострений в год; в среднем 5,3±0,9 раза в год). Основными сенсибилизирующими факторами были бытовые (36,7%), пищевые (13,4%) и эпидермальные (11,9%) аллергены. У большинства больных ХИК обострение процесса отмечалось на фоне сопутствующей соматической патологии. Преобладали заболевания желудочно-кишечного тракта — у 13 (25,4%) пациентов; ЛОР-заболевания — у 9 (17,6%) больных и эндокринная патология — у 12 (23,5%).
Обследование больных ХИК проводилось согласно стандартам диагностики аллергических заболеваний и включало общеклинические методы исследования и специфическое аллергологическое обследование (Р.М. Хаитов и др., 2009).
Во время первичной консультации проводились сбор и анализ анамнестических данных, объективный осмотр, изучались данные направительной документации, амбулаторных карт наблюдения по месту жительства.
Лабораторное обследование включало исследование общего анализа крови с подсчетом лейкоцитарной формулы, общего анализа мочи, биохимического анализа крови (функциональные пробы печени, уровень креатинина, мочевины, холестерина, белка, глюкозы), ревматологических проб, с целью определения уровня ревматоидного фактора, циркулирующих иммунных комплексов, С-реактивного белка, IgA, IgM, IgG, копроовоцистоскопия, а также исследование сыворотки крови больных на наличие маркеров RW, ВИЧ, HBsAg. Из инструментальных методов исследования обязательными являлись назначение ультразвукового исследования органов брюшной полости и проведение фиброгастродуоденоскопии. В случае выявления сопутствующей патологии больной направлялся на консультацию к смежным специалистам.
Специфическое аллергологическое обследование включало анализ данных аллергологического анамнеза, проведение кожных проб с бытовыми, эпидермальными, пыльцевыми аллергенами. Кроме того, при подозрении на наличие физической формы крапивницы проводились холодовая аппликационная проба, определение наличия уртикарного дермографизма, проба с физической нагрузкой при подозрении на наличие холинергической формы крапивницы. С целью определения аутоиммунной формы ХИК выполнялся внутрикожный тест с аутосывороткой. Также проводилось определение уровня общего IgE в сыворотке крови больных. С целью объективизации степени выраженности основных клинических симптомов ХК и оценки эффективности проводимой терапии был разработан индивидуальный дневник пациента, в котором фиксировались динамические изменения характерной симптоматики заболевания. Следует отметить, что пациентов распределяли на группы методом случайной выборки.
Критерии включения в исследование:
1) возраст старше 18 лет;
2) хроническое непрерывное течение крапивницы;
3) лечение антигистаминными и/или антилейкотриеновыми препаратами.
Критерии исключения из исследования:
1) крапивница с установленной причиной инфекционного, аллергического, лекарственного или физического характера;
2) гистологически подтвержденный уртикарный васкулит;
3) лечение глюкокортикостероидами, циклоспорином или метотрексатом в момент начала исследования или в течение последнего месяца перед исследованием;
4) беременность и лактация;
5) носительство вирусов гепатитов В и С;
6) психические заболевания, низкий уровень кооперации, склонность к антагонизму, нежелание участвовать в исследовании.
Все пациенты получали лечение: препарат Никсар
(биластин) в дозе 20 мг/сут (1-я группа,
n
=24) и в дозе 40 мг/сут (2-я группа,
n
=27). Длительность назначаемой медикаментозной терапии составляла 15 дней.
Эффективность лечения у пациентов с ХИК оценивали с использованием дерматологического индекса качества жизни (ДИКЖ) и шкалы для определения тяжести активности крапивницы UAS 7 (Urticarial Activity Score), которая позволяет пациенту провести суммарную оценку основных симптомов заболевания (количество высыпаний и интенсивность зуда). Оценка активности заболевания проводится каждые 24 ч в течение 15 последовательных дней (см. таблицу).
Оценка активности крапивницы Примечание. Оценка показателей: 0 — отсутствие зуда и высыпаний; 0—6 баллов — хорошо контролируемая крапивница; 7—15 баллов — легкая степень тяжести крапивницы; 16–27 баллов — крапивница средней степени тяжести; 28—42 балла — тяжелое течение крапивницы. Указанная шкала позволяет объективизировать оценку тяжести заболевания и динамики его течения, а также осуществить мониторинг лечения. Показатели UAS7 могут быть значимым критерием для обоснования смены терапии.
Физическое и психоэмоциональное состояние пациентов, а также комфортность лечения оценивали с помощью индекса качества жизни. Использовали стандартизированный опросник в форме оценки пациентами своего состояния, что имеет преимущества с точки зрения простоты и быстроты применения. ДИКЖ включал 10 вопросов, каждый из которых оценивался по 3-балльной системе (максимально возможный результат — 30 баллов). Опросник заполняется пациентами самостоятельно.
Результаты
При проведении исследовательской работы было получено информированное согласие пациентов об участии в данном научном проекте. В 1-й группе пациенты применяли препарат в суточной дозе 20 мг, во 2-й больные ХИК использовали Никсар
(биластин) в суточной дозе 40 мг. Увеличение дозы антигистаминного препарата II поколения проводилось в соответствии с федеральными клиническими рекомендациями по ведению больных крапивницей РОДВК (2015) у пациентов 2-й группы, в анамнезе которых была отмечена резистентность к ранее проводимой терапии.
Для объективной оценки терапевтической эффективности применения Никсара
(биластина) у пациентов с ХИК наблюдали динамику клинических проявлений крапивницы (количество морфологических элементов в течение суток) с помощью шкалы тяжести активности крапивницы UAS7, психоэмоциональное состояние пациентов, а также комфортность лечения оценивали с помощью ДИКЖ до лечения, на 5, 10- и 15-е сутки.
В ходе наблюдений за пациентами с ХИК были получены следующие результаты: изменения по шкале активности крапивницы (рис. 1)
Рис. 1. Изменение по шкале активности крапивницы UAS 7 при приеме Никсара в дозе 20 мг/сут (n=24) и 40 мг/сут (n=27). в группе с суточной дозой 20 мг составляли 30,4, 23,6, 15,2 и 9,4 балла (
р
<0,05) до лечения, на 5-, 10- и 15-е сутки соответственно; в группе с суточной дозой 40 мг данный показатель был зарегистрирован на уровне 31,1, 20,1, 12,1 и 3,6 балла (
р
<0,05) соответственно до лечения, на 5, 10 и 15-е сутки. В соответствии с полученными данными в группе с повышенной суточной дозой препарата
Никсар
(биластин) регистрировалось снижение баллов по шкале активности крапивницы UAS 7 (Urticarial Activity Score) на 61,8% в сравнении с 1-й группой, где препарат применялся в суточной дозе 20 мг.
При проведении анализа стандартизованных опросников ДИКЖ пациентов, участвующих в пострегистрационном клиническом исследовании, были получены следующие результаты (рис. 2):
Рис. 2. ДИКЖ при приеме Никсара в дозе 20 мг/сут (n=24) и 40 мг/сут (n=27). в 1-й группе на 5, 10 и 15-е сутки соответственно 18,3, 14,6, 8,4 и 5,3 (
р
<0,05), во 2-й — 19,1, 12,1, 4,2 и 2,3 (
р
<0,05). Согласно полученным данным, качество повседневной жизни в динамике изменялось более позитивно во 2-й группе, где суточная доза препарата
Никсар
(биласин) составляла 40 мг, что отражалось в более выраженном изменении индекса ДИКЖ на 46,6% в сравнении с 1-й группой.
Новый оригинальный антигистаминный препарат биластин в лечении аллергического ринита
Журнал «Медицинский совет. Оториноларингология» № 16 2017г.
А.А. Кривопалов
, к.м.н.,
О.И. Коноплев
, д.м.н., профессор,
С.В. Шервашидзе
,
В.А. Шаталов
Санкт-Петербургский научно-исследовательский институт уха, горла, носа и речи Минздрава России
Аллергический ринит – одно из наиболее широко распространенных заболеваний человека, связанное с серьезными ограничениями как в физических, психологических, так и в социальных аспектах жизни, являющееся причиной снижения качества жизни. Препаратами первого выбора у пациентов с симптомами сезонного и круглогодичного аллергического ринита как интермиттирующего, так и персистирующего течения являются антигистаминные препараты 2-го поколения, обладающие высоким сродством к Н1-рецепторам. В статье идет речь о новом представителе вышеуказанной группы лекарственных средств.
Ключ. слова:
аллергический ринит, риноконъюнктивит, антигистаминные препараты, биластин
А.А. Krivopalov, PhD in medicine, O.I. Konoplev, MD, Prof., S.V. Shervashidze, V.A. Shatalov Saint-Petersburg Scientific and Research Institute of Ear, Throat, Nose and Speech of the Ministry of Health of RF
NEW ORIGINAL ANTIHISTAMINE BILASTINE IN THE TREATMENT OF ALLERGIC RHINITIS Allergic rhinitis is one of most widespread human diseases associated with severe limitations in physical, psychological, and social aspects of life, which is the reason for the decline in quality of life. The drugs of first choice in patients with symptoms of seasonal and perennial allergic rhinitis of intermittent as well as of persistent courses are antihistamines of 2nd generation with high affinity to H1-receptors. The article is about a new representative of the above group of drugs, the original drug Niksar® (bilastine).
Keywords:
allergic rhinitis, rhinoconjunctivitis, antihistamines, bilastine
Загрузить этот файл PDF
Список литературы
1. Lucero ML, Gonzalo A, Mumford R, Betanzos M, Alejandro A. An overview of bilastine metabolism during preclinical investigations. Drug Chem Toxicol, 2012, 35(suppl l): 18-24. 2. Bousquet J, Khaltaev N, Cruz AA et al. Allergic Rhinitis and its impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organization, GA²LEN and AllerGen. Allergy, 2008, 63(Suppl. 86): 8-160. 3. Василевский И.В. Реабилитация детей и подростков с заболеваниями органов дыхания, пищеварения, почек, сердечно-сосудистой системы и аллергическими болезнями в условиях поликлиники. Минск: БелМАПО, 2007: 157-171. 4. Горячкина Л.А., Кашкин Е.П., Терехова Е.П. и соавт. Клиническая аллергология и иммунология: руководство для практикующих врачей. Под ред. Л.А. Горячкиной и Е.П. Кашкина. М.: Миклош, 2009: 121. 5. Graff C, Struijk JJ, Kanters JK, Andersen MP, Toft E, Tyl B. Effects ofbilastine on T-wave morphology and the QTc interval: a randomized, double-blind, placebo-controlled, thorough QTc study. Clin Drug Investig, 2012, 32: 339-351. 6. Feldberg W, Kellaway CH. Liberation of histamine and formation of lysocithin-like substances by cobra venom. J Physiol, 1988, 94:187-191. 7. Kellaway CH, Trethewie ER. The liberation of a slow-reacting smooth muscle-stimulating substance in anaphylaxis. Q J Exp Physiol, 1940, 30:121-145. 8. Brocklehurst W. The release of histamine and formation of a slow reacting substance (SRS-A) during anaphylactic shock. J Physiol, 1960, 151:416-435. 9. Sadaba B, Gomez-Guiu A, Azanza JR, Ortega I, Valiente R. Oral availability of bilastine. Clin Drug Investig, 2013, 33: 375-381. 10. Krause K, Spohr A, Zuberbier T, Church MK, Maurer M. Up-dosing with bilastine results in improved effectiveness in cold contact urticaria. Allergy, 2013, 68: 921-928. 11. Church MK. Safety and efficacy of bilastine: a new H1-antihistamine for the treatment of allergic rhinoconjunctivitis and urticaria. Expert Opin Drug Saf, 2011, 10(5): 779-793. 12. Corcostegui R, Labeaga L, Innerarity A, Berisa A, Oijales A. In vivo pharmacological characterisation of bilastine, a potent and selective histamine HI receptor antagonist. Drugs R D, 2006,7: 219-231. 13. Sastre J, Mullol J, Valero A, Bilastine Study Group. Efficacy and safety of bilastine 20 mg compared with cetirizine 10 mg and placebo in the treatment of perennial allergic rhinitis. Curr Med Res Opin, 2012, 28: 121-130. 14. Zuberbier T, Oanta A, Bogacka E. Bilastine International Working Group. Comparison of the efficacy and safety of bilastine 20 mg vslevocetirizine 5 mg forthe treatment of chronic idiopathic urticaria: a multi-centre, doubleblind, randomized, placebo-controlled study. Allergy, 2010, 65: 516-528. 15. Prepageran N, Wangde Y, Nair G, Maurer M. The status quo and unmet needs in the management of allergic rhinitis and chronic lhinosinusitis: a Malaysian perspective. Asia Рас Allergy, 2014, 4: 142-148. 16. Tashiro M, Sakurada Y, Iwabuchi K et al. Central effects of fexofenadine and cetirizine: measurement of psychomotor performance, subjective sleepiness, and brain histamineHI-receptor occupancy using 1 lC-doxepin positron emission tomography. JClinPharmacol,2004, 44: 890-900.