Введение
Ингибиторы натрий-глюкозного котранспортера 2 типа (ИНГТ2) продемонстрировали значимые кардиоваскулярные преимущества у пациентов с сахарным диабетом 2 типа (СД2) как с установленными сердечно-сосудистыми заболеваниями, так и с множественными факторами риска таковых [1–3]. Было выдвинуто несколько теорий, объясняющих положительное влияние ИНГТ2 на сердечно-сосудистые исходы. Так, в исследованиях получены данные по снижению преднагрузки на сердце вследствие усиления натрийуреза, улучшению метаболизма кардиомиоцитов, снижению выраженности фибротических и воспалительных процессов в миокарде и сосудистой стенке [4–6]. Однако данная тема продолжает оставаться предметом активного изучения.
Cахарный диабет 2 типа ассоциирован с развитием хронического воспаления вследствие действия различных механизмов. При этом показано, что ИНГТ2 могут снижать уровни некоторых цитокинов, таких как фактор некроза опухоли α, интерлейкин-6, высокочувствительный С-реактивный белок (вчСРБ) [7]. Кроме того, хорошо известно, что фибротические процессы в миокарде развиваются у пациентов с СД2 независимо от наличия артериальной гипертензии и выраженности коронарного атеросклероза [8]. В связи с этим изучение процессов фиброза и воспаления у пациентов с СД2 является актуальным.
Цель исследования:
оценить динамику уровня сывороточных маркеров, ассоциированных с процессами фиброза и воспаления при СД2, на фоне лечения дапаглифлозином.
Актуальность
У пациентов с хронической болезнью почек отмечается высокий риск развития неблагоприятных событий со стороны почек, сосудов и сердца.
До настоящего времени эффект дапаглифлозина у пациентов с хронической болезнью почек с или без сахарного диабета не был известен.
Материал и методы
Проведено одноцентровое проспективное исследование, одобренное этическим комитетом ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. До вступления в исследование все пациенты подписывали информированное согласие. Включали пациентов с СД2 длительностью более 1 года, уровнем гликированного гемоглобина от 7% до 10%, без верифицированной атеросклеротической болезни сердца и сосудов, но с множественными факторами риска сердечно-сосудистых событий (дислипидемией, ожирением, артериальной гипертензией). Кроме того, критериями включения были возраст от 40 до 65 лет, стабильная сахароснижающая, гиполипидемическая и антигипертензивная терапия как минимум в течение 12 нед. до включения в исследование. В исследование не включали пациентов с фибрилляцией предсердий, клапанными пороками сердца, ревматологическими заболеваниями, обострением хронических заболеваний, сахарным диабетом 1 типа, симптомами гипотензии и уровнем систолического артериального давления (САД) ниже 95 мм рт. ст., уровнем N-концевого пропептида натрийуретического гормона (NT-proBNP) >125 нг/мл, скоростью клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 и хронической болезнью почек, заболеваниями печени а также получающих инсулинотерапию, терапию глюкокортикостероидами, антагонистами минералокортикоидных рецепторов. Пациенты получали дапаглифлозин в дозе 10 мг/сут в течение 6 мес. в дополнение к базовой терапии СД2.
В ходе исследования проводили забор образцов крови до начала лечения дапаглифлозином и через 6 мес. лечения. Образцы крови забирали натощак (после 8 ч голодания), оценивали следующие показатели: гликированный гемоглобин (HbA1c), аланинаминотрансферазу, аспартатаминотрансферазу, креатинин, липидограмму (общий холестерин, липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП), триглицериды), NT-proBNP, вчСРБ, галектин-3, тканевой ингибитор матриксных металлопротеиназ-1 (TIMP-1), матриксную металлопротеиназу-9 (MMP-9), стимулирующий фактор роста, экспрессируемый геном 2 (ST2), карбокситерминальный фрагмент проколлагена I типа (PIСP). Уровень вчСРБ определяли на анализаторе Cobas Integra 400+ иммунотурбидиметрическим методом. Концентрацию NT-proBNP определяли электрохемилюминесцентным методом c применением тест-системы Elecsys (Roche Diagnostic). Оценку сывороточных уровней галектина-3 (R&D system), ММР-9 и TIMP-1 (R&D system), sST2 (Clinical diagnostics, Presage ST2 kit), PICP (USCN Life Science) проводили методом иммуноферментного анализа. Кроме того, в начале и в конце исследования оценивали массу тела, рост, окружность талии, уровень артериального давления (АД). С целью оценки нормальных значений биомаркеров фиброза в исследование дополнительно были включены 15 пациентов сходного возраста без СД2 и других хронических заболеваний, в том числе сердечно-сосудистых и заболеваний почек (группа контроля).
Для статистического анализа использовали программу SPSS Statistics. Количественные данные представлены в виде медианы и 25-го и 75-го квартилей — Me [Q25; Q75], качественные признаки — в виде абсолютного и относительного (%) показателей. Различия между количественными показателями выявляли с помощью критерия Вилкоксона. Корреляционный анализ проводили с использованием рангового коэффициента корреляции Спирмена. Нулевая гипотеза отвергалась при р<0,05.
В 2021г в NEJM были опубликованы результаты исследования DAPA-CKD, в котором оценивалось влияние дапаглифлозина на динамику почечной функции и риск смерти от сердечно-сосудистых заболеваний или патологии почек у пациентов с хронической болезнью почек. В рандомизированное плацебоконтролируемое исследование включались пациенты с расчетной скоростью клубочковой фильтрации 25- 75 мл/мин/1.73 м 2 и отношением альбумин/креатинин в моче 200-5000 мг/г. Наличие сахарного диабета не являлось обязательным критерием включения. Пациенты получали 10 мг дапаглифлозина или плацебо. Всего было включено 4304 пациента, медиана времени наблюдения составила 2,4 года. Исследование было прекращено досрочно вследствие очевидных преимуществ дапаглифлозина — у получающих данный препарат пациентов достоверно ниже оказалась частота первичной конечной точки «снижение СКФ на 50% и более/развитие терминальной ХБП/сердечно-сосудистая смерть/смерть от заболеваний почек»: 9,2% против 14,5%, ОШ 0.61; 95% ДИ 0.51 — 0.72; P<0.001; для предотвращения одного неблагоприятного события следует пролечить 19 пациентов). Применение дапаглифлозина ассоциировалось с достоверным снижением смертности от всех причин (4.7% против 6.8%, ОШ 0.69; 95% ДИ 0.53 — 0.88; P=0.004). Также дапаглифлозин снижал частоту комбинированной конечной точки «смерть от ССЗ/госпитализация в связи с декомпенсацией ХСН». Эффект дапаглифлозина не зависел от наличия сопутствующего сахарного диабета. Профиль безопасности препарата соответствовал ранее имеющимся данным.
30 апреля 2021г FDA опубликовало пресс-релиз об одобрении применения препарата Форсига (дапаглифлозин) у пациентов с хронической болезнью почек. Помимо перечисления преимуществ применения препарата у пациентов с ХБП, авторы документа напоминают об определенных ограничениях применения Форсиги по данным показаниям: препарат никогда не испытывался (и не ожидается его эффективность) у пациентов с поликистозом почек (как с аутосомно-доминантной, так и с рецессивной формой наследования), а также у пациентов, получающих или нуждающихся у иммуносупрессивной терапии по поводу почечной патологии. Также в документе перечисляются клинически значимые побочные эффекты препарата: жизнеугрожающие случаи гангрены Фурнье, дегидратация, урогенитальная инфекция, метаболический ацидоз или кетоацидоз.
1) Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2021 Oct 8;383(15):1436-1446. doi: 10.1056/NEJMoa2024816. Epub 2020 Sep 24. PMID: 32970396.
2) Пресс-релиз «FDA Approves Treatment for Chronic Kidney Disease» от 30.04.21.
https://www.fda.gov/
Результаты исследования
В исследование включено 27 пациентов (возраст 56 [49; 61] лет), у большинства из которых были СД2 длительностью более 4 лет (7 [4; 12] лет) и ожирение I степени. Базовая сахароснижающая терапия включала комбинацию метформина с препаратами сульфонилмочевины или ингибиторами дипептидилпептидазы 4 типа (иДПП-4).
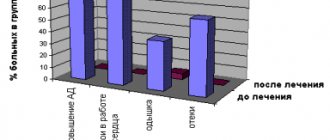
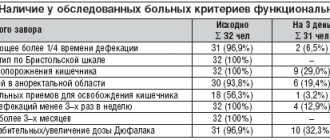
Основная характеристика пациентов и динамика изучаемых маркеров фиброза и воспаления представлена в таблице 1. За 6 мес. лечения дапаглифлозином наблюдалось значимое снижение уровня HbA1c с 8,2 [7,6; 8,8]% до 7,8 [7,2; 8,1]% (р=0,001), снижение ИМТ и уменьшение окружности талии. За время наблюдения не отмечено значимых изменений содержания липопротеинов и триглицеридов, СКФ и АД.
Содержание вчСРБ и NT-proBNP не отличалось от нормальных значений и не претерпело статистически значимых изменений по прошествии 6 мес. лечения дапаглифлозином. Исходно пациенты имели значимо бóльшие концентрации галектина-3, PICP и MMP-9 по сравнению с группой контроля (p=0,017, p=0,006 и p=0,008 соответственно). При оценке динамики содержания галектина-3, MMP-9, TIMP-1, ST2 не было получено значимых различий с исходными значениями (см. табл. 1). В то же время через 6 мес. лечения дапаглифлозином наблюдалось статистически значимое снижение концентрации PICP с 136,8 [100,4; 200,6] нг/мл до 104,8 [79,7; 162,0] нг/мл (р=0,019) и повышение концентрации TIMP-1 с 188 [138; 270] нг/мл до 234 [205; 315] нг/мл (р=0,011).
Обсуждение
Преобладание синтеза коллагена I типа над его деградацией приводит к накоплению в миокарде избытка волокон коллагена и указывает на процесс фиброза, который происходит в интерстициальном и периваскулярном пространстве, в том числе при диабетической кардиомиопатии [9]. Уровни PICP, который является маркером образования и деградации коллагена I типа, надежно коррелируют с объемом образующегося коллагена как у пациентов с хронической сердечной недостаточностью (ХСН), так и без таковой [9].
В исследованиях показано, что концентрации PICP выше у пациентов с СД2, чем у пациентов без СД2 [10]. Сходные различия были продемонстрированы и в нашем исследовании. Терапия дапаглифлозином в течение 6 мес. приводила к значимому снижению уровня P1CP по сравнению с исходным. Сходная динамика была получена в исследовании другого ИНГТ2 у пациентов с СД2 и очень высоким риском сердечно-сосудистых событий [11].
В нашем исследовании не установлено значимого снижения концентраций NT-proBNP на фоне лечения дапаглифлозином в течение 6 мес., что можно объяснить включенной в исследование популяцией пациентов без ХСН и без высоких концентраций NT-proBNP. Поскольку NT-proBNP является маркером ХСН и его уровень коррелирует с ее тяжестью, даже в исследованиях пациентов с СД2 и ХСН с сохранной фракцией выброса не было выявлено значимого снижения концентрации NT-proBNP [12]. Тем не менее исследование DAPA-HF продемонстрировало, что риск ухудшения течения ХСН или смерти от сердечно-сосудистых заболеваний был ниже в группе дапаглифлозина, чем в группе плацебо [13]. Таким образом, несмотря на ограниченное влияние на уровень NT-proBNP, ИНГТ2 улучшают клинические исходы у пациентов с ХСН, что говорит о несоответствии между краткосрочными изменениями уровней NT-proBNP и клиническими исходами.
Концентрации ST2, вчСРБ, MMP-9 и ее ингибитора TIMP-1 значимо не изменились на фоне терапии дапаглифлозином, что согласуется с данными других исследований [11, 14, 15]. Вероятно, отсутствие значимой динамики показателей ряда маркеров в ходе нашего исследования связано с тем, что пациенты без ХСН и сердечно-сосудистых событий находятся на том этапе сердечно-сосудистого континуума, когда концентрации маркеров не могут в полной мере отражать тяжесть и прогноз у данных пациентов, а их изменения не могут быть зафиксированы за 6-месячный период наблюдения. Кроме того, отсутствие отрицательной динамики содержания данных биомаркеров может говорить о замедлении воспалительных и фиброзных процессов, имеющих место при СД2, и потенциально реализовываться в улучшении сердечно-сосудистых исходов. Также стоит принимать во внимание наличие ожирения и других неучтенных факторов, которые могут влиять на значения оцениваемых нами маркеров.