Показания к применению
- Хирургия: вводный наркоз, премедикация, потенцирование общей и регионарной анестезии; нейролептанальгезия (одновременно с фентанилом); обеспечение седативного эффекта, устранение рвоты и боли в послеоперационном периоде, рвоты и тошноты во время хирургических и диагностических манипуляций;
- Терапия: шок и боль при травмах, тяжелые приступы стенокардии, инфаркт миокарда, гипертонический криз, отек легких;
- Психиатрическая практика: галлюцинации, психомоторное возбуждение.
Противопоказания
- Кома;
- Экстрапирамидные нарушения;
- Увеличение интервала QT на ЭКГ;
- Тяжелая депрессия;
- Гипокалиемия;
- Кесарево сечение;
- Артериальная гипотензия;
- Возраст до 2 лет;
- Гиперчувствительность к компонентам препарата и производным морфина.
Применение Дроперидола беременными женщинами возможно только в случаях, когда предполагаемая польза для здоровья матери выше потенциального риска для плода. В случае необходимости применения препарата женщинами во время лактации грудное вскармливание необходимо прекратить.
Удлиненный интервал QT , TdP и LQTS
Удлинение интервала QT является значительной проблемой безопасности пациента. Интервал QT означает время от деполяризации желудочков до конца реполяризации желудочков [8]. Интервал QT часто исправляется на частоту корректированного интервала QT (интервал QTc ) посредством математической формулы, известной как формула Bazett ( QTc = QT / v интервал R — R ). Расчет интервала QTc принимает в расчет такие переменные как возраст, частота сердечных сокращений и пол [9]. Согласно Moss «современные исследования обеспечивают усовершенствованное определение удлинения QTc и оценку, что риск злокачественных желудочковых аритмий экспоненциально связан с длиной интервала QTc » [8]. Однако Viskin считает, что действительный интервал QT является лучшим прогностическим критерием аритмогенного поражения перед интервалом QTc , когда имеет место выраженная брадикардия [10]. Удлиненный интервал QT более чем 0,44 сек считается патологическим, и является одним из основных компонентов, который приводит к развитию TdP [9]. Удлиненный интервал QTc на стандартной ЭКГ часто связан со злокачественной желудочковой дисритмией, приводящей к обморокам или к смерти. Удлинение QTc является только одним из многих факторов риска по развитию TdP и удлинение часто не является впечатляюще длинным. Пациент с удлиненным интервалом в сочетании с метаболическими нарушениями, с дисфункцией левого желудочка и мерцанием предсердий имеет повышенный риск развития злокачественной желудочковой дисритмии [11]. Точный механизм развития TdP неясен . Однако, есть доказательства, что начало TdP может быть связано с несколькими механизмами.
TdP — это жизне-угрожающая желудочковая тахикардия, которая часто связана с удлиненным интервалом QTc , гипокалиемией, гипомагниемией и препаратами, которые как известно удлиняют интервал QTc [12]. Другие факторы риска включают брадикардию, женский пол, застойную сердечную недостаточность, врожденный LQTS и изменения морфологии T -волны [10]. TdP имеет место, если ? 6 последовательных ударов полиморфных желудочковых дисритмий происходит [13], и частота составляет от 150 до 250 ударов в минуту [14]. TdP часто выявляется по паузе, которая предшествует дисритмии и по волне комплекса QRS вокруг оси [10]. Другой характерный признак, который часто сопровождает TdP – это изменение морфологии T -волны и развитие U -волны при ударах только до дисритмии [13].
LQTS – это врожденный синдром, связанный с TdP , который характеризуется длинным интервалом QT у больных со структурно нормальным сердцем [15]. LQTS может быть классифицирован как приобретённая и наследственная формы, обе связаны с TdP . TdP часто разрешается самостоятельно, вызывая умеренные пресинкопальные симптомы. Однако, TdP может иногда ухудшаться до фибрилляции желудочков и, следовательно, является потенциально фатальным. TdP не всегда предшествует удлиненный интервал QT. На самом деле, должны быть исключены такие источники как брадикардия, гипокалиемия и гипоксия [14]. Продольное исследование, включающее 3343 индивидуума, где один или более членов семьи, как было выявлено, страдают LQTS , нашло значительное соотношение к смерти, если определялся QTc , анамнез сердечного приступа или частота сердечных сокращений [15].
При LQTS нарушение работы ионных каналов клеточной мембраны миоцитов приводит к избытку положительных ионов, удлиняя интервал QT . Факторы риска смерти при LQTS включают симптомы в младенчестве, глухота, анамнез остановки сердца и отсутствие или недостаток терапии ?-блокаторами [10]. Терапия ?-блокаторами традиционно используется как терапия первой линии при LQTS .
Лечение TdP является критическим . TdP , как известно, прогрессирует до фибрилляции желудочков [14]. Снижение доставки кислорода к миокарду следует за развитием TdP . Фибрилляция желудочков может происходить в результате снижения доставки кислорода. Снижение кровотока вызывает острые ишемические нарушения в миокарде, приводя к механической, электрической и химической дезинтеграции клеток сердца. Остановка сердца может произойти быстро. Если TdP остается непролеченной, может произойти длительное повреждение органа и смерть [16].
Лечение TdP включает дефибрилляцию, внутривенное введение магнезии и возможно инфузию лидокаина [10]. Лечение метаболических таких нарушений как гипокалиемия и гипомагниемия имеет основное значение. Отмена препаратов, которые имеют продисритмические свойства, должна быть проведена немедленно [17]. Желудочковые дисритмии связаны с внезапной смертью в более чем 80% случаев. Раннее выявление и лечение дисритмии является критическим для выживания больного [16].
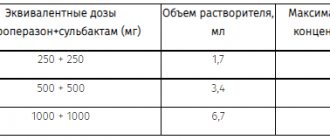
Способ применения и дозировка
Дозу Дроперидола определяют индивидуально, учитывая характер заболевания, возраст, общее физическое состояние, массу тела, применяемые одновременно препараты, вид предстоящей анестезии.
Взрослым для премедикации за 15-45 минут до начала хирургического вмешательства внутримышечно вводят 2,5-5 мг Дроперидола, детям – из расчета 100 мкг/кг.
Взрослым для введения в анестезию препарат назначают в дозе 15-20 мг (внутривенно). Детям возможно внутривенное (в дозе 200-400 мкг/кг) или внутримышечное (в дозе 300-600 мкг/кг) введение.
Для поддержания анестезии при длительных операциях возможно повторное внутривенное введение Дроперидола в дозе 2,5-5 мг.
В послеоперационный период взрослым каждые 6 часов назначают внутримышечно по 2,5-5 мг.
Ссылки
- United States Food and Drug Administration. Inapsine dear doc letter, December 4, 2001. Available at: https:// www.fda.gov/medwatch/safety/2001/inapsine.htm . Accessed March 07, 2002.
- Young D. FDA advisory panel discusses droperidol concerns. Am J Health Syst Pharm. 2004; 61: 219-222.
- American Regent Laboratories, Inc. Droperidol Injection, USP product insert. Reference number IN9702. Revised 1/02.
- Drolet B., Zhang S., Deschenes D., et al. Droperidol lengthens cardiac repolarization due to block of the rapid component of the delayed rectifier potassium current. J Cardiovasc Electrophysiol. 1999; 10: 1597-1604.
- Kao L.W., Kirk M.A., Evers S.J., et al. Droperidol, QT prolongation, and sudden death: What is the evidence? Ann Emerg teed. 2003; 41: 546-558.
- Pandit S.K., Kothary S.P., Pandit U.A., et al. Dose-response study of droperidol and metoclopramide as antiemetics for outpatient anesthesia. Anesth Analg. 1999; 68: 789-802.
- Caldwell M.A. Pharmacology of intravenous agents. In: LW, ed. McIntosh Essentials of Nurse Anesthesia. St Louis: McGraw-Hill; 1997: 61.
- Moss A. QTc interval prolongation: is it beneficial or harmful? Am J Cardiol. 1993; 72: 23B-25B.
- Lischke V., Bhene M., Doelken P., et al. Droperidol causes a dose-dependent prolongation of the QT interval. Anesth Analg. 1994; 79: 983-986.
- Viskin S. Long QT syndromes and torsades de pointes. Lancet. 1999; 354: 1625-1633.
- Morganroth J. QTc interval prolongation: Is it beneficial or harmful? Am J Cardiol. 1993; 72: 1B-3 В .
- Faigel D.O., Metz D.C., Kochman M.L. Torsades de pointes complicating the treatment of bleeding esophageal varices: Association with neuroleptics, vasopressin, and electrolyte imbalance. Am J Gastroenterol. 1995; 90: 822-824.
- Gbadebo T.D., Trimble R.W., Khoo M.S.C., et al. Calmodulin inhibitor ?-7 unmasks a novel electrocardiographic parameter that predicts initiation of torsades de pointes. Circulation. 2002; 105: 770-774.
- Tan H.L., Hou C.J.Y., Lauer M.R., et al. Electrophysiologic mechanisms of the long QT interval syndromes and torsades de pointes. Ann Intern Med. 1995; 122: 701-714.
- Moss A., Schwartz P.J., Crampton R.S., et al. The long QT syndrome prospective longitudinal study of 328 families. Circulation. 1991; 84: 1136-1144.
- Holmberg S., Chamberlain D.A. Cardiac arrest and cardiopulmonary resuscitation. In: Julian D.G., Camm A.J., Fox K.A., eds. Diseases of the Heart. Philadelphia: Saunders; 1996: 1459-1481.
- White R.D. Cardiopulmonary resuscitation: Basic and advanced cardiac life support. In: Miller R.D., ed. Anesthesia. Philadelphia: Churchill-Livingstone; 2000: 2533-2559.
- Buckley N.A., Sanders P. Cardiovascular adverse effects of antipsychotic drugs. Drug safety. 2000; 23: 215-228.
- Lawrence K.R., Nasraway S.A. Conduction disturbances associated with administration of butyrophenone antipsychotics in the critically ill: A review of the literature. Pharmacotherapy. 1997; 17: 531-537.
- Reilly J.G., Ayis S.A., Ferrier I.N., et al. QTc-interval abnormalities and psychotropic drug therapy in psychiatric patients. Lancet. 2000; 355: 1048-1052.
- White P.F., Song D., Abrao J., et al. Effect of low-dose droperidol on the QT interval during and after general anesthesia. Anesthesiology. 2005; 102: 1101-1105.
- Charbit B., Albaladejo P., Funck-Brentano C., et al. Prolon gation of QTc interval after postoperative nausea and vomiting treatment by droperidol or ondansetron. Anesthesiology. 2005; 102: 1094-1100.
- Horowitz B.Z., Bizwi K., Moreno R. Droperidol-behind the black box warning. Acad Emerg Med. 2002; 9: 615-618.
- University of Arizona Center for Education and Research on Therapeutics. Drugs to be avoided by congenital long QT patients. Available at: https://www.torsades.org/ . Accessed March 15, 2005.
Побочные действия
При применении Дроперидола возможно развитие нарушений со стороны некоторых систем организма:
- Центральная нервная система: сонливость, дисфория в послеоперационном периоде и, напротив, при применении повышенных доз – страх, моторная возбудимость, беспокойство; редко – экстрапирамидные симптомы; в отдельных случаях в послеоперационном периоде – депрессия, галлюцинации;
- Сердечно-сосудистая система: тахикардия и умеренная артериальная гипотензия (обычно специальная терапия не требуется); в очень редких случаях – артериальная гипертензия (наиболее вероятно – при комбинированном применении с фентанилом или другими вводимыми парентерально анальгетиками);
- Пищеварительная система: диспепсические явления, потеря аппетита, тошнота; редко – транзиторные нарушения функции печени, желтуха;
- Аллергические реакции: редко – головокружение, анафилактические реакции, дрожь, бронхоспазм, ларингоспазм.
Глубокоуважаемый Константин Михайлович!
Множество наших коллег по всей России и Вы, разумеется, знают о совершенно нетерпимой, нелепой ситуации, сложившейся много лет назад с легальной возможностью (вернее, невозможностью) использования фентанила при применении эпидуральной аналгезии/анестезии.
Как известно, фентанил был синтезирован в Бельгии в 1959 г. Paul Janssen для использования в качестве компонента нового метода анестезии, получившего название нейролептаналгезии — НЛА (De Castro и Mundeleer, 1959). Согласно идее НЛА, для ее клинической реализации было необходимо располагать мощным и короткодействующим анальгетиком. Так появился фентанил. В СССР фентанил был синтезирован в 60-х годах прошлого века Эдвардсом Лавриновичсом в лаборатории Академии наук Латвийской ССР, а фасовку препарата наладили на литовском . В отечественную медицинскую практику фентанил был введен приказом Минздрава СССР от 13 декабря 1972 г. После распада СССР снабжать фентанилом российские лечебные учреждения стал ФГУП «Московский эндокринный завод», что он делает и по сей день (последнее переоформление регистрационного удостоверения 12.12.19). Кроме него, право производить фентанил есть еще и у ФГУП «Государственный завод медицинских препаратов» (последнее переоформление регистрационного удостоверения 23.11.17).
Как Вам, да и всем российским коллегам хорошо известно, в инструкции к препарату фентанил, созданной на основе этих регистрационных удостоверений, сказано, что фентанил предназначен для внутривенного и внутримышечного введения. Эпидуральное введение не предусмотрено. Мотивы и авторы такого ограничения неизвестны.
Зато морфин разрешен к введению в эпидуральное и субарахноидальное пространство еще с советских времен. Кстати, с удивлением обнаружил, что в инструкции к промедолу (тримеперидину) еще относительно недавно существовавшее разрешение вводить в эпидуральное пространство таинственным образом исчезло. Ну да бог с ним, с промедолом, а вот отсутствие в инструкции к фентанилу указания на возможность эпидурального введения — прямой и значительный вред и неоправданные мучения массы наших сограждан, столкнувшихся с несчастьем подвергнуться травматичным хирургическим вмешательствам, особенно в грудной и брюшной полости.
Неплохо зная литературу на затронутую тему, не смогу назвать страну, кроме России, где фентанил не был бы разрешен для рутинного эпидурального применения, включая Белоруссию, Украину и Казахстан. ESRA (Европейское общество регионарной анестезии) и ASRA (Американское общество регионарной анестезии), NYSORA (Нью-Йоркское общество регионарной анестезии), известное на весь мир знаменитыми обучающими программами, наряду с руководствами по анестезиологии мирового масштаба (возьмем хотя бы Миллера и Моргана), «нам», разумеется, не указ. И наплевать, что замечательная, а порой единственно эффективная методика анестезиологической защиты становится значительно более мощной и безопасной при сочетании местного анестетика и фентанила, совместно введенных в эпидуральное пространство. Хорошо известно, что один только местный анестетик зачастую не дает достаточного обезболивающего эффекта, а наращивание его концентрации приводит только к трудно контролируемой артериальной гипотензии. Это особенно значимо и чувствительно при операциях, сопряженных с риском большой кровопотери, при однолегочной вентиляции, и, разумеется, в послеоперационном периоде.
Я берусь говорить об этом уверенно, располагая не только «книжными» знаниями, но и собственным опытом более 50 000 эпидуральных аналгезий в «трехкомпонентном» варианте, в котором мы сочетали малые дозы фентанила и адреналина с низкоконцентрированным местным анестетиком, как правило, 0,2% ропивакаином. Это слегка модифицированный нами высокоэффективный вариант, предложенный норвежскими анестезиологами H. Breivik и G. Niemi в 1998 г., и получивший большую популярность преимущественно в Северной Европе. Этой усовершенствованной методике предшествовал, начиная с конца 1993 г., опыт >10 000 эпидуральных аналгезий комбинацией местного анестетика и фентанила (без адреналина). Первоначально мы делали это под мощным прикрытием нашего бывшего директора и многолетнего президента Академии медицинских наук акад. М.И. Давыдова. Затем, воспользовавшись внезапно появившейся возможностью зарегистрировать методику в Росздравнадзоре в виде «новой медицинской технологии» под номером ФС №2010/339 от 15 сентября 2010 г., мы получили легальное основание вводить фентанил в эпидуральное пространство, тем более, что наш директор вскоре издал приказ по Онкологическому научному центру, предписывающий использовать методику при наличии перечисленных в приказе показаний. Относительно недавно стало известно, что Минздрав де-факто практически дезавуировал разрешения Росздравнадзора на применение «новых медицинских технологий», упразднив саму эту форму, правда, с оговоркой, что выданные разрешения вроде бы продолжают действовать и при соблюдении некоторых формальностей ими могут воспользоваться коллеги из других лечебных учреждений (бесплатно!) [Н.Г. Куракова, Т.Н. Эриванцева. Регистрация или патентование новых медицинских технологий: методология выбора. Медицинские технологии, оценка и выбор. 2011. №3 с. 49-53].
На самом деле это нельзя считать нормальным решением давно назревшей важной клинической (и юридической) проблемы. Со всей очевидностью радикальное и законное ее решение может быть только одно — внесение в регистрационные документы и соответственно в инструкцию по применению препарата «фентанил» еще одного показания и пути введения «в эпидуральное пространство» либо «для эпидурального обезболивания». Изменить регистрационные документы могут только производители препарата, а вот убедить их это сделать — кто еще, если не Общероссийская общественная организация «Федерация анестезиологов и реаниматологов»?
С моей точки зрения, эта задача и клиническая, и юридическая, и морально-этическая по отношению к нашим пациентам и коллегам. Ведь ни для кого не секрет, что на сегодняшний день эпидуральную аналгезию/анестезию освоили абсолютное большинство анестезиологов-реаниматологов. При этом часть из них вводят только местный анестетик, чего нередко недостаточно, либо идут на «хитрость» — вводят фентанил в эпидуральное пространство, а в протоколе записывают «внутривенно». С какой стати они рискуют собой, понимая благо своих пациентов? Давайте защитим наших пациентов и коллег!
С глубоким уважением и надеждой на успех, при полном отсутствии личной заинтересованности,
Е.С. Горобец
Доктор медицинских наук, профессор, Главный научный консультант отдела анестезиологии и реаниматологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» МЗ РФ
Дорогой Евгений Соломонович, дорогие друзья и коллеги!
Тема, которую поднял в своем письме профессор Горобец, действительно требует внимания со стороны нашей Федерации. Мы хорошо знаем, как много таких случаев: всем известно, что тот или иной препарат широко применяется, производится и продается повсюду в мире, повседневно необходим анестезиологам и интенсивистам в их рутинной практике — но в нашей стране по тем или иным причинам у него или нет регистрации, или он зарегистрирован, но не по тому показанию, или для введения не тем путем и т.д. Даже перечислять снова не хочется — начиная с дантролена (который, наконец, вроде бы будет зарегистрирован! — не сглазить бы…) и антидигоксина и заканчивая конакионом и ингибиторами фосфодиэстеразы третьего типа. При этом, само собой, гораздо более дорогие и оттого более интересные в коммерческом плане препараты куда меньшей значимости регистрируются весьма оперативно — за примерами тоже далеко ходить не надо. Что же делать, если по закону инициатором регистрации и внесения в нее любых последующих изменений может стать только будущий выгодоприобретатель?
Да, нам нужна возможность легитимного введения фентанила в эпидуральное пространство (почему так говорю — тоже всем понятно). Вопрос в том, чтобы Федерация выработала механизм, побуждающий руководство компаний — поставщиков и производителей, прежде всего, отечественных — выступать инициаторами таких регистраций и изменений, которые настоятельно нужны врачам. Как это сделать не в разовом порядке, а поставить на методическую основу? — я пока не знаю. Но среди важнейших стратегических задач ФАР на ближайшие годы эта тема — создание системного механизма профессионального влияния на оснащение рабочего места обычного анестезиолога-реаниматолога! — должна занять свое место. А пока давайте попросим Комитет по лечению боли — профессора Алексея Михайловича Овечкина вместе с Евгением Соломоновичем подготовить обоснование такой просьбы со стороны ФАР от имени нашего профессионального сообщества.
С признательностью за далеко идущую инициативу,
ваш К. Лебединский
Любопытно, что в этом приказе препарат упомянут как «фентанил (таламонал)». На самом деле, «таламонал» — это готовая лекарственная форма, содержавшая 50 мкг фентанила и 2,5 мг дроперидола в 1 мл, и выпускавшаяся бельгийской во флаконах по 10 мл для НЛА. Вряд ли авторы приказа не знали, что фентанил и таламонал — не одно и то же. По-видимому, они были сосредоточены на регламентации использования фентанила как наркотического анальгетика, подлежащего строгому учету. Эта неточность косвенно указывает на то, что во времена создания и внедрения фентанила в клиническую практику, скорее всего, никому и в голову не приходила возможность использования фентанила по другому медицинскому назначению, например для введения в эпидуральное пространство. Но это было полвека назад!
Особые указания
Дроперидол следует применять только в стационарных условиях.
Препарат нужно назначать с осторожностью больным с функциональными нарушениями почек и печени, депрессией, эпилепсией, а также при состояниях, предшествующих эпилептическому припадку.
При феохромоцитоме после введения Дроперидола может развиться тахикардия и тяжелая артериальная гипертензия.
Во время терапии нужно предвидеть возможность развития выраженной артериальной гипотензии. Также препарат может вызвать понижение давления в легочной артерии, что необходимо учитывать во время проведения диагностических и хирургических процедур. Получающим Дроперидол больным нужен тщательный врачебный контроль.
Начальную дозу препарата следует уменьшать пациентам пожилого возраста, истощенным и физически ослабленным больным. При увеличении дозы нужно руководствоваться полученным эффектом.
Дроперидол необходимо назначать в меньшей дозе при одновременном применении с лекарственными средствами, оказывающими угнетающее влияние на центральную нервную систему. Соответственно, после Дроперидола дозы таких препаратов также снижают.
Применение Дроперидола в повышенных дозах (25 мг и более) может привести к внезапной смерти больных с нарушениями сердечного ритма на фоне алкогольной абстиненции, гипоксии или нарушений электролитного баланса.
В хирургической практике при применении препарата нужно тщательно контролировать параметры физиологического состояния организма. При проведении перидуральной или спинальной анестезии возможно развитие блокады симпатической нервной системы и межреберных нервов, что, в свою очередь, может привести к затруднению дыхания, развитию артериальной гипотензии и расширению периферических сосудов.
Чтобы избежать возникновения ортостатической гипотензии рекомендуется соблюдать осторожность при транспортировке больного, избегать резкой перемены положения тела.
На фоне действия Дроперидола и в течение 24 часов после его применения необходимо избегать выполнения потенциально опасных работ, требующих быстрых психомоторных реакций и высокой концентрации внимания.
Лекарственное взаимодействие
При одновременном применении Дроперидола с некоторыми лекарственными средствами могут возникать нежелательные эффекты:
- Препараты, оказывающие угнетающее влияние на центральную нервную систему (производные бензодиазепина, средства для наркоза, опиоидные анальгетики, снотворные средства): усиление угнетающего влияния на центральную нервную систему;
- Антигипертензивные препараты: потенцирование их действия;
- Эпинефрин и другие адрено- и симпатомиметические средства: проявление в их отношении антагонизма;
- Агонисты допамина, включая бромокриптин, лизурид и леводопу: ингибирование их действия.