Что такое иммунотерапия рака?
Иммунотерапия — это совокупность методов лечения, которые направлены на то, чтобы активировать иммунную систему и заставить ее уничтожать опухолевые клетки. Бурное развитие этого направления в последние годы происходит благодаря достижениям молекулярной генетики, генной инженерии. Многие исследователи и врачи возлагают на иммунотерапию большие надежды. Зачастую она помогает продлить жизнь пациентов с запущенным раком, которым не помогают классические химиопрепараты.
В настоящее время в онкологии применяют разные виды иммунотерапии: противораковые вакцины, перепрограммированные T-лимфоциты, цитокины, онколитические вирусы.
Отдельную группу составляют ингибиторы контрольных точек, которые можно одновременно отнести к иммунопрепаратам и таргетным препаратам. Каждый из этих препаратов имеет определенную мишень — молекулу (контрольную точку), которая подавляет работу иммунной системы и мешает ей атаковать опухоль.
В корме контрольные точки нужны для того, чтобы иммунитет мог сдерживать себя и не атаковать здоровые ткани. Это предотвращает аутоиммунные заболевания. Раковые клетки могут использовать контрольные точки для защиты.
Какую контрольную точку блокирует опдиво?
Раковые клетки вырабатывают опухолевые антигены — вещества, которые иммунная система распознает как чужеродные. Для того чтобы иммунные клетки — T-лимфоциты — начали атаковать опухолевую ткань, они должны «познакомиться» с ее антигенами. В результате такого «знакомства» лимфоцит активируется, размножается, и его многочисленные клоны отправляются на поиски раковых клеток.
Однако, на поверхности T-лимфоцитов есть особые белки-рецепторы — PD-1. Опухолевые клетки могут выставлять на своей поверхности белок-лиганд этого рецептора — PD-L1. PD-1 и PD-L1 подходят друг к другу, как ключик к замочку. В итоге T-лимфоцит не может активироваться и не атакует опухоль.
Ниволумаб блокирует белок PD-1, в итоге T-лимфоцит больше не получает отрицательного сигнала. Он снова способен активироваться и уничтожать раковые клетки.
При каких онкологических заболеваниях применяют опдиво?
В настоящее время доказано, что опдиво может принести пользу при ряде онкологических заболеваний. Его применяют отдельно или в сочетании с другими противоопухолевыми препаратами.
Меланома. Ниволумаб часто применяют при меланоме на поздних стадиях, нередко его назначают в комбинации с другим ингибитором контрольных точек — ервоем (ипилимумабом). Показания к применению препарата:
- Меланома, которая не может быть удалена хирургическим путем, либо имеет метастазы.
- Меланома, которая была удалена хирургическим путем, но успела дать метастазы.
- Для предотвращения рецидива после того, как была удалена меланома и пораженные раковыми клетками лимфатические узлы.
Немелкоклеточный рак легкого. Опдиво применяют, если опухоль сопровождается метастазами, и если не помогает химиотерапия препаратами платины (на фоне лечения опухоль растет, состояние пациента ухудшается). Если в раковых клетках выявлены определенные мутации, лечение начинают соответствующими таргетными препаратами, если они не помогают — назначают ниволумаб.
Рак почки. Опдиво назначают при злокачественных опухолях почек на поздних стадиях, когда не помогают другие препараты.
Рак мочевого пузыря. Препарат применяют при уротелиальной карциноме, локальной или с метастазами, если опухоль растет на фоне терапии химиопрепаратами на основе платины.
Рак головы и шеи. Ниволумаб может быть эффективен при плоскоклеточном раке, который рецидивировал или метастазировал, если неэффективны химиопрепараты.
Рак печени. Препарат применяют при гепатоцеллюлярной карциноме, утратившей чувствительность к сорафенибу.
Колоректальный рак. Опдиво может помочь взрослым и детям старше 12 лет, страдающим раком толстой и прямой кишки, который метастазировал и не реагирует на препараты: фторпиримидин, оксалиплатин, иринотекан.
Лимфома Ходжкина. Препарат может помочь, если опухоль прогрессирует или рецидивировала после:
- аутологичной трансплантации стволовых клеток и лечения препаратом брентуксимаб ведотин;
- применения, как минимум, трех видов лечения, включая аутологичную трансплантацию стволовых клеток.
В настоящее время продолжаются исследования эффективности препарата опдиво при различных онкологических заболеваниях.
Ниволумаб во второй линии терапии немелкоклеточного рака легкого
Немелкоклеточный рак легкого (НМРЛ) остается ведущей причиной смерти от онкологических заболеваний в мире. Новое перспективное направление лечения пациентов с НМРЛ связано с использованием ингибиторов точек иммунного контроля, в частности препаратов, подавляющих активность пути PD-1. Эти препараты демонстрируют выраженную эффективность при различных гистологических подтипах диссеминированного НМРЛ, прогрессирующего на фоне предшествующей платиносодержащей химиотерапии. В статье рассмотрен клинический случай успешного применения ниволумаба во второй линии терапии при метастатической аденокарциноме легкого.
Введение
Рак легкого является наиболее часто диагностируемым злокачественным новообразованием в мире [1]. В Российской Федерации рак легкого в структуре заболеваемости злокачественными новообразованиями среди мужского населения и смертности у мужчин и женщин занимает лидирующие позиции – 17,6 и 17,4% соответственно. На немелкоклеточный рак легкого (НМРЛ) приходится 80–85% всех форм рака легкого, при этом к моменту установления диагноза почти в 70% случаев имеет место распространенная форма заболевания [2]. В связи с этим поиск эффективных методов лечения местнораспространенных и метастатических форм НМРЛ остается одной из основных проблем онкологии.
Современные стандарты лекарственной терапии больных НМРЛ, за исключением пациентов с драйверными мутациями, достаточно ограничены. Так, в первой линии применяются платиносодержащие препараты как в монорежиме, так и в комбинации. Эти препараты характеризуются сопоставимой эффективностью в отношении частоты общего ответа от 30 до 60%. Медиана выживаемости в группе платиносодержащих режимов составляет 8–10 месяцев, время до прогрессирования – 4–6 месяцев [3]. Варианты лечения при прогрессировании или резистентности НМРЛ крайне ограничены. К препаратам, рекомендуемым в настоящее время в качестве второй линии терапии НМРЛ, относятся цитостатики доцетаксел и пеметрексед (последний предусмотрен для пациентов с неплоскоклеточным раком) [4, 5]. Поскольку пеметрексед – один из препаратов выбора в терапии первой линии больных неплоскоклеточным НМРЛ, доцетакселу принадлежит ведущая роль в последующем лекарственном лечении [6]. Клиническая эффективность лекарственной терапии второй линии незначительна: частота объективного ответа не превышает 10%, медиана выживаемости без прогрессирования (ВБП) и общей выживаемости – 3–4 и 7–9 месяцев соответственно [5].
Последние годы в терапии больных НМРЛ наблюдается устойчивая позитивная динамика благодаря внедрению новых методов. В частности, назначение высокоэффективных таргетных препаратов с учетом молекулярного подтипа опухоли позволило улучшить прогноз заболевания, повысить эффективность лечения, увеличить общую выживаемость до 20 месяцев и более у пациентов с драйверными мутациями (EGFR, ALK и т.д.). Между тем частота выявления мутаций составляет 15–20% всех случаев заболевания НМРЛ [7].
Сегодня активно развивается новое направление – иммуноонкология. Понимание механизмов взаимодействия опухоли и иммунной системы сделало реальной разработку новых иммунотерапевтических препаратов – блокаторов точек иммунного контроля.
В 2015 г. в США для клинического применения во второй линии терапии больных НМРЛ были одобрены ниволумаб и пембролизумаб. Эти препараты блокируют взаимодействие между рецептором программируемой смерти (programmed cell death 1, PD-1) и его лигандами PD-L1 и PD-L2. Ингибирование PD-1 и его лигандов PD-L1 и PD-L2 способствует реактивации опухолеспецифических Т-лимфоцитов и пролонгированию их противоопухолевого эффекта [8].
В клинических исследованиях активно изучаются другие ингибиторы точек иммунного контроля.
Применение препаратов анти-PD-1 и анти-PD-L1 коренным образом изменило взгляд на прогноз пациентов с распространенным НМРЛ, прогрессирующим после предшествующей платиносодержащей химиотерапии. Подтверждение тому – результаты международных рандомизированных исследований III фазы, в частности CheckMate 017 с участием больных плоскоклеточным раком легкого и CheckMate 057 с участием пациентов с неплоскоклеточным НМРЛ [8, 9].
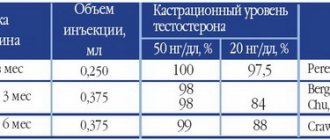
При первом промежуточном анализе CheckMate 017 было показано значительное увеличение медианы общей выживаемости в группе ниволумаба – 9,2 месяца по сравнению с 6,0 месяца в группе доцетаксела (р
В исследовании CheckMate-057 частота объективного ответа достигла 19 против 12%, медиана общей выживаемости – 12,2 против 9,4 месяца, одногодичная выживаемость – 51 против 39% в пользу ниволумаба. Профиль безопасности ниволумаба в отличие от такового доцетаксела более благоприятный [11].
Согласно данным приведенных исследований, ингибиторы PD-1, в частности ниволумаб, становятся новой опцией в борьбе за увеличение выживаемости, времени до прогрессирования, улучшение качества жизни больных диссеминированным НМРЛ.
Клинический случай
Пациентка Т. 1965 года рождения. В январе 2013 г. при выполнении по месту жительства рентгенографии легких в проекции верхней доли правого легкого выявлена инфильтративная тень. К врачам по этому поводу не обращалась. В январе 2015 г. появились жалобы на кашель. Пациентка обратилась в клинику.
Компьютерная томография (КТ) органов грудной клетки от 21 марта 2015 г.: признаки поствоспалительнго фиброза субсегмента верхней доли правого легкого, на фоне которого не исключен бронхоальвеолярный рак.
26 марта в Иркутском областном онкологическом диспансере выполнено оперативное лечение – расширенная верхняя лобэктомия справа с билатеральной медиастинальной лимфаденэктомией.
Гистологическое заключение: аденокарцинома легкого с участками высоко- и умеренно дифференцированного строения. Активирующих мутаций в гене EGFR, транслокации ALK не выявлено.
На основании данных гистологического заключения, проведенного обследования установлен диагноз: рак верхней доли правого легкого рТ2N2M0, стадия IIIа. В рамках комплексного лечения проведено шесть курсов адъювантной полихимиотерапии (ПХТ) по схеме «пеметрексед 500 мг/м2 внутривенно + цисплатин 75 мг/м2 внутривенно в первый день 21-дневного цикла» (последний курс – август 2015 г.). Курсы ПХТ переносила с выраженной эметогенной токсичностью. При очередном контрольном обследовании в марте 2021 г., по данным КТ, выявлено бессимптомное прогрессирование заболевания за счет появления дополнительного объемного образования в левой надключичной области, метастазов по костальной плевре.
Дополнительное ультразвуковое исследование (УЗИ) над- и подключичных лимфатических узлов показало поражение надключичных лимфоузлов слева, с инвазией в мягкие ткани.
Выполнена биопсия под УЗИ-контролем. Морфологически подтвержден метастаз аденокарциномы.
21 апреля 2021 г. начат первый курс ПХТ первой линии по схеме «пеметрексед 500 мг/м2 + карбоплатин AUC6» (цисплатин не назначали из-за выраженной эметогенной токсичности в анамнезе). Проведено три курса, отмечалась гематологическая токсичность (лейкопения) 2-й степени по критериям СТС. По данным контрольной КТ, состояние без отрицательной динамики, уменьшение образования в надключичной области.
ПХТ увеличена до шести курсов в прежних дозах с применением гранулоцитарного колониестимулирующего фактора. После шести курсов состояние пациентки ухудшилось: появились болевой синдром в левой половине грудной клетки, одышка при умеренной физической нагрузке.
Контрольная КТ в августе 2021 г.: гидроторакс слева, увеличение количества образований по плевре, рост надключичного лимфоузла слева.
Результаты медико-генетического тестирования гистологического блока показали позитивную экспрессию PD-L1.
Решением врачебной комиссии пациентке в качестве второй линии с сентября 2021 г. назначена иммунотерапия ниволумабом 3 мг/кг (200 мг на одно введение) внутривенно один раз в две недели, длительно, с оценкой эффекта через три месяца.
Введение препарата пациентка переносила удовлетворительно, нежелательных явлений, в том числе иммуноопосредованных реакций, не зафиксировано.
После четырех введений препарата состояние пациентки улучшилось.
Контрольное обследование в декабре 2021 г. (после шести введений): уменьшение размеров и количества образований по плевре слева, уменьшение количества содержимого в плевральной полости слева, признаков увеличения надключичного лимфоузла слева не выявлено. Динамика расценивалась как частичная регрессия по критериям RECIST 1.1. Продолжено введение препарата в прежнем режиме до прогрессирования, с оценкой эффекта каждые три месяца.
В марте 2021 г. рентгенологическая картина не отличалась от таковой в декабре 2021 г.: частичная регрессия опухоли сохранялась. Продолжено введение препарата.
Клинически состояние пациентки (на август 2021 г.) без отрицательной динамики, ECOG – 0. Введение препаратов переносит удовлетворительно, качество жизни не страдает. Пациентка ведет активный образ жизни. Следующее контрольное обследование запланировано на сентябрь 2021 г. Обсуждение
При выборе и проведении терапии распространенного неплоскоклеточного НМРЛ следует учитывать, что заболевание на этой стадии неизлечимо. Поэтому основной задачей лечения является сбалансированность терапевтического эффекта (в том числе выживаемости) и качества жизни пациентов [12, 13].
Рассмотренный клинический случай показывает потенциальный благоприятный эффект в отношении отдаленных результатов лечения при использовании ниволумаба во второй линии терапии распространенного НМРЛ. На фоне проводимого лечения (пациентка получает ниволумаб в течение года) отмечается частичная ремиссия. Кроме того, качество жизни и социальный статус пациентки сохраняются на протяжении всего периода применения иммуноонкологического препарата.
Ниволумаб значительно улучшает показатели выживаемости больных метастатическим НМРЛ, прогрессирующим после предшествующей платиносодержащей терапии, и сохраняет качество жизни, что подтверждают результаты международных исследований.
На конгрессе AACR-2017 были представлены данные исследования первой фазы применения монотерапии препаратом ниволумаб у предлеченных пациентов с НМРЛ с анализом пятилетней общей выживаемости. У сильно предлеченных пациентов с НМРЛ, получавших три линии терапии и более, на фоне применения ниволумаба частота ответа достигла 17,6%, при одногодичной общей выживаемости – 42%, двухлетней – 23% и пятилетней – 16% [11, 14]. С учетом положительных результатов исследований ранних фаз были проведены исследования третьей фазы, в которых сравнивали эффективность ниволумаба и стандартной терапии второй линии. Поскольку во второй линии терапии гистологический подтип НМРЛ имеет значение при выборе режима, были проведены два отдельных исследования для плоскоклеточного и неплоскоклеточного НМРЛ.
В международное рандомизированное исследование CheckMate 017 включались пациенты с плоскоклеточным НМРЛ, прогрессирующим после платиносодержащей химиотерапии. Исследователи сравнивали эффективность и безопасность ниволумаба 3 мг/кг внутривенно каждые две недели и доцетаксела 75 мг/м2 внутривенно каждые три недели. Первичной конечной точкой служила общая выживаемость. Кроме того, оценивались ВБП, частота объективного ответа и качество жизни [11]. Медиана выживаемости составила 9,2 месяца (95% доверительный интервал (ДИ) 7,3–13,3) в группе ниволумаба и 6,0 месяца (95% ДИ 5,1–7,3) в группе доцетаксела. При использовании ниволумаба риск смерти был на 41% ниже, чем при применении доцетаксела (относительный риск (ОР) 0,59; 95% ДИ 0,44–0,79; p
В международном рандомизированном исследовании CheckMate 057 участвовали пациенты с неплоскоклеточным НМРЛ, прогрессирующим после платиносодержащей химиотерапии. Ученые сравнивали эффективность и безопасность терапии ниволумабом 3 мг/кг внутривенно каждые две недели и доцетакселом 75 мг/м2 внутривенно каждые три недели. Первичной конечной точкой служила общая выживаемость. В исследовании оценивали также ВБП, частоту объективного ответа и качество жизни [11]. Общая выживаемость в группе ниволумаба превысила таковую в группе доцетаксела. Медиана общей выживаемости в группе ниволумаба (292 пациента) составила 12,2 месяца (95% ДИ 9,7–15,0), в группе доцетаксела (290 пациентов) 9,4 месяца (95% ДИ 8,1–10,7) (ОР 0,73; 95% ДИ 0,59–0,89; p = 0,002). Одногодичная общая выживаемость составила 51% (95% ДИ 45,0–56,0) в группе ниволумаба и 39% (95% ДИ 33,0–45,0) в группе доцетаксела. При продленном периоде наблюдения показатель общей выживаемости на 18-м месяце достиг 39% (95% ДИ 34,0–45,0) на фоне применения ниволумаба и 23% (95% ДИ 19,0–28,0) при использовании доцетаксела. Частота ответа в группе ниволумаба составила 19%, в группе доцетаксела – 12% (p = 0,02). Несмотря на то что медиана ВБП у пациентов, получавших ниволумаб, существенно не отличалась от таковой у больных, получавших доцетаксел (2,3 и 4,2 месяца соответственно), показатель годовой ВБП в группе ниволумаба был выше, чем в группе доцетаксела (19 и 8% соответственно). Ниволумаб ассоциировался с более высокой эффективностью в сравнении с доцетакселом по всем конечным показателям в подгруппах, выделенных в зависимости от заданных уровней экспрессии PD-1 лиганда на мембранах опухолевых клеток (≥ 1%, ≥ 5% и ≥ 10%). Нежелательные явления 3–4-й степени тяжести наблюдались у 10% пациентов в группе ниволумаба и у 54% пациентов в группе доцетаксела – показатели, аналогичные данным исследования CheckMate 017 [15, 16].
Результаты приведенных исследований позволяют сделать вывод, что ниволумаб является препаратом выбора во второй линии терапии НМРЛ [6].
Заключение
Рассмотренный клинический случай подтверждает высокую эффективность иммуноонкологических препаратов, таких как блокатор PD-1 ниволумаб, при метастатическом неплоскоклеточном НМРЛ. Важно, что на фоне применения ниволумаба не только достигается объективный ответ, но также длительно сохраняются достигнутый эффект и качество жизни.
Таким образом, ингибиторы PD-1 становятся новым стандартом второй линии терапии пациентов с НМРЛ.
Как применяют ниволумаб?
Препарат производится в виде раствора для внутривенных инфузий. Используют обычную капельницу или порт-систему, если она была имплантирована пациенту по показаниям. Процедура в среднем продолжается один час.
У некоторых пациентов возникает реакция на инфузию, она проявляется в виде таких симптомов, как лихорадка, озноб, зуд, покраснение и сыпь на коже, нарушение дыхания, сильная слабость, головокружение. О любых неприятных ощущениях нужно сообщить врачу. Доктор может замедлить скорость инфузии или прекратить ее совсем.
Периодичность процедур бывает разной:
- Если ниволумаб применяют отдельно: 1 раз в 2 недели.
- Если ниволумаб применяют в сочетании с ипилимумабом: 1 раз в 3 недели — первые 4 дозы; затем 1 раз в 2 недели.
Лечение продолжают до тех пор, пока оно приносит положительный эффект, и у пациента не возникают серьезные побочные эффекты.
Как контролируют состояние пациента во время лечения?
В целом все таргетные препараты, включая ниволумаб, считаются более безопасными по сравнению с химиопрепаратами. Тем не менее, опдиво иногда может вызывать серьезные и даже опасные для жизни осложнения. Поэтому к курсу лечения нужно правильно подготовиться, а во время него регулярно контролировать состояние пациента.
На этапе подготовки проводят обследование. Врач задает пациенту некоторые вопросы, чтобы выяснить важную информацию:
- Были ли у вас прежде аллергические реакции на лекарства?
- Принимаете ли вы сейчас какие-либо препараты, витамины, БАДы?
- Была ли у вас пересадка органов?
- Были ли у вас когда-либо диагностированы аутоиммунные заболевания?
Женщина должна сообщить врачу, если она беременна или подозревает у себя беременность, если кормит ребенка грудью.
Во время курса лечения придется регулярно сдавать общий и биохимический анализы крови: это нужно, чтобы контролировать количество эритроцитов, лейкоцитов и тромбоцитов, функцию почек и печени.
Ниволумаб в лечении метастатического плоскоклеточного рака анального канала
В журнале «The Lancet» за февраль 2021 года опубликованы данные об эффективности иммунотерапии ниволумабом в лечении ВИЧ-инфицированных пациентов с рефрактерным метастатическим плоскоклеточным раком анального канала.
«Плоскоклеточный рак анального канала — редкое заболевание, на долю которого приходится только 2% всех случаев злокачественных опухолей ЖКТ. Сиротское заболевание. Ничего нового за 20 лет. Пациенты с местными или региональными рецидивами, как правило, получают хирургическое лечение. Его можно излечить на ранних стадиях, используя комбинацию лучевой терапии и химиотерапии на основе 5-фторурацила и митомицина» (Энг). «Этот режим не изменился в течение 20 лет, отсутствуют рандомизированных исследований» (Каскину) [3].
В исследовании, проведенном в 10 академических центрах в США, участвовали пациенты, которые прошли, по меньшей мере, одну линию системной терапии для хирургически неоперабельного или метастатического рака анального канала в период с 14 мая 2015 по 11 ноября 2015 года. У всех ожидаемая продолжительность жизни была минимум 6 месяцев при соматическом статусе по ECOG 0-1. Пациенты с аденокарциномой анального канала, активным аутоиммунным заболеванием или аутоиммунным заболеванием в анамнезе или другими сопутствующими заболеваниями, которые требовали применение кортикостероидов, были исключены из исследования.
Ниволумаб вводили внутривенно каждые 2 недели в дозе 3 мг/кг. Пациенты достигли медианы терапии (6 введений ниволумаба) в течение 10-месячного периода наблюдения. Токсичность оценивали на начальном этапе до терапии и каждые 2 недели до того, как пациенты получали следующую дозу ниволумаба. Кроме того, необязательные образцы опухоли были получены при биопсии на начальном этапе и после 2-х доз ниволумаба. Рентгенологические исследования состояли из КТ или МРТ в начале исследования и повторялись с интервалом в 6 недель. Первичная конечная точка исследования, а именно ответ, подтвержденный лучевыми методами диагностики, оценивалась с использованием критериев оценки ответа при солидных опухолях версия 1.1 (RECIST 1.1).
В исследовании не упоминалось о каких-либо серьезных побочных эффектах. Ни у одного пациента с ВИЧ-инфекцией не развились нежелательные явления 4 степени, также ни один из пациентов не выбыл из исследования по причине токсичности, связанной с лечением. У одного пациента развился аутоиммунный гипотиреоз, связанный с терапией, который разрешился после короткого курса кортикостероидов. В другом случае у одного пациента был диагностирован пневмонит 2 степени, связанный с лечением, который был успешно купирован применением кортикостероидов и временным прекращением приема ниволумаба.
Результаты анализов крови у 30 пациентов, у которых кровь была взята до лечения, перед 2-ой, 4-ой и 6-ой дозой ниволумаба, показали более высокую концентрацию PD-1 по сравнению с пациентами, у которых не было эффекта. Исследование образцов, полученных при биопсии до лечения, методом проточной цитометрии выявил экспрессию PD-1 на 40% выше у пациентов, ответивших на ниволумаб. Этот показатель значительно выше, чем экспрессия PD-1 лиганда, наблюдаемая у тех пациентов, которые не ответили на ниволумаб, сообщают исследователи [3].
При промежуточной оценке базы данных (от 16 мая 2021 года) у 24 из 37 пациентов (24%) было зарегистрировано прогрессирование заболевания; 16 пациентов умерли, хотя смертей, связанных с лечением, не было. Доктор Энг и его коллеги сообщают, что общая выживаемость ВИЧ-ассоциированных больных с метастатическим плоскоклеточным раком анального канала в исследовании составила 11,5 месяцев и была значительно ниже по сравнении с 17 месяцами по данным Центра по контролю и профилактике заболеваний (the Centers for Disease Control and Prevention) за период с 2008 по 2012 гг [4].
«Ингибиторы иммунных точек контроля могут продлить общую выживаемость по сравнению с доступными в настоящее время опциями лечения, особенно если они были применены на первых линиях лечения». Для подтверждения этого необходимы дополнительные исследования. «В будущих исследованиях будет целесообразно рассмотреть использование ниволумаба до появления отдаленных метастазов, также может быть перспективным изучение комбинация ниволумаба с лучевой терапией», — утверждает Каскину.
По словам исследователей, иммунотерапия ниволумабом обещает улучшить результаты у пациентов с рефрактерным метастатическим раком анального канала, в том числе при наличии ВИЧ инфекции. Первые результаты исследования были представлены на ASCO, окончательные результаты были опубликованы 17 февраля в журнале Lancet Oncology [1, 2]. Результаты клинического исследования без контрольной группы II фазы показали, что у 37 ранее получавших лечение пациентов с метастатическим плоскоклеточным раком анального канала, получивших по меньшей мере одну дозу ниволумаба, в 24% случаев были получены ответы с ограниченной токсичностью, подтвержденные лучевыми методами диагностики. Медиана выживаемости без прогрессирования составила 4,1 месяца, а медиана общей выживаемости составила 11,5 месяцев, при общей выживаемости 48%. Авторы исследования также отмечают, что почти через 1 год после начала исследования 6 из 9 участников продолжали получать лечение после окончания исследования. В сопроводительном комментарии Стефано Каскину, доктор медицинских наук из Университета ди Модене и Реджио, Италия (the Università di Modena e Reggio Emilia, Italy), признает, что эти результаты дают надежду. «Впервые за 20 лет в лечении метастатического плоскоклеточного рака анального канала появилось что-то новое» [3]. Тем не менее, многое ещё предстоит узнать о применении иммунотерапии при метастатическим плоскоклеточным раком анального канала, говорит доктор Каскину, отмечая, что 75-80% участников исследования не получали выгоды от терапии ниволумабом.
Это исследование может быть первым завершенным исследованием для лечения метастатического рака анального канала с использованием ингибиторов иммунных точек контроля, говорят исследователи. Оно также может быть первым, кто включил ВИЧ-инфицированных пациентов из группы высокого риска. Исследователи отмечают, что до 90% случаев метастатического плоскоклеточного рака анального канала связаны с предыдущим инфицированием вируса папиллом человека. «При условии поддержания адекватного уровня CD4+ лимфоцитов и тщательном наблюдении инфекциониста мы рекомендуем рассматривать пациентов с ВИЧ-инфекцией для участия в будущих клинических испытаниях с использованием ингибиторов иммунных точек контроля, чтобы эти препараты могли быть изучены далее на более широкой группе пациентов», пишут они.
Справка (NB!):
В России ниволумаб (ингибитор PD-1) зарегистрирован 22 декабря 2016 года только по трем показаниям:
- монотерапия неоперабельной или метастатической меланомы у взрослых;
- монотерапия неоперабельного или метастатического НМРЛ после прогрессирования на фоне химиотерапии;
- монотерапия распространенного почечно-клеточного рака после предшествующей системной терапии.
Ниволумаб — человеческое моноклональное антитело, которое блокирует взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами (PD-L1 и PD-L2). Ниволумаб потенцирует иммунный ответ посредством блокады связывания PD-1 с лигандами PD-L1 и PD-L2.
Ниволумаб вводится внутривенно в дозе 3 мг/кг в течение 60 мин каждые 2 недели до прогрессирования или непереносимой токсичности. Пациенты должны находиться под непрерывным контролем (как минимум 5 мес после последней дозы ниволумаба), так как нежелательные иммуно-опосредованные реакции могут развиться в любой момент во время применения или отмены препарата.
При применении ниволумаба чаще всего наблюдаются иммуно-опосредованные побочные реакции. Большинство таких побочных реакций, включая тяжелые, купировались при помощи соответствующей терапии или отмены препарата. В случае проведения иммуносупрессивной терапии глюкокортикостероидами, предназначенной для устранения нежелательных явлений, после улучшения состояния снижение дозы глюкокортикостероидов проводят медленно, в течение по меньшей мере 1 мес. Повышение или понижение дозы препарата не рекомендуется.
Источники:
- Roxanne Nelson. Encouraging Results With Nivolumab in Metastatic Anal Cancer. https://www.medscape.com/viewarticle/864873
- Van K Morris et al. Nivolumab for previously treated unresectable metastatic anal cancer (NCI9673): a multicentre, single-arm, phase 2 study. The Lancet 2021. — Volume 18, No. 4, p446–453.
- Stefano Cascinu et al. Anal cancer: from an orphan disease to a curable malignancy? https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(17)30091-8/abstract
- Laura J. Viens et al. Human Papillomavirus–Associated Cancers — United States, 2008–2012. https://www.cdc.gov/mmwr/volumes/65/wr/mm6526a1.htm
- https://www.ascopost.com/https://clinicaltrials.gov/ct2/show/NCT02387996https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=7560c36a-e8e8-4092-8c46-e85f14a121e4&t
- https://www.pharmvestnik.ru/
Материал подготовлен Отделом НОИМТОиР: д.м.н. Т.Ю. Семиглазовой, клиническим ординатором Е.А. Коробейниковой
Какие возможны побочные эффекты?
Чаще всего при применении опдиво возникают такие побочные эффекты, как повышенная утомляемость, боли в мышцах, костях и суставах, диарея, снижение аппетита, головные боли, повышенный риск инфекции дыхательных путей, кашель, тошнота, зуд и сыпь на коже, лихорадка, боли в спине и животе, запоры.
В более редких случаях возможны более серьезные осложнения:
- Воспаление и процессы рубцевания в легких (пневмонит). Проявляется в виде упорного кашля, одышки, болей в груди.
- Воспаление в кишечнике (колит) с образованием язв. Проявляется в виде диареи, увеличения количества стула, примесей крови, сильных болей в животе.
- Воспаление печени (гепатит). Проявляется в виде желтухи, сильной тошноты и рвоты, потемнения мочи, болей под правым ребром, повышенной кровоточивости.
- Проблемы с эндокринной системой (гипофизом, щитовидной, поджелудочной железой, надпочечниками). Наиболее распространенные симптомы: повышенная утомляемость, упорные головные боли, увеличение или снижение веса, головокружение, обмороки, нарушение памяти, повышенная раздражительность, запоры, выпадение волос, увеличение количества мочи, постоянная жажда, снижение сексуального влечения.
- Нарушения со стороны почек (нефрит, почечная недостаточность). Возможные симптомы: уменьшение количества мочи, примесь крови в моче, отеки в области лодыжек, снижение аппетита.
- Нарушения со стороны кожи. Проявляются в виде сыпи, зуда, волдырей, язв на слизистых оболочках.
- Воспаление мозга (энцефалит). Проявляется в виде лихорадки, головных болей, слабости, повышенной утомляемости, спутанности сознания, напряжения мышц шеи, галлюцинаций, судорог.
- Нарушения со стороны нервной системы. Проявляются в виде слабости, онемения и покалывания в руках и ногах. Могут возникать параличи.
- Нарушения со стороны глаз. Проявляются в виде болей, покраснения глаз, нарушения четкости зрения, двоения изображения.
Предотвратить эти состояния помогает правильное применение препарата, с учетом всех показаний и противопоказаний, тщательный контроль состояния пациента.
Опдиво 10 мг/мл 10 мл №1 флакон
Применение препарата Опдиво
Монотерапия у взрослых — неоперабельная или метастатическая меланома; местнораспространенный или метастатический немелкоклеточный рак легкого после предшествующей химиотерапии; распространенный почечноклеточный рак после предшествующей системной терапии.
Противопоказания
Гиперчувствительность; беременность и кормление грудью; возраст до 18 лет (данные по эффективности и безопасности отсутствуют).
Ограничения к применению
Тяжелые аутоиммунные заболевания в активной стадии, при которых дальнейшая активация иммунной системы может представлять потенциальную угрозу жизни; нарушение функции печени средней и тяжелой степени; нарушение функции почек тяжелой степени.
Отдельные
группыпациентов
В клинических исследованиях не принимали участие следующие группы пациентов:
- пациенты с показателями исходного функционального статуса >2, неизлеченными метастазами головного мозга, аутоиммунными заболеваниями и пациенты, получавшие системные иммунодепрессанты до начала проведения исследования;
- пациенты с симптоматическими интерстициальными заболеваниями легких и меланомой глаза были исключены из проведения клинических исследований немелкоклеточного рака легкого и меланомы;
- пациенты с 4-й степенью тяжести нежелательных реакций, связанных с ранее проводимой анти-CTLA-4-терапией в анамнезе.
Ввиду отсутствия данных, ниволумаб должен применяться с осторожностью у данных групп пациентов после проведения оценки соотношения риск-польза, основанной на индивидуальных показателях.
Применение при беременности и кормлении грудью
Препарат противопоказан к применению во время беременности и в период кормления грудью.
Побочные действия препарата Опдиво
- Инфекции и инвазии: инфекция верхних дыхательных путей; бронхит, пневмония; редкоэнцефалит.
- Новообразования доброкачественные, злокачественные и неустановленной природы (в т.ч.кисты и полипы): редкогистиоцитарный некротический лимфаденит (лимфаденит Кикучи).
- Со стороны крови и лимфатической системы: эозинофилия.
- Со стороны иммунной системы: инфузионные реакции анафилактические реакции, гиперчувствительность.
- Со стороны эндокринной системы: гипергликемия, гипотиреоз, гипертиреоз; недостаточность функции надпочечников, гипопитуитаризм, гипофизит, тиреоидит, диабетический кетоацидоз, сахарный диабет.
- Со стороны обмена веществ и питания: снижение аппетита; дегидратация, метаболический ацидоз.
- Со стороны нервной системы: периферическая нейропатия, головная боль, головокружение; полинейропатия; редкосиндром Гийена-Барре, демиелинизация, миастенический синдром, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов).
- Со стороны органа зрения: нечеткость зрения, сухость глаз; увеит.
- Со стороны сердечно-сосудистой системы: повышение артериального давления, тахикардия, васкулит; редкоаритмия (включая желудочковую), мерцательная аритмия.
- Со стороны дыхательной системы: пневмонит, одышка, кашель; плеврит; редкоинфильтрация легких.
- Со стороны желудочно-кишечного тракта: диарея, тошнота; колит, стоматит, рвота, боль в животе, запор, сухость во рту; панкреатит; редкогастрит, язва двенадцатиперстной кишки.
- Со стороны печени и желчных путей: гепатит, гипербилирубинемия; редкохолестаз.
- Со стороны кожи и подкожной клетчатки: сыпь, зуд; витилиго, сухость кожи, эритема, алопеция; многоформная эритема, псориаз, розацеа, крапивница; редкотоксический эпидермальный некролиз3.
- Со стороны опорно-двигательного аппарата: костно-мышечная боль, артралгия; ревматическая полимиалгия.
- Со стороны почек и мочевыводящих путей: тубулоинтерстициальный нефрит, почечная недостаточность.
- Общие нарушения и реакции на введение: повышенная утомляемость; повышение температуры тела, отеки (включая периферические); боль в груди.
- Со стороны лабораторных показателей: снижение массы тела; повышение активности трансаминаз, липазы, амилазы и ЩФ, повышение уровня креатинина, лимфопения, лейкопения, тромбоцитопения, анемия, гипонатриемия; повышение концентрации общего билирубина, гиперкальциемия, гипокальциемия, гиперкалиемия. гипокалиемия, гипомагнезиемия, нейтропения, снижение абсолютного числа нейтрофилов, гипернатриемия; редкогипермагнезиемия.
- Иммуногенность. Ниволумаб, как и другие моноклональные антитела, обладает иммуногенностью.
Передозировка
Случаев передозировки выявлено не было.
Лечение: при передозировке лечение должно заключаться в симптоматической лекарственной терапии в соответствии с возникающими побочными реакциями при тщательном наблюдении за пациентом.
Пути введения
Внутривенно.
Ниволумаб и беременность
Беременность во время лечения препаратом опдиво и в течение 5 месяцев после завершения курса противопоказана. Если пациент находится в репродуктивном возрасте и планирует вести половую жизнь, нужно подобрать вместе с врачом эффективные способы контрацепции.
Кормить ребенка грудью также запрещено во время лечения и в течение 3 месяцев после него.
Неизвестно, влияет ли лечение ниволумабом на репродуктивную функцию. Если пациент планирует в будущем иметь детей, нужно сообщить об этом врачу.
Опдиво® (Opdivo®)
Препарат Опдиво® может вызывать тяжелые, в том числе с летальным исходом, побочные реакции, вызванные влиянием на иммунную систему и обусловленные специфическим механизмом его действия. Пациенты должны находиться под непрерывным контролем (как минимум 5 месяцев после введения последней дозы), так как нежелательные реакции, обусловленные воздействием препарата Опдиво®, могут развиться в любой момент во время применения или после отмены терапии. При подозрении на развитие иммуно-опосредованной нежелательной реакции должна быть проведена адекватная оценка для подтверждения или исключения иной этиологии. Основываясь на тяжести нежелательной реакции, применение препарата Опдиво® должно быть прекращено с возобновлением или без с назначением глюкокортикостероидов.
В случае проведения иммуносупрессивной терапии глюкокортикостероидами, предназначенной для устранения нежелательных реакций, после улучшения состояния снижение дозы глюкокортикостероидов проводят медленно, в течение по меньшей мере 1 месяца. Быстрое снижение дозы может привести к ухудшению тяжести или рецидиву нежелательных реакций. Иммуносупрессивная терапия, препаратами, отличными от глюкокортикостероидов, назначается в случае наступления ухудшения или отсутствия улучшения при применении глюкокортикостероидов.
Применение препарата Опдиво® следует прекратить во время получения пациентом иммуносупрессивной дозы глюкокортикостероидов или проведения иммуносупрессивной терапии.
Препарат Опдиво® должен быть отменен при любых рецидивирующих иммуно-опосредованных нежелательных реакциях от средней до тяжелой степени и отменен без возобновления при тяжелом иммуно-опосредованном пневмоните и иммуноопосредованном гепатите а также жизнеугрожающих иммуно-опосредованных нежелательных реакциях.
Применение препарата Опдиво® у пациентов с быстрым прогрессированием меланомы
Врачи должны обсудить эффект отсроченного действия препарата Опдиво® до начала проведения лечения у пациентов с быстро прогрессирующим заболеванием.
Иммуно-опосредованный пневмонит
При терапии препаратом Опдиво® были отмечены случаи тяжелого пневмонита или интерстициального заболевания легких, включая случаи с летальным исходом. Пациенты должны наблюдаться на наличие признаков и симптомов пневмонита, таких как рентгенографические изменения (например, затемнение по типу матового стекла, очаги воспаления), одышка и гипоксия. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3 или 4 степени тяжести пневмонита применение препарата Опдиво® следует отменить без возобновления и начать прием глюкокортикостероидов в дозе эквивалентной 2-4 м г/ кг/день метил преднизолона.
При 2 степени тяжести (симптоматической) пневмонита применение препарата Опдиво® следует приостановить и начать прием глюкокортикостероидов в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона. При наступлении улучшения применение препарата Опдиво® может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются, несмотря на прием глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 2-4 мг/кг/день метилпреднизолона и применение ниволумаба должно быть отменено без возобновления.
Иммуно-опосредованный колит
При терапии препаратом Опдиво® были отмечены случаи тяжелой диареи или колита. Пациенты должны наблюдаться на наличие признаков диареи и дополнительных симптомов колита, таких как боль в животе, слизь или кровь в стуле. Инфекции и связанные заболеванием симптомы должны быть исключены.
При 4 степени тяжести диареи или колита применение препарата Опдиво® следует отменить окончательно и начать прием глюкокортикостероидов в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона.
При 3 степени тяжести диареи или колита применение ниволумаба следует приостановить и начать прием глюкокортикостероидов в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона. При наступлении улучшения применение препарата Опдиво® может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются, несмотря на прием глюкокортикостероидов, применение ниволумаба должно быть отменено без возобновления.
При 2 степени тяжести диареи или колита применение препарата Опдиво® следует приостановить. Персистирующую диарею или колит следует устранять при помощи введения глюкокортикостероидов в дозе эквивалентной 0,5-1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются, несмотря на прием глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1-2 мг/кг/день метилпреднизолона и применение ниволумаба должен быть отменено без возобновления.
Иммуно-опосредованный гепатит
При терапии препаратом Опдиво® были отмечены случаи тяжелого гепатита. Пациенты должны наблюдаться на наличие признаков и симптомов гепатита, таких как повышение уровня трансаминаз и общего билирубина. Инфекции и связанные с заболеванием симптомы должны быть исключены.
При 3 или 4 степени тяжести повышения уровня трансаминаз и общего билирубина применение препарата Опдиво® следует отменить без возобновления и начать прием глюкокортикостероидов в дозе эквивалентной 1 — 2 мг/кг/день метилпреднизолона.
При 2 степени тяжести повышения уровня трансаминаз и общего билирубина применение препарата Опдиво® следует приостановить. Персистирующий подъем уровня этих лабораторных показателей должен быть устранен при помощи введения глюкокортикостероидов в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются, несмотря на прием глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1 — 2 мг/кг/день метилпреднизолона и применение ниволумаба должен быть отменено без возобновления.
Иммуно-опосредованные нефрит и почечная дисфункция
При терапии препаратом Опдиво® были отмечены случаи тяжелого нефрита или почечной дисфункции, поэтому пациенты должны наблюдаться на наличие их признаков и симптомов. У большинства пациентов отмечено бессимптомное повышение сывороточного креатинина. Должна быть исключена этиология, связанная с заболеванием.
При 4 степени тяжести повышения уровня сывороточного креатинина применение препарата Опдиво® следует отменить окончательно и начать прием глюкокортикостероидов в дозе эквивалентной 1 — 2 мг/кг/день метилпреднизолона.
При 2 или 3 степени тяжести повышения уровня сывороточного креатинина применение препарата Опдиво® следует приостановить и начать прием глюкокортикостероидов в дозе эквивалентной 0,5 — 1 мг/кг/день метилпреднизолона. При наступлении улучшения применение ниволумаба может быть продолжено после медленного снижения дозы глюкокортикостероидов. В случае наступления ухудшения или отсутствия улучшения, которые продолжаются, несмотря на прием глюкокортикостероидов, дозу глюкокортикостероидов следует увеличить до эквивалентной 1-2 мг/кг/день метилпреднизолона и применение ниволумаба должно быть отменено без возобновления.
Иммуно-опосредованная эндокринопатия
При терапии препаратом Опдиво® были отмечены случаи тяжелой эндокринопатии, включая гипотиреоз, гипертиреоз, недостаточность коры надпочечников, гипофизит, сахарный диабет и диабетический кетоацидоз.
Пациенты должны наблюдаться на наличие признаков и симптомов эндокринопатий и изменения функции щитовидной железы (в начале лечения, периодически во время лечения и основываясь на клинической оценке). У пациентов может отмечаться усталость, головная боль, изменение психического состояния, боль в животе, необычный ритм работы кишечника и гипотония или неспецифические симптомы, которые могут иметь сходство с другими состояниями, такими как метастазы в головной мозг или сопутствующие заболевания. В случае отсутствия выявления иной этиологии, признаки и симптомы эндокринопатий должны считаться иммуно-опосредованными.
При симптоматическом гипотиреозе применение препарата Опдиво® следует приостановить и, в случае необходимости, провести заместительную терапию гормонами щитовидной железы. При симптоматическом гипертиреозе применение препарата Опдиво® следует приостановить, и в случае необходимости, провести терапию антитиреоидными препаратами. В случае острого тиреоидита должны назначаться глюкокортикостероиды в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона. При наступлении улучшения применение препарата Опдиво® может быть продолжено после медленного снижения дозы глюкокортикостероидов. Необходимо продолжать наблюдение за функцией щитовидной железы для контроля адекватности проводимой заместительной гормональной терапии гормонами щитовидной железы.
При симптоматической недостаточности коры надпочечников 2 степени применение ниволумаба следует приостановить и, в случае необходимости, провести физиологическое замещение глюкокортикостероидов. При симптоматической недостаточности коры надпочечников 3-4 степени применение ниволумаба следует отменить окончательно и, в случае необходимости, провести физиологическое замещение глюкокортикостероидов. Необходимо продолжать наблюдение за функцией надпочечников и уровнем гормонов для контроля адекватности проводимой заместительной терапии глюкокортикостероидами.
При симптоматическом гипофизите 2-3 степени применение препарата Опдиво® следует приостановить и провести, в случае необходимости, гормонозаместительную терапию. В случае острого гипофизита назначаются глюкокортикостероиды в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона. При наступлении улучшения применение препарата Опдиво® может быть продолжено после медленного снижения дозы глюкокортикостероидов.
При симптоматическом гипофизите 4 степени терапия ниволумабом должна быть отменена окончательно. Необходимо продолжать наблюдение за функцией гипофиза и уровнем гормонов для контроля адекватности проводимой гормонозаместительной терапии.
При симптоматическом диабете применение ниволумаба следует приостановить и провести, в случае необходимости, заместительную терапию инсулином. Необходимо контролировать уровень сахара в крови для контроля адекватности проводимой заместительной терапии инсулином.
Иммуно-опосредованная сыпь
При терапии препаратом Опдиво® были отмечены случаи тяжелой формы сыпи (включая редкие случаи летального токсического эпидермального некролиза), которые могут иметь иммуно-опосредованную природу. Применение ниволумаба следует прекратить при сыпи 3 степени тяжести и отменить без восстановления при 4 степени тяжести. При сыпи тяжелой степени назначается лечение глюкокортикостероидами в дозе эквивалентной 1-2 мг/кг/день метилпреднизолона.
Препарат Опдиво® следует назначать с осторожностью у пациентов, у которых ранее отмечались тяжелые или жизнеугрожающие нежелательные кожные реакции при лечении иными иммуностимулирующими противоопухолевыми препаратами.
Иные иммуно-опосредованные нежелательные реакции
Следующие иммуно-опосредованные нежелательные реакции были отмечены у менее 1% пациентов, получавших лечение препаратом Опдиво® во время проведения клинических исследований при любом дозировании и типе опухоли: панкреатит, увеит, демиелинизация, аутоиммунная нейропатия (включая парез лицевого и отводящего нервов), синдром Гийена-Барре, гипопитуитаризм, миастенический синдром и энцефалит.
При подозрении на иммуно-опосредованные нежелательные реакции должна быть проведена адекватная оценка для подтверждения их этиологии или исключения иных причин их появления. Исходя из тяжести нежелательной реакции, применение препарата Опдиво® следует прекратить и начать терапию глюкокортикостероидами. При наступлении улучшения прием ниволумаба может быть продолжен после медленного снижения дозы глюкокортикостероидов. Препарат Опдиво® должен быть отменен без возобновления при проявлении любых рецидивирующих тяжелых иммуно-опосредованных нежелательных реакций и любых жизнеугрожающих иммуно-опосредованных нежелательных реакций.
Инфузионные реакции
Во время клинических исследований отмечались случаи тяжелых инфузионных реакций. В случае развития тяжелых инфузионных реакций, введение препарата Опдиво® должно быть прекращено с назначением соответствующей лекарственной терапии. Пациенты с легкой или умеренной инфузионной реакцией могут продолжать терапию препаратом Опдиво® под непрерывным наблюдением и проведением премедикации в соответствии с действующими стандартами профилактики инфузионных реакций.
Пациенты на диете с контролируемым содержанием натрия
Каждый миллилитр лекарственного препарата Опдиво® содержит 0,1 ммоль (или 2,5 мг) натрия, что должно учитываться при лечении пациентов, находящихся на диете с контролируемым содержанием натрия.