Фармакологические свойства препарата Элигард
Лейпрорелина ацетат — синтетический непептидный аналог естественного гонадотропин-рилизинг-гормона, который при продолжительном применении ингибирует секрецию гипофизарного гонадотропина и угнетает тестикулярный стероидогенез у мужчин. Имеет более высокую эффективность, чем естественный гормон, и его влияние обратимо после прекращения лечения. Назначение лейпрорелина ацетата вначале приводит к повышению уровня циркулирующего ЛГ и ФСГ, вследствие чего на протяжении некоторого времени происходит повышение уровня гонадных стероидов, тестостерона и дигидротестостерона у мужчин. При продолжительном применении лейпрорелина ацетата уровень ЛГ и ФСГ снижается. У мужчин уровень тестостерона снижается до кастрационного уровня (50 нг/дл). Это происходит на протяжении 3–5 нед после начала лечения. Средний уровень тестостерона через 6 мес лечения составляет для лейпрорелина ацетата 7,5 мг — 6,1 (±0,4) нг/дл и лейпрорелина ацетата 22,5 мг — 10,1 (±0,7) нг/дл соответственно, что сравнимо с его уровнем после выполнения билатеральной орхэктомии. У всех пациентов, принимавших участие в клиническом исследовании, при применении лейпрорелина ацетата 7,5 мг кастрационный уровень был достигнут через 6 нед (у 94% пациентов из них — до 28-го дня и у 98% — до 35-го дня); лейпрорелина ацетата 22,5 мг — у всех пациентов кастрационный уровень был достигнут через 5 нед (у 99% из них — до 28-го дня). У большинства пациентов уровень тестостерона был ниже 20 нг/дл. Уровень простатоспецифичного антигена снизился на 94% при дозе 7,5 мг на протяжении 6 мес и при дозе 22,5 мг — на 98% соответственно. Результаты исследований показали, что при продолжительном лечении уровень тестостерона сохраняется ниже кастрационного до 7 лет и даже до конца жизни. Абсорбция: у пациентов с карциномой предстательной железы в поздней стадии после первой инъекции лейпрорелина ацетата 7,5 мг максимальная концентрация лейпрорелина в сыворотке крови резко повышается до 25,3 нг/дл через 4–8 ч (Сmax) после инъекции; после введения лейпрорелина ацетата 22,5 мг — Сmax повышается до 127 нг/дл через 4,6 ч. После начального повышения после каждой инъекции (фаза плато от 2 до 28 дней после введения лейпрорелина ацетата 7,5 мг и от 3 до 84 дней после введения лейпрорелина ацетата 22,5 мг) уровень в сыворотке крови оставался относительно стабильным для лейпрорелина ацетата 7,5 мг 0,28–1,67 нг/мл и лейпрорелина ацетата 22,5 мг — 0,2–2,0 нг/мл. Данные о накоплении вещества при повторных инъекциях отсутствуют. Распределение: средний объем распределения лейпрорелина после в/в введения здоровым мужчинам-добровольцам составлял 27 л. Связывание с белками плазмы крови человека in vitro для лейпрорелина ацетата 7,5 мг составляло 43–49%, для лейпрорелина ацетата 22,5 мг — 47–49% соответственно. Выведение: при введении 1 мг лейпрорелина ацетата в/в здоровым добровольцам средний клиренс составлял 8,34 л/ч с окончательным периодом полувыведения 3 ч. Исследования относительно выведения препарата не проводились.
Роль препарата Элигард в лечении рака предстательной железы
| Константин Михайлович Фигурин Д.м.н., профессор отделения урологии РОНЦ им. Н.Н. Блохина РАМН [email protected] |
| Александр Владимирович Хачатурян Научный сотрудник отделения урологии РОНЦ им. Н.Н. Блохина РАМН [email protected] |
Рак предстательной железы (РПЖ) в 2007 г. занимал в России 4-е место (8,9%) в структуре онкологических заболеваний и 1-е место (60%) по величине прироста.
Выбор метода лечения зависит от стадии и распространенности опухолевого процесса. Так, для стадий T1–T3a при отсутствии региональных и отдаленных метастазов оптимальным является выполнение радикального хирургического вмешательства, для группы пациентов с хорошим прогнозом при данных стадиях заболевания показано применение дистанционной лучевой терапии.
Гормональная терапия РПЖшироко применяется у пациентов с различными стадиями заболевания: как паллиативный метод лечения у больных с распространенным и метастатическим опухолевым процессом, в качестве неоадъювантной терапии у больных перед проведением лучевой терапии, а также в качестве адъювантной терапии у больных РПЖгруппы высокого риска после хирургического лечения и лучевой терапии.
Большой вклад в развитие гормональной терапии РПЖвнес американский хирург-онколог и физиолог Чарльз Брентон Хаггинс. В 1939 г. он провел серию экспериментов, показавших изменение объема и химического состава секрета предстательной железы у собаки в различных гормональных условиях. В 1941 г. вышла серия его статей, в которых описывается опыт лечения больных РПЖс применением эстрогенов или хирургической кастрации. В 1966 г. Ч. Хаггинс был удостоен Нобелевской премии по физиологии и медицине за открытия в области гормонального лечения РПЖ. Аденокарцинома простаты – это гормонально-зависимая опухоль, которая представлена тремя популяциями клеток:
- гормонально-зависимыми, для роста которых необходима андрогенная стимуляция;
- гормонально-чувствительными, растущими без андрогенной стимуляции, однако при отсутствии андрогенов замедляющими свой рост;
- гормонально-нечувствительными, на рост которых андрогенная стимуляция не оказывает влияния. Таким образом, главным направлением работы ученых при разработке методов гормональной терапии РПЖявлялись различные способы снижения уровня тестостерона с целью блокирования роста опухоли. Для этого применялись следующие методы:
- хирургическая кастрация;
- препараты на основе эстрогенов;
- агонисты лютеинизирующего гормона-рилизинг-гормона (ЛГРГ);
- антагонисты ЛГРГ;
- антиандрогены;
- ингибиторы альфа-редуктазы;
- применение кетокеназола.
Необходимо отметить, что к существенным недостаткам первых двух методов относятся психологическая травма у больных и невозможность интермиттирующей терапии при хирургической кастрации; гинекомастия, повышенный риск кардиоваскулярных осложнений и тромбоэмболии у больных, получавших эстрогены.
В 1974 г. впервые был синтезирован лейпрорелин – синтетический непептидный аналог естественного гонадотропин-рилизинг-гормона. Гонадотропные гормоны относятся к подклассу тропных гормонов передней доли гипофиза, физиологической функцией которых является регуляция работы половых желез. Это событие можно считать прорывом в гормональной терапии РПЖ, поскольку применение агонистов ЛГРГ позволило достичь уровня тестостерона ниже 50 нг/дл, что было эквивалентно выполнению хирургической кастрации. При этом побочные эффекты были менее выражены, чем при лечении эстрогенами.
К побочным эффектам агонистов ЛГРГ относятся приливы, снижение либидо и ухудшение эрекции, снижение минеральной плотности костной ткани.
В 1989 г. впервые было предложено применение агонистов ЛГРГ в виде препаратов депо. При этом лейпрорелин вводится в жировую клетчатку в виде восстановленного раствора и формирует депо, оказывая действие на протяжении периода от 1 до 6 мес в зависимости от дозировки препарата.
В современном применении агонистов ЛГРГ в лечении больных РПЖ широко используется препарат Элигард, действующим веществом в котором является лейпрорелин.
В приведенной ниже таблице указаны данные различных авторов о применении Элигарда в виде депо в различных дозировках.
Таблица 1. Применение Элигарда в виде депо в различных дозировках
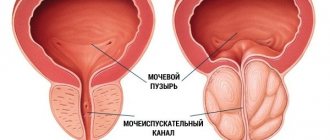
В настоящее время кастрационным уровнем тестостерона считается 20 нг/дл. Применение Элигарда позволяет в 95% случаев достичь этого уровня, что является преимуществом препарата в сравнении с традиционными аналогами ЛГРГ. Чтобы понять, как действует Элигард, рассмотрим физиологическую цепочку: гипоталамус – гипофиз – яички – предстательная железа. Рилизинг-фактор лютеинизирующего гормона ЛГРГ, который также называют гонадотропин-рилизинг гормоном (ГнРГ) относится к гипоталамическим нейрогормонам и продуцируется нейросекреторными клетками гипоталамуса.
ЛГРГ стимулирует переднюю долю гипофиза, что приводит к выбросу в системную циркуляцию фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ). Введение агонистов ЛГРГ приводит к кратковременному увеличению секреции гонадотропных гормонов, так называемому синдрому вспышки. Затем наступает десенсибилизация рецепторов ЛГРГ гипофиза, что приводит к угнетению его гонадотропной функции. На 3–5-й неделе после введения лейпрорелина уровень тестостерона снижается до кастрационного – 50 нг/дл. Преимуществом препарата Элигард являются его различные дозировки, позволяющие создавать депо препарата на 1 мес – 7,5 мг, 3 мес – 22,5 мг, 6 мес – 45 мг.
Зарубежными авторами был проведен ряд исследований с целью определения возможностей применения Элигарда в различных дозировках – 7,5; 22,5 и 45 мг.
В исследование Perrez-Mareno было включено 120 пациентов, из которых 117 (97,5%) в течение 6 мес получали терапию Элигардом в дозировке 7,5 мг, 1 раз в месяц. Уровень ПСА был от 0,1 до 639,0 нг/мл, средний уровень ПСА составил 32 нг/мл. По достижению 42 дней от начала исследования у всех больных был достигнут кастрационный уровень тестостерона – менее 50 нг/дл. После проведения 6-месячной терапии у 96% больных уровень ПСА опустился ниже 4 нг/мл, средний уровень ПСА составил 3,2 нг/мл. Средний уровень тестостерона на тот же момент равнялся 6,12 нг/дл при значениях в группе от 3 до 27 нг/дл.
Chu и соавт. в 2002 г. провели мультицентровое исследование, длившееся 6 мес, в которое вошли 117 больных РПЖ. Из них 111 на протяжении всего исследования получали терапию Элигардом в дозировке 22,5 мг каждые 3 мес. Как и в случае с применением данного препарата в дозировке 7,5 мг, эффект «вспышки», сопровождавшийся повышением концентрации в крови ЛГ наблюдался на первой неделе лечения. Затем в течение 2–4 нед уровень ЛГ снижался до нормы, а на 48-й день практически не определялся.
На 35-й день от начала исследования у всех больных был достигнут кастрационный уровень тестостерона – менее 50 нг/дл. На 6-м месяце лечения у 104 из 111 пациентов уровень тестостерона был менее 20 нг/дл, что составило 94%. Средний уровень тестостерона на данном сроке равнялся 10,1 нг/дл.
Средний уровень ПСА до начала лечения составил 86,4 нг/мл и снизился более чем на 98% на 6-м месяце лечения, достигнув уровня 1,7 нг/мл. В 2006 г. Crawford и соавт. провели мультицентровое 12-месячное исследование, в которое были включены 111 больных РПЖ, из них 103 (93%) прошли его полностью. Средний период, за который тестостерон достигал кастрационного уровня – ниже 50 нг/дл, составил 21 день.
По прошествии года от начала исследования у 99% больных уровень тестостерона был ниже 50 нг/дл и у 88% – ниже 20 нг/дл. Средний уровень ПСА на тот же срок составил 1,2 нг/мл. При анализе побочных эффектов Элигарда авторы отметили приливы от слабовыраженных (33,3%) до средневыраженных (24,35%), жжение в зоне инъекции (14,4 и 0,9% соответственно), тошноту (7,2 и 4,5%), атрофию яичек (5,4%) и гинекомастию (3,6%). Уникальность препарата Элигард заключается в применении инновационной системы Атригель. Упаковка препарата включает в себя 2 шприца: первый содержит активное вещество – лиофилизат лейпрорелина ацетата, второй содержит биодеградирующий полимер Атригель.
Для приготовления раствора препарата необходимо извлечь шприцы из упаковки, снять с них защитные крышки и осторожно соединить. Затем смешать раствор, попеременно нажимая на поршни шприцев. После смешивания необходимо отсоединить шприц, в котором находился Атригель, и зафиксировать на его место стерильную иглу.
Препарат вводится в клетчатку передней брюшной стенки, попадание его в кровеносные сосуды недопустимо.
Под действием воды в подкожной жировой клетчатке происходит осаждение полимера Атригель и препарат затвердевает. По мере постепенной биодеградации препарата происходит высвобождение активного вещества. Благодаря применению Атригеля стало возможным создание лекарственных форм с повышенным содержанием лекарственного вещества – 7,5, 22,5 и 45 мг.
B. Tombal в своей статье от 2005 г. приводит мнение ряда авторов о том, что использование данной системы введения в сочетании с высокими дозами препарата ведет к улучшению его фармакокинетики, что обеспечивает лучший лечебный эффект – снижение тестостерона до кастрационного уровня менее 20 нг/дл отмечается у 95% пациентов.
Abouelfadel и соавт. отмечают также, что применение препарата в форме 6-месячного депо способствует значительному улучшению качества жизни пациентов. Элигард оказывает стабильный и хорошо контролируемый эффект, при его применении уменьшается частота местных нежелательных явлений в зоне введения, требуется меньше посещений врача, что актуально для больных с ограниченной подвижностью и живущих в удаленных районах. Также препарат можно примененять для неоадъювантной терапии РПЖ.
Таким образом, Элигард – удобный и эффективный препарат для лечения больных РПЖ, он также является единственным препаратом-депо из группы агонистов ЛГРГ, введение которого можно выполнять 1 раз в 6 мес, что существенно улучшает качество жизни пациентов.
0
Ваша оценка: Нет
Применение препарата Элигард
Элигард 7,5 мг назначается в виде п/к инъекции 1 раз в месяц. Введенный р-р образует депо препарата, который обеспечивает постоянное высвобождение лейпрорелина ацетата на протяжении 1 мес. Элигард 22,5 мг назначается в виде п/к инъекции 1 раз в 3 мес. Введенный р-р образует депо препарата, который обеспечивает постоянное высвобождение лейпрорелина ацетата на протяжении 3 мес. Терапия гормонзависимого рака предстательной железы с применением Элигарда представляет собой продолжительное лечение и не должна прерываться после наступления улучшения или ремиссии. Введение. Содержимое двух предварительно наполненных стерильных шприцев должно быть смешано непосредственно перед введением Элигарда в виде п/к инъекции. Попадание препарата в артерию или вену недопустимо! Как и при применении других препаратов, которые назначаются п/к, место введения Элигарда нужно периодически изменять. Реакция на лечение препаратом должна контролироваться путем наблюдения клинических проявлений заболевания и измерения уровня простатоспецифичного антигена в сыворотке крови. Если ответ пациента на лечение недостаточен, желательно проверить, достиг ли уровень тестостерона кастрационного уровня или продолжает находиться на нем. Приготовление смеси проводится по инструкции. После смешивания р-р должен быть немедленно введен. Неиспользованный р-р не должен применяться. Клинические исследования у пациентов с печеночной или почечной недостаточностью не проводились.
Рак предстательной железы (РПЖ) в 2009 году в структуре онкозаболеваемости занимал в России 2 место или 10,7% и первое место или 153,27% по величине прироста заболеваемости за последние 10 лет. [1] Выбор метода лечения РПЖ зависит от стадии и распространённости опухолевого процесса. Так, для стадий T1-T3a при отсутствии региональных и отдалённых метастазов оптимальным является выполнение радикального хирургического вмешательства, для группы пациентов хорошего прогноза при данных стадиях заболевания показано применение дистанционной лучевой терапии. Гормональная терапия РПЖ широко применятся у пациентов с различными стадиями заболевания: как паллиативный метод лечения у больных с распространённым и метастатическим опухолевым процессом, в качестве неоадъювантной терапии у больных перед проведением лучевой терапии, а также в качестве адъювантной терапии у больных РПЖ группы высокого риска после хирургического лечения и лучевой терапии. Большой вклад в развитие гормонотерапии РПЖ внёс американский хирург-онколог и физиолог Чарльз Брентон Хаггинс. В 1939 году он провёл серию экспериментов, показавших изменение объёма и химического состава секрета предстательной железы у собаки в различных гормональных условиях. В 1941 году выходит серия его статей, в которых описывается опыт лечения больных РПЖ с применением эстрогенов или хирургической кастрации. В 1966 году Ч. Хаггинс был удостоен Нобелевской премии по физиологии и медицине за открытия в области гормонального лечения РПЖ. Аденокарцинома простаты – это гормонально-зависимая опухоль, которая представлена тремя популяциями клеток
- гормонально-зависимыми, для роста которых необходима андрогенная стимуляция.
- гормонально-чувствительными, растущими без андрогенной стимуляции, однако при отсутствии андрогенов замедляющими свой рост.
- гормонально-нечувствительными, на рост которых андрогенная стимуляция не оказывает влияния.
Таким образом, главным направлением работы учёных при разработке методов гормонотерапии РПЖ, являлись различные способы снижения уровня тестостерона, с целью блокирования роста опухоли. Для этого применялись следующие методы:
- хирургическая кастрация.
- препараты на основе эстрогенов.
- агонисты лютеинизирующего гормона рилизинг-гормона (ЛГРГ).
- антагонисты ЛГРГ.
- анти-андрогены.
- ингибиторы альфа-редуктазы.
- применение кетокеназола.
Необходимо отметить, что к существенным недостаткам первых двух методов относятся психологическая травма у больных и невозможность интермиттирующей терапии при хирургической кастрации; гинекомастия, повышенный риск кардиоваскулярных осложнений и тромбоэмболии у больных, получавших эстрогены. В 1974 году впервые был синтезирован лейпрорелин — синтетический непептидный аналог естественного гонадотропин-рилизинг-гормона. Гонадотропные гормоны относятся к подклассу тропных гормонов передней доли гипофиза, физиологической функцией которых является регуляция работы половых желёз. Это событие можно считать прорывом в гормональной терапии РПЖ, поскольку применение агонистов ЛГРГ позволило достичь уровня тестостерона ниже 50 нг/дл, что было эквивалентно выполнению хирургической кастрации. При этом побочные эффекты были менее выражены, чем при лечении эстрогенами. К побочным эффектам агонистов ЛГРГ относятся приливы, снижение либидо и ухудшение эрекции, снижение плотности костной ткани. В 1989 году впервые было предложено применение агонистов ЛГРГ в виде препаратов-депо. При этом лейпрорелин вводится в жировую клетчатку в виде восстановленного раствора и формирует депо, оказывая действие на протяжении от 1 до 6 месяцев, в зависимости от дозировки препарата. В современном применении агонистов ЛГРГ в лечении больных РПЖ широко применяется препарат Элигард, действующим веществом в котором является лейпрорелин. В приведённой ниже таблице указаны данные различных авторов о применении Элигарда в виде депо в различных дозировках: Таблица 1. Клинические исследования с использованием Элигарда
| Дозировка лейпрорелина | Объём инъекции (мл) | Кастрационный уровень тестостерона | Авторы | |
| 50 нг/дл | 20 нг/дл | |||
| 7.5 мг, 1 раз в месяц | 0.250 | 100% | 98% | Perez-Mareno 2002 |
| 22.5 мг, 1 раз в 3 месяца | 0.375 | 98% | 84% | Chu 2002 |
| 45.0 мг, 1 раз в 6 месяцев | 0.375 | 99% | 88% | Crawford 2006 |
В настоящее время кастрационным уровнем тестостерона считается 20 нг/дл. Применение Элигарда позволяет в 95% случаев достичь этого уровня, что является конкурентным преимуществом препарата в сравнении с традиционными аналогами ЛГРГ. Чтобы понять, как действует Элигард, рассмотрим физиологическую цепочку: гипоталамус – гипофиз – яички – предстательная железа. Рилизинг-гормон лютеинизирующего гормона (ЛГРГ), который также называют гонадотропин-рилизинг гормоном (ГнРГ), относится к гипоталамическим нейрогормонам и продуцируется нейросекреторными клетками гипоталамуса. ЛГРГ стимулирует переднюю долю гипофиза, что приводит к выбросу в системную циркуляцию фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ). Введение агонистов ЛГРГ приводит к кратковременному увеличению секреции гонадотропных гормонов, так называемому «феномену вспышки». Затем наступает десенсибилизация рецепторов ЛГРГ гипофиза, что приводит к угнетению его гонадотропной функции. На 3-5 неделе после введения лейпрорелина уровень тестостерона снижается до кастрационного – 50 нг/дл. Преимуществом препарата Элигард являются его различные дозировки, позволяющие создавать депо препарата на 1 месяц – 7.5 мг, 3 месяца – 22.5 мг, 6 месяцев – 45 мг. Зарубежными авторами был проведен ряд исследований с целью определения возможностей применения Элигарда в различных дозировках – 7.5 мг, 22.5 мг и 45мг. В исследование Perrez-Mareno включено 120 пациентов, из которых 117 (97.5%) в течение 6 месяцев получали терапию Элигардом в дозировке 7.5 мг, 1 раз в месяц. Уровень ПСА был от 0.1 до 639.0 нг/мл, средний уровень ПСА составил 32 нг/мл. По достижению 42 дней от начала исследования у всех больных был достигнут кастрационный уровень тестостерона менее 50 нг/дл. После проведения 6-ти месячной терапии у 96% больных уровень ПСА опустился ниже 4 нг/мл, средний уровень ПСА составил 3.2 нг/мл. Средний уровень тестостерона на тот же момент составил 6.12 нг/дл, при значениях в группе от 3.0 до 27.0 нг/дл. [4] Chu и соавт. в 2002 году провели мультицентровое исследование, длившееся 6 месяцев, в которое вошли 117 больных РПЖ. Из них 111 на протяжении всего исследования получали терапию Элигардом в дозировке 22.5 мг каждые три месяца. Как и в случае с применением данного препарата в дозировке 7.5 мг, эффект «вспышки», сопровождавшийся повышением концентрации в крови лютеинизирующего гормона (ЛГ) наблюдался на первой неделе лечения. Затем, в течение 2-4 недель уровень ЛГ снижался до уровня нормы, а на 48-й день практически не определялся. На 35-й день от начала исследования у всех больных был достигнут кастрационный уровень тестостерона менее 50 нг/дл. На 6-м месяце лечения у 104 из 111 пациентов уровень тестостерона был менее 20 нг/дл, что составило 94%. Средний уровень тестостерона на данном сроке составил 10.1 нг/дл. Средний уровень ПСА до начала лечения составил 86.4 нг/мл и снизился более чем на 98% на 6-м месяце лечения, достигнув уровня 1.7 нг/мл. [5] В 2006 году Crawford и соавт. провели мультицентровое 12-ти месячное исследование, в которое было включено 111 больных РПЖ, из которых 103 (93%) завершили его полностью. Среднее время, за которое тестостерон достигал кастрационного уровня ниже 50 нг/дл, составило 21 день. По прошествии года от начала исследования у 99% больных уровень тестостерона был ниже 50 нг/дл и у 88% — ниже 20 нг/мл. Средний уровень ПСА на том же сроке составил 1.2 нг/мл. При анализе побочных эффектов Элигарда, авторы отметили приливы от слабо выраженных (33.3%) до средне выраженных (24.35%), жжение в зоне инъекции (14.4% и 0.9% соответственно), тошноту (7.2% и 4.5%), атрофию яичек (5.4%) и гинекомастию (3.6%). [6] Уникальность препарата Элигард заключается в применении инновационной системы Атригель. Упаковка препарата включает в себя два шприца: один содержит активное вещество – лиофилизат лейпрорелина ацетата, второй содержит биодеградирующий полимер Атригель. Для приготовления раствора препарата необходимо извлечь шприцы из упаковки, снять с них защитные крышки и осторожно соединить. Затем смешать раствор, попеременно нажимая на поршни шприцев. После смешивания, необходимо отсоединить шприц, в котором находился Атригель, и фиксировать на его место стерильную иглу. Препарат вводится в клетчатку передней брюшной стенки, попадание его в кровеносные сосуды недопустимо. Под действием воды в подкожной жировой клетчатке происходит осаждение полимера Атригель и препарат затвердевает. По мере постепенной биодеградации препарата происходит высвобождение активного вещества. Благодаря применению Атригеля стало возможным создание лекарственных форм с повышенным содержанием лекарственного вещества – 7.5, 22.5 и 45 мг. B. Tombal в своей статье от 2005 года [7] приводит мнение ряда авторов о том, что использование данной системы введения в сочетании с высокими дозами препарата приводит к улучшению его фармакокинетики, что обеспечивает лучший лечебный эффект – снижение тестостерона до кастрационного уровня менее 20 нг/дл отмечается у 95% пациентов. Abouelfadel и соавт. [3]отмечают также, что применение препарата в форме 6-ти месячного депо способствует значительному улучшению качества жизни пациентов. Элигард оказывает стабильный и хорошо контролируемый эффект, при его применении уменьшается частота местных нежелательных явлений в зоне введения, требуется меньше посещений врача, что актуально для больных с ограниченной подвижностью и живущих в удалённых районах. Также препарат можно применять для неоадъювантной терапии РПЖ. Таким образом, Элигард — это удобный и эффективный препарат для лечения больных РПЖ, он также является единственным препаратом-депо из группы агонистов ЛГРГ, введение которого возможно выполнять 1 раз в 6 месяцев, что существенно улучшает качество жизни пациентов. Литература:
- «Злокачественные новообразования в России в 2009 году (заболеваемость и смертность)». Под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой.? М.: ФГУ «МНИОИ им. П.А. Герцена Минздравсоцразвития России», 2011.
- A subcutaneous delivery system for the extended release of leuprolide acetate for the treatment of prostate cancer. Ramon Perez-Marrero, Robert C Tyler Expert Opin. Pharmacother. (2004) 5(2):447-457
- Leuprorelin depot injection: patient considerations in the management of prostatic cancer. Zinelabidine Abouelfadel, E David Crawford. Therapeutics and Clinical Risk Management 2008:4(2) 513–526
- A six-month, open label study assessing a new formulation of leuprolide 7.5 mg for suppression testosterone in patients with prostate cancer. Perez-Marrero, Chu F.M. Clin. Ter. 2002;24 1092-14
- A clinical study of 22.5 mg LA – 2550: a new subcutaneous depot delivery system for leuprolide acetate for the treatment of prostate cancer. Chu F.M., Jayson M., Dineen M.K. J.Urol 2002; 168:1199-203
- A 12-Month Clinical Study of LA-2585 (45.0 MG): A New 6-Month Subcutaneous Delivery System for Leuprolide Acetate for the Treatment of Prostate Cancer. E. David Crawford, Oliver Sartor, Franklin Chu, Ramon Perez, Gary Karlin, J. Steve Garrett. J.Urol 2006; 175:533-536
- How good to current LHRH agonists control testosterone? Can this be improved by Eligard? B. Tombal, R. Berges. Eur. Urol. Suppl. 4 (2005) 30-36
Побочные эффекты препарата Элигард
В основном возникают в связи со специфическим фармакологическим действием лейпрорелина ацетата, а именно: повышением и снижением гормонального уровня. Со стороны сердечно-сосудистой системы: приливы, лабильность АД, потеря сознания, периферические отеки, эмболия легочных сосудов, ощущение сердцебиения, озноб, одышка. Со стороны нервной системы: гипоэстезия, головокружение, головная боль, бессонница, расстройства вкуса, зрения, обоняния, произвольные движения, нарушение сна, депрессия, амнезия, и гиперэстезия кожи. Со стороны ЖКТ: тошнота, сухость во рту, запор или диарея, метеоризм. Со стороны дыхательной системы: ринорея. Со стороны мочеполовой системы: дизурия, никтурия, олигурия, инфекции мочевых путей, мягкость и гипертрофия грудных желез, атрофия яичек, боль в яичках, бесплодие, гематурия, острая задержка мочи, гинекомастия, импотенция, болезненность грудных желез, снижение либидо. Со стороны костно-мышечной системы: артралгия, боль в спине, мышечные судороги, миалгия, мышечная слабость. Со стороны лабораторных показателей: изменения в общем анализе крови, повышение содержания креатинина, фосфокиназы, АлАТ, ТГ в крови, удлинение времени свертывания крови и протромбинового времени, в отдельных случаях — тромбоцитопения и лейкопения. Распространенные побочные эффекты — недомогание и усталость. Местные побочные эффекты: очень часто — преходящее незначительное жжение/покалывание после инъекции; часто — боль, эритема, кровоподтек, зуд, редко — уплотнение и образование язв. В целом эти побочные рекции незначительны и быстро преходящие. Также может быть кожная сыпь, алопеция, повышенная потливость. Сообщалось об изменении толерантности к глюкозе.
Особые указания по применению препарата Элигард
Исследования относительно влияния Элигарда на способность управлять транспортными средствами и работать со сложными механизмами не проводились. Из-за ощущения усталости, головокружения, нарушения зрения (побочные эффекты лечения или следствие основного заболевания) может ухудшаться способность к управлению автомобилем и механизмами. Лейпрорелина ацетат, как и другие агонисты гонадотропин-рилизинг-гормона, вызывает кратковременное повышение концентрации тестостерона, дигидротестостерона и кислой фосфатазы в сыворотке крови на протяжении первой недели лечения. У пациентов могут усилиться симптомы или возникнуть новые, такие как боль в костях, неврологические расстройства, гематурия, обструкция мочеточника или инфравезикальная обструкция. Эти симптомы обычно проходят при продолжении лечения. При применении агонистов гонадотропин-рилизинг-гормона сообщалось о случаях обструкции мочеточника и компрессии спинного мозга, что может приводить к параличу с наличием или отсутствием фатальных осложнений. При компрессии спинного мозга или почечной недостаточности проводят стандартное лечение этих осложнений. Следует проводить тщательное наблюдение на протяжении нескольких первых недель лечения пациентов с метастазами в позвоночнике и/или головном мозгу, а также пациентов с обструкцией мочевых путей. Дополнительно назначать антиандроген следует за 3 дня до начала терапии лейпрорелином и применять на протяжении первых 2–3 нед лечения (для предотвращения последствий начального повышения уровня тестостерона в сыворотке крови). При гормонрезистентной опухоли (отсутствие клинического улучшения, несмотря на снижение уровня тестостерона) дальнейшая терапия препаратом Элигард не имеет смысла. Имеются сообщения о снижении плотности костной ткани у мужчин, которым проводилась билатеральная орхэктомия или которых лечили агонистом гонадотропин-рилизинг-гормона. Антиандрогенная терапия повышает риск переломов вследствие возникновения остеопороза. Кроме длительного дефицита тестостерона, на развитие остеопороза могут также влиять такие факторы: пожилой возраст, курение, употребление алкоголя, избыточная масса тела, недостаточные физические нагрузки. У некоторых больных, которым проводилась терапия агонистом гонадотропин-рилизинг-гормона, были зафиксированы изменения толерантности к глюкозе, поэтому пациенты с сахарным диабетом требуют тщательного наблюдения. После кастрации хирургическим путем Элигард не приводит к дальнейшему снижению уровня тестостерона в сыворотке крови у мужчин.