Рак предстательной железы (РПЖ) на сегодняшний день остается одной из актуальных проблем мужского населения старшего возраста. В РФ число мужчин заболевших раком предстательной железы (РПЖ) в 2012 г.составило 29082, тогда как в 2000 г. было выявлено 11580.[1]
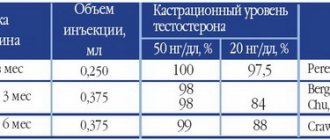
Учитывая критическую важность тестостерона для роста РПЖ, обязательным условием успешного лечения является сведение к минимуму выработки данного андрогена. Стандартные методы андроген-депривационной терапии, в частности орхиэктомии, и применение аналогов гонадолиберина, приводят к остановке выработки андрогенов в яичках, не обладая эффектом в отношении выработки андрогенов в надпочечниках.
В настоящее время проводятся многоцентровые рандомизированные исследования II–III фазы с использованием новых химиотерапевтических агентов (кабазитаксел), иммунопрепаратов (ипилимумаб, EMD525797 и др.), вакцин (сипулейцел-T), таргетных агентов, а также группы блокаторов синтеза андрогенов (абиратерона ацетат, ортеронел).
В исследование C0U-AA-301, посвященное оценке эффективности терапии абиратерона ацетата у пациентов с метастатическим кастрационно-резистентным РПЖ (мКРРПЖ) после неэффективности химиотерапии таксанами, было включено 1195 пациентов из 13-ти стран мира. Первая группа пациентов получала ежедневно абиратерона ацетат однократно вместе с преднизоном, а 2-я — плацебо с преднизоном перорально. Терапия продолжалась до прогрессии. Основной целью исследования была оценка общей выживаемости (ОВ), также оценивались время до прогрессирования (ВДП), выживаемость без прогрессии (ВБП) и общий клинический ответ. Медиана наблюдения больных составила 12,8 мес. Согласно опубликованным Johann S. de Bono результатам исследования, ОВ была выше в группе абиратерона ацетата, чем в группе плацебо с преднизоном, значения составили 14,8 мес и 10,9 мес соответственно. Все дополнительные оцениваемые показатели, такие как время до ПСА-прогрессии (10,2 мес и 6,6 мес), ВБП (5,6 мес и 3,6 мес) и частота ПСА-ответа (29% и 6%), свидетельствовали в пользу абиратерона ацетата. Так же в ходе исследования были доказаны преимущества для пациентов, получавших терапию абиратерона ацетатом, по сравнению с группой пациентов, находящихся на терапии плацебо, по следующим показателям: качество жизни (общий функциональный статус), снижение степени и продолжительности выраженности болевого синдрома, снижение риска развития скелетных осложнений.
С момента первой регистрации в 2011 году в США препарат Зитига® был зарегистрирован в более чем 50 странах. Препарат получают более 30 000 мужчин во всем мире, и в настоящее время он быстро становится основным препаратом для лечения мКРРПЖ.
Федеральная служба по надзору в сфере здравоохранения и социального развития зарегистрировала препарат Зитига® (абиратерона ацетат) в России в 2012 г.
Под нашим наблюдением в онкоурологических стационарах и поликлиниках ДЗ г. Москвы с ноября 2013 г. по октябрь 2014 г. находятся 42 пациента с гормонорезистентным метастатическим раком предстательной железы, ранее получавших химиотерапию.
До включения в исследование 32 пациента получили в 1- ой линии от 3–24 курсов Таксотера в дозе 85 мг\м2- 1 день интервал 21 день на фоне стандартной премедикации дексаметазоном, из них:
8 человек получили 3 курса, у 1 больного лечение было отменено в связи с проявлениями гематологической токсичности (стойкая нейтропения III- ст); у 7 из которых отмечено прогрессирование заболевания в виде появления новых метастатических очагов в костях, легких, лимфатических узлах, (4-м больным во второй линии химиотерапии проводилось лечение Кабазитакселом в дозе 25 мг\м2 1 день в комбинации с преднизолоном 10 мг в сутки ежедневно,2 больных получили 6 курсов химиотерапии, лечение было завершено в связи с прогрессированием заболевания в виде появления новых метастатических очагов в костях, у 1 больного лечение окончено после 4-го курса химиотерапии в связи с развитием стойкой гематологической токсичности (анемия II–III) , у 1 больного лечение окончено в связи с явлениями нейропатии II степени);
10 пациентов получили 6 курсов химиотерапии, у 4-х отмечено прогрессирование заболевания в виде появления костных метастазов, метастазов в легкие и плевру, стойкого роста ПСА, у 2 больных отмечена гематологическая токсичность (нейтропения III–IV ст, анемия III ст), у 2-х больных астения II–III ст, у 2-х больных гастроинтестинальная токсичность II–III ст.;
9 больных получили 9 курсов химиотерапии из них у 4-х отмечено появление новых костных метастазов, а также метастазов в легкие на фоне стойкого роста ПСА, у 3 больных был отмечен стойкий рост ПСА, у 1-го больного отмечена гематологическая токсичность (стойкая нейтропения III- ст), у 1 больного нейропатия II–III ст.;
4 пациента получили 12 курсов химиотерапии, у 3- х отмечено прогрессирование заболевания в виде появления новых костных метастазов, увеличение количества и размеров метастазов в легких, забрюшинных лимфоузлах, у одного больного стойкое повышение ПСА.
1 больной получил 24 курса химиотерапии лечение прекращено в связи с прогрессированием заболевания в идее появления новых костных метастазов и стойкого роста ПСА.
10 больных получили от 3-х до 9 курсов химиотерапии Митоксантроном в дозе 10 мг\и2 -1 день с интервалом 21 день и 10 мг преднизолона в сутки ежедневно. 1 больной получил во второй линии Кабазитаксел в дозе 25 мг\м2 1 день в комбинации с преднизолоном 10 мг в сутки ежедневно. Пациенту проведено 8 курсов химиотерапии Кабазитаксел, лечение завершено в связи с прогрессированием заболевания в виде появления новых костных метастазов, а также метастатического поражения забрюшинных лимфоузлов. У всех больных после проведенного лечения выявлено прогрессирование заболевания. Среди них у 7 выявлены новые костные метастазы, у 6 обнаружены и морфологически верифицированы метастазы в подвздошные и забрюшинные л/узлы, у 2 больных выявлены метастазы в легкие.
Всем больным проводились общеклинические лабораторные исследования: общий развернутый анализ крови, биохимический анализ крови, определение уровня простатспецифического антигена (ПСА) и тестостерона, ЭКГ и Эхо-КГ с учетом значения фракции выброса не менее 50%, обзорную рентгенографию органов грудной клетки, эхографическое исследование органов брюшной полости, трансректальное эхографическое исследование предстательной железы, мочевого пузыря.
Следующим этапом обследования была остеосцинтиграфия и компьютерная томография с исследованием органов брюшной полости, малого таза, регионарных и отдаленных лимфатических узлов. У всех больных качество жизни определялось оценкой статуса активности по системе Карновского и уровня болевого синдрома по четырехбальной системе, одобренной ВОЗ.
Статус активности больных до начала лечения.
| Градация | Активность по Карновскому, % |
| 80–100 | 21(50%) |
| 60–70 | 11(26,1%) |
| 50–60 | 8 (19,04%) |
| 30–50 | 2(4,7) |
Таким образом, 21 пациентов было включено со статусом активности 80–100%,11 со статусом активности 60–70% и 8 больных со статусом активности 50–60%,2 больных со статусом активности 30–50 по системе Карновского.
У всех пациентов к началу лечения имелось морфологическое подтверждение диагноза рака предстательной железы. В большинстве случаев это были низкодифференцированные формы рака. В 100% случаев мы столкнулись с различными вариантами аденокарциномы. Распределение по шкале Глисона было следующим: 4 балла у 1 больного, 5 баллов у 6 больных, 6 баллов- у 8 больных, 7 баллов у 11 больных,8 баллов 10 больных, 9 балов у 6 больных.
Возраст больных распределился между 60 и 84 годами. Средний возраст больных составил 72,2 + 11,8 лет. В возрасте 60 лет и старше было 78,4% пациентов. Комплексное обследование до начала проведения лечения позволило выявить у 33 больных (78,5%) пациентов сопутствующие заболевания различной степени тяжести. У 26 больных ведущее место занимали заболевания сердечно-сосудистой системы: гипертоническая болезнь различной степени (в т. ч. с перенесенным ОНМК в анамнезе), хроническая ишемическая болезнь сердца (в т. ч. с перенесенным инфарктом миокарда в анамнезе), общий атеросклероз, атеросклероз коронарных артерий и сосудов головного мозга, заболевания желудочно-кишечного тракта — хронический гастрит, хронический холецистопанкреатит, хронический колит, ожирение.
Абиратерон НВ, 250 мг, таблетки, 120 шт.
Прием препарата Абиратерон НВ одновременно с пищей значительно увеличивает всасывание абиратерона ацетата. Эффективность и безопасность препарата Абиратерон НВ, принятого с пищей, не установлена. Препарат Абиратерон НВ нельзя принимать с пищей.
Повышение артериального давления, гипокалиемия и задержка жидкости вследствие избытка минералокортикоидов
Препарат Абиратерон НВ может вызвать повышение артериального давления, гипокалиемию и задержку жидкости из-за повышения концентрации минералокортикоидов вследствие ингибирования фермента CYP17. Прием кортикостероидов ослабляет стимулирующее действие адренокортикотропного гормона (АКТГ), что приводит к снижению частоты и тяжести этих побочных реакций. Следует проявлять осторожность при лечении пациентов, клиническое состояние которых может ухудшиться при повышении артериального давления, развитии гипокалиемии или задержке жидкости в организме (например, у пациентов с сердечной недостаточностью, недавно перенесенным инфарктом миокарда или с желудочковой аритмией).
Препарат Абиратерон НВ следует с осторожностью назначать пациентам с сердечно-сосудистыми заболеваниями в анамнезе. Безопасность препарата у пациентов с фракцией выброса левого желудочка
Артериальное давление, концентрацию калия в плазме крови и степень задержки жидкости следует контролировать, как минимум, один раз в месяц.
Гепатотоксичность
В клинических исследованиях зарегистрировано выраженное повышение активности печеночных ферментов, требовавшее отмены или коррекции дозы препарата. Активность сывороточных трансаминаз и билирубина следует измерять до начала применения препарата Абиратерон, каждые 2 недели в первые 3 месяца лечения, а затем ежемесячно. При развитии клинических симптомов и признаков, позволяющих предположить нарушение функции печени, следует немедленно измерить активность сывороточных трансаминаз, в частности аланинаминотрансферазы. При повышении активности аланинаминотрансферазы в 5 раз выше верхней границы нормы или концентрации билирубина в 3 раза выше верхней границы нормы применение препарата Абиратерон НВ следует немедленно прекратить и тщательно контролировать функцию печени.
Препарат Абиратерон НВ можно применять снова только после возвращения показателей функции печени к исходным значениям и только при лечении более низкими дозами.
Если у пациентов в любой период терапии развивается тяжелая форма гепатотоксичности (активность аланинаминотрансферазы превышает верхнюю границу нормы в 20 раз), препарат Абиратерон НВ следует отменить, повторное назначение препарата у таких пациентов невозможно.
Коррекция дозы у пациентов с нарушением функции печени легкой степени не требуется. Нет данных об эффективности и безопасности неоднократного применения абиратерона ацетата у пациентов с нарушением функции печени умеренной или тяжелой степени (класс В или С по Чайлд-Пью), поэтому необходимость коррекции дозы невозможно предсказать. Препарат Абиратерон НВ следует применять с осторожностью у пациентов с нарушениями функциями печени умеренной степени, только в том случае, если польза от лечения явно превышает возможный риск. Препарат Абиратерон НВ нельзя назначать пациентам с нарушениями функции печени тяжелой степени.
Женщины детородного возраста
Препарат Абиратерон НВ не предназначен для применения у женщин. Предполагается, что прием ингибиторов CYP17 беременными женщинами изменит концентрацию гормонов, что может повлиять на развитие плода. Для предотвращения случайного воздействия беременные или способные забеременеть женщины не должны работать с препаратом без перчаток.
Контрацепция у мужчин и женщин
Неизвестно, присутствует ли абиратерона ацетат или его метаболиты в сперме. Необходимо использовать презерватив, если планируется половой акт с беременной женщиной. Если половой акт планируется с женщиной детородного возраста, необходимо использовать презерватив наряду с другими эффективными методами контрацепции.
Способность к зачатию
Исследования токсичности абиратерона ацетата для репродуктивной системы не проводились, данных о влиянии препарата на способность к зачатию нет.
Отмена глюкокортикостероидов и купирование стрессовых ситуации
При отмене преднизолона следует проявлять осторожность и контролировать признаки недостаточности функции коры надпочечников. Если применение препарата Абиратерон НВ продолжается после отмены глюкокортикостероидов, то следует контролировать появление симптомов избытка минералокортикоидов. У пациентов, получающих преднизолон, при развитии стрессовых ситуаций может потребоваться повышенная доза глюкокортикостероидов перед, во время и после стрессовой ситуации.
Одновременное назначение препарата Абиратерон НВ и химиотерапии
Безопасность и эффективность одновременного назначения препарата Абиратерон НВ и цитотоксической химиотерапии не установлены.
Информация о некоторых вспомогательных веществах, входящих в состав препарата Абиратерон НВ
Данный лекарственный препарат содержит 1 ммоль (27,2 мг) натрия в каждой дозе (4 табл.), что необходимо принимать во внимание при лечении пациентов, получающих диету с контролируемым содержанием натрия.
Влияние на способность к вождению автотранспорта и управлению механизмами
Препарат Абиратерон НВ не влияет или оказывает ничтожно малое влияние на способность управлять автомобилем и движущимися механизмами.
Сравнительная характеристика пациентов, в зависимости от уровня ПСА до начала лечения.
| ПСА < 10 нг/мл | 0(0%) |
| ПСА 10–50 нг/мл | 16(38,1%) |
| ПСА > 50 нг/мл | 26 (61,9%) |
Таким образом, основная масса больных имела уровень простатспецифического антигена больше 50 нг/мл (при норме до 4 нг/мл).
Суточная доза препарата Зитига для всех больных составляла 1 г (4 таб. по 250 мг) 1 раз/сут за 1 ч до еды или через 2 ч после еды.
Препарат Зитига применялся вместе с низкими дозами преднизолона. Рекомендуемая доза преднизолона составляла 10 мг/сут- ежедневно.
Больные с костными метастазами получали бисфосфонаты. Пациенты получали Золендроновую кислоту в дозе 4 мг в\в капельно с интервалом 28 дней.
До настоящего времени больным было проведено от 1 до 11,5 месяцев терапии абиратероном. По достижению 6 месяцев лечения оценивалась динамика проводимой терапии. В случае положительной динамики и функциональной сохранности пациента лечение продолжалось в прежнем режиме. Минимальное время проведения лечения — два месяца, максимальное — 11,5 месяцев.
На данный момент 2 пациента получили 2 курса, 6 пациентов 3 курса,2 пациента 4 курса, 4 пациента 5 курсов, 8 пациентов 6 курсов, 9 пациентов 7 курсов, 4 пациента 8 курсов,3 пациента 9 курсов, 2 пациента 10 курсов 1 больной 11 курсов и 1 больной 11,5 курсов. Шесть курсов и более получили 28 человек (66,6%). Среднее время лечения составило 8,25 мес.
Количество проведенных курсов химиотерапии
| До 6 мес | ≥ 6 мес | ≥11 мес | Ср. кол-во курсов | |
| Абиратерон | 14(33,3%) | 26(61,9%) | 2 (4,7%) | 7,42±1,01 |
Традиционным основополагающим критерием ответа в лечении рака предстательной железы является динамика уровня ПСА крови. В ответ на лечение, снижение уровня ПСА более чем на 50% от исходного, до начала лечения отмечено у 22 пациентов (52,3%). Из этого числа, снижение уровня ПСА ниже 80% зарегистрировано у 7 пациентов (16,6%). Стабилизация уровня ПСА отмечена у 9 пациентов (21,4%). Прогрессивный рост ПСА определялся у 11 больных (26,1%).
Ведущим критерием эффективности лекарственной химиотерапии является оценка динамики уровня ПСА. В зависимости от продолжительности цикла химиотерапии проводилась оценка уровня ПСА, каждые три недели (перед планируемым введением). Положительная динамика изменения уровня ПСА в ответ на проводимое лечение оценивалась нами как:
- снижение уровня ПСА на 50% от исходного до начала терапии;
- снижение уровня ПСА на 80% и более от исходного до начала терапии;
- повышение уровня ПСА, т. е. прогрессирование;
- стабилизация уровня ПСА, которая оценивалась как отсутствие прогрессирования с одной стороны и отсутствие снижения уровня ПСА на 50% и более с другой стороны.
Период ответа по уровню ПСА определялся от момента его снижения до возврата на первоначальный уровень и выше.
Для изучения объективного ответа со стороны костных метастазов оценка проводилась по системе M. S. Soloway. Критериями оценки по данным остеосцинтиграфии являлись:
- отсутствие новых очагов поражения;
- исчезновение ранее выявленных очагов поражения;
- снижение % накопления радиофармпрепарата в участках поражения костных тканей.
Для пациентов с поражением лимфатических узлов и висцеральными метастазами применялись критерии оценки регрессии измеряемых солидных опухолей (RECIST).
Оценка эффекта, показала следующие результаты: снижение уровня ПСА более чем на 50% зафиксировано у 22 пациентов, а снижение ПСА более чем на 80% у 7 больных.
Материал и методы
Исследование проводилось с 2013 г. по начало 2015 г. В него были включены 53 пациента с метастатическим КРРПЖ (мКРРПЖ), ранее получившие химиотерапию (ХТ) и антагонисты ЛГРГ.
В первой линии ХТ 35 пациентов с мКРРПЖ получали химиотерапию доцетакселом (5—21 курс) в дозе 85 мг/м2 со стандартной премедикацией дексаметазоном. У 8 пациентов была отмечена стойкая гематологическая токсичность (III—IV степени), в связи с чем лечение было отменено. Во второй линии ХТ 13 больных получили 5 курсов кабазитаксела 25 мг/м2 в комбинации с преднизолоном 10 мг в сутки. У 2 больных наблюдалась сильная гематологическая токсичность (анемия, нейтропения III степени).
В первой линии терапии 18 больных мКРРПЖ после прогрессирования заболевания на фоне лечения агонистами ЛГРГ и развития кастрационной резистентности получали антагонист ЛГРГ — дегареликс подкожно в начальной дозе 240 мг и поддерживающей дозе 80 мг. У 2 больных лечение было прекращено в связи с непереносимостью препарата (анемия, диарея, тошнота, приливы) (табл. 1).
Таблица 1. Предшествующая терапия
Всем больным, включенным в исследование, регулярно проводили лабораторные анализы: общий и биохимический анализ крови, определение уровня ПСА, тестостерона, ЭКГ, рентгенографию грудной клетки, трансректальное ультразвуковое исследование (УЗИ) предстательной железы, УЗИ брюшной полости и органов малого таза, а также остеосцинтиграфию и компьютерную томографию грудной клетки, органов брюшной полости, малого таза и регионарных и отдаленных лимфатических узлов.
Качество жизни больных оценивали на основе опросника EORTC, статуса активности по системе Карновского и уровню болевого синдрома по пятибалльной шкале.
В исследование были включены 24 больных со статусом активности по Карновскому 80—100%, 15 больных со статусом 60—70%, 10 больных со статусом 50—60% и 9 больных со статусом 30—50%.
Медиана возраста пациентов составляла 72,0±7,6 года. Распределение больных в зависимости от возраста: до 60 лет было 5 (9,4%) больных, 60—69 лет — 30 (56,6%), свыше 69 лет — 18 (33,9%) больных.
На момент начала исследования 47 (88,6%) больных предъявляли жалобы на нарушения мочеиспускания, 38 (71,6%) — на слабость, 14 (26,4%) — на боль различной локализации (табл. 2).
Таблица 2. Жалобы больных на момент начала исследования
С целью гистологической верификации диагноза до начала лечения была выполнена трансректальная биопсия предстательной железы с последующей оценкой дифференцировки опухоли по шкале Глисона. Всем больным, которым была выполнена биопсия, за 1 день до процедуры были назначены антибиотики широкого спектра для профилактики инфекционных осложнений. По результатам биопсии у всех (100%) больных выявлена аденокарцинома и определена степень дифференцировки по шкале Глисона: менее 7 — 7 (13,2%), 7 — 28 (52,8%), более 7 — 18 (34%).
Средняя концентрация ПСА до начала исследования составила 134 (6,7—497) нг/мл (табл. 3).
Таблица 3. Распределение больных в зависимости от уровня ПСА до начала исследования
Распространенность опухолевого процесса была оценена на основе классификации TNM. Из 53 больных, включенных в исследование, стадия T2 была у 6 (11,3%) больных, T3 — у 29 (54,7%), T4 — у 18 (33,9%) (табл. 4).
Таблица 4. Распределение больных в зависимости от категории Т по классификации TNM
Отдаленные метастазы (M1) выявлены у всех больных, включенных в исследование (100%). Метастазы в лимфатических узлах (N1) обнаружены у 36 (67,9%) больных, в костях — у всех больных: 23 (43,3%) из них имели менее пяти метастатических очагов, 30 (56,7%) — более пяти очагов, метастазы в легких имели 27 (50,9%) больных (табл. 5).
Таблица 5. Распределение больных в зависимости от локализации метастазов
У всех 53 пациентов в качестве следующей линии терапии использовали препарат абиратерон ацетат (зитига). Абиратерон применяли в суточной дозе 1000 мг (4 таблетки по 250 мг) за 1 ч до приема пищи или через 2 ч после приема пищи вместе с преднизолоном в дозе 10 мг в день.
В связи с костными метастазами больные получали бисфосфонаты (золендроновую кислоту в дозе 4 мг внутривенно капельно каждые 28 дней) или деносумаб в дозе 170 мл подкожно каждые 4 нед.
Каждые 6 мес терапии оценивали динамику лечения и функциональный статус больных. В случае положительной динамики и отсутствия функционального ухудшения терапию продолжали в прежнем режиме. Минимальный курс терапии составил 3 мес, максимальный 1 год, среднее время лечения составило 7,26 курса (табл. 6). Следует отметить, что наши результаты сопоставимы с литературными данными о терапии абиратероном во второй линии терапии мКРРПЖ [12]. При этом можно ожидать, что длительность терапии составила в среднем более 15 мес, если бы лечение абиратероном было начато в первой линии терапии мКРРПЖ [9].
Таблица 6. Длительность терапии абиратероном
Уровень ПСА определяли каждые 3 нед. Положительная динамика уровня ПСА расценивалась как снижение его на 50% и более от исходного до начала терапии абиратероном, стабилизация уровня ПСА оценивалась как отсутствие прогрессирования и снижения уровня ПСА на 50% и более. Период ответа на лечение определялся от момента снижения уровня ПСА до его возврата на первоначальный уровень и выше.
Результаты изменения ПСА в группе монотерапии Абиратероном
| Динамика ПСА | |
| Снижение ПСА>80% (%) | 7(16,6%) |
| Снижение ПСА >50% (%) | 22(52,3%) |
| Стабилизация ПСА | 9(21,4%) |
| Прогрессирование ПСА | 11(26,1%) |
Таким образом, общий ответ по уровню ПСА отмечен у 31 пациента (73,8%). Было отмечено, что у 11 пациентов с положительной динамикой ПСА произошла стабилизация патологических процессов в костной системе, у 6 больных стабилизация отмечена в лимфатической системе, частичная регрессия лимфоузлов отмечена у 4 больных; у 6 больных с метастатическим поражением легких, в том числе и 1 больной с поражением плевры- отмечена стабилизация процесса у 2 больных частичный эффект в виде уменьшения количества и размеров метастатических очагов.
У 11 пациентов отмечено прогрессирующее повышение уровня ПСА, из них у 5 больных отмечено прогрессирование со стороны костных метастазов, у 2 больных прогрессирование заболевания со стороны лимфатической системы, у 3 больных появились, увеличились и появились новые очаги в легких, у 1 больного отмечено стойкое повышение Пса без признаков висцеральных и костных метастазов.
Следовательно, с точки зрения изменения ПСА можно утверждать о статистической достоверности эффективности лечения.
Ответ на лечение пациентов с депозитами в костной системе в виде стабилизации процесса имелся в 11 случаях из 16 (68,7%). Отмечалась стабилизация патологических процессов в костном метастатическом очаге по данным остеосцинтиографии. Фиксировалось отсутствие новых очагов накопления радиофармпрепарата по окончанию лечения.
В связи с прогрессированием опухолевого процесса в костях после проведенных 3х курсов х/терапии 5 пациентов были переведены на другие варианты лечения, также у этих больных было зафиксировано стойкое повышение ПСА.
Определяющий критерий эффективности ХТ представлен продолжительностью жизни больных после окончания лечения, которая составила 11,5 мес.
Нами проанализированы показатели одногодичной выживаемости. Одногодичная выживаемость составила 71,4%.
Следует обратить внимание на тот факт, что у 4-х больных отмечен частичный эффект на терапию Абиратероном и все эти больные в 1-ой линии х\терапии получали Таксотер и были сняты с лечения в связи с развитием различного рода токсичности.
У 23-х больных отмечена стабилизация процесса, из них 8 больных получали в 1-ой линии х\терапии Таксотер, лечение было прекращено в связи с развитием различного рода токсичности, 13 больных получивших в 1-ой линии Таксотер переведены на Абиратерон в связи с развитием прогрессирования заболевания. А еще у 2-х больных отмечена стабилизация процесса после Кабазитаксела во 2-ой лини химиотерапии.
Таким образом ответ на лечение Абиратероном был выше у тех больных которые были сняты с лечения Таксанами по причине токсичности, а не по причине прогрессирования заболевания.
Среди нежелательных явлений I–II степени мы наиболее часто (≥10%) отмечали периферические отеки, гипокалиемия, повышение АД, инфекции мочевыводящих путей, увеличение активности АЛТ или АСТ.
Нежелательные реакции систематизированы относительно каждой из систем органов с использованием следующей классификации частоты встречаемости: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10 000,<1/1000), очень редко (<1/10 000, включая единичные случаи).
Летальные исходы по причине прогрессирования болезни, в течение 30 дней с момента приема последней дозы исследуемого препарата отмечены не были.
Редукция дозы Абиратерона не проводилась. В случае развития у 4 больных токсического эффекта (печеночной и кардиотоксичности) препарат был отменен.
У 3 больных отмечена печеночная токсичность III–IV ст, у 2 больных после 3 курса и у 1 больного после 5 курса, в виде повышения уровня билирубина, а также печеночных трансаминаз, которая не купировалась гепатопротекторной терапией более 23 дней. У 6 больных наблюдалась печеночная токсичность I–II ст, успешно купировалась применение гепатопротекторов.
У 1 пациента после проведения 3-х курсов лечения была отмечена левожелудочковая недостаточность, уменьшение ФВ левого желудочка до 38%, стенокардия напряжения 2 ф.к. Лечение было приостановлено, больному поводилась кардиопротекторная терапия в течении 46 дней, по истечении которых при контрольном обследовании было выявлено прогрессирование заболевания в виде роста ПСА, также у этого больного было отмечено прогрессирование метастазов в костях.
Самым частым токсическим осложнением являлись периферические отеки 1–2 степени у 19 пациентов (45,2%). Отеки носили преходящий характер на фоне проведения лечения, после прекращения лечения у 2 больных в связи с развитием печеночной токсичности и у 1 одного больного в связи с кардиотоксичностью, а также у 8 больных, выбывших в связи с прогрессированием заболевания, отеки самостоятельно купировались без применения медикаментозного лечения, у 3-х больных выбывших в связи с прогрессированием заболевания, отеки сохранялись на протяжении более 25 дней этим пациентам была проведена мочегонная терапия, с полным эффектом. Объективного ухудшения состояния больных не приносили. Вторым по частоте побочным эффектам была гипокалиемия, которая имела место у 18 пациентов (42,8%), в 7-ми случаях сопровождаясь тахикардией, 11 больных перенесли бессимптомно. Проводилась сопроводительная терапия инфузионным введением Калия хлорида 0,4% 20 мл в\в кап до нормализации показателей, с последующим перманентным пероральным приемом Панангина.
Аналогичный умеренный характер носила артериальная гипертензия, наблюдалась у 16 пациентов, которая успешно купировалась приемом ИАПФ эналаприл 2,5 мг х 2 раза в день перорально перманентно длительно.
Тошнота наблюдалось у 12 больных, успешно купирована приемом метоклопрамида 10 мг х 4 раза в день перорально длительно у 8 больных, 4 больным была проведена противорвотная терапия ондансетроном 16 мг в сутки парентерально, до купирования симптомов с дальнейшим поддерживающим режимом 8 мг в сутки перорально.
Инфекции мочевыводящих путей отмечена у 14 больных лечение проводилось нитроксолином 600 мг х 3 раза в сутки перорально, в 9 случаях, на 7–10 день лечения наступало полное выздоровление, у 5 пациентов не принесло должного эффекта, проводилась терапия урофосфаболом в сочетании с уросептиками, однако у 3 больных сохранялась стойкая бактериурия в связи, с чем лечение Абиратероном было остановлено, у 2 больных во время проведения высокодозной антибактериальной терапии было отмечено стойкое повышение креатинина, в связи с чем лечение Абиратероном также было прекращено.
Стенокардия отмечена у 6 больных, в 5 случаях успешно купировалась пероральным приемом нитроглицерина, в одном случае введение нитроглицерина было парентеральным.
В общем, имели место предполагаемые побочные эффекты данного режима ХТ, контролируемые этиотропной и симптоматической терапией.
Результаты
Критерием ответа на лечение являлась динамика уровня ПСА крови. В нашем исследовании снижение уровня ПСА более чем на 50% от исходного было отмечено у 27 (50,9%) пациентов. В данной группе снижение уровня ПСА ниже 80% наблюдалось у 15 (28,3%) пациентов. Стабилизация ПСА отмечена у 14 (26,4%) больных. Прогрессивный рост ПСА был отмечен у 12 (22,7%) больных. Общий ответ по уровню ПСА отмечен у 40 (75,4%) больных.
Таким образом, мы можем предположить, что изменение уровня ПСА на фоне лечения абиратероном отображает клиническую эффективность терапии.
В связи с прогрессированием опухолевого процесса и стойкого повышения уровня ПСА после 4 курсов терапии у 7 больных лечение пришлось прекратить и перевести их на другие виды терапии.
Объективный ответ костных метастатических очагов на терапию оценивался по системе Soloway. Критериями оценки являлись: отсутствие новых костных очагов, исчезновение ранее выявленных очагов, процентное снижение накопления радиофармпрепарата в пораженных костях.
Для пациентов с метастазами в лимфатических узлах и легких ответ на лечение был определен по критериям оценки ответа на терапию солидных опухолей (RECIST 1.1).
При анализе проведенного исследования отмечено, что частичный ответ на терапию давали как больные, которые получали дегареликс, так и больные, которые получали одну или более линий ХТ таксанами. Ответ также наблюдали среди больных, которым ХТ таксанами была отменена вследствие непереносимости.
Проанализирован спектр нежелательных явлений на фоне терапии абиратероном. Наиболее часто (более 10%) отмечали периферические отеки, повышение АД, инфекции мочевыводящих путей, повышение печеночных ферментов (I—II степень). При этом большинство нежелательных явлений легко купировались, и терапия соответствовала благоприятному профилю безопасности.
Не было отмечено летальных исходов вследствие прогрессирования заболевания в течение 30 дней с момента приема последней дозы абиратерона. В ходе исследования дозу препарата не корректировали, в 6 случаях препарат был отменен по причине непереносимости (печеночная и кардиотоксичность III степени). У больных, которым препарат был отменен, на контрольном обследовании по поводу сопутствующей патологии отмечены прогрессирование костных очагов и стойкий рост уровня ПСА.
Другие нежелательные явления, такие как тошнота, рвота, слабость и боль, успешно купировались приемом метоклопрамида, ондасетрона и анальгетиков. Больным с инфекциями мочевыводящих путей успешно проводилась антибиотикотерапия фторхинолонами. Можно сделать вывод, что нежелательные явления на фоне терапии абиратероном соответствовали благоприятному профилю безопасности препарата.
Динамику болевого статуса больных оценивали по 5-балльной шкале до лечения абиратероном и после (табл. 7).
Таблица 7. Динамика болевого статуса больных
В ходе лечения было отмечено, что 12 больных перестали принимать анальгетики на фоне проводимой терапии, 3 пациента отказались от приема наркотических анальгетиков, а 2 стали принимать наркотические препараты реже.
Отмечена положительная динамика в изменении статуса активности больных (табл. 8). После проведенного анализа отмечено, что у 14 больных произошло изменение статуса активности в лучшую сторону.
Таблица 8. Динамика статуса активности больных
Проявление токсичности режима монотерапии Абиротероном
| Токсичность | 1 ст. | 2 ст. | 3 ст. | 4 ст. |
| Инфекционные заболевания: — инфекции мочевыводящих путей | 6 | 3 | 5 | 0 |
| Со стороны эндокринной системы: — недостаточность функции н\поч | 0 | 0 | 0 | 0 |
| Со стороны лабораторных показателей: — гипокалиемия, — гипертриглицеридемия, — повышение активности АЛТ или АСТ. | 11 1 4 | 7 0 2 | 0 0 0 | 0 0 2 |
| Со стороны костно-мышечной системы и соединительной ткани: — переломы | 0 | 0 | 0 | 0 |
| Со стороны почек и мочевыводящих путей: — гематурия | 0 | 0 | 0 | 0 |
| Со стороны сердечно-сосудистой системы: — повышение АД; — левожелудочковая недостаточность, — уменьшение фракции — левого желудочка, — стенокардия — аритмия — фибрилляция предсердий — тахикардия | 12 0 0 4 0 0 7 | 4 0 0 1 0 0 0 | 0 0 1 1 0 0 0 | 0 1 0 1 0 0 0 |
| Со стороны пищеварительной системы: — диспепсия | 2 | 0 | 0 | 0 |
| Общие нарушения: — периферические отеки | 7 | 9 | 3 | 0 |
Качество жизни пациентов при монотерапии Абиратероном представлено ниже:
Абиратероном
| Градация боли | Количество пациентов | |
| До лечения | После лечения | |
| 0 — аналгетики не требуются | 11(26,1%) | 24(57,1%) |
| 1 — иногда ненаркотические | 14(33,3%) | 10(23,8%) |
| 2 — регулярно ненаркотические | 12(28,5%) | 7(16,6%) |
| 3 — иногда наркотические | 3(7,1%) | 1(2,4%) |
| 4 — регулярно наркотические | 2(4,7) | 0 |
Как видно из полученных данных количество пациентов, не требующих приема аналгетических препаратов, увеличилось на 13 человек 30,9% на фоне проводимой терапии. В тоже время мы смогли добиться полного отказа от регулярного приема наркотических препаратов у 1 больного, 1 больной ранее регулярно получавший наркотическую анальгезию не смог полностью отказаться от приема наркотических препаратов, но снизил прием до 1 раза в сутки (ранее получал 2 раза в сутки), 3 больных ранее получавших нерегулярную наркотическую анальгезию, смогли полностью от нее отказаться в пользу не наркотической.
Положительная динамика в данной группе наблюдалась также и в изменении статуса активности больных.
Абиратерон (Abiraterone)
Прием абиратерона одновременно с пищей значительно увеличивает всасывание абиратерона. Эффективность и безопасность абиратерона, принятого с пищей, не установлена. Абиратерон нельзя принимать с пищей.
Повышение артериального давления, гипокалиемия, задержка жидкости и сердечная недостаточность вследствие избытка минералокортикоидов
Абиратерон может вызвать повышение артериального давления, гипокалиемию и задержку жидкости из-за повышения концентрации минералокортикоидов вследствие ингибирования фермента CYP17. Прием кортикостероидов ослабляет стимулирующее действие адренокортикотропного гормона (АКТГ), что приводит к снижению частоты и тяжести этих побочных реакций. Следует проявлять осторожность при лечении пациентов, клиническое состояние которых может ухудшиться при повышении артериального давления, развитии гипокалиемии или задержке жидкости в организме (например, у пациентов с сердечной недостаточностью, недавно перенесенным инфарктом миокарда или с желудочковой аритмией).
Абиратерон следует с осторожностью назначать пациентам с сердечно-сосудистыми заболеваниями в анамнезе. Безопасность препарата у пациентов с фракцией выброса левого желудочка < 50% или с сердечной недостаточностью III-IV функционального класса по классификации NYHA не установлена.
Перед началом применения абиратерона следует скорректировать гипокалиемию и повышение артериального давления.
Артериальное давление, концентрацию калия в плазме крови и степень задержки жидкости следует контролировать, как минимум, 1 раз в месяц.
Гепатотоксичностъ и нарушение функции печени
В клинических исследованиях зарегистрировано выраженное повышение активности печеночных ферментов, требовавшее отмены или коррекции дозы препарата. Активность сывороточных трансаминаз и билирубина следует измерять до начала применения абиратерона, каждые 2 недели в течение первых 3 месяцев лечения, а затем ежемесячно. При развитии клинических симптомов и признаков, позволяющих предположить нарушение функции печени, следует немедленно измерить активность сывороточных трансаминаз.
При повышении активности аланинаминотрансферазы или аспартатаминотрансферазы в 5 раз выше верхней границы нормы или концентрации билирубина в 3 раза выше верхней границы нормы применение абиратерона следует немедленно прекратить, и следует тщательно контролировать функцию печени. Абиратерон можно применять снова только после возвращения показателей функции печени к исходным значениям, и только при условии назначения более низких доз.
Если у пациентов в любой период терапии развивается тяжелая форма гепатотоксичности (активность аланинаминотрансферазы или аспартатаминотрансферазы превышает верхнюю границу нормы в 20 раз), абиратерон следует отменить, повторное назначение препарата у таких пациентов невозможно.
Коррекция дозы у пациентов с нарушением функции печени легкой степени не требуется. Нет данных об эффективности и безопасности неоднократного применения абиратерона ацетата у пациентов с нарушением функции печени умеренной или тяжелой степени (класс В или С по Чайлд-Пью), поэтому необходимость коррекции дозы невозможно предсказать. Абиратерон нельзя назначать пациентам с нарушением функции печени средней и тяжелой степени.
Женщины детородного возраста
Абиратерон не предназначен для применения у женщин. Предполагается, что прием ингибиторов CYP17 беременными женщинами изменит концентрацию гормонов, что может повлиять на развитие плода. Для предотвращения случайного воздействия беременные или способные забеременеть женщины не должны работать с препаратом без перчаток.
Контрацепция у мужчин и женщин
Неизвестно, присутствует ли абиратерон или его метаболиты в сперме. Необходимо использовать презерватив, если планируется половой акт с беременной женщиной. Если половой акт планируется с женщиной детородного возраста, необходимо использовать презерватив наряду с другими эффективными методами контрацепции.
Способность к зачатию
Исследований токсического воздействия абиратерона ацетата на репродуктивную систему не проводилось, данных о влиянии препарата на способность к зачатию нет.
Отмена глюкокортикостероидов и купирование стрессовых ситуаций
При отмене преднизолона следует проявлять осторожность и контролировать признаки недостаточности функции коры надпочечников. Если применение абиратерона продолжается после отмены глюкокортикостероидов, то следует контролировать появление симптомов избытка минералокортикоидов. У пациентов, получающих преднизолон, при развитии стрессовых ситуаций может потребоваться повышенная доза глюкокортикостероидов перед, во время и после стрессовой ситуации.
Плотность костной ткани
У мужчин с метастатическим кастрационно-резистентным раком предстательной железы может наблюдаться снижение плотности костной ткани. При одновременном применении абиратерона и глюкокортикостероидов этот эффект может усиливаться.
Предшествующее применение кетоконазола
У пациентов, ранее получавших кетоконазол для терапии рака простаты, можно ожидать более низкий уровень ответа на терапию абиратероном.
Гипергликемия
Применение глюкокортикостероидов может приводить к гипергликемии, поэтому у пациентов с сахарным диабетом необходимо часто измерять концентрацию сахара в крови.
Одновременное назначение абиратерона и химиотерапии
Безопасность и эффективность одновременного назначения абиратерона и цитотоксической химиотерапии не установлены.
Влияние на костно-мышечную систему
При применении абиратерона были зарегистрированы случаи миопатии. У некоторых пациентов наблюдался рабдомиолиз с почечной недостаточностью. В большинстве случаев указанные состояния развивались в течение первого месяца лечения, а после отмены абиратерона происходило восстановление. Следует соблюдать осторожность при одновременном применении абиратерона и других препаратов, способных вызвать миопатию/рабдомиолиз.
Динамика статуса активности больных в группе монотерапии Абиратероном
| Градация | Количество пациентов | |
| До лечения | После лечения | |
| 80–100 | 21(50%) | 26(61,9%) |
| 60–70 | 11(26,1%) | 8(19,04%) |
| 50–60 | 8(19,04%) | 9(21,4%) |
| 30–50 | 2(4,7%) | 0 |
| < 30 | 0 | 0 |
Изменение статуса активности в положительную сторону произошло у 6 пациентов (14,2%).
Таким образом, последовательное назначение таксанов — доцетаксел (Таксотер) в первой линии, кабазитаксел во второй линии, абиратерон во 2 и 3 линии терапии — позволяет увеличить продолжительность жизни больных с метастатическим РПЖ и повысить качество их жизни.
Авторы: И. Г. Русаков, Т. Н. Скворцова, С. В. Мишугин.