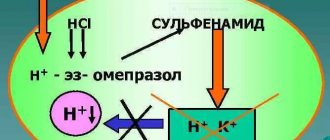
Симбикорт турбухалер
Симбикорт® Турбухалер® не предназначен для первоначального лечения бронхиальной астмы интермиттирующего и легкого персистирующего течения.
Подбор дозы препаратов, входящих в состав Симбикорта Турбухалера, проводится индивидуально и в зависимости от степени тяжести заболевания. Это необходимо учитывать не только при начале лечения комбинированными препаратами, но и при изменении дозы препарата.
В том случае, если отдельным пациентам требуется иная комбинация доз активных веществ, чем в препарате Симбикорт® Турбухалер®, следует назначить отдельно бета2-адреномиметики и/или ГКС в отдельных ингаляторах.
Бронхиальная астма
Симбикорт® Турбухалер® 80/4.5 мкг/доза и 160/4.5 мкг/доза
Пациенты должны находиться под постоянным контролем врача для адекватного подбора дозы Симбикорта Турбухалера. Дозу следует снизить до наименьшей, на фоне которой сохраняется оптимальный контроль симптомов бронхиальной астмы. При достижении полного контроля над симптомами бронхиальной астмы на фоне минимальной рекомендуемой дозы препарата, на следующем этапе можно попробовать назначение монотерапии ингаляционными ГКС.
Существуют два подхода к назначению терапии Симбикортом Турбухалером:
- в качестве поддерживающей терапии Симбикорт® Турбухалер® назначаетсядля постоянной поддерживающей терапии в комбинации с отдельным бета2-адреностимулятором короткого действия для купирования приступов;
- в качестве поддерживающей терапии и для купирования приступов Симбикорт® Турбухалер® назначается как для постоянной поддерживающей терапии, так и по требованию при появлении симптомов.
В качестве поддерживающей терапии
Пациенту необходимо постоянно иметь при себе отдельный ингалятор с бета2-адреностимулятором короткого действия для купирования приступов.
Взрослым (18 лет и старше) назначают Симбикорт® Турбухалер® 80/4.5 мкг/доза и 160/4.5 мкг/доза по 1-2 ингаляции 2 раза/сут. При необходимости возможно увеличение дозы до 4 ингаляций 2 раза/сут.
Подросткам (12-17 лет) назначают Симбикорт® Турбухалер® 80/4.5 мкг/доза и 160/4.5 мкг/доза по 1-2 ингаляции 2 раза/сут.
Детям в возрасте старше 6 лет назначают Симбикорт® Турбухалер® 80/4.5 мкг/доза по 1-2 ингаляции 2 раза/сут.
После достижения оптимального контроля симптомов бронхиальной астмы на фоне приема препарата 2 раза/сут рекомендуется титровать дозу до наименьшей эффективной, вплоть до приема 1 раз/сут, в тех случаях, когда по мнению врача пациенту требуется поддерживающая терапия в комбинации с бронходилататорами длительного действия.
Увеличение частоты применения бета2-адреностимуляторов короткого действия является показателем ухудшения общего контроля над заболеванием и требует пересмотра противоастматической терапии.
В качестве поддерживающей терапии и для купирования приступов
Пациенту необходимо постоянно иметь при себе Симбикорт® Турбухалер® для купирования приступов.
В данном случае препарат особенно показан пациентам с недостаточным контролем над бронхиальной астмой и необходимостью в частом использовании препаратов для купирования приступов; при указаниях в анамнезе обострений бронхиальной астмы, требовавших медицинского вмешательства.
Требуется тщательно контролировать появление дозозависимых побочных эффектов у пациентов, использующих большое количество ингаляций для купирования приступов.
Взрослым (18 лет и старше) назначают Симбикорт® Турбухалер® 80/4.5 мкг/доза и 160/4.5 мкг/доза; рекомендуемая доза — 2 ингаляции в сутки: по 1 ингаляции утром и вечером, или 2 ингаляции 1 раз/сут только утром или только вечером. Некоторым пациентам может быть назначена поддерживающая доза препарата Симбикорт® Турбухалер® 160/4.5 мкг/доза 2 ингаляции 2 раза/сут. При возникновении симптомов необходимо назначение 1 дополнительной ингаляции. При дальнейшем нарастании симптомов в течение нескольких минут назначают еще 1 дополнительную ингаляцию, но не более 6 ингаляций для купирования 1 приступа.
Обычно не требуется назначения более 8 ингаляций в сутки, однако можно увеличить число ингаляций до 12 в сутки на непродолжительное время. У пациентов, которые применяют более 8 ингаляций в сутки, рекомендуется пересмотр терапии.
Симбикорт® Турбухалер® 80/4.5 мкг/доза и 160/4.5 мкг/доза в качестве поддерживающей терапии и для купирования приступов не рекомендуется детям и подросткам в возрасте до 18 лет.
Симбикорт® Турбухалер® 320/9 мкг/доза
Взрослым (18 лет и старше) препарат назначают по 1 ингаляции 2 раза/сут. При необходимости возможно увеличение дозы до 2 ингаляций 2 раза/сут. После достижения оптимального контроля симптомов бронхиальной астмы на фоне приема препарата 2 раза/сут рекомендуется титровать дозу до наименьшей эффективной, вплоть до приема 1 раз/сут.
Подросткам в возрасте 12-17 лет назначают по 1 ингаляции 2 раза/сут.
Симбикорт® Турбухалер® 320/9 мкг/доза не рекомендован детям в возрасте до 12 лет ввиду отсутствия клинических данных.
Пациентам следует регулярно посещать врача для контроля оптимальной дозы препарата. Дозу следует снизить до наименьшей, на фоне которой сохраняется оптимальный контроль симптомов бронхиальной астмы. После достижения оптимального контроля симптомов бронхиальной астмы на фоне приема препарата 2 раза/сут рекомендуется титровать дозу до наименьшей эффективной, вплоть до приема 1 раз/сут, в тех случаях, когда по мнению врача пациенту требуется поддерживающая терапия в комбинации с бронходилататорами длительного действия.
ХОБЛ
Взрослым назначают Симбикорт® Турбухалер® 160/4.5 мкг/доза по 2 ингаляции 2 раза/сут или Симбикорт® Турбухалер® 320/9 мкг/доза по 1 ингаляции 2 раза/сут.
Нет необходимости в специальном подборе дозы препарата для пациентов пожилого возраста.
Нет данных о применении Симбикорта Турбухалера у пациентов с почечной или печеночной недостаточностью. Т.к. будесонид и формотерол выводятся главным образом при участии печеночного метаболизма, то у пациентов с тяжелым циррозом печени можно ожидать замедления скорости выведения препарата.
Правила использования турбухалера
Механизм действия турбухалера таков, что когда пациент вдыхает через мундштук, потоки воздуха увлекают за собой лекарственное вещество в дыхательные пути.
Необходимо инструктировать пациента:
- внимательно изучить «Инструкцию по применению» турбухалера;
- вдыхать сильно и глубоко через мундштук, чтобы гарантировать попадание оптимальной дозы препарата в легкие;
- никогда не выдыхать через мундштук;
- для того чтобы минимизировать возможность развития грибкового поражения ротоглотки, полоскать рот водой после каждой ингаляции. Также необходимо полоскать рот водой после проведения ингаляций для купирования симптомов и в случае развития кандидоза слизистой оболочки полости рта и глотки.
Пациент может не почувствовать вкус или не ощутить препарат после использования турбухалера, что обусловлено небольшим количеством доставляемого вещества.
Инструкция по применению турбухалера
Турбухалер- многодозовый ингалятор, позволяющий дозировать и вдыхать препарат в очень маленьких дозах. При вдохе порошок из турбухалера доставляется в легкие, поэтому важно, чтобы пациент сильно и глубоко вдохнул через мундштук.
Перед первым использованием турбухалер необходимо подготовить к работе:
1. Отвинтить и снять колпачок.
2. Держать ингалятор вертикально красным дозатором вниз. Не держать ингалятор за мундштук во время поворота дозатора. Повернуть дозатор до упора в одном направлении, а затем также до упора — в противоположном направлении. Выполнить описанную процедуру дважды.
Теперь ингалятор готов к использованию, повторять данную процедуру подготовки турбухалера к работе перед каждым использованием не требуется.
Для приема одной дозы пациент должен выполнить следующую процедуру:
1. Отвинтить и снять колпачок.
2. Держать ингалятор вертикально красным дозатором вниз. Не держать ингалятор за мундштук во время поворота дозатора. Для того, чтобы отмерить дозу, повернуть дозатор до упора в одном направлении, а затем также до упора — в противоположном направлении. Во время этой процедуры будет слышен щелчок.
3. Выдохнуть. Не выдыхать через мундштук.
4. Осторожно поместите мундштук между зубами, сожмите губы и вдохните сильно и глубоко через рот. Мундштук не жевать и не сжимать зубами.
5. Перед тем как выдохнуть, выньте ингалятор изо рта.
6. Если требуется ингаляция более чем одной дозы, следует повторить пп. 2-5.
7. Закрыть ингалятор колпачком, проверить, чтобы колпачок ингалятора был тщательно завинчен.
8. Прополоскать рот водой, не глотая.
Нельзя снимать мундштук, т.к. он закреплен на ингаляторе и не снимается. Мундштук турбухалера вращается, но не следует поворачивать его без необходимости.
Поскольку количество вдыхаемого порошка очень мало, можно не почувствовать вкус порошка после ингаляции.
Однако абсолютно точное соблюдение инструкции обеспечивает вдыхание (ингалирование) необходимой дозы препарата.
Если перед приемом препарата по ошибке была повторена процедура для загрузки ингалятора больше чем один раз, то при ингаляции пациентов все равно получит одну дозу препарата. При этом индикатор доз покажет общее количество отмеренных доз.
Звук, который слышен при потряхивании ингалятора, производится осушающим агентом, а не лекарственным веществом.
Необходимость замены ингалятора
Индикатор доз показывает приблизительное количество доз, оставшихся в ингаляторе, отсчет доз по заполнению турбухалера начинается с 60-й или 120-й дозы (в зависимости от общего количества доз приобретенного турбухалера). Индикатор показывает интервал в 10 доз, поэтому он не показывает каждую отмеренную (загруженную) дозу.
Турбухалер доставляет необходимую дозу препарата, даже если не заметны изменения в окне индикатора доз.
Появление красного фона в окне индикатора доз означает, что в турбухалере осталось 10 доз препарата. При появлении цифры 0 на красном фоне в середине окна доз ингалятор следует выбросить.
Следует обратить внимание на то, что даже когда окно индикатора показывает цифру 0, дозатор продолжает поворачиваться. Однако индикатор доз прекращает фиксировать количество доз (престает двигаться) и в окне доз ингалятора остается цифра 0.
Очистка
Регулярно (1 раз в неделю) следует очищать мундштук снаружи сухой тканью. Не использовать воду или другие жидкости для очистки мундштука.
Утилизация
Следует соблюдать осторожность при обращении с использованным ингалятором и помнить о том, что внутри ингалятора может оставаться некоторое количество препарата.
Передозировка
Симптомы: при острой передозировке будесонида, даже в значительных дозах, не ожидается клинически значимых симптомов. При хроническом приеме будесонида в чрезмерных дозах может проявиться системное действие ГКС, такое как гиперкортицизм и подавление функции надпочечников.
При передозировке формотерола — тремор, головная боль, учащенное сердцебиение; в отдельных случаях сообщалось о развитии тахикардии, гипергликемии, гипокалиемии, удлинении интервала QTc, аритмии, тошноты, рвоты.
При острой бронхиальной обструкции прием формотерола в дозе 90 мкг в течение 3 ч был безопасен.
Лечение: показано поддерживающее и симптоматическое лечение.
В случае необходимости отмены Симбикорта Турбухалера вследствие передозировки формотерола, входящего и состав комбинированного препарата, следует рассмотреть вопрос о назначении соответствующего ГКС.
Симбикорт в лечении больных стабильной ХОБЛ
Достижения в области изучения и терапии хронической обструктивной болезни легких (ХОБЛ) в течение последних лет позволили рассматривать ее как заболевание, которое можно предупредить и лечить [1]. Парадокс ХОБЛ заключается в том, что до сих пор не найдено эффективных средств противовоспалительной терапии этого заболевания, имеющего в своей основе хроническое воспаление, которое приводит к структурным изменениям в проксимальных и дистальных отделах бронхов, паренхиме и сосудах легких. Воспаление при ХОБЛ имеет свои особенности, отличающие ее от других заболеваний. Центральное место в патогенезе бронхиальной астмы (БА) принадлежит эозинофилам, тучным клетка и CD4+ лимфоцитам. ХОБЛ в отличие от БА характеризуется воспалительной реакцией с участием нейтрофилов, макрофагов и CD8+ лимфоцитов. Различия механизмов воспаления при ХОБЛ и БА лежат в основе значительных отличий патоморфологических изменений, симптомов и подходов к лечению. БА свойственна преходящая бронхоконстрикция, и воспалительный процесс хорошо поддается кортикостероидной терапии, как топической, так и системной. В случае ХОБЛ имеет место прогрессирующее, мало обратимое сужение бронхов и формирование эмфиземы [2]. Нестероидные противовоспалительные средства и антилейкотриеновые препараты при ХОБЛ не эффективны. Антибиотики и системные кортикостероиды целесообразно применять при обострениях, но не для лечения стабильной ХОБЛ. Ингаляционные глюкокортикостероиды при ХОБЛ Если при БА, начиная со 2 ступени тяжести заболевания (т.е. у большинства пациентов), доказана целесообразность длительного регулярного применения ингаляционных глюкокортикостероидов (ИГКС) в качестве базисной терапии, то при ХОБЛ показания для ИГКС терапии, приведенные в последней редакции руководства GOLD 2006 г., обоснованные данными доказательной медицины, распространяются только на больных с III (тяжелой) стадией заболевания, протекающего с частыми (более 1 в год) обострениями. У названной категории пациентов добавление к терапии ИГКС уменьшает частоту обострений и улучшает состояние здоровья. Предполагается, что длительная ИГКС терапия способствует снижению смертности от всех причин среди больных ХОБЛ, но для уточнения этого положения требуются дополнительные проспективные исследования. Безопасность длительной терапии ИГКС также требует дальнейшего изучения [1]. Проведенный недавно мета–анализ результатов 47 первичных исследований, включавших в общей сложности 13139 пациентов, подтвердил перечисленные выше положения GOLD. ИГКС терапия длительностью от 2 до 6 месяцев у больных ХОБЛ приводила к небольшому увеличению ОФВ1. Длительная (более 6 месяцев) ИГКС терапия в сравнении с плацебо не замедляла темпов падения ОФВ1 и не приводила к уменьшению смертности среди пациентов, но сокращала частоту обострений ХОБЛ и темпы ухудшения индекса качества жизни по данным респираторного вопросника Св. Георгия. Эффект терапии ИГКС нельзя было предсказать на основании результата лечения системными кортикостероидами, ответа на бронходилататоры и наличия гиперреактивности бронхов. Длительная терапия ИГКС создавала повышенный риск развития орофарингеального кандидоза и охриплости голоса. За 3 года наблюдения не было отмечено неблагоприятного воздействия на минеральную плотность костей скелета и частоту развития переломов костей [3]. В другой обобщающей публикации говорится о возможности развития более широкого спектра нежелательных эффектов в результате длительной терапии ИГКС: охриплости голоса, раздражения слизистой глотки, парадоксального бронхоспазма, орофарингеального кандидоза, аллергических реакций, угнетения функции коры надпочечников, остеопороза, задержки роста у детей, катаракты, глаукомы, стероидной миопатии и увеличения риска пневмонии [4]. Таким образом, монотерапию ИГКС у больных ХОБЛ в отличие от БА можно признать нецелесообразной, а включение ИГКС в программы лечения требует соблюдения баланса между доказанными преимуществами и возможными побочными эффектами, а также стоимостью лечения. Ингаляционная терапия больных ХОБЛ комбинацией бронходилататоров и ИГКС Особенности воспалительного процесса при ХОБЛ и отсутствие средств, способных эффективно воздействовать на него, привели к тому, что на сегодня основу лечения больных ХОБЛ составляют бронходилататоры – ?2–агонисты, антихолинергики и метилксантины, которые применяют отдельно или по необходимости в комбинациях или на регулярной основе для предупреждения или уменьшения симптомов и частоты обострений. Революция в лечении БА и ХОБЛ произошла благодаря созданию в конце прошлого века длительнодействующих бронходилататоров – ?2–агонистов сальметерола и формотерола. На сегодня доказано, что регулярная терапия длительнодействующими бронходилататорами более эффективна и удобна, чем применение бронходилататоров короткого действия [1]. Следующим шагом было создание препаратов для ингаляционного применения, представляющих собой комбинацию ИГКС и длительнодействующих ?2–агонистов. В настоящее время существуют два комбинированных препарата, содержащих ИГКС и бронходилататор длительного действия: сальметерол/флютиказона пропионат и формотерол/будесонид (Симбикорт). Оба они широко и успешно используются для лечения БА. Показания к применению названных препаратов у пациентов с ХОБЛ ограничены рамками III (тяжелой) стадии, протекающей с частыми обострениями. В России и Европейском союзе как средство симптоматической терапии тяжелой ХОБЛ зарегистрирован Симбикорт турбухалер (формотерол 4,5 мкг + будесонид 80, 160 мкг), в скором времени в России ожидается появление Симбикорта 9/320 мкг. 5–летний опыт использования комбинаций ИГКС с длительнодействующими бронходилататорами у больных ХОБЛ показал, что комбинированные препараты безопасны и более эффективны, чем их компоненты по отдельности. Результаты одного из первых сравнительных исследований показали, что применение у больных с тяжелой ХОБЛ комбинации формотерол/будесонида (160/4,5 мкг по 2 ингаляции 2 раза в сутки) в течение года сокращало среднее количество обострений ХОБЛ на 24% в год по сравнению с плацебо и на 23% – по сравнению с формотеролом (4,5 мкг по 2 ингаляции 2 раза в сутки). Достоверно уменьшалась выраженность всех симптомов и потребность в ингаляциях ?2–агонистов короткого действия по сравнению с плацебо и будесонидом (200 мкг по 2 ингаляции 2 раза в день). Показатель ОФВ1 увеличивался на 15% по сравнению с плацебо и на 9% по сравнению с будесонидом. Утренняя пиковая скорость выдоха достоверно улучшалась после первого дня лечения комбинированным препаратом по сравнению с плацебо и формотеролом, через неделю – по сравнению с плацебо, формотеролом и будесонидом, и это преимущество сохранялось в течение всех 12 месяцев наблюдения. Лечение формотерол/будесонидом достоверно улучшало показатель качества жизни по сравнению с плацебо. Не было отмечено выраженных нежелательных эффектов комбинированной терапии по сравнению с плацебо [5]. Другое крупномасштабное длительное исследование аналогичного дизайна, проведенное в то же время, что и первое, также выявило явные преимущества комбинации формотерол/будесонида в дозе 320/9 мкг 2 раза в сутки по сравнению с плацебо, будесонидом (по 400 мкг 2 раза в сутки) и формотеролом (по 9 мкг 2 раза в сутки) по отдельности. Комбинированная ингаляционная терапия приводила к достоверно более существенному приросту ОФВ1, пиковой скорости выдоха до ингаляции бронходилататора, улучшению показателя качества жизни, сокращению обострений ХОБЛ и увеличению продолжительности периода до развития первого обострения, чем применение ее отдельных компонентов или плацебо [6]. Исследование экономической целесообразности применения комбинации формотерол/будесонида у пациентов с ХОБЛ III–IV стадий по GOLD, проведенное в Швеции, показало, что расходы на лечение 1 больного в год при использовании формотерол/будесонида составили, в среднем, 2518 евро, будесонида – 3194 евро, формотерола – 3653 евро и плацебо – 3213 евро, что явно свидетельствовало в пользу комбинированной терапии [7]. Если учесть масштабы распространенности ХОБЛ во всем мире, то уменьшение частоты обострений заболевания под влиянием эффективной комбинированной ингаляционной терапии оказывается еще более значимым как с клинической, так и с экономической точек зрения [8]. Мета–анализ, опубликованный в 2007 г., обобщил итоги 11 исследований, включавших 6427 больных ХОБЛ. Сравнение результатов применения комбинаций сальметерол/флютиказона и формотерол/будесонида с плацебо показало, что комбинированная ингаляционная терапия способствует сокращению частоты обострений ХОБЛ на 1/4, уменьшению выраженности симптомов, улучшению функциональных показателей и улучшению состояния здоровья. Повышенный риск развития пневмонии вследствие комбинированной ингаляционной терапии требует специального изучения [9]. Оценка быстроты наступления бронхорасширяющего эффекта сальметерол/флютиказона и формотерол/будесонида у больных с ХОБЛ II–III стадий выявила достоверное преимущество формотерол/будесонида, действие которого начиналось через 5 минут после ингаляции, что было сравнимо с быстротой наступления эффекта сальбутамола [10]. Симбикорт в лечении больных с сочетанием БА и ХОБЛ Длительное течение тяжелой БА приводит к ремоделированию дыхательных путей и формированию необратимого компонента бронхиальной обструкции. Развитие ХОБЛ у больного с неконтролируемой БА в 12 раз более вероятно, чем в случаях полного контроля БА. ХОБЛ и БА могут сочетаться, например, у курящих пациентов с астмой. Наличие двух заболеваний предполагает взаимно отягощающее влияние различных патогенетических механизмов поддержания хронического воспаления дыхательных путей, которое обусловливает особенности клинических проявлений и течения сочетанной патологии. Целесообразность применения комбинаций ИГКС и длительнодействующих ?2–агонистов в случаях сочетанной патологии обоснована с точки зрения хорошо известных механизмов патогенеза обоих заболеваний. Можно предполагать, что взаимное потенцирование действия ИГКС и длительнодействующих ?2–агонистов реализуется за счет их взаимодействия на уровне рецепторов [11–13]. Возможность комбинаций ИГКС и длительнодействующих бронходилататоров различных фармакологических групп Целесообразность одновременного применения длительнодействующих бронходилататоров различных фармакологических групп и ИГКС в качестве базисной терапии у больных с тяжелой и крайне тяжелой ХОБЛ, а также в случаях сочетания ХОБЛ и тяжелой БА однозначно не доказана, но вопрос этот заслуживает внимания исследователей и практиков, поскольку результаты немногочисленных работ свидетельствуют в пользу этой комбинации. Преимущество использования у пациентов с тяжелой ХОБЛ комбинации тиотропиума и формотерола по сравнению с каждым из препаратов в отдельности было показано в исследовании J. van Noord et al. [14]. Влияние комбинации формотерола и тиотропиума на функцию легких у больных ХОБЛ средней тяжести оказалась более эффективным, чем применение сальметерола/флютиказона [15]. В исследовании, проведенном у пациентов с тяжелой и крайне тяжелой ХОБЛ, добавление тиотропиума (18 мкг в сутки) к комбинации сальметерола/флютиказона (50/500 мкг 2 раза в сутки) достоверно усиливало воздействие лечения на функцию дыхания. К концу третьего месяца исследования показатель ОФВ1 увеличился на 140 мл в группе пациентов, получавших тиотропиум, на 141 мл – сальметерол/флютиказон и на 186 мл – в группе получавших сочетание тиотропиума и сальметерола/флютиказона [16]. Мы не нашли сообщений о совместном использовании Симбикорта и тиотропиума у пациентов с ХОБЛ, однако располагаем собственным скромным опытом лечения пациентов с сочетанием тяжелой ХОБЛ и БА указанной комбинацией препаратов [17]. У наших пациентов длительная ингаляционная базисная терапия Симбикортом и тиотропиумом позволяла добиться стойкого контроля бронхиальной астмы, заметного прироста ОФВ1 и длительного (до 2 лет) отсутствия обострений ХОБЛ. Заключение Таким образом, накопленный опыт применения комбинированной ингаляционной терапии ИГКС и длительнодействующими ?2–агонистами, в частности, препаратом Симбикорт у пациентов со стабильной тяжелой ХОБЛ и в случаях сочетания ХОБЛ с тяжелой бронхиальной астмой свидетельствует о значительном преимуществе комбинированной терапии по сравнению с монотерапией ИГКС. Длительная базисная терапия с использованием Симбикорта у названных категорий пациентов позволяет значительно сократить частоту обострений ХОБЛ, уменьшить выраженность симптомов заболеваний и улучшить качество жизни. Литература 1. Global Initiative for Chronic Obstructive Lung Disease. Revised 2006. 2. Sutherland E.R., Martin R.J.. Airway inflammation in chronic obstructive pulmonary disease: comparisons with asthma. J. Allergy Clin. Immunol. 2003;112:819–827. 3. Yang I.A., Fong K.M., Sim E.H., et al. Inhaled corticosteroids for stable chronic obstructive pulmonary disease. Cochrane Database Syst. Rev. 2007;18:CD002991. 4. Inhaled Corticosteroids for Chronic Obstructive Pulmonary Disease. A Status report. Am. J. Respir. Crit. Care. Med. 2007;175:103–107. 5. Szafranski W., Cukier A., Ramirez A. et al. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. Eur. Respir. J. 2003;21:74–81. 6. Calverley P.M., Boonsawat W., Cseke Z. et al. Maintenance therapy with budesonide and formoterol in chronic obstructive pulmonary disease. Eur. Respir. J. 2003;22:912–919. 7. Lofdahl C.G., Ericsson A., Svensson K., Andreasson E. Cost effectiveness of budesonide/formoterol in a single inhaler for COPD compared with each monocomponent used alone. Pharmacoeconomics. 2005;23:365–375. 8. Buist A.S., Vollmer W.M., Sullivan S.D. et al. The burden of obstructive lung disease initiative (BOLD): rationale and design. J. COPD. 2005; 2: 277–283. 9. Nannini L., Cates C.J., Lasserson T..J, Poole P. Combined corticosteroid and long–acting beta–agonist in one inhaler versus placebo for chronic obstructive pulmonary disease. Cochrane Database Syst. Rev. 2007.17;CD003794. 10. Lindberg A., Szalai Z., Pullerits T., Radeczky E. Fast onset of effect of budesonide/formoterol versus salmeterol/fluticasone and salbutamol in patients with chronic obstructive pulmonary disease and reversible airway obstruction. Respirology. 2007;12:732–739. 11. Guerra S. Overlap of asthma and chronic obstructive pulmonary disease. Curr Opin Pulm Med. 2005;11:7–13. 12. Decramer M., Selroos O. Asthma and COPD: differences and similarities. With special reference to the usefulness of budesonide/formoterol in a single inhaler (Symbicort) in both diseases. Int. J. Clin. Pract. 2005;59:385–398. 13. Miller–Larsson A., Selroos O. Advances in asthma and COPD treatment: combination therapy with inhaled corticosteroids and long–acting beta 2–agonists. Curr. Pharm. Dis. 2006;12:3261–3279. 14. van Noord J. A., Aumann J. L., Janssens E. et al. Effects of tiotropium with and without formoterol on airflow obstruction and resting hyperinflation in patients with COPD. Chest. 2006; 129: 509–517. 15. Rabe K.F., Timmer W., Sagriotis A., Viel K. Comparison of a combination of tiotropium and formoterol to salmeterol and fluticasone in moderate COPD. Eur. Respir. J. 2005; 26: Suppl. 49: 14s. 16. Cazzola M. , Ando F. , Santus P. еt al.. A pilot study to assess the effects of combining fluticasone propionate/salmeterol and tiotropium on the airflow obstruction of patients with severe–to–very severe COPD Pulm. Pharmacol. Ther. 2006:7. 17. Степанян И.Э. Эффективное использование тиотропиума в комплексной ингаляционной терапии пациентов с сочетанием ХОБЛ и БА .Трудный пациент.– 2007; 5:33–36.