Опыт применения атозибана при угрозе преждевременных родов
Проведена оценка эффективности атозибана – токолитика, разработанного специально для применения при самопроизвольной сократительной деятельности матки, у 19 пациенток с угрозой преждевременных родов. Отмечена высокая эффективность препарата (89,5%). Побочных эффектов ни в одном случае отмечено не было.
Введение
В настоящее время частота преждевременных родов в мире не снижается и составляет 5–10% от всех родов [1, 2]. На долю недоношенных детей приходится 60–70% случаев ранней неонатальной смертности, 50% неврологических заболеваний, в том числе детским церебральным параличом, у недоношенных детей высока распространенность нарушений зрения, слуха, тяжелых хронических заболеваний легких [3, 4].
Если на сроке 28–30 недель беременности можно ускорить созревание легких у плода путем применения кортикостероидов, а пролонгирование беременности на сроке 34–37 недель не оказывает существенного влияния на показатели перинатальной смертности, то наименее благоприятные показатели перинатальной заболеваемости и смертности имеют дети, рожденные на сроке до 28 недель беременности. По данным литературы, при родах на сроке 24 недели гестации в 80% случаев следует летальный исход (при родах на сроке более 30 недель эта цифра сокращается до 10%). 65% детей, родившихся на 22–26-й неделе, умирают в родовом отделении или отделении интенсивной терапии новорожденных. Все недоношенные дети, которые доживают до 30 месяцев, имеют какие-либо формы инвалидности, причем в 50% случаев – тяжелые [5].
Так, частота преждевременных родов в Москве в 2012 г. составила 5,8% от общего количества родов. Из них на сроке от 22 до 27 недель произошло 699 родов (0,54% от общего количества). На сроке гестации 22–27 недель родилось 754 новорожденных: 362 (48,1%) мертворожденных и 392 (51,9%) живорожденных. Из всех живорожденных только 239 (31,7%) пережили 168 часов, 153 (20,2% от всех родившихся) умерли в первые семь суток.
Около 70–80% преждевременных родов происходит спонтанно или самопроизвольно, при этом частота преждевременного разрыва плодных оболочек, по данным разных авторов, составляет от 5 до 40%. Остальные причины связаны с осложнениями, возникшими во время беременности со стороны матери или плода (индуцированные роды): многоплодная беременность (10–30%), тяжелые формы гестоза (12%), кровотечение во время беременности из-за отслойки нормально расположенной плаценты или предлежания плаценты (6–9%), задержка роста плода (2–4%) [1, 5].
Согласно приказу Министерства здравоохранения от 1 ноября 2012 г. № 572н «Об утверждении Порядка оказания медицинской помощи по профилю „акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)“» при угрозе преждевременных родов рекомендуется применение нифедипина, индометацина (до 32-й недели беременности), бета-агонистов (при непереносимости нифедипина), атозибана.
Нифедипин в нашей стране в качестве токолитической терапии не лицензирован. В проведенных ранее исследованиях, посвященных токолитикам, доказано, что ингибиторы циклооксигеназы являются эффективными препаратами для пролонгирования беременности. Однако их применение вызывает ряд побочных эффектов не только со стороны матери, но и плода: снижение функции почек, преждевременное закрытие боталлова протока, повышенный риск внутрижелудочкового кровоизлияния и некротического энтероколита. Зарубежные исследователи рекомендуют назначать бета-миметики на короткий промежуток времени только для того, чтобы достичь эффекта от кортикостероидных препаратов или для транспортировки ребенка in utero
в акушерский стационар, имеющий отделение реанимации и интенсивной терапии новорожденных.
Атозибан представляет собой синтетический конкурентный ингибитор вазопрессина и окситоцина. Связываясь с рецепторами окситоцина, атозибан снижает частоту маточных сокращений и тонус миометрия, что приводит к угнетению сократимости матки. Атозибан также связывается с рецепторами вазопрессина, таким образом угнетая эффект последнего.
Атозибан – единственный токолитик, разработанный специально для применения при самопроизвольной сократительной деятельности матки. Во многих европейских странах атозибан является препаратом выбора для терапии угрозы преждевременных родов.
В России атозибан – препарат Трактоцил был зарегистрирован в 2012 г., и в январе 2013 г. на базе стационаров группы была проведена оценка его эффективности у пациенток с угрозой преждевременных родов.
Материал и методы
Всего в акушерских стационарах группы (Перинатальный медицинский центр и клинический госпиталь «Лапино») препарат атозибан был применен у 19 пациенток.
Показаниями к назначению атозибана явилась угроза преждевременных родов на сроке беременности 25–34 недели: шесть пациенток (31,6%) на сроке 25–27 недель, пять пациенток (26,3%) – 28–31 неделя, восемь пациенток (42,1%) – 32–34 недели. В группу наблюдения не включались пациентки с гестозом, предлежанием плаценты, отслойкой нормально расположенной плаценты, преждевременным излитием околоплодных вод, задержкой внутриутробного роста плода, хронической гипоксией плода.
Возраст обследованных варьировал от 24 до 39 лет и в среднем составил 32 ± 4,5 года. Сопутствующих хронических соматических заболеваний выявлено не было. Из гинекологических заболеваний неспецифический кольпит диагностирован у четырех (21,0%), а эрозия шейки матки – у трех (15,9%) беременных.
У 12 (63,2%) пациенток беременность была первая, у семи (36,8%) – повторная (из них вторая беременность у четырех (21%) женщин, третья – у трех (15,7%)). Из группы повторнородящих у четырех (21%) женщин имелся рубец на матке после операции кесарева сечения. Беременность у двух (10,5%) пациенток наступила в результате экстракорпорального оплодотворения. У двух (10,5%) женщин беременность была многоплодная (двойня). Никто из пациенток не имел преждевременных родов в анамнезе.
Оценка эффективности препарата атозибан проводилась на основании клинической картины (жалобы, данные наружного осмотра), а также результатов ультразвукового и кардиотокографического исследования.
Все беременные предъявляли жалобы на тянущие боли внизу живота различной степени интенсивности, из них 15 пациенток (78,9%) указывали на регулярные маточные сокращения по 15 секунд четыре – шесть раз в течение часа.
При двуручном исследовании у шести (31,6%) пациенток диагностировано укорочение шейки матки до 0,5 см, цервикальный канал проходим свободно для двух пальцев, у одной из пациенток отмечались скудные кровяные выделения.
По данным токографического исследования у десяти (52,6%) пациенток отмечался повышенный тонус матки.
При поступлении 17 пациенткам проводилось ультразвуковое исследование с цервикометрией трансвагинальным доступом. У шести (31,6%) обследованных длина шейки матки составила от 28 до 35 мм, у девяти (47,4%) длина сомкнутой части была менее 28 мм, а внутренний зев был воронкообразным или расширен от 3 мм и более. У двух (10,5%) беременных плодный пузырь пролабировал в просвет цервикального канала.
Препарат атозибан всем пациенткам вводился внутривенно в три последовательных этапа по следующей схеме:
1) болюсное введение в начальной дозе 6,75 мг;
2) сразу после болюсного введения инфузия концентрата в высокой дозе 300 мкг/мин в течение трех часов;
3) длительная (до 45 часов) инфузия концентрата в низкой дозе 100 мкг/мин.
Общая доза атозибана на курс терапии не превышала 330 мг. В основном внутривенное введение атозибана проводилось в условиях родильного отделения с последующим продолжением курса в отделении патологии беременности. Четырем (21,0%) беременным курс препарата атозибан был проведен в условиях отделения патологии беременности.
Результаты исследования
В течение двух – шести часов введения атозибана 17 (89,5%) у беременных отмечали снижение интенсивности и частоты маточных сокращений. К концу курса лечения атозибаном (через 48 часов) у этих пациенток отсутствовали жалобы на тянущие боли внизу живота. В начале терапии и после 48 часов при объективном наружном обследовании и по данным кардиотокографии матка была в нормальном тонусе. С целью профилактики респираторного дистресс-синдрома новорожденных всем пациенткам дважды вводился дексаметазон 12 мг внутримышечно с интервалом в 12 часов. Динамическая оценка шейки матки проводилась при ультразвуковой цервикометрии каждые две недели: у 17 ответивших на лечение беременных отрицательной динамики не выявлено.
Из обследованных 19 женщин своевременные роды произошли у 17 (89,5%), из них у 12 (73,7%) были самопроизвольные роды без осложнений в интранатальном и послеродовом периодах. Кесарево сечение выполнено пяти (26,3%) пациенткам. У четырех женщин показанием к проведению оперативного родоразрешения явилось наличие рубца на матке после кесарева сечения: трое были прооперированы в плановом порядке на сроке 39 недель беременности, у четвертой операция кесарева сечения была произведена в экстренном порядке в связи с преждевременным излитием околоплодных вод на сроке беременности 38–39 недель. Еще одной роженице абдоминальное родоразрешение было выполнено в связи с начавшейся острой гипоксией плода, причиной которой явилось тугое обвитие пуповиной вокруг шеи.
Масса детей при рождении колебалась от 2900 до 4350 г с оценкой по шкале Апгар 8–9 баллов. Новорожденные наблюдались в детском отделении, были выписаны домой на третьи – пятые сутки. В послеродовом периоде у пациенток не было отмечено никаких осложнений.
У двух (10,5%) беременных терапия препаратом атозибан была неэффективной. Одна пациентка поступила на сроке 25–26 недель с жалобами на регулярные сокращения матки четыре-пять раз в течение часа. При влагалищном исследовании диагностировано пролабирование плодного пузыря. Пациентке проводилось два курса атозибана: на сроке 25–26 недель и на сроке 26–27 недель. Через десять дней после поступления, учитывая начало регулярной родовой деятельности, повышение температуры тела до 38°С, появление гноевидных выделений, а также лейкоцитарный сдвиг влево в клиническом анализе крови, пациентка была родоразрешена путем операции кесарева сечения в экстренном порядке. Масса плода при рождении составила 890 г, ребенок наблюдался в отделении детской реанимации, ему проводилась искусственная вентиляция легких в течение 20 суток, после чего он был переведен на второй этап выхаживания. В результате применения препарата атозибан у данной пациентки удалось пролонгировать беременность на две недели. При поступлении предполагаемая масса плода была 670 г, при родоразрешении – 890 г.
Другая пациентка, повторнородящая, поступила на сроке гестации 33 недели с жалобами на схваткообразные боли внизу живота через 8–10 минут по 15–20 секунд. При влагалищном исследовании шейка матки сглажена, открытие 2–3 см, плодный пузырь цел. Атозибан вводился в течение 16 часов. Несмотря на проведенную терапию, развилась регулярная родовая деятельность, через пять часов произошли самопроизвольные роды плодом массой 2250 г. Ребенок наблюдался в отделении детской реанимации, ему проводилась искусственная вентиляция легких в течение 12 часов.
Побочных эффектов на фоне терапии атозибаном ни у одной пациентки выявлено не было.
Выводы
Преждевременные роды являются важной медицинской, социальной и экономической проблемой, в связи с чем актуальным вопросом является оптимизация терапии, направленной на пролонгирование беременности. У 89,5% наблюдаемых пациенток атозибан оказался высокоэффективным лекарственным средством для лечения угрожающих преждевременных родов. Ни у одной из 19 пациенток не было выявлено побочных эффектов.
В настоящее время число случаев преждевременных родов (ПР) в мире не имеет тенденции к снижению и составляет 5-10% от всех родов [1, 4]. Актуальность проблемы ПР обусловлена высокой частотой ранней неонатальной смертности среди недоношенных (60-70%), неврологических заболеваний (до 50%), в том числе детского церебрального паралича, нарушений зрения, слуха и других хронических заболеваний [2, 5].
По данным литературы [3], при родах в сроке 24 нед беременности 80% новорожденных умирают, тогда как при родах в сроке более 30 нед гестации 90% новорожденных выживают. Из детей, родившихся в период с 22-й по 26-ю неделю беременности, 65% умирают в родильном отделении или отделении интенсивной терапии новорожденных, а у всех, кто доживает до 30 мес выявляются какие-либо формы инвалидности, причем в 50% наблюдений — тяжелые.
Наименее благоприятные показатели перинатальной заболеваемости и смертности имеют дети, рожденные в сроке до 28 нед беременности, тогда как в 28-30 нед гестации удается добиться ускоренного созревания легких с помощью кортикостероидов. Пролонгирование беременности в сроки 34-37 нед не оказывает существенного влияния на показатели перинатальной смертности [6].
Около 70-80% преждевременных родов происходят самопроизвольно, при этом число случаев преждевременного разрыва плодных оболочек, по данным разных авторов [1-3], составляет от 5 до 40%. Остальные причины связаны с осложнениями, возникшими во время беременности со стороны матери или плода (индуцированные роды): многоплодная беременность в структуре причин ПР составляет 10-30%, тяжелые формы преэклампсии — 12%, кровотечения во время беременности (отслойка нормально расположенной плаценты, предлежание плаценты) — 6-9%, задержка роста плода — 2-4%.
Преждевременные роды в Москве в 2012 г. составили 5,8% от общего количества родов. Среди них в сроки от 22 до 27 нед произошло 699 (0,54%) родов. Анализ выживаемости новорожденных, родившихся в 2012 г. в сроки гестации 22-27 нед, показал, что в данные сроки беременности родились 754 новорожденных, среди них мертворожденных были 362 (48,1%), живорожденных — 392 (51,9%). Причем из всех родившихся только 239 (31,7%) живорожденных пережили 168 ч, 153 (20,2%) — умерли в первые 7 сут.
Согласно приказу МЗ РФ №572н от 01.11.12 «Об утверждении порядка оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)» при угрозе преждевременных родов рекомендуется применение нифедипина, индометацина (до 32 нед беременности), β-адреномиметиков (при непереносимости нифедипина), атозибана.
Нифедипин в нашей стране не лицензирован в качестве токолитической терапии. В проведенных ранее исследованиях, посвященных токолитикам, доказано, что ингибиторы циклооксигеназы являются эффективными препаратами для прологирования беременности, однако их применение вызывает ряд побочных эффектов не только со стороны матери, но и плода: снижение функции почек плода, преждевременное закрытие боталлова протока, повышенный риск внутрижелудочкового кровоизлияния и некротического энтероколита. Зарубежные исследователи рекомендуют назначать β-адреномиметики на короткий промежуток времени только для того, чтобы достичь эффекта от кортикостероидных препаратов или для транспортировки ребенка in utero
в акушерский стационар, имеющий отделение реанимации и интенсивной терапии новорожденных.
Атозибан представляет собой синтетический конкурентный ингибитор вазопрессина и окситоцина, который связывается с мембраносвязанными рецепторами клеток миометрия. Это приводит к закрытию потенциалзависимых каналов в клетках миометрия, в результате чего уменьшается внутриклеточное содержание кальция, который обычно стимулирует сокращения.
Атозибан — единственный токолитик, разработанный специально для применения при самопроизвольной сократительной деятельности матки. Во многих европейских странах атозибан является препаратом выбора для терапии беременных с угрозой преждевременных родов.
В России трактоцил (атозибан) был зарегистрирован в 2012 г. и в январе 2013 г. на базе Перинатального медицинского центра и Клинического госпиталя «Лапино» группой была проведена оценка эффективности вышеуказанного препарата у пациенток с угрозой преждевременных родов.
Материал и методы
В акушерских стационарах группы (Перинатальный медицинский центр и Клинический госпиталь «Лапино») атозибан был применен у 19 пациенток.
Показанием к применению явилась угроза преждевременных родов в сроке беременности 25-34 нед: у 6 (31,6%) пациенток в сроки 25-27 нед, у 5 (26,3%) со сроком беременности 28-31 нед, у 8 (42,1%) в сроки беременности 32-34 нед. В группу наблюдения не были включены пациентки с преэклампсией, предлежанием плаценты, отслойкой нормально расположенной плаценты, преждевременным излитием околоплодных вод, задержкой внутриутробного роста плода, хронической гипоксией плода.
Возраст обследованных варьировал от 24 до 39 лет и в среднем составил 32±4,5 года. Сопутствующих хронических соматических заболеваний выявлено не было. Из гинекологических заболеваний неспецифический кольпит был диагностирован у 4 (21,0%) обследованных, эктопия шейки матки — у 3 (15,9%).
У 12 (63,2%) пациенток беременность была первая, у 7 (36,8%) — повторная. Беременность у 2 (10,5%) пациенток наступила в результате экстракорпорального оплодотворения. Среди 19 пациенток первые роды предстояли 12 (63,2%) пациенткам, вторые роды — 4 (21%), третьи роды — 3 (15,7%). В группе повторнородящих у 4 (21%) женщин был рубец на матке после кесарева сечения. У 2 (10,5%) пациенток беременность была многоплодной (двойня). Ни у одной пациентки в анамнезе не было преждевременных родов.
Оценка эффективности атозибана проводилась на основании клинических данных (жалобы, данные наружного осмотра), а также данных ультразвукового и кардиотокографического исследований.
Все беременные предъявляли жалобы на тянущие боли внизу живота различной степени интенсивности, из них 15 (78,9%) пациенток указывали на регулярные маточные сокращения по 15 с 4-6 раз в течение 1 ч.
При двуручном исследовании у 6 (31,6%) пациенток диагностировано укорочение шейки матки до 0,5 см, цервикальный канал был свободно проходим для двух пальцев, у одной из пациенток отмечались скудные кровяные выделения.
По данным токографического исследования у 10 (52,6%) пациенток отмечался повышенный тонус матки.
При поступлении проводилось ультразвуковое исследование с цервикометрией трансвагинальным доступом у 17 из 19 пациенток. У 6 (31,6%) обследованных длина шейки матки составила от 28 до 35 мм, у 9 (47,4%) — длина сомкнутой части была менее 28 мм, а внутренний зев был воронкообразным или расширенным от 3 мм и более. У 2 (10,5%) беременных плодный пузырь пролабировал в просвет цервикального канала.
Атозибан всем пациенткам вводился внутривенно в 3 последовательных этапа по следующей схеме:
1. Болюсное введение в начальной дозе — 6,75 мг.
2. Сразу после болюсного введения проводилась инфузия концентрата в высокой дозе — 300 мкг/мин — в течение 3 ч.
3. Далее проводилась длительная (до 45 ч) инфузия концентрата в низкой дозе 100 мкг/мин.
Общая доза на курс терапии не превышала 330 мг.
В основном внутривенное введение атозибана проводилось в условиях родильного отделения с последующим продолжением курса в отделении патологии беременности. Четырем (21,0%) беременным курс лечения атозибаном был проведен в условиях отделения патологии беременности.
Результаты и обсуждение
В течение первых 2-6 ч введения атозибана 17 (89,5%) из 19 беременных отмечали снижение интенсивности и частоты маточных сокращений. При объективном исследовании и по данным токографии матка была в нормальном тонусе. К концу курса лечения атозибаном (через 48 ч) у пациенток отсутствовали жалобы на тянущие боли внизу живота, при объективном наружном исследовании и по данным КТГ матка была в нормальном тонусе. С целью профилактики респираторного дистресс-синдрома новорожденных всем пациенткам вводился дважды дексаметазон 12 мг внутримышечно с интервалом в 12 ч. Динамическая оценка шейки матки проводилась при ультразвуковой цервикометрии каждые 2 нед: у 17 из 19 наблюдаемых отрицательной динамики не выявлено.
Среди обследованных 19 женщин своевременные роды произошли у 17 (89,5%), из них у 12 (73,7 %) роды были самопроизвольными, без осложнений в интранатальном и послеродовом периодах. Кесарево сечение было произведено у 5 (26,3%) из 17 пациенток. У 4 женщин показанием к проведению оперативного родоразрешения явилось наличие рубца на матке после кесарева сечения: 3 были прооперированы в плановом порядке в сроке 39 нед беременности, у 1 из вышеуказанных беременных кесарево сечение было произведено в экстренном порядке в связи с преждевременным излитием околоплодных вод в сроке беременности 38-39 нед. Еще одной роженице было проведено оперативное родоразрешение в связи с начавшейся острой гипоксией плода, причиной которой явилось тугое обвитие пуповины вокруг шеи. Масса детей при рождении колебалась от 2900 до 4350 г, оценка по шкале Апгар составила 8-9 баллов. Все дети наблюдались в детском отделении, были выписаны домой на 3-5-е сутки. В послеродовом периоде у пациенток не было отмечено никаких осложнений.
У 2 (10,5%) беременных терапия атозибаном была неэффективной. Одна пациентка поступила в сроке беременности 25-26 нед с жалобами на регулярные сокращения матки 4-5 раз в течение 1 ч. При влагалищном исследовании диагностировано пролабирование плодного пузыря. Пациентке проводилось 2 курса атозибана: в сроке 25-26 нед и в сроке 26-27 нед. Через 10 дней после поступления, учитывая начало регулярной родовой деятельности, повышение температуры тела до 38 °С, появление гноевидных выделений, а также лейкоцитарный сдвиг влево в клиническом анализе крови, пациентка была родоразрешена путем кесарева сечения в экстренном порядке. Масса плода при рождении составила 890 г. Ребенок наблюдался в отделении детской реанимации, проводилась искусственная вентиляция легких в течение 20 сут, после чего ребенок был переведен на второй этап выхаживания. В результате применения атозибана у данной пациентки удалось пролонгировать беременность на 2 нед. При поступлении предполагаемая масса плода — 670 г, при родоразрешении — 890 г.
Другая пациентка, повторнородящая, поступила в сроке беременности 33 нед с жалобами на схваткообразные боли внизу живота через 8-10 мин, по 15-20 с. При влагалищном исследовании установлено: шейка матки сглажена, открытие 2-3 см, плодный пузырь цел. Проводилось введение атозибана в течение 16 ч. Несмотря на проведенную терапию, развилась регулярная родовая деятельность; через 5 ч произошли самопроизвольные роды плодом массой 2250 г. Ребенок наблюдался в отделении детской реанимации, проводилась искусственная вентиляция легких в течение 12 ч.
Побочных эффектов на фоне терапии атозибаном ни у одной пациентки выявлено не было.
Таким образом, преждевременные роды составляют серьезную медицинскую, социальную и экономическую проблему, в связи с чем актуальным вопросом является оптимизация терапии, направленной на пролонгирование беременности.
Выводы
1. Установлено, что у 89,5% наблюдаемых беременных с угрожающими преждевременными родами трактоцил (атозибан) оказался высокоэффективным лекарственным средством.
2. Результаты исследования показали, что ни у одной из 19 пациенток не было выявлено побочных эффектов применения атозибана.
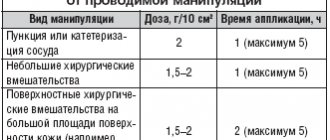
Атозибан (Atosiban)
Терапию препаратом Атозибан должен назначать и проводить квалифицированный врач, имеющий опыт ведения преждевременных родов. Препарат Атозибан вводят внутривенно, незамедлительно после диагностики преждевременных родов, в З последовательных этапа: 1) вначале в течение 1 мин болюсно вводится 1 флакон препарата Атозибан, раствор для внутривенного введения, 6,75 мг/0,9 мл, без разведения (начальная доза 6,75 мг); 2) сразу после этого в течение 3-х ч проводится инфузия препарата Атозибан, концентрат для приготовления раствора для инфузий, 37,5 мг/5 мл, в высокой дозе (нагрузочная инфузия) 300 мкг/мин; З) после этого проводится продолжительная (до 45 ч) инфузия препарата Атозибан, концентрат для приготовления раствора для инфузий, 37,5 мг/5 мл, в низкой дозе 100 мкг/мин. Общая продолжительность лечения не должна превышать 48 ч. Максимальная доза препарата Атозибан на весь курс лечения не должна превышать 330,75 мг атозибана. Внутривенное одномоментное введение препарата необходимо осуществлять сразу после постановки диагноза «преждевременные роды». После введения болюсной инъекции следует начинать внутривенную инфузию (готовится из концентрата для приготовления раствора для инфузий, содержащего атозибан 37,5 мг/5 мл). Если сократительная активность матки сохраняется без изменений на фоне терапии препаратом Атозибан, следует рассмотреть вопрос об альтернативном лечении. В таблице представлено полное описание режима дозирования препарата для болюсного введения и последующей инфузии:
| Этап | Режим | Скорость инъекции/инфузии | Доза атозибана |
| 1 | Внутривенная болюсная инъекция 0,9 мл в течение 1 мин | Не применимо | 6,75 мг |
| 2 | Внутривенная нагрузочная инфузия в течение 3-х ч | 24 мл/ч (300 мкг/мин) | 54 мг |
| 3 | Дальнейшая продолжительная инфузия длительностью до 45 ч | 8 мл/ч (100 мкг/мин) | до 270 мг |
Повторное применение Если возникает необходимость в повторном применении атозибана, его также следует начинать с болюсного введения раствора для внутривенного введения 6,75 мг/0,9 мл (этап 1), за которым следует инфузионное введение концентрата для приготовления раствора для инфузий 37 ,5 мг/5 мл (этапы 2 и З). Применение препарата в особых клинических группах пациенток У Девочек-пофостков в возрасте до 18 лет Эффективность и безопасность атозибана у беременных в возрасте до 18 лет не установлены. У пациенток с почечной недостаточностью Применение атозибана у пациенток с почечной недостаточностью не изучалось. Коррекция дозы у таких пациенток не требуется, так как через почки выводится очень незначительное количество атозибана. У пациенток с печеночной недостаточностью Клинические данные о применении атозибана у пациенток с печеночной недостаточностью отсутствуют. У пациенток с нарушением функции печени атозибан следует применять с осторожностью. Способ применения препарата Этап 2 и З. Приготовление раствора для инфузии Перед введением раствора флаконы следует осмотреть визуально на предмет наличия нерастворенных частиц и изменения цвета раствора. Для внутривенной инфузии, которую проводят сразу после введения болюсной дозы, концентрат для приготовления раствора для инфузий, 37,5 мг/5 мл, разводят в одном из следующих растворов: — 0,9 % раствор натрия хлорида; — раствор Рингера; — 5 % раствор глюкозы. Из флакона, содержащего 100 мл одного из вышеперечисленных растворов для разведения, отбирают 10 мл. Затем во флакон вводят 10 мл (2 флакона по 5 мл) препарата Атозибан, концентрат для приготовления раствора для инфузий, 37,5 мг/5 мл, для получения концентрации 75 мг атозибана в 100 мл. Полученный таким образом раствор должен быть прозрачным, бесцветным и не содержать нерастворенных частиц. Нагрузочную инфузию проводят путем введения приготовленного раствора со скоростью 24 мл/ч (т.е. 18 мг/ч) в течение З ч. Введение препарата следует проводить под надлежащим медицинским контролем в акушерском отделении. Через З ч скорость инфузии снижается до 8 мл/ч. Для продолжения инфузии необходимо приготовить следующие 100 мл раствора методом, описанным выше. Необходимо пересчитать количество препарата для соблюдения указанной пропорции в случае использования емкости другого объема. Для того чтобы достичь точного дозирования препарата, необходимо откалибровать скорость введения в приборе для дозированной внутривенной инфузии в каплях в минуту. Камера для внутривенной микрокапельной инфузии (инфузомат) может обеспечить удобный диапазон скорости инфузии в пределах рекомендованных доз препарата Атозибан. В случае необходимости одновременного внутривенного введения других лекарственных средств возможно применение разделенной канюли для внутривенного введения или использования другого места введения. Такой способ позволяет применять независимое управление скоростью инфузии в процессе введения. Срок годности приготовленного раствора для инфузий 24 ч.