ШПОРЫ. Фармакология. / агонисты к имидазолиновым рецепторам
Агонисты имидазолиновых рецепторов
Механизм действия
Имидазолиновые рецепторы локализуются как в ЦНС (в ядрах ретикулярной формации, ростральной вентролатеральной области продолговатого мозга) — подтип 1, так и на периферии (например, в почках, поджелудочной железе) — подтип 2. Последние найдены также на митохондриях. Описан еще один тип рецепторов, не относящихся ни к одному из упомянутых типов и локализующихся в симпатических нервных окончаниях. Их активация приводит к снижению выработки норадреналина.
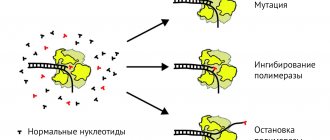
Активация имидазолиновых рецепторов приводит к увеличению синтеза арахидоновой кислоты и ингибированию Na+/H+ ионообменных каналов. Активация центральных I1-рецепторов приводит к снижению АД и уменьшению частоты сердечных сокращений, вследствие центрального подавляющего воздействия на периферическую симпатическую нервную систему. Различия в терапевтическом и гемодинамическом эффекте лекарств центрального действия обусловлено неодинаковой аффинностью к разным типам рецепторов. Препарат центрального действия первого поколения клонидин обладает сродством к двум типам рецепторов — центральным а-адеронорецепторам и имидазолиновым рецепторам. Его гипотензивный эффект в большей степени связан со стимуляцией имидазолиновых рецепторов, в то время как основные побочные эффекты опосредуются кортикальными a1-адренорецепторами.
Рилменидин и моксонидин обладают высокой селективностью в отношении I1-рецепторов. Их аффинность к I1-рецепторам более чем в 100 раз превосходит сродство к а2-адренорецепторам. Для обоих лекарств характерен выраженный гипотензивный эффект, иногда сопровождающийся незначительным седативным действием. Гипотензивное действие агонистов имидазолиновых рецепторов и вызываемое ими снижение периферического сосудистого сопротивления связаны с их выраженной периферической симпатолитической активностью. При этом стимуляция I1-рецепторов вызывает лишь незначительное уменьшение частоты сердечных сокращений (ЧСС). Показано, что брадикардия при применении клонидина в большей степени связана со стимуляцией а-адренорецепторов.
Фармакокинетика
Рилменидин (1-2 мг/сут однократно, Биодоступность 100% Связывание с белками плазмы 10% Т_ — около 8 ч, Основной путь элиминации — через почки в неизменном виде, Начало действия — через 1 -1,5 ч, Максимум — 2-5 ч Продолжительность — 24 ч, Нет синдрома отмены и ортостатической гипотонии)
Моксонидин (0,2-0,4 мг/сут однократно, Биодоступность 90% Связывание с белками плазмы — 8%, T — 2-3 ч, Основной путь элиминации почечная экскреция, Начало действия — 0,5 ч Максимум действия — 2-5 ч Продолжительность — 24 ч, Отсутствие толерантности при длительном применении Отсутствие синдрома отмены
Оба агониста I1-рецепторов обладают сходными фармакокинетическими характеристиками. Следует отметить, что несмотря на относительно короткий период полувыведения, гипотензивный эффект препаратов при однократном приеме сохраняется в течение суток. Максимальное снижение диастолического АД на пике концентрации составляло 30,9 мм. рт. ст. Однократный прием моксонидина, по данным суточного мониторирования АД, обеспечивая длительный гипотензивный эффект, не изменяет циркадный ритм АД [14]. Длительность терапевтического действия имидазолиновых агонистов связывают с их накоплением в ядрах головного мозга.
Побочные эффекты, переносимость
Наиболее частыми побочными эффектами рилменидина являются сухость во рту (4,9%), астения (4,1%), бессонница (4,5%) . Их выраженность зависит от дозы препарата и уменьшается при длительной терапии. При применении моксонидина чаще всего отмечалась сухость во рту (у 12,9% пациентов). Однако в целом многочисленные регистрационные и постмаркетинговые исследования свидетельствуют об очень хорошей переносимости моксонидина — он вызывал сухость во рту и седативный эффект менее чем у 10% больных, что значительно реже, чем при применении других антигипертензивных препаратов центрального действия. Помимо сухости во рту и седативного действия, при применении моксонидина наблюдались бессонница (5-8%) и головная боль (6%). Наибольшей частота побочных эффектов была у больных старших возрастных групп.
Метаболический синдром — основы патогенетической терапии
В 1948 г. известный клиницист Е. М. Тареев писал: «Представление о гипертонике наиболее часто ассоциируется с ожирелым гиперстеником, с возможным нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза — холестерином, мочевой кислотой…» Таким образом, более 50 лет назад было практически сформировано представление о метаболическом синдроме (МС). В 1988 г. G. Reaven описал симптомокомплекс, включающий гиперинсулинемию, нарушение толерантности к глюкозе, низкий уровень ХС ЛПВП и артериальную гипертонию, дав ему название «синдром Х» и впервые высказав предположение, что в основе всех этих изменений лежит инсулинорезистентность (ИР) с компенсаторной гиперинсулинемией. В 1989 г. J. Kaplan показал, что существенной составляющей «смертельного квартета» является абдоминальное ожирение. В 90-х гг. появился термин «метаболический синдром», предложенный M. Henefeld и W. Leonhardt. Распространенность этого симптомокомплекса приобретает характер эпидемии и в некоторых странах, в том числе и в России, достигает 25—35% среди взрослого населения.
Общепризнанные критерии МС до настоящего времени не разработаны, надо полагать, по причине отсутствия единых взглядов на его патогенез. Продолжающаяся дискуссия о правомочности использования терминов «полный» и «неполный» МС иллюстрирует недооценку единого механизма, обусловливающего параллельное развитие всех каскадов метаболических расстройств при инсулинорезистентности.
ИР — полигенная патология, в развитии которой могут иметь значение мутации генов субстрата инсулинового рецептора (IRS-1 и IRS-2), β3-адренорецепторов, разобщающего протеина (UCP-1), а также молекулярные дефекты белков сигнального пути инсулина (глюкозные транспортеры). Особую роль играет снижение чувствительности к инсулину в мышечной, жировой и печеночной тканях, а также в надпочечниках. В миоцитах нарушаются поступление и утилизация глюкозы, в жировой ткани развивается резистентность к антилиполитическому действию инсулина. Интенсивный липолиз в висцеральных адипоцитах приводит к выделению большого количества свободных жирных кислот (СЖК) и глицерина в портальный кровоток. Поступая в печень, СЖК, с одной стороны, становятся субстратом для формирования атерогенных липопротеидов, а с другой — препятствуют связыванию инсулина с гепатоцитом, потенциируя ИР. ИР гепатоцитов ведет к снижению синтеза гликогена, активации гликогенолиза и глюконеогенеза. Долгое время ИР компенсируется избыточной продукцией инсулина, поэтому нарушение гликемического контроля манифестирует не сразу. Но, по мере истощения функции β-клеток поджелудочной железы, наступает декомпенсация углеводного обмена, сначала в виде нарушенных гликемии натощак и толерантности к глюкозе (НТГ), а затем и сахарного диабета 2 типа (Т2СД). Дополнительное снижение секреции инсулина при МС вызывается длительным воздействием высоких концентраций СЖК на β-клетки (так называемый липотоксический эффект). При имеющихся генетически обусловленных дефектах секреции инсулина развитие Т2СД значительно ускоряется.
Согласно другой гипотезе, ведущую роль в развитии и прогрессировании инсулинорезистентности играет жировая ткань абдоминальной области. Особенность висцеральных адипоцитов — высокая чувствительность к липолитическому действию катехоламинов и низкая к антилиполитическому действию инсулина.
Помимо веществ, непосредственно регулирующих липидный обмен, жировая клетка продуцирует эстрогены, цитокины, ангиотензиноген, ингибитор активатора плазминогена-1, липопротенлипазу, адипсин, адинопектин, интерлейкин-6, фактор некроза опухолей-α (ФНО-α), трансформирующий фактор роста В, лептин и др. Показано, что ФНО-α способен воздействовать на инсулиновый рецептор и транспортеры глюкозы, потенциируя инсулинорезистентность, и стимулировать секрецию лептина. Лептин («голос жировой ткани») регулирует пищевое поведение, воздействуя на гипоталамический центр насыщения; повышает тонус симпатической нервной системы; усиливает термогенез в адипоцитах; подавляет синтез инсулина; воздействует на инсулиновый рецептор клетки, снижая транспорт глюкозы. При ожирении наблюдается лептинорезистентность. Полагают, что гиперлептинемия оказывает стимулирующее действие на некоторые гипоталамические релизинг-факторы (РФ), в частности на АКТГ-РФ. Так, при МС часто отмечается легкий гиперкортицизм, который играет определенную роль в патогенезе МС.
Следует особо остановиться на механизмах развития артериальной гипертонии (АГ) при МС, некоторые из них до недавнего времени были неизвестны, ввиду чего патогенетический подход к лечению МС был не до конца разработан.
Существуют многочисленные исследования, посвященные изучению тонких механизмов влияния инсулинорезистентности и гиперинсулинемии на уровень АД.
В норме инсулин обладает сосудистым протективным эффектом за счет активации фосфатидил-3-киназы в эндотелиальных клетках и микрососудах, что приводит к экспрессии гена эндотелиальной NO-синтазы, высвобождению NO эндотелиальными клетками и инсулин-обусловленной вазодилатации.
В настоящее время установлены следующие механизмы воздействия хронической гиперинсулинемии на АД:
- стимуляция симпатоадреналовой системы (САС);
- стимуляция ренин-ангиотензин-альдостероновой системы (РААС);
- блокада трансмембранных ионообменных механизмов с повышением содержания внутриклеточного Na+ и Са++, уменьшением К+ (увеличение чувствительности сосудистой стенки к прессорным воздействиям);
- повышение реабсорбции Na+ в проксимальных и дистальных канальцах нефрона (задержка жидкости с развитием гиперволемии), задержка Na+ и Са++ в стенках сосудов с повышением их чувствительности к прессорным воздействиям;
- стимуляция пролиферации гладкомышечных клеток сосудистой стенки (сужение артериол и увеличение сосудистого сопротивления).
Инсулин принимает участие в регуляции активности симпатической нервной системы в ответ на прием пищи. В экспериментальных работах установлено, что при голодании активность САС снижается, а при потреблении пищи повышается (особенно жиров и углеводов).
Предполагается, что инсулин, проходя через гематоэнцефалический барьер, стимулирует захват глюкозы в регуляторных клетках, связанных с вентромедиальными ядрами гипоталамуса. Это уменьшает их тормозящее воздействие на центры симпатической нервной системы ствола мозга и повышает активность центральной симпатической нервной системы.
В физиологических условиях этот механизм явлется регуляторным, при гиперинсулинемии же приводит к стойкой активации САС и стабилизации АГ.
Повышение активности центральных отделов САС приводит к периферической гиперсимпатикотонии. В почках активация β-рецепторов ЮГА сопровождается выработкой ренина, усиливается задержка натрия и жидкости. Постоянная гиперсимпатикотония на периферии в скелетных мышцах влечет нарушение микроциркуляторного русла, вначале с физиологической разреженностью микрососудов, а затем и к морфологическим изменениям, таким, как снижение количества функционирующих капилляров. Уменьшение числа адекватно кровоснабжаемых миоцитов, которые являются главным потребителем глюкозы в организме, ведет к нарастанию инсулинорезистентности и гиперинсулинемии. Таким образом, порочный круг замыкается.
Инсулин через митоген-активированную протеинкиназу усиливает повреждающие сосудистые эффекты за счет стимуляции различных факторов роста (тромбоцитарный фактор роста, инсулиноподобный фактор роста, трансформирующий фактор роста Р, фактор роста фибробластов и др.), что ведет к пролиферации и миграции гладкомышечных клеток, пролиферации фибробластов сосудистой стенки, накоплению внеклеточного матрикса. Эти процессы вызывают ремоделирование сердечно-сосудистой системы, приводя к потере эластичности сосудистой стенки, нарушению микроциркуляции, прогрессированию атерогенеза и, в конечном счете, к росту сосудистого сопротивления и стабилизации АГ.
Некоторые авторы полагают, что нарушение функции эндотелия играет основную роль в патогенезе АГ, связанной с метаболическими нарушениями. У лиц с инсулинорезистентностью и гиперинсулинемией наблюдается снижение реакции на вазодилатационное и усиление на вазоконстрикторное воздействие, что ведет к кардиоваскулярным осложнениям.
Для метаболического синдрома характерна гиперурикемия (встречается, по разным данным, у 22—60% больных с МС).
В настоящее время показано, что концентрация мочевой кислоты в крови коррелирует с триглицеридемией и степенью выраженности абдоминального ожирения; в основе этого явления лежит тот факт, что усиление синтеза жирных кислот активирует пентозный путь окисления глюкозы, способствуя образованию рибозо-5-фосфата, из которого происходит синтез пуринового ядра.
С учетом всех рассмотренных выше аспектов проблемы и должен формироваться терапевтический алгоритм патогенетического подхода к лечению метаболического синдрома.
Лечение метаболического синдрома
Комплекс лечения метаболического синдрома включает в себя следующие равнозначные позиции: изменение образа жизни, лечение ожирения, лечение нарушений углеводного обмена, лечение артериальной гипертонии, лечение дислипидемии.
Изменение образа жизни
Этот аспект лежит в основе успешного лечения метаболического синдрома.
Цель врача в данном случае — сформировать у больного устойчивую мотивацию, направленную на длительное выполнение рекомендаций по питанию, физическим нагрузкам, приему лекарственных препаратов. «Установка на успех» позволяет пациенту легче переносить те лишения, которых требует изменение образа жизни.
Изменение режима питания. Диета больного метаболическим синдромом должна не только обеспечивать снижение массы тела, но и не вызывать обменных нарушений не провоцировать повышения артериального давления. Голодание при синдроме Х противопоказано, так как является тяжелым стрессом, и при имеющихся метаболических нарушениях может привести к острым сосудистым осложнениям, депрессии, срыву в «пищевой запой». Питание должно быть частым, пищу следует принимать малыми порциями (обычно три основных приема пищи и два-три промежуточных) при суточной калорийности пищи не более 1500 ккал. Последний прием пищи — за полтора часа до сна. Основа питания — сложные углеводы с низким гликемическим индексом, они должны составлять до 50–60% пищевой ценности. Единица гликемического индекса пищи — это изменение гликемии после еды, равное изменению гликемии после потребления 100 г белого хлеба. Высоким гликемическим индексом обладают большинство кондитерских изделий, сладкие напитки, сдоба, мелкие крупы; их потребление следует исключить или свести до минимума. Низкий ГИ у цельнозерновых продуктов, овощей, фруктов, богатых пищевыми волокнами. Общее количество жиров не должно превышать 30% от общей калорийности, сатурированных жиров — 10%. Каждый прием пищи должен включать адекватное количество белка для стабилизации гликемии и обеспечения насыщения. Не менее двух раз в неделю следует употреблять рыбу. Овощи и фрукты должны присутствовать в рационе не менее пяти раз в день. Допустимое количество сладких фруктов зависит от степени нарушения углеводного обмена; при наличии сахарного диабета 2 типа их следует резко ограничить.
Пищевой соли — не более 6 г в день (одна чайная ложка).
Алкоголь, как источник «пустых калорий», стимулятор аппетита, дестабилизатор гликемии, следует исключить из рациона или свести до минимума. В случае невозможности отказа от алкоголя предпочтение следует отдавать красному сухому вину, не более 200 мл в день.
Пациентам рекомендуется ведение пищевого дневника, где они записывают, что, в каком количестве и в какое время было съедено и выпито.
Необходим отказ от табакокурения, это значительно снижает риск сердечно-сосудистых и онкологических осложнений.
Физическая активность. По оценкам G. Reaven, у 25% лиц, ведущих малоподвижный образ жизни, можно обнаружить инсулинорезистентность. Сама по себе регулярная мышечная активность приводит к метаболическим изменениям, снижающим инсулинорезистентность. Для достижения терапевтического эффекта достаточно ежедневно практиковать 30-минутную интенсивную ходьбу или три-четыре раза в неделю проводить 20—30-минутные пробежки.
Лечение ожирения
При лечении метаболического синдрома удовлетворительным результатом может считаться снижение массы на 10—15% в первый год лечения, на 5—7% на второй год и отсутствие рецидивов прибавки массы тела в дальнейшем.
Соблюдение низкокалорийной диеты и режима физической активности не всегда выполнимо для пациентов. В этих случаях показана лекарственная терапия ожирения.
В настоящее время в России зарегистрированы и рекомендованы для длительного лечения ожирения препараты орлистат и сибутрамин. Механизм их действия принципиально различен, что позволяет в каждом конкретном случае подбирать оптимальное лекарственное средство, а при тяжелых случаях ожирения, резистентных к монотерапии, назначать эти препараты комплексно.
Лечение нарушений углеводного обмена
Степень выраженности нарушений углеводного обмена при метаболическом синдроме колеблется от минимальной (нарушенные гликемия натощак и толерантность к глюкозе (НТГ)) до развития сахарного диабета 2 типа.
Лекарственные препараты, влияющие на углеводный обмен, в случае метаболического синдрома должны назначаться не только при наличии Т2СД, но и при менее тяжелых (обратимых!) нарушениях углеводного обмена. Гиперинсулинемия требует агрессивной терапевтической тактики. Имеются данные о наличии осложнений, характерных для сахарного диабета, уже на стадии нарушенной толерантности к глюкозе. Полагают, что это связано с частыми эпизодами постпрандиальной гипергликемии.
Мощный арсенал современных сахароснижающих средств позволяет выбрать в каждом конкретном случае оптимальную терапию.
Препараты, снижающие инсулинорезистентность
При метаболическом синдроме — препараты выбора.
А. Бигуаниды
В настоящее время единственным бигуанидом, снижающим инсулинорезистентность, является метформин. По результатам UKPDS, лечение метформином при Т2СД снижает риск смерти от сахарного диабета на 42%, инфаркта миокарда — на 39%, инсульта — на 41%.
Может считаться препаратом первого ряда в лечении метаболического синдрома.
Механизм действия: повышение чувствительности тканей к инсулину; подавление глюконеогенеза в печени; изменение фармакодинамики инсулина за счет снижения соотношения связанного инсулина к свободному и повышения соотношения инсулина к проинсулину; подавление окисления жиров и образования свободных жирных кислот, снижение уровня триглицеридов и ЛПНП, повышение ЛПВП; по некоторым данным — гипотензивный эффект; стабилизация или снижение массы тела. Снижает гипергликемию натощак и постпрандиальную гипергликемию. Гипогликемий не вызывает.
Может назначаться при НТГ, что особенно важно с точки зрения профилактики развития Т2СД.
Б. Тиазолидиндионы («глитазоны», инсулин-сенситайзеры)
К клиническому применению разрешены пиоглитазон и розиглитазон.
В России — малоприменяемая группа препаратов, вероятно, из-за относительной новизны, известного риска острой печеночной недостаточности и высокой стоимости.
Механизм действия: повышают захват глюкозы периферическими тканями (активируют GLUT-1 и GLUT-4, подавляют экспрессию фактора некроза опухолей, усиливающего инсулинорезистентность); уменьшают продукцию глюкозы печенью; снижают концентрацию свободных жирных кислот и триглицеридов в плазме за счет подавления липолиза (через повышение активности фосфодиэстеразы и липопротеинлипазы). Действуют только в присутствии эндогенного инсулина.
Ингибриторы α-глюкозидаз
Препарат акарбоза
Механизм действия: конкурентно ингибирует интестинальные α-глюкозидазы (сахаразу, мальтазу, глюкоамилазу) — ферменты, расщепляющие сложные сахара. Препятствует всасыванию простых углеводов в тонком кишечнике, что приводит к снижению постпрандиальной гипергликемии. Снижает массу тела и, как следствие, оказывает гипотензивное действие.
Секрeтогены инсулина
Препараты этого класса назначаются при метаболическом синдроме в случаях, когда не удается добиться удовлетворительного гликемического контроля с помощью средств, снижающих инсулинорезистентность, и/или акарбозы, а также при наличии противопоказаний к ним. Риск развития гипогликемий и увеличения массы тела при длительном применении требует строго дифференцированного подхода при выборе препарата. Назначение при НТГ не практикуется. Весьма эффективно сочетание секретогенов инсулина с бигуанидами.
А. Препараты сульфонилмочевины
Клинический опыт показывает, что монотерапия некоторыми секретогенами инсулина (в частности, глибенкламидом) у больных с метаболическим синдромом обычно оказывается неэффективной даже в максимальных дозах из-за нарастающей инсулинорезистентности — наступает истощение секреторной способности β-клеток и формируется инсулинопотребный вариант Т2СД. Предпочтение следует отдавать высокоселективным лекарственным формам, не вызывающим гипогликемий. Желательно, чтобы препарат можно было принимать один раз в день — для повышения комплаентности лечения.
Этим требованиям удовлетворяют препарат второй генерации гликлазид в фармакологической форме МВ (модифицированного высвобождения) и препарат третьей генерации глимепирид.
Гликлазид — высокоселективный препарат (специфичный к SUR1 субъединице АТФ-чувствительных калиевых каналов β-клетки), восстанавливает физиологический профиль секреции инсулина; повышает чувствительность периферических тканей к инсулину, вызывая посттранскрипционные изменения GLUT-4 и активируя действие инсулина на мышечную гликоген-синтетазу; снижает риск развития тромбозов, ингибируя агрегацию и адгезию тромбоцитов и повышая активность тканевого плазминогена; снижает уровень липидных пероксидов в плазме.
Глимепирид комплексируется с SURX рецептора сульфонилмочевины. Обладает выраженным периферическим действием: увеличивает синтез гликогена и жира за счет активации транслокации GLUT-1 и GLUT-4; снижает скорость глюконеогенеза в печени, повышая содержание фруктозо-6-бифосфата. Обладает более низкой, чем другие препараты сульфонилмочевины, глюкагонотропной активностью. Обеспечивает низкий риск гипогликемий — вызывает при минимальной секреции инсулина максимальное снижение глюкозы в крови. Обладает антиагрегационным и антиатерогенным эффектами, избирательно ингибируя циклооксигеназу и снижая превращение арахидоновой кислоты в тромбоксан А2. Комплексируется с кавеолином жировых клеток, что, вероятно, обусловливает специфичность влияния глимепирида на активизацию утилизации глюкозы в жировой ткани.
Б. Прандиальные регуляторы гликемии (секретогены короткого действия)
Быстродействующие гипогликемические препараты, производные аминокислот. В России представлены репаглинидом и натеглинидом.
Механизм действия — быстрая, кратковременная стимуляция секреции инсулина β-клеткой за счет быстрого обратимого взаимодействия со специфическими рецепторами АТФ-чувствительных калиевых каналов.
Считается, что натеглинид безопаснее в отношении развития гипогликемий: секреция инсулина, вызванная натеглинидом, зависит от уровня гликемии и снижается по мере уменьшения уровня глюкозы в крови. Исследуется возможность применения низких дозировок натеглинида при НТГ у больных с высоким риском сердечно-сосудистых осложнений (NAVIGATOR).
Инсулинотерапия
Раннее начало инсулинотерапии при метаболическом синдроме (за исключением случаев декомпенсации диабета) представляется нежелательным, так как, скорее всего, будет усугублять клинические проявления гиперинсулинизма. Однако следует отметить, что, во избежание осложнений сахарного диабета, компенсация углеводного обмена должна быть достигнута любой ценой. При неудовлетворительном эффекте от ранее перечисленных видов лечения должна быть назначена инсулинотерапия, возможно, в допустимых комбинациях с пероральными сахароснижающими препаратами. В отсутствии противопоказаний предпочтительна комбинация с бигуанидами.
Лечение артериальной гипертонии
Целевой уровень АД при развитии сахарного диабета 2 типа — < 130/85 мм рт. ст.; при нарушении функции почек — < 125/75 мм рт. ст.
Идеальный антигипертензивный препарат в данной клинической ситуации должен обладать доказанным влиянием на конечные сердечно-сосудистые точки, не иметь отрицательных метаболических эффектов, воздействовать на патогенетические звенья АГ при инсулинорезистентности и обладать целым рядом протективных эффектов (кардио-, нефро-, вазопротекция) с благоприятным воздействием на эндотелиальную функцию, тромбоцитарно-сосудистый гемостаз и фибринолиз.
Ингибиторы АПФ
Ингибиторы АПФ являются препаратами выбора в обсуждаемой клинической группе. Это связано, во-первых, с патогенетической обоснованностью их применения (активация РААС при ИР) и, во-вторых, с целым рядом преимуществ препаратов этого класса:
- снижение инсулинорезистентности и улучшение гликемического контроля;
- отсутствие отрицательного влияния на липидный и пуриновый обмены (FASET, ABCD, CAPPP, HOPE, UKPDS);
- вазопротективное действие — регресс сосудистого ремоделирования; антиатеросклеротическое действие (SECURE — HOPE-substudy);
- нефропротективное действие при диабетической и недиабетической формах нефропатии (FACET, MICRO-HOPE, REIN, EUCLID, AIPRI, BRILLIANT);
- коррекция эндотелиальной дисфункции, благоприятное воздействие на тромбоцитарный гемостаз и фибринолиз: ↑NO, ↑простациклина, ↓эндотелина, ↑эндотелий-зависимого фактора гиперполяризации, ↓прокоагулянтного потенциала, ↑тканевого активатора плазминогена, ↓агрегации тромбоцитов (TREND).
Таким образом, ингибиторы АПФ отвечают всем требованиям, предъявляемым к антигипертензивному препарату для пациентов с метаболическим синдромом.
β-адреноблокаторы
Назначение β-адреноблокаторов больным с метаболическим синдромом имеет неоспоримое патогенетическое преимущество ввиду наличия у них гиперсимпатокотонии, механизмы которой обсуждались выше. Однако долгое время в этой клинической группе данные препараты назначались с учетом целого ряда ограничений, считалось также, что пациентам с сахарным диабетом они противопоказаны ввиду их отрицательного влияния на углеводный и липидный обмен.
Однако,результаты UKPDS и других иследований доказали эффективность и безопасность применения селективных β-блокаторов у пациентов с метаболическими нарушениями и сахарным диабетом 2 типа. Все неблагоприятные побочные эффекты в основном оказались связаны с применением неселективных и низкоселективных β-адреноблокаторов.
Таким образом, у пациентов с метаболическим синдромом возможно применение высокоселективных β-адреноблокаторов (бетаксолол, бисопролол, небиволол и др.) в составе комбинированной терапии в малых дозах.
Диуретики
Наряду с β-адреноблокаторами, тиазидные и тиазидоподобные диуретики считаются препаратами первого ряда для длительной терапии больных неосложненной АГ. Однако, как и в случае с β-блокаторами, применение препаратов этой группы имеет целый ряд ограничений из-за развития побочных эффектов: снижение чувствительности периферических тканей к инсулину с компенсаторной гиперинсулинемией, повышение гликемии, неблагоприятное влияние на липидный профиль (повышение содержания в крови триглицеридов, общего холестерина, холестерина липопротеидов низкой плотности), нарушение обмена мочевой кислоты (гиперурикемия).
Во многих многоцентровых проспективных исследованиях отмечалась высокая частота развития сахарного диабета у больных АГ при лечении тиазидными и тиазидоподобными диуретиками. Тиазидоподобный диуретик индапамид, сочетающий в себе свойства диуретика и вазодилататора, в меньшей степени влияет на метаболические факторы риска. По данным литературы, при длительной терапии индапамид не оказывает отрицательного влияния на углеводный и липидный обмен, не ухудшает почечной гемодинамики, что делает его препаратом выбора в данной клинической группе.
Антагонисты кальция
В настоящее время подведен итог многолетней дискуссии об эффективности и безопасности антагонистов кальция.
В многочисленных многоцентровых исследованиях доказано снижение риска сердечно-сосудистых осложнений (STOP-2, NORDIL, INSIGHT, VHAT, NICS-EH, HOT, ALLHAT) на фоне терапии этими препаратами. Кроме того, антагонисты кальция обладают целым рядом преимуществ, обосновывающих возможность их применения у пациентов с метаболическим синдромом:
- снижение инсулинорезистентности, уменьшение базального и стимулированного глюкозой уровня инсулина;
- отсутствие отрицательного воздействия на углеводный, липидный пуриновый обмены;
- вазопротективное действие — регресс сосудистого ремоделирования, антиатеросклеротическое действие (INSIGHT, MIDAS, ELSA);
- нефропротективное действие (доказано для негидропиридиновых препаратов);
- коррекция эндотелиальной дисфункции — увеличение NO за счет антиоксидантных механизмов (↑активности супероксиддисмутазы, ↓разрушения NO), улучшение показателей тромбоцитарно-сосудистого и фибринолитического звеньев гемостаза (↓агрегации тромбоцитов, ↓тромбомодулина).
Предпочтение необходимо отдавать негидропиридиновым и дигидропиридиновым препаратам длительного действия ввиду способности короткодействующих антагонистов кальция, назначаемых в больших дозах, увеличивать риск сердечно-сосудистых осложнений.
Блокаторы АТ1-ангиотензиновых рецепторов
На современном этапе эта группа препаратов является одной из наиболее активно изучаемых.
Снижение риска сердечно-сосудистых осложнений у больных с АГ на фоне лечения лосартаном было показано в исследовании LIFE. Доказано нефропротективное действие для диабетической нефропатии при Т2СД (RENALL, IDNT, CALM). Кроме того, показана способность блокаторов АТ1-ангиотензиновых рецепторов снижать уровень мочевой кислоты (лосартан).
Влияние блокаторов АТ1-ангиотензиновых рецепторов на патогенетические звенья АГ при метаболическом синдроме и отсутствие негативного воздействия на углеводный и липидный обмены делают эти препараты перспективными в данной клинической группе. В настоящее время проводится многоцентровое исследование по оценке влияния валсартана на сердечно-сосудистые осложнения у пациентов с нарушением толерантности к углеводам (NAVIGATOR). Дальнейшее изучение этой группы препаратов может поставить их в один ряд с ингибиторами АПФ, когда речь идет о терапии метаболического синдрома.
α1-адреноблокаторы
До промежуточного анализа результатов исследования ALLHAT, в ходе которого было выявлено увеличение количества сердечно-сосудистых событий, в частности новых случаев сердечной недостаточности на фоне применения доксазозина, препараты этой группы рассматривались среди наиболее перспективных средств, используемых для лечения пациентов с метаболическим синдромом. Это связано со способностью α-адреноблокаторов повышать чувствительность тканей к инсулину и вследствие этого улучшать гликемический контроль, коррегировать липидный профиль, благоприятно воздействовать на гемостаз и эндотелиальную функцию.
Однако на данном этапе α1-адреноблокаторы могут быть использованы лишь как дополнительные препараты в комбинированной терапии АГ, в том числе и при метаболическом синдроме.
Агонисты I1-имидазолиновых рецепторов
Препараты этой группы занимают особое место в терапии метаболического синдрома из-за коррекции одного из основных звеньев патогенеза АГ — центральной гиперсимпатикотонии. Эти препараты, уменьшая центральную симпатическую импульсацию, позволяют повышать чувствительность периферических тканей к инсулину, улучшать гликемический контроль и снижать активность РААС.
К сожалению, нет данных о влиянии агонистов I1-имидазолиновых рецепторов на прогноз у больных АГ, что не позволяет рекомендовать препараты указанного класса в качестве средств первой линии в терапии АГ. Однако они с успехом могут быть использованы в комбинированной терапии.
Лечение дислипидемии
Гиполипидемическая терапия должна обязательно проводиться у пациентов с МС и сочетаться с лечебными воздействиями на ИР и гликемию.
Препаратами первого ряда в лечении дислипидемии у пациентов с метаболическим синдромом бесспорно являются статины благодаря хорошей клинической эффективности (снижение ЛПНП на 25—61%, снижение триглицеридов) и хорошей переносимости.
При изолированной гипертриглицеридемии или гипертриглицеридемии тяжелой степени препаратами выбора являются фибраты, которые уступают статинам по влиянию на ЛПНП, хуже переносятся и взаимодействуют с большим числом лекарственных средств. Исследования DAIS и VA HIT также доказали положительное влияние фибратов на сердечно-сосудистый риск при Т2СД.
Заключение
Таким образом, рассматривая МС как «генерализованное сердечно-сосудисто-метаболическое заболевание» (термин L. M. Resnick), мы предлагаем акцентировать внимание на патогенетических подходах к его терапии. Важны также разработка единых диагностических критериев и включение диагноза «метаболический синдром» в список Медицинских экономических стандартов. С точки зрения доказательной медицины желательно целенаправленное проведение многоцентровых исследований лекарственных препаратов, применяющихся для лечения метаболического синдрома.
Т. В. Адашева, кандидат медицинских наук, доцент О. Ю. Демичева Московский государственный медико-стоматологический Университет Городская клиническая больница №11
Купить Моксонидин СЗ таблетки 0,4мг №28 в аптеках
Инструкция по применению
Моксонидин-СЗ таб. 0,4мг №28
Лекарственные формы
таблетки 0,4мг Синонимы Моксарел Моксонидин Канон Моксонитекс Тензотран Физиотенз Группа Антигипертензивные — агонисты имидазолиновых рецепторов Международное непатентованное названиеМоксонидин Состав Действующее вещество — Моксонидин. Производители Северная звезда (Россия)
Фармакологическое действиеАнтигипертензивное. Является агонистом пре- и постсинаптических альфа2-адренорецепторов. Быстро и практически полностью абсорбируется в ЖКТ. Выводится с мочой в неизмененном виде. Интервал между достижением максимальной концентрации и выраженным снижением артериального давления составляет 2-4 ч. Продолжительность действия — более 12 ч (медленно выводится из ЦНС и на длительное время уменьшает концентрацию адреналина в плазме). Уменьшает гипертрофию миокарда левого желудочка, нивелирует признаки миокардиального фиброза, микроартериопатии, нормализует капиллярное кровоснабжение миокарда. Снижает общее периферическое сопротивление сосудов, легочное сосудистое сопротивление, содержание в крови ренина и ангиотензина II, адреналина и норадреналина в покое и при нагрузке, предсердного натрийуретического фактора (при нагрузке), альдостерона. Уменьшает резистентность тканей к инсулину, стимулирует высвобождение гормона роста. Побочное действиеСухость во рту (в начале лечения), утомляемость, слабость, головные боли, головокружение, угнетение ЦНС, периферические отеки. Показания к применениюАртериальная гипертензия; метаболический синдром. Противопоказания Гиперчувствительность, синдром слабости синусного узла, нарушение синоатриальной и AV проводимости II-III степени, брадикардия менее 50 ударов в мин, тяжелые нарушения ритма сердца, сердечная недостаточность (IV функциональный класс по NYHA), нестабильная стенокардия, выраженные нарушения функции печени и почек, нарушения периферического кровообращения (облитерирующий атеросклероз сосудов нижних конечностей с синдромом перемежающейся хромоты, болезнь Рейно), болезнь Паркинсона, депрессивные состояния, эпилепсия, глаукома, беременность, кормление грудью (на время лечения прекращают), подростковый возраст (до 16 лет). Способ применения и дозировкаВнутрь, во время или после еды, запивая небольшим количеством жидкости, — 0,2 мг 1 раз в сутки (утром). При отсутствии эффекта (через 3 нед) — 0,4 мг однократно (утром) или по 0,2 мг 2 раза в сутки (утром и вечером). Разовая доза не должна превышать 0,4 мг, суточная 0,6 мг, при почечной недостаточности разовая доза не должна превышать 0,2 мг, суточная 0,4 мг. Передозировка Симптомы: гипотония, сухость во рту, сердцебиение, слабость, сонливость.Лечение: симптоматическое. В качестве специфического антидота вводят идазоксан (антагонист имидазолинов). Взаимодействие Усиливает (взаимно) эффект др. гипотензивных препаратов, депримирующих средств (алкоголь, транквилизаторы, барбитураты, нейролептики). Особые указанияС осторожностью применяют при почечной недостаточности. Во время лечения исключается употребление алкоголя, не рекомендуется (особенно в начале лечения) работа с механизмами, требующая повышенного внимания и быстроты реакции. Условия храненияСписок Б. При комнатной температуре.
Особенности антигипертензивной терапии при ожирении
С.В. НЕДОГОДА
, д.м.н.,
А.С. САЛАСЮК
,
И.Н. БАРЫКИНА
,
В.В. ЦОМА
,
Е.В. ЧУМАЧЕК
,
В.Ю. ХРИПАЕВА
,
Волгоградский государственный медицинский университет
В настоящее время ожирение является одной из наиболее важных междисциплинарных медицинских проблем. Оно является одной из основных причин повышения АД. Так, по данным Фраменгемского исследования, ожирение вероятно играет основную роль в развитии гипертонической болезни у 78% мужчин и 65% женщин [10]. При этом сами жировые клетки играют важную роль в развитии артериальной гипертензии, т. к. продуцируют самые различные биологически активные субстанции, часть из которых обладает прессорными и провоспалительными эффектами. Особенно важным в этом плане является лептин, который посредством активации симпатической нервной системы и прямого действия на почки (усиление реабсорбции натрия) способствует повышению АД. Кроме этого, ожирение само по себе негативно влияет на структуру почечной ткани и повышает риск развития почечной недостаточности и прогрессирования артериальной гипертензии. Также жировая ткань, обладая собственной ренин-ангиотензиновой системой, может активно продуцировать ангиотензин.
Основными факторами развития артериальной гипертензии на фоне ожирения являются гиперинсулинемия, гиперлептинемия, гиперкортизолемия, почечная дисфункция, измененные структура и функция сосудов, повышенная активность симпатической и ренин-ангиотензиновой систем, снижение активности натрийуретического гормона [12].
Основные механизмы формирования артериальной гипертензии при ожирении:
• изменения почечной гемодинамики, • структурные изменения в почках, • активация симпато-адреналовой нервной системы, • инсулинорезистентность, • свободные жирные кислоты (СЖК), • лептин.
Рассмотрим перечисленные механизмы подробнее.
Изменения почечной гемодинамики.
Выявлена прямая связь между повышением массы тела и задержкой натрия. Основным механизмом задержки натрия и жидкости при артериальной гипертензии на фоне ожирения является активация ренин-ангиотензиновой системы (РАС), симпато-адреналовой системы (САС) и гиперинсулинемия [7]. На первоначальном этапе развивается компенсаторное снижение почечного сосудистого сопротивления, происходит повышение тока плазмы через почки, скорости почечной фильтрации, что частично препятствует усиленной реабсорбции натрия. Однако впоследствии на этом фоне усиливается продукция ангиотензина II и цитокинов в сочетании с активацией САС. У пациентов с ожирением отмечается неадекватно низкий натриуретический ответ. Эти изменения усиливают «стресс» стенок клубочков и на фоне других факторов риска (гиперлипидемия и гипергликемия) и достаточно быстро приводят к развитию гломерулосклерза, протеинурии, микроальбуминурии и функциональной недостаточности нефронов. Ранняя почечная гиперфильтрация при ожирении схожа с таковой при сахарном диабете 1-го типа.
Cтруктурные изменения в почках.
На фоне ожирения развивается особый вариант гломерулопатии с фокальным сегментарным гломерулосклерозом и увеличением самих клубочков (ретроспективное исследование с 6 800 биопсиями почек). Интересно, что на фоне такого фокального гломерулосклероза отмечается меньшая частота развития нефротического синдрома, менее выраженные проявления сегментарного склероза и больший размер клубочков. Считается, что эти изменения также обусловлены сопутствующей патологией (прежде всего артериальной гипертензией и дислипидемией). В исследовании German WHO MONICA (Monitoring of Trends and Determinants in Cardiovascular Disease) было показано, что повышение частоты микроальбуминурии было достоверно выше у лиц с большим соотношением объем талии/объем бедер. Повышение внутрипочечного давления играет важную роль в задержке натрия, в основном за счет замедления скорости тубулярного тока. Многочисленные исследования показали, что при ожирении увеличивается вес почек, что связано с пролиферацией эндотелиальных клеток, накоплением интраренально липидов и отложением солей гиалуроновой кислоты в матриксе и мозговом слое почек. Эти отложения в плотно инкапсулированной почке приводят к механическому повышению внутрипочечного давления. Повышение давления и объема вызывают паренхиматозный пролапс и обструкцию при оттоке мочи, приводя к замедлению интраренального тока и повышению почечной реабсорбции натрия. Особенно важно повышение реабсорбции натрия в петле Генле, что приводит к компенсаторной вазодилатации в почках, повышению скорости клубочковой фильтрации и стимуляции РАС [8]. Однако увеличение объема жидкости лишь не на долгий период может обеспечить поддержание нормальной концентрации натрия в крови. В дальнейшем постоянная гломерулярная гиперфильтрация в комбинации с нарушением толерантности к глюкозе, гиперлипидемией и гипертензией быстро приводит к развитию гломерулосклероза и почечной недостаточности.
Активация симпато-адреналовой нервной системы.
Механизмы и последствия гипертактивации САС носят разноплановый характер — инсулинорезистентность, усиление афферентной иннервации почек с повышением внутрипочечного давления, приводящего к активации почечных механорецепторов, повышение уровня свободных жирных кислот, ангиотензина II, лептина, потенцирование чувствительности центральных хеморецепторов и нарушение барорефлекторной регуляции [5]. Активация САС в мышцах и почках при ожирении подтверждена микронейрографическим методом. Интересно, что препараты, подавляющие центральную симпатическую активность, вызывают большее снижение АД у пациентов с ожирением, чем у пациентов без ожирения.
Инсулинорезистентность.
В настоящее время гиперинсулинемия считается ключевым фактором в развитии артериальной гипертензии при ожирении. Известно, что при ожирении значительно повышается уровень инсулина, что обусловлено необходимостью поддержания метаболизма углеводов и жирных кислот на более высоком уровне, причем это происходит на фоне инсулинорезистентности периферических тканей [11]. Имеющиеся в настоящее время данные позволяют говорить о том, что при инсулинорезистентности нарушается инсулин-опосредованная вазодилатация, что способствует повышению АД [9].
Cвободные жирные кислоты (СЖК).
Считается, что высокий уровень СЖК повышает АД за счет повышения симпатической активности, или вазоспатического эффекта, реализуемого через α- адренергические рецепторы. При висцеральном ожирении в печень поступает слишком много СЖК, что активирует печеночные афферентные пути, повышает активность САС и способствует развитию инсулинорезистентности. При ожирении уровень СЖК примерно в 2 раза выше, чем у людей без ожирения.
Лептин
— пептид, состоящий из 167 аминокислот и играющий важную роль как в патогенезе ожирения, так и артериальной гипертензии, что связано с наличием у него различных механизмов прессорного эффекта [9]. Лептин секретируется белыми адипоцитами и его уровень прямо коррелирует с количеством жировой ткани и всегда повышен у людей с ожирением. У женщин уровень лептина выше, чем у мужчин. Лептин проходит через гематоэнцефалический барьер в ЦНС посредством эндоцитоза, где он связывается с рецепторами (Ob-R) в латеральной и медиальной областях гипоталамуса. Связывание лептина с рецепторами вызывает их активацию, которая обеспечивает регуляцию энергетического баланса через снижение аппетита и повышение энерготрат за счет стимуляции САС. Данные о том, что лептин снижает потребление пищи и регулирует массу тела, подтверждены как экспериментальными, так и клиническими данными. При нарушенной способности синтезировать лептин или имеющихся мутациях рецепторов к лептину всегда развивается тяжелое ожирение. Гипертензивный эффект лептина усиливается при эндотелиальной дисфункции, которая практически всегда имеет место при ожирении. Прессорный эффект лептина почти полностью исчезает на фоне α– и β-адренергической блокады [17].
Жировая ткань и активность ренин-ангиотензиновой системы
При ожирении происходит активация РАС на фоне увеличения объема жидкости и задержки натрия. Отличительной особенностью является значительное повышение уровня альдостерона [15], что может быть связано с выделением специфического печеночного фактора (возможно, жирной кислоты), оказывающего стимулирующее влияние на его синтез. Также имеется взаимосвязь между уровнем ангиотензина плазмы (Анг II), активностью ренина (АРП) и АПФ плазмы с ИМТ [6].
Известно, что жировая ткань обладает собственной РАС, которая играет важную роль в функционировании жировой ткани. Адипоциты способны синтезировать все компоненты РАС. Они также стимулируют рецепторы Анг II, повышая их афинность к паракринному Анг II. Не исключено, что локальный Анг может быть фактором роста жировых клеток. Было показано, что при повышенном уровне 11β-гидроксистероидной дегидрогеназы, участвующей в процессе образования кортизола, развивается артериальная гипертензия со всеми признаками метаболического синдрома. У женщин с ожирением выявлена гиперэкспрессия гена, кодирующего ренин, АПФ и рецепторы к Анг II тип 1 подкожной абдоминальной жировой ткани. Важно отметить, что повышенный уровень Анг II возникает прежде всего из-за излишней массы жировой ткани, приводя к повышению АД.
Естественно, что все описанные выше гуморальные нарушения при артериальной гипертензии и ожирении приводят к изменениям со стороны сердечно-сосудистой системы:
• сосудистые изменения; • изменения со стороны сердца; • изменение микроциркуляции; • маркеры воспаления.
Сосудистые изменения.
При ожирении изменения происходят на клеточном и молекулярном уровнях, приводя к повышению сосудистого тонуса [18]. В норме инсулин обладает свойствами вазодилататора за счет способности подавлять потенциалозависимый поток ионов Ca2+. Это приводит к стимуляции транспорта глюкозы и ее фосфорилирования с образованием глюкозо-6-фосфата, который потом активирует транскрипцию Ca-АТФ-азы и в конечном итоге снижает уровень внутриклеточного кальция и сосудистое сопротивление. При ожирении на фоне инсулинорезитентности указанные механизмы нарушаются и это приводит к повышению сосудистого сопротивления.
Выявлено снижение эластичности крупных сосудов по данным ядерно-магнитного резонанса, которое прямо коррелировало с повышением массы абдоминального висцерального жира. Важно отметить, что снижение массы тела при ожирении сопровождается выраженным уменьшением сосудистого сопротивления и среднего АД.
Изменения со стороны сердца.
Артериальная гипертензия без ожирения чаще всего приводит к концентрической гипертрофии левого желудочка, в то время как при сочетании артериальной гипертензии и ожирения преимущественно развивается его эксцентрическая гипертрофия. Известно, что при концентрической ГЛЖ дилатация сердца наступает поздно, в отличие от эксцентрической гипертрофии [13]. Сочетание повышения АД и ожирения также может приводить к смешанному типу кардиальной гипертрофии, вызванной повышением пред- (прямое следствие ожирения) и постнагрузки (последствие активации САС и повышения АД). После поправки и стандартизации пациентов по основным факторам риска становится очевидным, что на каждую единицу повышения ИМТ риск развития сердечной недостаточности повышается на 5% у мужчин и 7% у женщин. При выраженном ожирении риск развития хронической сердечной недостаточности повышен в 2 раза. Анализ данных аутопсий в Mayo Clinic показал, что средний вес сердца при ожирении и артериальной гипертензии составлял 467 г, по сравнению с 367 г у пациентов с ожирением, но без заболеваний сердца и 272 г у пациентов без ожирения. Так как ГЛЖ является независимым фактором риска внезапной смерти и смерти в результате декомпенсации сердечных заболеваний, это может частично объяснить высокую сердечно-сосудистую заболеваемость и смертность при ожирении.
Инфильтрация мононуклеарными клетками в области синоатриального узла и отложение жировых клеток в проводящей системе являются еще одними типичными изменениями в сердце при ожирении. Липоматозная гипертрофия в межпредсердной перегородке также очень часто выявляется при ожирении. Поэтому состояние миокарда при ожирении является «идеальным» фоном для развития аритмий и внезапной смерти.
Изменение микроциркуляции. Повышенный риск тромбообразования может вносить существенный вклад в ухудшение прогноза при сердечно-сосудистой патологии на фоне избыточной массы тела. При ожирении часто имеет место полицитемия. Эпидемиологические данные показывают, что гиперкоагуляция и нарушения фибринолиза прямо взаимосвязаны с повышением массы тела или отношения объем талии/объем бедер. При ожирении повышен уровень фактора VII, фибриногена, плазминогена, ингибитора активатора плазминогена (ИАП-1) и ряда других факторов, повышающих риск развития сердечно-сосудистых осложнений [18]. Продукция жировой тканью лептина или медиаторов воспаления также повышает риск тромбоза.
Mаркеры воспаления.
Адипоциты продуцируют воспалительные цитокины: фактор некроза опухоли α (ФНО-α), интерлейкин–6 (ИЛ-6), С-реактивнй белок (СРБ) и ИАП-1. Фактически ожирение можно рассматривать как состояние «хронического воспаления» [3]. Несомненно, что имеющаяся взаимосвязь между ожирением и повышением риска сердечно-сосудистых осложнений в значительной мере предопределяется высоким уровнем медиаторов воспаления [4].
Антигипертензивная фармакотерапия
В настоящее время можно достаточно точно сформулировать требования [1] к антигипертензивной терапии при ожирении:
Стандартные цели:
• Достижение целевого АД. • Улучшение прогноза. • Замедление конверсии в СД. • Органопротекция.
Специфические цели:
• Уменьшение инсулинорезистентности. • Положительное влияние на адипоциты (лептин, грелин, резистин, адипонектин). • Стабилизация /снижение массы тела. • Коррекция метаболических нарушений. • Снижение гиперактивации САС и РААС. • Положительное влияние на протромбогенный статус и воспаление. • Уменьшение гиперволемии. • Снижение эпизодов СНОА.
Естественно, что для практического врача очень важно знать, какие классы антигипертензивных препаратов наиболее эффективны у пациентов с сочетанием артериальной гипертензии и ожирением. Но парадоксальность ситуации заключается в том, что ни в одних международных и национальных руководствах не даны рекомендации по выбору лечения в этой клинической ситуации (естественно, что понятие метаболического синдрома не является синонимичным ожирению). Одним из объяснений этого пробела является очень небольшое количество исследований по антигипертензивной терапии при ожирении. Данные метаанализа (рис. 1
) однозначно не идентифицируют антигипертензивный препарат выбора для обсуждаемой клинической ситуации. Правда, они анализировали не антигипертензивную эффективность, а влияние антигипертензивных препаратов на вес пациентов [16].
Эти же авторы отметили существенную прибавку в весе пациентов при использовании пропранолола, атенолола и метопролола, что заставило говорить о возможном антилиполитическом эффекте «старых» бета-адреноблокаторов. Считается, что «старые» бета-адреноблокаторы способствуют прибавке 1,2 кг/год благодаря снижению энерготрат в покое и уменьшению термогенеза (до 10% в некоторых РКИ). По данным этого же метаанализа, ИАПФ способны снижать вес пациента от 0,3 до 5,3 кг.
Последние европейские рекомендации 2013 г. по лечению артериальной гипертензии (ESH/ESC Guidelines for the management of arterial hypertension) декларируют, что «поскольку метаболический синдром часто расценивается как «предиабетическое» состояние, то предпочтение отдается блокаторам ренин-ангиотензиновой системы и антагонистам кальция поскольку они потенциально могут улучшать или, по крайней мере, не ухудшать чувствительность к инсулину, в то время как бета-блокаторы (за исключением бета-блокаторов с вазодилатирующими свойствами) и диуретики должны рассматриваться как дополнительные препараты, использовать которые предпочтительно в низких дозах. В них в разделе «Препараты, которым отдается предпочтение в определенных ситуациях» также указывается на то, что ИАПФ, блокаторы рецепторов ангиотензина II (БРА) и антагонисты кальция являются препаратами выбора при метаболическом синдроме. Это важно и для выбора препарата при сочетании артериальной гипертензии и ожирения, поскольку последнее является обязательным компонентом метаболического синдрома [2].
Среди существующих исследований по антигипертензивной терапии при ожирении наиболее значимыми являются следующие:
Исследование «The Treatment in Obese Patients with Hypertension» (TROPHY).
Сравнение эффективности лизиноприла и ГХТЗ на протяжении 12 нед. лечения у 232 пациентов с ожирением и артериальной гипертензией с ИМТ 28—40 кг/м2 у мужчин и 27—40 кг/м2 у женщин и ДАД 90—109 мм рт. ст. выявило, что в группе лизиноприла (10 мг/сут) было 57% респондеров, в то время как на низкой дозе дозе ГХТЗ (12,5 мг/сут) их было 29 и 46% респондеров на высокой дозе ГХТЗ (50 мг/сут). Естественно, что на последнем режиме терапии проявились негативные метаболические эффекты классического тиазидного диуретика.
Исследование «Candesartan Role on Obesity and on Sympathetic System» (CROSS study)
. Сравнение эффективности кандесартана (8—16 мг) и ГХТЗ (25—50 мг) на протяжении 12 нед. лечения у 127 пациентов с ожирением и артериальной гипертензией (ИМТ >30 кг/м2) выявило одинаковый гипотензивный эффект в группах. Однако снижение мышечной нервной симпатической активности было достоверным только в группе кандесартана (20,7% (p < 0,05) против 3,1% (p > 0,05) на ГХТЗ) и повышение чувствительности к инсулину в группе кандесартана на 24,7% (p < 0,05) против ее снижения в группе ГХТЗ — на 9,2% (p > 0,05).
Исследование «A comparison of Telmisartan plus HCTZ with amlodipine plus HCTZ in Older patients with predominantly Systolic hypertension» (SMOOTH)
. Сравнение эффективности комбинации телмисартан/ГХТЗ (80/12,5 мг/cут) против валсартан/ГХТЗ (160/12,5 мг/cут) на протяжении 10 нед. лечения у 840 пациентов с ожирением (ИМТ > 27 кг/м2) и артериальной гипертензией (САД 140—179 мм рт. ст. и ДАД 95—109 мм рт. ст.) выявило, что комбинация телмисартан/ГХТЗ снижает САД и ДАД больше, чем валсартан/ГХТЗ на 3,9 и 2,0 мм рт. ст. (< 0,001).
Исследование «Пациенты с Метаболическим сИНдрОмом — эффекТивность и переносимость Арифона Ретард в лечении АГ» (Минотавр).
На терапии атипичным диуретиком Арифоном ретард было достигнуто значение целевого уровня АД в 64% против 41% на обычной терапии, снижение веса через год на 3,2 кг против 3,0 кг на обычной терапии и улучшение липидного спектра и гликемического профиля.
Открытое многоцентровое исследование эффективности и безопасности трандолаприла у пациентов с артериальной гипертензией и избыточной массой тела
(ИМТ ≥ 25 кг/м2) выявило, что через 3 мес. лечения 84,7% пациентов достигли целевого АД. Схожие результаты были получены и в открытом многоцентровом исследовании эффективности и безопасности трандолаприла у пациентов с артериальной гипертензией и избыточной массой тела в Турции. Такая высокая эффективность трандолаприла у этой категории пациентов может быть связана с его наиболее высокой липофильностью и продолжительностью антигипертензивного эффекта среди всех ИАПФ.
Исследование «The Hypertension-Obesity-Sibutramine Study» (HOS)
. В этом многоцентровом проспективном двойном слепом рандомизированном плацебо-контролируемом исследовании участвовал 171 пациент в возрасте от 20 до 65 лет с сочетанием ожирения и артериальной гипертензии (ИМТ 27—45 кг/м2 и САД от 140 до 160 мм рт. ст. и/или ДАД от 90 до 100 мм рт. ст.) После 2-недельного вводного перода (run-in period) пациенты были рандомизированы на один из трех вариантов комбинированной антигипертензивной терапии: фелодипин 5 мг/рамиприл 5 мг (57 пациентов), верапамил 180 мг/трандолаприл 2 мг (55 пациентов) и метопролол сукцинат 95 мг/гидрохлортиазид 12,5 мг (59 пациентов). В каждой из этих групп пациенты были также рандомизированы в подгруппы, получавшие сибутрамин (15 мг). Вместе с этим было установлено, что снижение веса и степени висцерального ожирения, улучшение показателей углеводного и липидного обменов, связанное с приемом сибутрамина, было минимальным в группе пациентов, находившихся на терапии метопрололом/гидрохлортиазидом 12,5 мг при сравнении с другими режимами антигипертензивной терапии. А наиболее благоприятный эффект на все анализируемые параметры оказывал ИАПФ рамиприл.
Прямое сравнительное исследование ИАПФ и сартанов у лиц с избыточной массой тела
[14]. В это клиническое исследование было включено 120 пациентов (61 мужчина и 59 женщин) в возрасте от 18 до 60 лет включительно и имеющие индекс массы тела (ИМТ) >27 кг/м2. Нарушение толерантности глюкозы определяли при ее уровне в плазме крови натощак <7 ммоль/л и после перорального приема 75 мг глюкозы >7,8 и <11,1 ммоль/л. Систолическое АД (САД), определенное методом Короткова, согласно критериям включения должно было быть в положении сидя > 140 мм рт. ст. и < 160 мм рт. ст. и/или диастолическое АД (ДАД) > 90 мм рт. ст. и < 100 мм рт. ст. Пациенты были рандомизированы «методом конвертов» на 4 группы: I группа принимала периндоприл (Престариум «А», ) в суточной дозе 10 мг, II группа принимала эналаприл (Ренитек, ) в суточной дозе 20 мг, III группа принимала лозартан (Козаар, ) в суточной дозе 100 мг, IV группа принимала телмисартан (Микардис, ) 80 мг на протяжении 24 недель.
Всем пациентам исходно и после курсовой терапии проводилось суточное мониторирование артериального давления (СМАД), ЭхоКГ, исследование сосудистой эластичности и лабораторное обследование.
Результаты проведенного исследования позволяют сделать однозначный вывод о том, что имеются существенные различия между антигипертензивными препаратами как внутри одного класса, так и между этими классами. Причем эти различия касаются всего спектра фармакодинамических эффектов — от степени снижения АД до органопротекции и метаболических эффектов. В том, что терапия периндоприлом (Престариум «А») позволила достичь значительно лучшего контроля АД, нет ничего удивительного, т. к. известно, что в суточной дозе 10 мг он является наиболее эффективным ингибитором АПФ у пациентов, не отвечающих на терапию другими ингибиторами АПФ или антагонистами рецепторов ангиотензина. Кроме этого, высокая эффективность периндоприла была подтверждена в российском исследовании ПРЕМИЯ, где у 70% пациентов имелась избыточная масса тела и исследовании во Франции, где у трети пациентов имелось ожирение. Важным клиническим аспектом является то, что при терапии периндоприлом не происходит активации САС. Более того, данные спектрального анализа ритма сердца указывают на нормализацию симпатической активности. Подтверждением того, что препарат, уменьшая инсулинорезистентность, способен уменьшать ЧСС (показатель, который в условиях реальной клинической практики является косвенным маркером гиперактивации САС), являются результаты исследования ПРЕМИЯ, в котором на терапии периндоприлом было отмечено урежение ЧСС на 6,1 уд/мин. Мощный кардио-, ангио- и нефропротективный эффект периндоприла хорошо доказан, и его преимущества перед другими препаратами в проведенном исследовании очевидны, но они лишь отчасти могут быть связаны с лучшим контролем АД при его применении. Значительный вклад в органопротекцию вносит влияние препарата на метаболические показатели, каждый из которых сам по себе (гиперлипидемия, гипергликемия, гиперурикемия, гиперлептинемия) является мощным фактором риска сосудистых поражений.
Улучшение липидного спектра крови и особенно триглицеридов нельзя считать случайным артефактом, т. к. и в других исследованиях было отмечено повышение ЛПВП на 0,16 ммоль/л при одногодичной терапии пациентов с артериальной гипертензией и сахарным диабетом 2-го типа и снижение триглицеридов на 0,6 ммоль/л при терапии пациентов с артериальной гипертензией по результатам двойного слепого РКИ.
Периндоприл так же благоприятно влиял на показатели пуринового обмена. Кроме того, он благоприятно [1] влияет на ключевые гормоны ожирения и инсулинорезистентность (рис. 2
).
Рис. 2. Влияние различных классов антигипертензивных препаратов на основные звенья патогенеза ожирения
Если же анализировать возможности применения отдельных классов антигипертензивных препаратов при ожирении и повышенном АД, то можно констатировать, что, помимо предпочтительности применения отдельных классов (ИАПФ, сартаны, агонисты имидазолиновых рецепторов), внутри самих классов существуют большие внутриклассовые различия.
Диуретики
Одним из основных механизмов повышения АД при артериальной гипертензии на фоне ожирения является гиперволемия, возникающая вследствие повышенной реабсорбции натрия и воды в проксимальных отделах почечных канальцев на фоне гиперинсулинемии и повышение сосудистого сопротивления. Поэтому диуретики могли бы стать одним из основных классов антигипертензивных препаратов, применяющихся при данной патологии. Однако несомненные достоинства классических тиазидных диуретиков оказываются явно недостаточными, для того чтобы компенсировать их негативные эффекты (прежде всего метаболические — гипокалиемию, ухудшение углеводного, липидного и пуринового обменов).
Согласно результатам клинических наблюдений, все тиазидные диуретики ухудшают углеводный обмен и даже в суточной дозе 12,5 мг. При этом чем выше исходный уровень гликемии, тем в большей степени он повышается на фоне их применения. У лиц молодого возраста нарушение толерантности к глюкозе развивается в среднем через 5 лет непрерывного приема тиазидных диуретиков, а у лиц пожилого возраста — через 1—2 года после начала их применения. В случае сопутствующего сахарного диабета показатели гликемического контроля ухудшаются уже в течение первых нескольких дней от начала приема тиазидных диуретиков. Помимо неблагоприятного влияния на углеводный обмен, тиазидные диуретики могут оказывать негативное действие на липидный и пуриновый обмены.
Особняком среди диуретиков стоит индапамид ретард (Арифон ретард), который, в отличие от классических тиазидных диуретиков, не оказывает отрицательного влияния на метаболизм глюкозы, липидов и мочевой кислоты. При этом необходимо иметь в виду, что индапамид ретард (Арифон ретард) обладает доказанным и выраженным кардио-, ангио- и нефропротективным действием, что делает его препаратом выбора из группы диуретиков для лечения пациентов с ожирением и нарушениями углеводного, липидного обмена как при монотерапии, так и при комбинированной терапии.
Бета-адреноблокаторы
Повышение активности САС у пациентов с ожирением диктует необходимость применения β-блокаторов для нормализации у этой категории пациентов. Однако неселективные β-блокаторы (атенолол, пропранолол) негативно влияют на углеводный и липидный обмен. Кроме этого, β-блокаторы (в т. ч. и селективные β1-блокаторы в высоких дозах), блокируя β-адренорецепторы поджелудочной железы, тормозят высвобождение инсулина. Так как β-блокаторы вызывают развитие НТГ и прибавку в весе, их использование при неосложненной гипертензии и ожирении не рекомендуется в качестве первой линии терапии. Однако эта группа препаратов может применяться при ожирении и артериальной гипертензии в тех случаях, когда не удается добиться целевого уровня АД из-за выраженной активации САС и тахикардии.
«Новые» высокоселективные β1-блокаторы (бисопролол, карведилол, небиволол) практически лишены тех неблагоприятных побочных эффектов, которые ограничивали их широкое применение у пациентов с нарушением углеводного и липидного обмена. Кроме этого, небивилол обладает рядом уникальных свойств, которые позволяют существенно расширить возможности его клинического применения (улучшение эндотелиальной и эректильной функции, повышение уровня тестостерона у мужчин).
Антагонисты кальция
Как известно, в этой группе выделяют дигидропиридиновые (нифедипидин, амлодипин, фелодипин, лацидипин) и недигидропиридиновые (верапамил и дилтиазем) антагонисты кальция. Представители первой подгруппы на фоне снижения АД, развивающегося за счет периферической вазодилатации, могут увеличивать частоту сердечных сокращений (ЧСС) и способствовать активации САС. Представители второй группы, сохраняя выраженную антигипертензивную активность, обладают значительно менее выраженным периферическим вазодилатирующим действием, чем дигидропиридиновые антагонисты кальция. Более того, они способны уменьшать ЧСС (за счет подавления активности автоматизма синусового узла) и уменьшать активность САС (данные исследования VAMPHYR), что важно для пациентов с ожирением.
Ингибиторы ангиотензинпревращающего фермента (ИАПФ)
Периндоприл, рамиприл и трандолаприл благодаря своей высокой липофильности и высокой афинности к АПФ плазмы и тканей способны существенно снижать инсулинорезистентность.
Антагонисты рецепторов ангиотензина II (АРА II)
Так как действие данного класса препаратов связано с подавлением активности РАС, то они имеют много общих черт с ИАПФ (наличие выраженной кардио-, ангио- и нефропротективных свойтсв), однако обладают лучшей переносимостью.
Липофильные АРА II (телмисартан, ирбесартан) обладают дополнительным свойством улучшать чувствительность тканей к инсулину, углеводный и липидный обмен. Лосартан снижает уровень мочевой кислоты и является препаратом выбора при гиперурикемии на фоне ожирения. Валсартан улучшает эректильную функцию и повышает уровень тестостерона у мужчин.
Агонисты имидазолиновых рецепторов
Предпосылкой к назначению агонистов I2-имидазолиновых рецепторов (АИР) пациентам с ожирением и артериальной гипертензией является их способность улучшать чувствительность тканей к инсулину и углеводный обмен. При этом, по данным российского многоцентрового исследования АЛМАЗ и еще двух международных исследований, у больных с метаболическим синдромом и ожирением терапия моксонидином достоверно улучшала показатели липидного и углеводного обмена, чувствительность тканей к инсулину, способствовали снижению массы тела и уровня лептина в крови и улучшению функции эндотелия сосудов.
Альфа-адреноблокаторы
Альфа-адреноблокаторы сохраняют свой терапевтический потенциал, несмотря на результаты исследования ALLHAT, при лечении артериальной гипертензии у больных с ожирением благодаря своей способности уменьшать инсулинорезистентность, улучшать углеводный и липидный обмен и оказывать положительное влияние на почечную гемодинамику. Однако применение должно ограничиваться только использованием в комбинации с другими антигипертензивными средствами.
Для практического врача можно предложить следующий алгоритм антигипертензивной терапии у пациентов с ожирением (рис. 3
). В целом анализ имеющейся литературы указывает на то, что ИАПФ или АРА II должны быть обязательным компонентом гипотензивной терапии при сочетании артериальной гипертензии и ожирения. Но для разрыва «порочного» круга артериальной гипертензии и ожирения практически все пациенты нуждаются в комбинированной антигипертензивной терапии на фоне назначения препаратов для снижения веса.
Литература
1. Недогода С.В. Ожирение и артериальная гипертензия: теория и практика выбора оптимального гипотензивного препарата. М.: Медиком, 2012. С. 1-80. 2. Bergman RN, Van Citters GW, Mittelman SD et al. Central role of adipocyte in the metabolic syndrome. J Invest Med, 2001, 49: 119-126. 3. Chu NF, Spiegelman D, Hotamisligil GS et al. Plasma insulin, leptin, and soluble TNF receptors levels in relation to obesity-related atherogenic and thrombogenic cardiovascular disease factors among men. Atherosclerosis, 2001, 157: 495-503. 4. Drenick EJ, Bale GS, Seltzer F, Johnson DG. Excessive mortality and cause of death in morbidly obese men. JAMA, 1980, 243: 443-445. 5. Esler M The sympathetic system and hypertension. Am J Hypertens, 2000, 13: 99S-105S. 6. Gorzelniak K, Engeli S, Janke J et al. Hormonal regulation of the human adipose-tissue renin-angiotensin system: relationship to obesity and hypertension. J Hypertens, 2002, 20: 1115-1120. 7. Gupta AK, Clark RV, Kirchner KA. Effects of insulin on renal sodium excretion. Hypertension,1992, 19 (suppl. 1): I78-I82. 8. Hall JE. Mechanisms of abnormal renal sodium handling in obesity hypertension. Am J Hypertens, 1997, 10: 49S-55S. 9. Kuo J, Jones OB, Hall JE. Inhibition of NO synthesis enhances chronic cardiovascular and renal actions of leptin. Hypertension, 2001, 37: 670-676. 10. Licata G, Scaglione, Capuana G, Parrinello G, Divincenzo D, Mazzola G. Hypertension in obese subjects: distinct hypertensive subgroup. J Hum Hypertens, 1990, 4: 37-41. 11. Laasko M, Edelman SV, Brechtel G, Baron AD. Decreased effect of insulin to stimulate skeletal muscle blood flow in obese men. J Clin Invest, 1990, 85: 1844-1852. 12. Mansuo K, Mikami H, Ogihara T, Tuck ML 2000 Weight gain-induced blood pressure elevation. Hypertension, 35: 1135-1140. 13. Messerli FH, Sundgard-Riiske K, Reisin E, Frohlich ED, Dunn FG. Dimorphic cardiac adaptation to obesity and arterial hypertension. Ann Intern Med, 1998, 99: 757-761. 14. Nedogoda S et al. Randomized Trial of Perindopril, Enalapril, Losartan And Telmisartan in Overweight or Obese Patients With Hypertension. Clin Drug Investig, 2013, 33: 553-561. 15. Rumantir MS, Vaz M, Jennings GL, Collier G, Kaye DM, Seals DR, Wiesner GH, Brunner-LaRocca HP, Esler MD. Neural mechanisms in human obesity-related hypertension. J Hypertens, 1999, 17: 1125-1133. 16. Sharma AM, Pischon T, Engeli S et al. Choice of drug treatment for obesity-related hypertension: where is the evidence? J Hypertens, 2001, 19: 667-674. 17. Shek EW, Kim PK, Hall JE. Adrenergic blockade prevents leptin-induced hypertension. FASEB J, 1999, 13: A456. 18. Zhang R, Reisin E Obesity-hypertension: the effects on cardiovascular and renal systems. Am J Hypertens, 2000, 13: 1308-1314.
Источник:
Медицинский совет, № 17, 2014