Спазмолитики – это группа лекарственных средств, способных купировать спазмы внутренних органов, и связанный с ними болевой синдром.
Внутренние органы, имеющие трубчатую структуру (сосуды, матка, бронхи, мочеточники и мочевой пузырь, кишечник, желчные протоки и др.) имеют в своём составе гладкомышечный матрикс – слой мышц, расположенных в стенке органа. В физиологических условиях эта гладкая мускулатура регулирует просвет органа и находится в постоянном тоническом сокращении.
Гладкая мускулатура является непроизвольной. Это означает что мы не можем управлять ей используя сознание, как например поперечнополосатой мускулатурой. Мы можем произвольно поднять или опустить руку, но не можем усилием воли расширить бронхи или остановить сокращения кишечника. Управляет гладкой мускулатурой автономная (вегетативная) нервная система. Автономная потому, что ее функционирование не зависит от нашей воли.
Нервные окончания автономной нервной системы не прилегают плотно к гладким мышцам, между ними и мышцей всегда есть зазор, называемый синапсом. При возбуждении вегетативного нерва, под действием его импульса, выделяется особое вещество, называемое медиатор ацетилхолин. Это вещество диффундирует (проникает) от нервного окончания к мышце и активирует ацетилхолиновый рецептор на мембране гладкомышечной клетки. При этом происходит ее сокращение. Это нормальный физиологический процесс.
В тех случаях, когда тонус вегетативной нервной системы повышается, например, при раздражении мочеточника шипами почечного камня, ацетилхолина вырабатывается больше, и сокращение гладких мышц становится чрезмерно сильным или хаотичным. Это приводит к болезненному ощущению – спазму.
Спазм — это тоническое, схваткообразное сокращение внутренних органов, имеющих гладкую мускулатуру и проявляющийся специфической болью. Спазм как правило возникает вследствие воспалительного повреждения внутренней, слизистой оболочки трубчатого органа.
Во время спастического сокращения органа, механически зажимаются чувствительные нервные окончания, и кровеносные сосуды, что ведет к нарушению кровообращения в органе и болевому синдрому. Болевой синдром, вызванный спазмом, называют колика.
Фармакологическое действие и его механизм
Препараты группы спазмолитики могут устранять спазм по двум механизмам. Первый механизм заключается в том, что лекарственный препарат соединяется с тем же рецептором на гладкой мышце что и медиатор ацетилхолин, но не активирует рецептор, а блокирует его, просто заняв посадочное место для ацетилхолина. Избыточное количество ацетилхолина не может взаимодействовать со своими рецепторами, и гладкая мышца расслабляется. Такое действие является нейротропным спазмолитическим эффектом. Нейротропным, потому что влияет на вегетативную нервную систему, делая ее активность не эффективной.
Второй механизм, по которому могут действовать спазмолитики, заключается в проникновении лекарственного вещества внутрь гладкомышечной клетки, которое изменяет ее сократительную физиологию и делает ее сокращение неэффективным. При этом разовьется спазмолитический эффект. Такой тип действия называют миотропным спазмолитическим эффектом от гр. myos мышца и thropos направленность действия.
Спазмолитики классифицируют в зависимости от механизма действия, указанного выше, поскольку с механизмом действия связаны хорошо прогнозируемые терапевтические и побочные эффекты.
Спазмолитическая терапия СРК
Итак, исходя из диагностических критериев СРК, абдоминальная боль и дискомфорт – кардинальные его симптомы, происхождение которых традиционно приписывают в т. ч. и спазму гладкомышечной стенки кишечника. И хотя данные по изучению этого вопроса остаются противоречивыми, многочисленные публикации и клинические исследования подтверждают, что чрезмерный ответ моторики тонкой и ободочной кишки на внешниестимулы ассоциирован с проявлением боли и дискомфорта при СРК [4–6, 9].
Группа спазмолитиков включает несколько различных по своему механизму действий классов препаратов – антимускариновые срества, гладкомышечные миорелаксанты, антихолинергические средства, а также такие уникальные в своем роде лекарственные вещества, как пинаверия бромид – селективный блокатор кальциевых каналов, и тримебутин – периферический агонист опиатных рецепторов [21].
Применение антихолинергических препаратов с учетом их механизма действия возможно при вариантах СРК с преобладанием болевого синдрома в сочетании с нарушением дефекации – в большей степени с диареей. Однако такие общие для этой группы лекарств побочные эффекты, как сухость во рту, головокружение, нарушение зрения, задержка мочеиспускания, центральные эффекты (особенно у пожилых), существенно ограничивают их использование в клинической практике, а с учетом высокого риска развития запора и вовсе делают их назначение при СРК с преобладанием запоров нецелесообразным [14, 18].
Из-за недостачного количества международных высококачественных исследований, посвященных изучению специфических спазмолитиков, оценить эффективность применения препаратов этого класса при СРК возможно, используя систематические обзоры и мета-анализы. Специальная комиссия Американской коллегии гастроэнтерологов изучила этот вопрос, подвергнув анализу 22 клинических исследования. Было выявлено, что в целом каждое исследование содержало достаточно большое количество методологических ошибок в отношении используемых диагностических критериев, критериев включения, режима дозирования лекарственных препаратов и длительности терапии, оценки конечных точек. Кроме того, только 3 исследования включало более 100 пациентов. С учетом этих ограничений анализу были подвергнуты данные 1778 пациентов с СРК. Обобщение результатов показало, что коэффициент риска неэффективности спазмолитиков по сравнению с плацебо составил 0,68 (95 % доверительный интервал [ДИ] – 0,57–0,81), а показатель NNT (число пациентов, которых необходимо пролечить, чтобы получить эффект у одного из них) равнялся 5. При оценке риска развития нежелательных явлений при приеме спазмолитиков было выявлено, что они наблюдались у 1379 больных. С учетом значительной гетерогенности этой группы пациентов коэффициент риска развития побочных эффектов составил 1,62 (95 % ДИ – 1,05–2,50), а показатель NNT – 18 (95 % ДИ – 7–217).
Опубликовав в 2009 г. результаты мета-анализа, специальная комиссия сделала следующий вывод: “некоторые спазмолитики (гиосцин, циметропий и пинаверия бромид) могут обеспечить кратковременный эффект в отношении купирования боли или дискомфорта при СРК (уровень доказательности 2С), доказательств длительной эффективности нет (уровень доказательности 2В), доказательства безопасности и переносимости ограничены (уровень доказательности 2С)” [3].
Подобные выводы прозвучали и в Кокрейновском систематическом обзоре, опубликованном в 2011 г., в котором на основании изучения данных метаанализов сравнивалась эффективность использования различных представителей группы спазмолитиков с плацебо [19]. Главными критериями были влияние препаратов на абдоминальную боль и улучшение общего состояния. В итоге пинаверия бромид подтвердил свою эффективность и в том и в другом случае [3, 19]. В России пинаверия бромид зарегистрирован под торговым названием “Дицетел ®” и в дозировке 100 мг 2 раза в день призван помогать пациентам с СРК для купирования проявлений висцеральной гиперчувствительности.
Таким образом, спазмолитики были и остаются основой терапии СРК. Более того, их назначение целесообразно с позиций не только купирования спастических реакций кишечника, но и воздействия на висцеральную гиперчувствительность как одно из основных патогенетических звеньев синдрома посредством уменьшения чувствительности ноцицепторов.
Литература
1. Agreus I, Svardsudd K, Nyreu O, Tibblin G. Irritable bowel syndrome and dyspepsia in the population: overlap and lack of stability over time. Gastroenterology 1995;109:671–80. 2. Barbara G, Stanghellini V, DeGiorgio R, et al. Activated mast cells in proximity to colonic nerves correlate with abdominal pain in irritable bowel syndrome. Gastroenterology 2004: 126:693–702. 3. Brandt LJ, Chey WD, Foxx-Orenstein AE, et al. An evidence-based position statement on the management of irritable bowel syndrome. Am J Gastroenterol 2009;104(1):S1–35. 4. Chey WY, Jin HO, Lee MH, et al. Colonic motility abnormality in patients with irritable bowel syndrome exhibition abdominal pain and diarrhea. Am J Gastroenterol 2001;96(5): 1499–506. 5. Clemens CH, Samsom M, Roelofs JM, et al. Association between pain episodes and high amplitude propagated pressure waves in patients with irritable bowel syndrome. Am J Gastroenterol 2003;98(8):1838–43. 6. Drossman DA, Camileri M, Mayer EA, et al. AGA technical review on irritable bowel syndrome. Gastroenterology 2002;123(6):2108–31. 7. Drossman DA. The Functional Gastrointestinal Disorders and the Rome III Process. Gastroenterology 2006;130(5):1377–90. 8. Drossman DA, Morris CB, Hu Y, et al. A prospective assessment of bowel habit in irritable bowel syndrome: defining an alternator. Gastroenterology 2005;128:580–89. 9. Fukudo S, Kanazava M, Kano M, et al. Exagerrated motility of the descending colon with repetitive distention of the sigmoid colon in patient with irritable bowel syndrome. J Gastroenterol 2002;37(14):145–50. 10. Guilera M, Balboa A, Mearin F. Bowel habit subtypes and temporal patterns in irritable bowel syndrome: systematic review. Am J Gastroenterol 2005:100:1174–84. 11. Heaton KW, O’Donnell LJD, Braddon FEM, at al. Symptoms of irritable bowel syndrome in a British urban community: consulters and nonconsalters. Gastroenterology 1992;102:1962–67. 12. Holzer P. Tachykinin Receptor Antagonists: Silencing Neuropeptides with a Role in the Disturbed Gut. A Basis for Understanding Functional Diseases. Edited by R. Spiller and D. Grundy Blackwell Publishing, 2004. 13. Hyams JS, Burke G, Davis PM, et al. Abdominal pain and irritable bowel syndrome in adolescents: a community-based study. J Pediatr 1996;129(2):220–26. 14. Irritable colon syndrome treated with an antispasmodic drug. Practitioner 1976;217(1298): 276–80. 15. Locke GR III, Pemberton JH, Phillips SF. AGA technical review on constipation. Gastroenterology 2000;119:1766–78. 16. Longstreth GF, Thompson WG, Chey WD, et al. Functional Bowel Disorders. The Functional Gastrointestinal Disorders and the Rome III Process. Gastroenterology 2006;130(5): 1377–90. 17. Mearin F, Balboa A, Badia X, et al. Irritable bowel syndrome subtypes according to bowel habit: revisiting the alternating subtype. Eur J Gastroenterol Hepatol 2003;15:165–72. 18. O’Donnell LJD, Virjee J, Heaton KW. Detection of pseudodiarrhoea by simple clinical assessment of intestinal transit rate. Br Med J 1990; 300:439–40. 19. Page JG, Dirnberger GM. Treatment of the irritable bowel syndrome with Bentyl (dicyclomin hydrochlorid). J Clin Gastroenterol 1981;3(2):153–56. 20. Ruepert T, Quartero АО, de Wit NJ, et al. Bulking agents, antispasmodics and antidepressants for the treatment of irritаble bowel syndrome (Review). Тhе Cochrane Library 2011, Issue 8. 21. Talley NJ, Weaver AI, Zinsmeister AR, Melton LI. Onset and disappearence of gastrointestinal symptoms and functional gastrointestinal disorders. Am J Epidimiol 1992;136:165–77. 22. Talley NJ. Pharmacologic therapy for the irritable bowel syndrome. Am J Gastroenterol 2003;98(4):750–58. 23. Taub E, Cuevas JL, Cook EW, Crowell M, Whitehead WE. Irritable bowel syndrome defined by factor analysis, gender and race comparisons. Dig Dis Sci 1995;40:2647–55.
Об авторах / Для корреспонденции
Маев Игорь Вениаминович – член-корр. РАМН, доктор медицинских наук, профессор, заведующий кафедрой пропедевтики внутренних болезней и гастроэнтерологии лечебного факультета МГМСУ. Черемушкин Сергей Викторович – кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии лечебного факультета МГМСУ. e-mail; Кучерявый Юрий Александрович – кандидат медицинских наук, доцент кафедры пропедевтики внутренних болезней и гастроэнтерологии ГОУ ВПО МГМСУ. E-mail; Черемушкина Наталья Васильевна – кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ. e-mail
Основы терапии и особенности применения
Не все спазмолитики действуют одинаково на те или иные органы. Некоторые из них действуют преимущественно на гладкие мышцы в одних органах, и совсем, или почти совсем не действуют на гладкие мышцы других органов. Такая избирательность действия называется селективностью.
Например, атропин, экстракт красавки, папаверин и дротаверин, универсальные спазмолитики, бендазол действует преимущественно на сосуды, теофиллин преимущественно на бронхи, мебеверин и прифиния бромид преимущественно на органы желудочно-кишечного тракта. В зависимости от направленности действия спазмолитика, его назначают при той или иной патологии.
Нейротропные и миотропные спазмолитики несмотря на то, что и те, и другие снимают спазм внутренних органов, у них есть общие положительные и отрицательные стороны. Например, нейротропные спазмолитики вызывают сухость слизистых оболочек и могут вызывать запор. Миотропные спазмолитики лишены таких побочных эффектов, но они расширяют сосуды и снижают артериальное давление. Из-за этого их назначают с осторожностью лицам с пониженным давлением, или они им могут быть противопоказаны. Пациентам, получающим препараты от повышенного давления, возможно понадобится коррекция доз гипотензивных средств, при назначении миотропного спазмолитика. Нейротропные спазмолитики лишены таких недостатков.
Положительной чертой спазмолитиков является неспособность маскировать угрожающие симптомы в области брюшной полости, в отличие от анальгетиков. Это означает что, если есть серьезная патология брюшной полости, например, воспаление брюшины, применение спазмолитика не будет маскировать это состояние. Боль будет сохранятся, несмотря на применение спазмолитического средства. При этом необходимо срочно обратится за врачебной помощью.
В любом случае, препараты спазмолитической группы можно применять только после консультации с врачом, или если препарат безрецептурный, после консультации с фармацевтом.
Эпидемиология СРК
Данные о распространенности СРК базируются в основном на больших исследованиях, проведенных в США и Великобритании, в то время как данные из развивающихся стран остаются малорепрезентативными. При сравнении данных эпидемиологических исследований разных стран мира обнаруживаются явные различия. Распространенность СРК также широко варьируется в различных популяциях в пределах одной страны [1, 11, 20]. До конца не известно, чем вызваны эти различия: расой, социально-экономическим статусом, уровнем развития страны, различной трактовкой определения СРК или используемой методикой?
Опубликованные данные позволяют предположить, что заболеваемость СРК в среднем составляет 1 % в год.
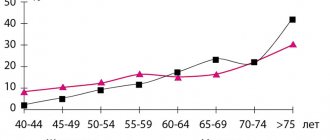
Симптомы СРК распространены во всех возрастных группах, начало симптомов обычно происходит в молодом возрасте [13, 23]. Средний возраст больных СРК составляет 24–41 год. По данным одного национального исследования, в США распространенность симптомов СРК понижается после достижения среднего возраста. Симптомы СРК во всем мире имеют бóльшую распространенность среди женщин, соотношение мужчин и женщин среди больных составляет приблизительно 1 : 2. Этот факт отмечен независимо от используемых диагностических критериев [23].
Судороги
Можно подумать, что судороги возникают только при эпилепсии. Поэтому при их появлении обязательно нужны противосудорожные препараты. Кроме эпилепсии может быть еще множество состояний, не имеющих к ней никакого отношения, но которые могут сопровождаться судорогами:
- Заболевания сосудов головного мозга, возраст более 75 лет и геморрагические инсульты нередко служат причиной начала острых симптоматических судорожных приступов.
- Черепно-мозговые травмы.
- Инфекционные болезни центральной нервной системы (менингит, энцефалит, ВИЧ-инфекция).
- Кислородное голодание головного мозга.
- Интоксикация организма.
- Прием лекарственных препаратов.
- Острые обменные нарушения, например, гипогликемия при лечении сахарного диабета, нарушения электролитного баланса.
- Синдром отмены при прекращении употребления алкоголя.
- Прием больших доз алкоголя.
- Прием психотропных препаратов (психотропных стимуляторов — кокаин, крэк, «экстази»).
- Температура выше 38,5°C у детей до 7 лет может давать фебрильные судороги.
- Печеночная недостаточность.
- Болезнь Паркинсона.
Поэтому самостоятельный прием противосудорожных препаратов без назначений врача запрещен. Сначала нужно установить причину проблемы и только потом лечить.