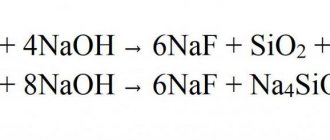Соли, добываемые из гидроксида натрия и ортофосфорной кислоты, получили общее название фосфатов натрия. Эта пищевая добавка имеет полностью синтетическое происхождение и ни в каком виде не встречается в живой природе.
В продуктах питания чаще всего используется как антиоксидант и консервант, хотя имеет также свойства эмульгатора и стабилизатора. Кроме того, вещество выступает и регулятором кислотности, так как влияет на установление и поддержание определённого уровня кислой среды в продукте. Также оказывает влагоудерживающее действие.
Встретив в составе выбираемой пищи код Е339, покупатель может определить для себя, что продукт подвергался обработке фосфатами натрия, и решить, стоит ли его покупать и употреблять. Согласно мировым стандартам и нормам, вещество относится к пищевым добавкам низкой степени опасности.
Свойства фосфата натрия
Физические свойства
| Свойство | Описание |
| Внешний вид | Кристаллическое вещество белого цвета |
| Молярная масса | 163,941 г/моль |
| Плотность | 2,536 г/см3 |
| Температура плавления | 1340°С |
| Cтандартная мольная энтальпия образования при 298К Δ G \Delta G ΔG °298, кДж/моль | -1922,8 |
| Cтандартная мольная энергия Гиббса образования при 298 К Δ \Delta Δ кДж/моль | -1819 |
| Стандартная мольная энтропия при 298 К S°298, Дж/(моль•К) | 224,7 |
| Растворимость в воде, 100 г | при 0°С — 5,4 при 25°С — 14,5 при 100°С — 94,6 |
Химические свойства
В водных растворах гидролизуется по аниону:
Na3P04 + H2O = Na2HP04 + Na0H.
Раствор имеет щелочную реакцию.
При взаимодействии с кислотами образует кислые соли:
Na3P04 + HСl = Na2HP04 + NaCl,
Na3P04 + H2SO4 = NaH2P04 + Na2SO4.
Вступает в реакции обмена с образованием нерастворимых фосфатов:
2Na3P04 + 3CaCl2 = 6NaCl + 2Ca3(P04)2↓,
Na3P04 + AlCl3 = 3NaCl + AlP04↓,
Na3P04 + 3AgNO3 = 6NaCl + Ag3P04↓.
Последняя реакция является качественной реакцией на растворимые фосфаты щелочных металлов и аммония. При добавлении к их раствором раствора нитрата серебра AgNO3 выпадает осадок фосфата серебра Ag3P04 желтого цвета. А натрий можно определить окрашиванию пламени в желтый цвет.
Свойства
| Показатель | Стандартные значения |
| Цвет | белый |
| Состав | соль ортофосфорной кислоты |
| Внешний вид | порошок, гранулы или кристаллическое вещество |
| Запах | отсутствует |
| Растворимость | хорошо в воде; не растворяются в этаноле |
| Содержание основного вещества | от 92 до 98% |
| Вкус | приятный кисловатый |
| Плотность | не постоянная |
| Другие | безводная форма гигроскопична; термоустойчив |
Получение химического соединения
Лабораторные способы получения
Фосфат натрия получают взаимодействием фосфорной кислоты с гидроксидом или карбонатом натрия:
H3PO4 + 3NaOH = Na3PO4 + 3H2O; 2H3PO4 + 3Na2CO3 =2Na3PO4 + 3H2O + 3CO2↑.
Получение фосфата натрия в промышленности
В промышленности фосфат натрия получают в два этапа.
Сначала взаимодействием кальцинированной соды Na2CO3 с фосфорной кислотой H3PO4 получают гидрофосфат натрия Na2HP04:
Н3Р04 + Na2C03 = Na2HP04 + С02↑+ Н20,
а затем взаимодействием едкого натра NaOH с полученным гидрофосфатом натрия Na2HP04 получают фосфат натрия Na3PO4:
Na2HP04 + Na0H = Na3P04 + H20.
После охлаждения нейтрализованных растворов до 30°С фосфат натрия кристаллизуются в виде Na3PO4·12H2O. Он плавится при 70°С. Чтобы получить безводный фосфат натрия, кристаллогидрат прокаливают 2 часа при температуре 120°С, а затем 30 мин при температуре 800°С.
Основные производители
Пищевые натрия фосфаты производят:
- Группа (головной офис в г. Санкт-Петербург);
- Воскресенский завод фосфорных кислот;
- Казфосфат (Казахстан);
- CHEMICO GROUP (Китай).
Ученые всего мира требуют запретить использование ортофосфорной кислоты и ее солей в стиральных порошках: добавки разрушают клеточные мембраны, изменяют состав крови, провоцируют серьезные заболевания.
Но почему-то никто не поставил вопрос о запрете натрия фосфатов в продуктах питания, мотивируя это тем, что вещество добавляют в незначительном количестве.
Потребитель вынужден надеяться на добросовестность производителей.
Применение
Фосфат натрия в быту используют как чистящее средство, так как он прекрасно отмывает жир. Благодаря этому свойству он также входит в состав моющих средств. Кроме того, фосфат натрия смягчает воду, переводя соли жесткости в нерастворимые фосфаты:
3Ca(HCO3)2 + 2Na3P04 = 6NaHCO3 + Ca3(P04)2↓, 3Mg(HCO3)2 + 2Na3P04 = 6NaHCO3 + Mg3(P04)2↓. Применяется он также и в стекольной промышленности для получения оптических стекол.
В строительстве фосфат натрия используют для упрочнения бетона. Его добавка увеличивает также влагостойкость бетона, так как он становится менее пористым.
В медицине фосфат натрия изредка применяют как слабительное и средство от изжоги.
В пищевой промышленности он известен как пищевая добавка Е339(iii). Фосфат натрия используют в качестве эмульгатора, стабилизатора, влагоудерживающего агента. Добавляют его в майонезы и кетчупы, плавленные сыры и хлебобулочные изделия, правда чаще применяют гидрофосфат (пищевая добавка Е339(i)) и дигидрофосфат натрия (пищевая добавка Е339(iii)). Фосфатом натрия обрабатывают куриные окорочка, мясо и рыбу, чтобы удержать воду и сохранить вес.
Относится к малоопасным веществам (4 класс опасности), но при передозировке в пищевых продуктов приводит к расстройствам пищеварения, а у детей нередко вызывает возбуждение и гиперактивность.
Название продукта
Основное название вещества — натрия фосфаты E 339 (ГОСТ Р 52823-2007). Цифровой индекс (другое написание E–339) обозначает европейский код, присвоенный пищевой добавке.
Международный синоним — Sodium phosphates.
Встречаются названия:
- пищевые монофосфаты натрия;
- ортофосфаты натрия;
- фосфорнокислый натрий;
- Phosphate de sodium (французское наименование);
- Mononatrium-phosphat, Natriumdihydrophosphat (немецкие синонимы).
Чем можно заменить?
Пищевую добавку Е339 можно заменить:
- Е452 — полифосфаты, пищевая добавка категории стабилизаторы, являются ингибиторами;
- Е450 — пирофофаты, пищевая добавка категории стабилизаторы, чрезмерное употребление грозит ухудшением усвоения кальция;
- Е343 — ортофосфаты магния, пищевая добавка категории антиоксиданты бывают как натуральными, так и синтезированными;
- Е340 — ортофосфаты, пищевая добавка категории антиоксиданты;
- Е333 — цитраты кальция, пищевая добавка категории антиоксидантов представляет собой как натуральные, так и синтезированные добавки.
Если на маркировке продукта нет пищевой добавки Е339, значит, там будет присутствовать один из перечисленных выше заменителей.
Влияние на организм
Вредного влияния на организм официально не доказано, как и не доказано обратное. Поэтому ученые решили считать пищевую добавку как малоопасное вещество. Конкретных норм потребления безопасного для человека тоже не установлено.
Польза
Польза пищевой добавки Е339:
- используются в качестве слабительного;
- добавляются в БАДы и спортивные напитки.
Вред
Вред пищевой добавки Е339:
- мешает усвоению кальция;
- вымывает воду из организма, тем самым нанося вред желудочно-кишечному тракту;
- возможны аллергические реакции, выраженная сыпь, гиперактивность, агрессивность.
Пищевую добавку не рекомендуется употреблять детям до 10 лет.
Допустимое суточное потребление
По умолчанию считается ежедневной нормой 70 г добавок на 1 кг веса человека.
Химические свойства
- С горячей водой образует разные кислые соли:
NaPO3 →H2O,100oC Na3H2P3O10, Na2H2P2O7, NaH2PO4
- С горячим щелочным раствором образует разные фосфаты натрия:
NaPO3 →NaOH,40−100oC Na3P3O9, Na3PO4, Na5P3O10, Na4P2O7, Na6P4O13
- Вступает в обменные реакции:
NaPO3 + AgNO3 → AgPO3↓ + NaNO3
| Соединения натрия | |
| |
Как определить добавку в продукте?
Признаками избыточной дозировки натрия фосфатов являются металлический или вяжущий привкус и «мыльный» срез на продукте ( при надрезе ощущение липкости и чрезмерной влажности).
По внешнему виду присутствие пищевой добавки Е339 в продукте определить на глаз невозможно. Но особенность Е339 заключается в предохранении продуктов питания от пригорания, сохранении их естественного цвета при термической обработке.
Можно определить по надписи на этикетке. Возможными названиями пищевой добавки при маркировке продуктов могут быть:
- натриевые соли ортофосфорной кислоты;
- ортофосфат натрия трехзамещенный;
- ортофосфат натрия монозамещенный;
- ортофосфат натрия двузамещенный;
- Monosodium Ortophosphate (II);
- Disodium Ortophosphate (iii);
- Trisodium Ortophosphate;
- Sodium Ortophosphates;
- триполифосфат натрия;
- Sodium phosphates;
- Фосфаты натрия;
- Фосфат натрия;
- Е 339, E-339, Е339.