Изопринозин
Иммуностимулирующее средство с неспецифическим противовирусным действием. Представляет собой комплекс, содержащий инозин и соль 4-ацетамидобензойной кислоты с N,N-диметиламино-2-пропанолом в молярном соотношении 1:3. Эффективность комплекса определяется присутствием инозина, второй компонент повышает его доступность для лимфоцитов. Восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, предупреждает снижение активности лимфоцитарных клеток под влиянием глюкокортикоидов, нормализует включение в них тимидина. Изопринозин оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию IgG, интерферона гамма, интерлейкинов (ИЛ)-1 и ИЛ-2, снижает образование провоспалительных цитокинов — ИЛ-4 и ИЛ-10, потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов.
Проявляет противовирусную активность in vivo в отношении вирусов Herpes simplex, цитомегаловируса и вируса кори, вирус Т-клеточной лимфомы человека тип III, полиовирусов, гриппа А и В, ЕСНО-вирус (энтероцитопатогенный вирус человека), энцефаломиокардита и конского энцефалита. Механизм противовирусного действия связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации некоторых вирусов. Усиливает подавленный вирусами синтез мРНК лимфоцитов, что сопровождается подавлением биосинтеза вирусной РНК и трансляции вирусных белков, повышает продукцию лимфоцитами интерферонов альфа и гамма, обладающих противовирусными свойствами
Уменьшает клинические проявления вирусных заболеваний, ускоряет реконвалесценцию, повышает резистентность организма.
При применении в качестве вспомогательного лекарственного средства при инфекционном поражении слизистых оболочек и кожи, вызванном вирусом Herpes simplex, происходит более быстрое заживление пораженной поверхности, чем при лечении традиционным способом. Реже возникают новые пузырьки, отек, эрозии и рецидивы болезни. При своевременном применении инозина пранобекса уменьшается частота возникновения вирусных инфекций, снижается длительность и тяжесть заболевания.
Фармакокинетика
После приема внутрь быстро и практически полностью (> 90 %) всасывается и обладает хорошей биодоступностью. При приеме внутрь в дозе 1500 мг Сmax инозина пранобекса достигается через 1 ч и составляет 600 мкг/мл. Не определяется в крови спустя 2 часа после приема.
Инозин пранобекс состоит из инозина и соли р-ацетамидобензойной кислоты с N,N-диметиламино-2-пропанолом. Каждый из компонентов инозина пранобекса быстро подвергается метаболизму. Практически 100% метаболитов обнаруживаются в моче в интервале от 8 до 24 часов после приема. Инозин подвергается метаболизму по циклу, типичному для пуриновых нуклеотидов, с образованием мочевой кислоты, концентрация которой в сыворотке крови может повышаться. В результате возможно образование кристаллов мочевой кислоты в мочевых путях. Повышение концентрации мочевой кислоты носит нелинейный характер и может изменяться на ±10% в течение 1-3 ч после приема внутрь. В результате метаболизма р-ацетамидобензойной кислоты образуется о-ацилглюкуронид; N,N- диметиламино-2-пропанол метаболизируется до N-оксида. AUC р-ацетамидобензойной кислоты >88 %, AUC N,N — диметиламино-2-пропанола >77%. Кумуляции в организме не обнаружено.
Инозин и его метаболиты экскретируются с мочой. При достижении равновесной концентрации при приеме в ежедневной дозе 4 г суточная экскреция с мочой р-ацетамидобензойной кислоты и ее метаболита составляет примерно 85% принятой дозы; T1/2 — 50 мин. T1/2 N,N-диметиламино-2-пропанола — 3-5 ч.
Инозин пранобекс и его метаболиты полностью выводятся из организма в течение 48 ч.
Одной из важных медико-социальных проблем отечественного здравоохранения является высокая заболеваемость гриппом и другими острыми респираторными вирусными инфекциями (ОРВИ), обусловленными более чем 250 вирусами. В период эпидемий гриппа, особенно вызванных новыми разновидностями вирусов, регистрируют значительное число больных тяжелыми и осложненными формами инфекции. Летальность при гриппе среди госпитализированных взрослых пациентов, несмотря на определенные успехи интенсивной терапии, остается достаточно высокой (до 2,5%) [1]. Ежегодно в России регистрируется 27,3–41,2 млн случаев ОРВИ. Расходы на лечение гриппа и его осложнений в мире ежегодно составляют около 14,6 млрд долл. В России экономические потери от гриппа за год оцениваются в 10 млрд руб. [2, 3].
Все эти обстоятельства требуют своевременного проведения комплекса организационно-противоэпидемических, профилактических и экстренных лечебных мероприятий. Однако на сегодняшний день постановка правильного диагноза с определением возбудителя ОРВИ на амбулаторном этапе затруднена.
А выбор препаратов для лечения и профилактики этих заболеваний настолько огромен, что порождает проблему полипрагмазии, особенно в первичном звене здравоохранения.
В современной врачебной практике с точки зрения клинической фармакологии используется простой алгоритм выбора лекарственных препаратов для лечения конкретного заболевания. Выделяют препараты, влияющие на причину заболевания (этиотропное лечение); препараты, влияющие на механизмы развития заболевания (патогенетическое лечение), и препараты, воздействующие на симптомы заболевания (симптоматическое лечение).
Рассмотрим с данной позиции известные группы препаратов для лечения гриппа и ОРВИ.
Лекарственные препараты, подавляющие разные этапы репродукции вируса гриппа и других респираторных вирусов, относятся к этиотропным средствам.
К лекарственным средствам патогенетической направленности относят препараты интерферона (ИФН) и его индукторы, поскольку они оказывают опосредованное этиотропное и иммунокорригирующее действие.
Третья группа – симптоматические средства, облегчающие или купирующие отдельные симптомы ОРВИ (гипертермия, головная боль, кашель, ринит и пр.), включает нестероидные противовосполительные средства, антигистаминные, муколитические, противокашлевые, противоконгестивные и некоторые другие препараты.
Известно, что терапию при ОРВИ и гриппе необходимо начинать как можно раньше после появления первых симптомов: все этиотропные препараты наиболее эффективны при приеме их в течение первых 24–36 часов болезни.
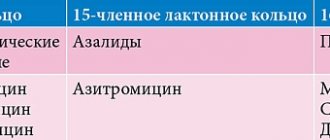
К средствам этиотропной терапии относятся блокаторы М2-каналов вируса гриппа А (амантадин, римантадин) и ингибиторы нейраминидазной активности вируса гриппа А и В (осельтамивир, занамивир).
Действие противовирусного препарата направлено на конкретную стадию репликационного цикла вируса. Основными антигенами вируса гриппа являются гемагглютинин и нейраминидаза. Наиболее существенный вклад в патогенность вирусов гриппа А вносят белки гемагглютинина — PB1, PB2, NS1. Кроме того, 2 белка (нейраминидаза, M2) связаны с развитием устойчивости вирусов к противовирусным препаратам. Лечение больных гриппом представляет определенные трудности в связи с такими недостатками противовирусных лекарственных препаратов, как формирование резистентности штаммов вируса, сохранение терапевтического эффекта только на фоне приема препарата, побочные реакции и др. [4, 5].
Блокаторы М2-каналов (амантадин, римантадин и адапромин) блокируют ионные каналы М2-белка и подавляют репликацию вируса на ранней стадии. Эти препараты эффективны при гриппе, вызванном вирусом А, и до сих пор успешно используются в нашей стране. Главным недостатком данной группы препаратов является селективное ингибирование вируса гриппа А (вирус гриппа В не содержит белка М2). В практике встречаются назначения врачами блокаторов М2-каналов без четких на то показаний (при лечении гриппа, вызванного вирусом В, или при других острых респираторных инфекциях), проводится их широкая реклама, препараты свободно продаются в аптеках. Все это привело к развитию лекарственной устойчивости. Также необходимо учитывать, что при назначении блокаторов М2-каналов пожилым пациентам с сопутствующими заболеваниями почек и печени необходима коррекция суточной дозы. Все это ограничивает применение данных препаратов, несмотря на их доступную цену.
Ингибиторы нейраминидазы (занамивир и озельтамивир) высокоэффективны при лечении гриппа, вызванного вирусом как А, так и В, имеют более благоприятный, чем блокаторы М2-каналов, профиль безопасности и практически не вызывают лекарственной устойчивости. Данные препараты блокируют нейраминидазу вируса гриппа, играющую важную роль в выделении и распространении вновь образованных вирионов после окончания цикла репликации вируса в клетке – в результате нарушается способность вируса проникать в здоровые клетки [6].
Озельтамивир является пролекарством мощного ингибитора нейраминидазы вируса гриппа – озельтамивира карбоксилата. В основе механизма действия лежит превращение озельтамивира в активный метаболит и блокада выхода новых вирионов. Препарат легко всасывается в желудочно–кишечном тракте, концентрация активного метаболита в плазме достигает максимального уровня через 2–3 часа и составляет не менее 75% принятой дозы. Препарат, как правило, хорошо переносится, при назначении в первые 36 часов болезни сокращает продолжительность основных симптомов и заболевания в целом. Клиническая эффективность озельтамивира при гриппе показана в крупных многоцентровых рандомизированных исследованиях. Однако отсутствие действия на другие респираторные вирусы (парагрипп, аденовирусы, респираторно-синцитиальный вирус и др.) и высокая стоимость препарата ограничивают его широкое применение в амбулаторной практике.
Применяемые при гриппе и ОРВИ средства патогенетического действия – препараты ИФН и его индукторы – более многочисленны.
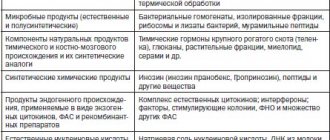
Существующие препараты ИФН делятся на природные человеческие ИФН первого поколения и рекомбинантные ИФН второго поколения (см. таблицу).
Разрешенные к клиническому использованию индукторы ИФН делятся на две основные группы: высоко- и низкомолекулярные, каждая из которых подразделяется на природные и синтетические препараты. Для профилактики и лечения ОРВИ применяются препараты, обладающие высокой интерферониндуцирующей активностью, вызывающие в организме больного продукцию разных типов ИФН. Индукторы ИФН обладают противовирусным, иммунокорригирующим действиями и другими характерными для ИФН эффектами [7].
Механизм действия данной группы препаратов обусловлен неспецифическим иммунитетом. Своеобразие неспецифических механизмов определяется ведущей ролью ряда факторов: клеточной и тканевой невосприимчивостью, температурной инактивацией вирусов, системой ИФН, гуморальными ингибиторами сыворотки крови. Особое значение придают системе мононуклеарных фагоцитов, нейтрофилам, естественным киллерам. При этом различные реакции иммунитета и неспецифической защиты находятся в согласованном взаимодействии. Большое значение в выздоровлении от вирусных инфекций имеет состояние Т-клеточного звена иммунитета. Особую опасность представляет способность ряда вирусов блокировать первичный неспецифический иммунный ответ фагоцитов и подавлять синтез ИФН, что способствует углублению иммунодефицита (угнетение функции макрофагов и нейтрофилов, блокада рецепторов фактора некроза опухолей, лимфоцитопения, нарушение механизмов клеточной дифференцировки в системе Т- и В-лимфоцитов) [8, 9].
Тяжелые и осложненные формы гриппа и ОРВИ протекают с развитием транзиторной Т-клеточной иммуносупрессии, снижением функциональной активности натуральных киллеров, фагоцитарной и метаболической активности нейтрофилов периферической крови, повышением содержания сывороточных иммунных комплексов, наличием ИФН-дефицита [10, 11].
При всем этом необходимо учитывать, что большинство препаратов из группы индукторов ИФН используются только в России и имеют слабую доказательную базу.
Исключение составляет препарат Изопринозин (инозин пранобекс), относящийся по анатомо-терапевтической классификации к «прочим противовирусным средствам» (код АТХ — J05AX05). Изопринозин обладает двойной – противовирусной и иммуномодулирующей – активностью. Препарат применяется в медицинской практике с 1971 г. для лечения клеточно-опосредованных иммунодефицитных состояний, связанных с различными вирусными инфекциями (простой герпес, опоясывающий герпес, цитомегаловирусная инфекция, вирус Эпштейна–Барр).
Синтезировал данную молекулу P. Gordon (Chicago Medical School, USA) на основе гипотезы о том, что пуриновый метаболит инозин и его аналоги оказывают влияние на мРНК, биосинтез белков и за счет этого способны вызывать повышение адаптивной способности клеток к вирусной инфекции и их иммунной защиты. Под названием Инозиплекс (Inosiplex) препарат был запатентован в США в 1972 г., а к 1990 г. был зарегистрирован и разрешен к применению более чем в 70 странах мира под различными торговыми наименованиями в двух лекарственных формах (таблетки, сироп), которые и в настоящее время используются в качестве противовирусных препаратов с иммуномодулирующей активностью [12].
Фармакокинетические свойства препарата определяются хорошим всасыванием из желудочно-кишечного тракта при приеме внутрь. Cmax в плазме крови определяется через 1–2 часа. Препарат быстро метаболизируется аналогично эндогенным пуриновым нуклеотидам с образованием мочевой кислоты и выделяется через почки. Не кумулируется в организме. T1/2 составляет 3,5 часа – для М-М-диметиламино-2-пропранолона и 50 минут – для пара-цетамидобензоата. Элиминация препарата и его метаболитов из организма происходит в течение 24–48 часов [13, 14]
Фармакодинамика препарата обусловлена способностью тормозить репликацию широкого спектра ДНК- и РНК-содержащих вирусов. Изопринозин обладает прямым противовирусным действием — подавляет репликацию ДНК и РНК вирусов посредством связывания с клеточными рибосомами и изменения их стереохимического строения, в результате чего в клетках нарушается синтез вирусных белков и снижается интенсивность размножения вируса [15]. Кроме того, препарат поддерживает функциональную активность иммунокомпетентных клеток, стимулируя дифференцировку Т-лимфоцитов в цитотоксические Т-клетки и Т-хелперы, а также повышает продукцию лимфокинов, стимулирует выработку интерлейкина-1 (ИЛ-1), ИЛ-2, ИФН γ и функциональную активность NK-клеток (естественные киллеры). Изопринозин также потенцирует морфофункциональную состоятельность нейтрофилов и моноцитов, усиливая хемотаксис макрофагов и фагоцитоз, тем самым нормализует клеточный иммунитет. В то же время, стимулируя дифференцировку В-лимфоцитов в плазматические клетки и повышая продукцию антител, он нормализует гуморальный иммунитет. При этом происходит повышение концентрации иммуноглобулинов IgG, IgA и IgM, а также поверхностных маркеров комплемента и вируснейтрализирующих антител [16]. Благодаря модуляции неспецифического иммунитета увеличивается резистентность организма к массе вирусов [17].
Противовирусная активность Изопринозина доказана и в отношении респираторных вирусов, включая вирусы гриппа А и В, парагриппа, аденовирусы, респираторно-синцитиальный вирус [18].
Еще в 1974 г. в исследованиях D.M. Pachuta и соавт. была установлена эффективность инозина относительно риновирусной инфекции [19]. Множество исследований подтверждают эффективность препарата относительно вирусов гриппа [20, 21].
Активность Изопринозина одинаково высока как в первые часы заболевания, так и в последующие дни [22].
Назначение Изопринозина в случаях наличия длительной поствирусной астении способствует нормализации энергетического обмена в клетках. Проникая в клетки, препарат повышает их энергетический уровень, усиливает устойчивость к цитопатогенному действию вирусов и препятствует развитию синдрома поствирусной астении, особенно характерного при гриппе и повторных ОРВИ [23].
Эффективность и безопасность Изопринозина с позиций доказательной медицины подтверждены зарубежными и отечественными исследованиями.
Применение Изопринозина при гриппе и ОРВИ сокращает продолжительность и выраженность симптомов заболевания (лихорадочного периода, интоксикации, катаральных симптомов в носоглотке). Показано уменьшение продолжительности болезни и купирование симптомов заболевания через 48–72 часа после назначения препарата детям в возрасте от месяца до 12 лет при ОРВИ (ринофарингит, острый ринофарингит), у пролеченных пациентов температура была невысокой и держалась не более 2 дней, общие симптомы исчезали за 1–2 дня [24].
Применение Изопринозина для лечения ОРВИ у пациентов с ослабленным иммунитетом позволяет снижать потребность в назначении антибиотиков, не требует дополнительного назначения других лекарственных средств, сокращает сроки госпитализации [24, 25].
Мета-анализ клинической и иммунологической эффективности Изопринозина при респираторных инфекциях у иммунокомпрометированных пациентов, по данным опубликованных исследований, в которых у 2,5 тыс. пациентов (дети и взрослые) препарат использовался с лечебно-профилактической целью, также подтвердил эффективность терапии [25].
При обзоре клинических исследований препарата Изопринозин серьезных нежелательных явлений выявлено не было. К наиболее часто встречающимся побочным явлениям относятся жалобы со стороны желудочно-кишечного тракта (небольшие боли в верхней части живота, тошнота, рвота). [17].
Кроме того, в исследованиях R.C. Batterman (1970) [26], H.W. Elliott и соавт. (1972) при применении препарата наблюдалось повышение уровня мочевой кислоты [27]. Следует, однако, отметить, что в этих работах средние сывороточные концентрации мочевой кислоты повышались, но оставались в пределах нормы (8 мг/100 мл или 480 мкмоль/л у мужчин). Концентрации уратов в сыворотке повышались с 4,7 мг до 6,3 мг/100 мл после одной недели терапии препаратом в дозе 1 г/сут, до 6,6 мг/100 мл после одной недели его приема в дозе 2 г/сут, 7,0 мг/100 мл после недельного курса в дозе 3 г/сут и до 7,2 мг/100 мл после недели лечения Изопринозином в дозе 4 г/сут. После прекращении терапии этим препаратом уровни мочевой кислоты в сыворотке крови и в моче возвращались к уровням до начала лечения. Пострегистрационные наблюдения в течение многих лет не выявили никаких факторов риска, связанных с влиянием Изопринозина на уровни мочевой кислоты в сыворотке крови.
Таким образом, препарат Изопринозин, обладающий двойной – противовирусной и иммуномодулирующей – активностью, имеющий благоприятный профиль безопасности, подтвержденный клиническими исследованиями не только в России, но и зарубежом, может быть рекомендован к широкому использованию в первичном звене здравоохранения как препарат выбора для лечения не только гриппа, но и ОРВИ.