Таблетки «Макропен®» применяются при следующих показаниях:
- инфекции респираторного и мочеполового тракта, вызванные микоплазмами, легионеллами, хламидиями и Ureaplasma urealyticum;
- инфекции респираторного тракта, кожи и мягких тканей и другие инфекции, вызванные чувствительными к мидекамицину и пенициллину бактериями, у пациентов с гиперчувствительностью к пенициллину;
- энтериты, вызванные бактериями Campylobacter spp.;
- лечение и профилактика дифтерии и коклюша.
Побочные эффекты
Со стороны крови и лимфатической системы: эозинофилия.
Со стороны желудочно-кишечного тракта: тошнота, снижение аппетита, рвота, диарея, стоматит, боль в животе, псевдомембранозный колит.
Со стороны кожи и подкожных тканей: сыпь, крапивница и зуд, ангионевротический отек, синдром Стивенса-Джонсона.
Со стороны печени и желчевыводящих путей: повышение уровня трансаминаз и желтуха.
При возникновении тяжелых побочных реакций лечение следует прекратить.
Фармакологические свойства препарата Мидекамицин
Макролидный антибиотик. Связывается с рибосомами и таким образом ингибирует синтез белков в бактериальных клетках. В низких дозах препарат действует бактериостатически, а в более высоких — бактерицидно. После приема внутрь мидекамицин хорошо всасывается. У взрослых после перорального приема 600 мг пpепаpата его максимальная концентрация в сыворотке крови достигается через 40 мин. Прием пищи не оказывает существенного влияния на концентpацию мидекамицина в сывоpотке крови. Мидекамицин хоpошо пpоникает в ткани, особенно в околоушные и подчелюстные железы, лимфатические узлы, в кожу и легкие. Концентрация мидекамицина в тканях существенно превышает его концентрацию в плазме крови. Два метаболита мидекамицина обладают противомикробным действием. Выводится с калом и мочой. К мидекамицину чувствительны грамположительные аэробы и анаэробы, некоторые грамотрицательные бактерии, а также микоплазмы, хламидии и легионеллы. Мидекамицин высокоэффективен в отношении стрептококков, пневмококков, стафилококков и микоплазм пневмонии. Эффективен в отношении стафилококков, резистентных к пенициллину, тетрациклинам и т.д. Действует на некоторые штаммы золотистого стафилококка, резистентные к эритромицину и ампициллину.
Обратите внимание!
Описание препарата Макропен табл. п/о 400мг №16 на этой странице — упрощенная авторская версия сайта apteka911, созданная на основании инструкции/ий по применению. Перед приобретением или использованием препарата вы должны проконсультироваться с врачом и ознакомиться с оригинальной инструкцией производителя (прилагается к каждой упаковке препарата).
Информация о препарате предоставлена исключительно с ознакомительной целью и не должна быть использована как руководство к самолечению. Только врач может принять решение о назначении препарата, а также определить дозы и способы его применения.
Применение препарата Мидекамицин
Суточная доза для взpослых обычно составляет 1200 мг мидекамицина в 2–3 приема. При тяжелых и умеренной тяжести инфекционных заболеваниях детям назначают 30–50 мг/кг в сутки в 2 приема. При более легких формах инфекций суточную дозу можно снизить до 20 мг/кг. Пpодолжительность лечения составляет 7–10 дней, при необходимости лечение можно продлить. Суспензию назначают обычно детям. разовая доза для ребенка с массой тела меньше 5 кг составляет 130 мг, 5–10 кг — 265 мг, 11–15 кг — 350 мг, 16–20 кг — 525 мг.
Применение мидекамицина в педиатрической практике
Антибиотикотерапия занимает одно из ведущих мест в комплексе лечебных мероприятий при различных инфекционных заболеваниях. Когда вопрос касается выбора препарата для маленького пациента, на первый план выходят безопасность и отсутствие серьезных побочных эффектов. В настоящее время препаратами с минимальным спектром нежелательных явлений и благоприятными фармакокинетическими свойствами признаны макролиды. Ярким представителем группы макролидов является мидекамицин. Благодаря высокой эффективности, отсутствию выраженных нежелательных явлений, удобству в применении, наличию двух детских лекарственных форм (таблетки и суспензия) антибиотик получил широкое распространение в педиатрической практике.
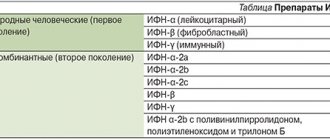
Таблица. Классификация макролидов
Макролидные антибиотики используют при многих инфекциях, прежде всего внебольничного происхождения. История их применения насчитывает свыше 40 лет. Первым антибиотиком-макролидом, нашедшим клиническое применение, стал эритромицин, полученный в 1952 г. из культуры почвенного гриба Streptomyces erythreus
. К настоящему времени создано около 20 макролидных антибиотиков, восемь из них активно применяются в клинической практике [1]. Макролиды считаются одним из интенсивно развивающихся классов антибиотиков благодаря высокой эффективности и относительной безопасности. Они характеризуются широким спектром антимикробной активности и благоприятными фармакокинетическими свойствами, хорошо переносятся маленькими пациентами. Важной составляющей клинического успеха макролидов является активность в отношении не только обычных возбудителей, но и внутриклеточных патогенов [1, 2].
По происхождению макролиды подразделяют на природные и полусинтетические. По химической структуре выделяют 14-, 15- и 16-членные макролиды в зависимости от числа атомов углерода в лактонном кольце (см. таблицу).
В педиатрической практике широкое применение нашли мидекамицин, рокситромицин, спирамицин, джозамицин, азитромицин.
Мидекамицин является природным 16-членным макролидом, продуцируемым грибком Streptomyces mycarofaciens
. Препарат применяется в клинической практике с 1985 г. Полусинтетическое производное мидекамицина – мидекамицина ацетат по сравнению с природным аналогом обладает улучшенными антимикробными и фармакологическими свойствами. Он лучше всасывается в желудочно-кишечном тракте и создает более высокие тканевые концентрации. Механизм действия мидекамицина состоит в связывании с каталитическим пептидил-трансферазным центром 50s-субъединицы рибосом, что приводит к нарушению процессов транслокации и транспептидации, преждевременному отщеплению растущей тРНК-полипептидной цепочки и, как следствие, подавлению синтеза белка в рибосомах микробных клеток [1, 3].
Мидекамицин высокоэффективен в отношении грамположительных микроорганизмов Streptococcus pneumoniae, St. pyogenes, Staphylococсus aureus,
Corynebacterium diphtheriae, Listeria monocytogenes,
грамотрицательных кокков и палочек
Neisseriagonorrhoeae,Moraxellacatarrhalis,Bordetellapertussis,Campylobacterjejuni,Helicobacterpylori.
Низкая чувствительность отмечается у
Haemophilus influenzae.
Как и другие макролиды, мидекамицин активен в отношении внутриклеточных микроорганизмов (
Chlamydiatrachomatis, Chlamydophilapneumoniae,Mycoplasmapneumoniae,M. hominis,Ureaplasmaurealyticum
).
Мидекамицина ацетат обладает постантибиотическим эффектом, что, по мнению ряда ученых, обусловлено необратимыми изменениями рибосом возбудителя, приводящими к блокированию транслокации [1, 3, 4]. Группа макролидов в целом и мидекамицин в частности характеризуются противовоспалительным и иммуномодулирующим действием. Макролиды повышают активность Т-киллеров, накапливаются в нейтрофилах и макрофагах, усиливают их фагоцитарную активность и миграцию в очаг воспаления. Кроме того, макролиды влияют на окислительные реакции в фагоцитах и способствуют их дегрануляции, повышают продукцию противовоспалительного цитокина (интерлейкина (ИЛ) 10) моноцитами, уменьшают выработку провоспалительных цитокинов моноцитами (ИЛ-1, фактор некроза опухоли альфа) и лимфоцитами (ИЛ-2), снижают образование медиаторов воспаления – простагландинов, лейкотриенов и тромбоксанов. Противовоспалительное действие проявляется даже при субтерапевтических концентрациях макролидов и сравнимо с эффектом нестероидных противовоспалительных препаратов.
Приобретенная устойчивость к макролидам вырабатывается быстро, но после прекращения контакта с антибиотиком чувствительность к нему со временем восстанавливается. К мидекамицину не вырабатывается резистентность по MLS-типу (модификация мишени действия – рибосомальной 50s-субъединицы). Кроме того, в меньшей степени характерно развитие других механизмов резистентности (изменение проницаемости клеточной стенки, инактивация антибиотика и эффлюкс) [1, 3].
Мидекамицин по сравнению с эритромицином обладает лучшими органолептическими и фармакокинетическими свойствами, лучше всасывается в желудочно-кишечном тракте, стабилен в кислой среде, быстро и достаточно полно абсорбируется в тканях, создавая высокие концентрации во внутренних органах из-за высокой растворимости в липидах, в частности миндалинах, бронхах и легких. Следовые концентрации обнаруживаются в гайморовых пазухах.
Мидекамицин в значительных количествах экскретируется с грудным молоком. Препарат быстро всасывается в кровь, достигая пиковой концентрации у детей в сыворотке крови через 1–3 часа после приема в дозе 10–30 мг/кг (0,76–2,3 мг/л).
После однократного приема регистрируются два пика максимальной концентрации. Второй пик (нередко превышающий первый) обусловлен способностью препаратов накапливаться в желчи с последующим повторным всасыванием из кишечника.
Связывание с белками плазмы составляет около 47%.
Препарат и его метаболиты выводятся в основном через печень (70%) и почки (10%).
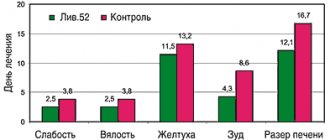
Результаты клинического многоцентрового исследования, проведенного в России, позволили подтвердить преимущества мидекамицина перед эритромицином в отношении безопасности применения у детей. Побочные реакции на фоне применения эритромицина наблюдались в два раза чаще, чем при использовании мидекамицина.
Согласно результатам трехлетнего постмаркетингового клинического наблюдения в Японии, включавшего 12 169 детей (87% пациентов младше шести лет), получавших сироп мидекамицина ацетата, побочные эффекты развились лишь у 66 из них (0,54% случаев, у детей до года – 0,97%). При этом лишь в 0,38% случаев отмечались нежелательные явления со стороны желудочно-кишечного тракта, в 0,15% – кожная сыпь и в 0,01% – повышение активности печеночных ферментов. Серьезных побочных эффектов не зарегистрировано. Ни у одного из 26 больных с аллергией на бета-лактамные антибиотики при назначении мидекамицина аллергических симптомов не зафиксировано [5]. На основании результатов исследования мидекамицина ацетат признан самым безопасным макролидом [4, 6, 7].
В Научном центре здоровья детей также проводилось исследование побочных эффектов мидекамицина и мидекамицина ацетата у 76 детей. Побочные реакции в виде болей в животе, диспепсических явлений отмечались у трех пациентов. У одного ребенка с пищевой и лекарственной аллергией в анамнезе на третий день лечения появилась аллергическая сыпь, которая была купирована в течение суток после отмены препарата. Это свидетельствовало о наличии нежелательных реакций только у 4% больных [2].
Результаты изучения проблемы межлекарственного взаимодействия показали, что мидекамицин в отличие от эритромицина является слабым ингибитором микросомальной системы цитохрома Р450 [1]. Поэтому он не оказывает существенного влияния на концентрацию теофиллина и антигистаминных препаратов, что позволяет применять его по показаниям у детей с аллергическими заболеваниями.
Мидекамицин в России выпускается в двух лекарственных формах – таблетки 400 мг и порошок для приготовления суспензии – 175 мг мидекамицина ацетата в 5 мл суспензии. Таблетированная форма имеет возрастные ограничения и противопоказана детям до трех лет. Для формы в виде суспензии возрастных ограничений не установлено.
Мидекамицин широко применяется в клинической педиатрической практике. Результатами многочисленных исследований, проведенных во многих отечественных и зарубежных медицинских центрах, подтверждена высокая клиническая и бактериологическая эффективность мидекамицина (98–85%) у детей при ринофарингитах, тонзиллитах, синуситах, пневмониях и хронических бронхитах [7, 8].
Возбудителями острого тонзиллита могут быть не только вирусы и бактерии, но также простейшие и грибы. Как правило, у детей в возрасте до трех лет острый тонзиллит связан с вирусами. У детей в возрасте от пяти лет преобладают бактериальные формы. При этом пик заболеваемости бета-гемолитическим стрептококком группы A (БГСА) приходится на возраст от пяти до десяти лет. БГСА является причиной острых бактериальных ангин в 25–30% случаев. Но при рецидивирующих тонзиллитах БГСА выделяют у 50% детей, в том числе в ассоциации с золотистым и эпидермальным стафилококком, H. influenzae
,
H. parainfluenzae
,
St. pneumoniae
,
M. сatarrhalis
у 52% детей [6].
В последние годы наметилась тенденция к увеличению доли внутриклеточных возбудителей (микоплазм и хламидий) в этиологии тонзиллофарингитов у детей, особенно дошкольного возраста. Частота обнаружения может превышать 10% [4]. Безусловно, высокая активность макролидов по отношению к внутриклеточным возбудителям, которые встречаются у 40–45% детей с рецидивирующим хроническим тонзиллитом, аденоидитом, обеспечивает им лидирующие позиции в борьбе с данной патологией. Особенно часто эти возбудители встречаются у иммунокомпрометированных детей, у детей с лимфатической конституцией, с перемежающейся инфекцией нижних и верхних дыхательных путей, у часто болеющих детей. Макролиды – единственные безопасные препараты для детей, инфицированных этими возбудителями. Подтверждение тому – опыт использования 16-членного макролида мидекамицина в терапии обострения хронического тонзиллита у детей с паратонзиллярными абсцессами. Отличные результаты, то есть практически полное выздоровление, у 87% детей свидетельствуют об устойчивом эффекте мидекамицина в терапии рецидивирующего осложненного хронического тонзиллита [6]. Препарат использовался в дозе 30–50 мг/кг/сут как в виде таблеток, так и в виде суспензии семь – десять дней при остром тонзиллите и от десяти до 14 дней при обострении хронического тонзиллита.
Таким образом, в настоящее время макролиды могут стать препаратами первого выбора при остром, обострениях хронического тонзиллита и их осложнениях у детей. В то же время макролиды не могут являться препаратами первого выбора у детей с такими заболеваниями ЛОР-органов, как острый средний отит, острый синусит. То есть речь идет о заболеваниях, в 15–32% случаев ассоциированных с H. influenzae.
Мидекамицин наряду с другими макролидами является препаратом выбора при острых бронхитах и обострении хронических бронхитов, атипичных пневмониях, вызванных внутриклеточными возбудителями, а также при внебольничной пневмонии, особенно у детей с аллергией и повышенной чувствительностью к пенициллиновым препаратам [2, 7].
При внебольничной пневмонии у детей в возрасте от одного до шести месяцев атипичные возбудители выявляются более чем в 30% случаев, чаще C. trachomatis
, реже
M. hominis
. У детей до года существенную роль играет стафилококк как возбудитель осложненных форм пневмонии (58%). В то же время в этиологии пневмоний детей второго полугодия жизни в качестве инфекционного агента заметную роль начинает играть
St. pneumoniae
. У детей в возрасте от шести месяцев до шести лет
M. pneumoniae
выявляется в 10–15% случаев. В возрасте от семи до 15 лет увеличивается доля атипичных пневмоний, вызванных
M. pneumoniae
(20–40%) и
C. pneumoniae
(7–24%). Частота выделения
St. pneumoniae
у детей в возрасте от года до трех лет возрастает до 62%, в возрасте старше трех лет – до 70%.
Было проведено отечественное контролируемое сравнительное исследование эффективности эритромицина и мидекамицина у детей в возрасте от года до 15 лет с неосложненной внебольничной пневмонией, обострением хронических бронхолегочных заболеваний и рецидивирующего бронхита [2]. Эритромицин назначали в дозе 30–50 мг/кг/сут четыре раза в сутки, мидекамицин – в дозе 30–50 мг/кг/сут два-три раза в сутки. Курс лечения при пневмонии и бронхите составлял семь – десять дней, при хронических заболеваниях органов дыхания – от десяти до 14 дней и более. Эритромицин и мидекамицин, как и другие пероральные антибиотики, назначались при легком и среднетяжелом течении заболеваний органов дыхания. Основанием для применения мидекамицина при внебольничных пневмониях, обострениях хронических бронхолегочных заболеваний служили данные, свидетельствовавшие о высокой чувствительности к нему пневмотропной флоры, в том числе атипичных возбудителей, а также его способности образовывать высокие концентрации в бронхиальном секрете и легких. Результаты данного исследования показали эффективность перорального препарата эритромицина при внебольничной пневмонии у 75% детей. Однако при этом достаточно часто (16% случаев) наблюдались побочные реакции (диспепсические явления, тошнота, рвота, боль в животе), что требовало у части больных отмены препарата. При обострении хронических бронхолегочных заболеваний эритромицин оказался эффективным в 71% случаев, но частота нежелательных явлений в этой группе была еще выше (19%). Более высокая эффективность мидекамицина зафиксирована при внебольничной пневмонии (70%). Только у одного ребенка отмечались побочные реакции со стороны желудочно-кишечного тракта (боль в животе). Более выраженный терапевтический эффект получен у детей при обострении рецидивирующего бронхита (93%). Только у одного ребенка наблюдались побочные реакции со стороны желудочно-кишечного тракта [2].
С учетом того что макролиды одинаково хорошо воздействуют как на внеклеточных, так и на внутриклеточных возбудителей, мидекамицин может быть использован при лечении ряда урогенитальных инфекций, вызванных хламидиями, микоплазмой и т.д. Урогенитальные хламидиозы и микоплазмозы в настоящее время занимают значительное место среди болезней, передаваемых половым путем. У новорожденных колонизация половых путей микоплазмами происходит во время родов. По данным Всемирной организации здравоохранения, 60–70% детей, родившихся от матерей с хламидийной и миколазменной инфекцией, были инфицированы [9]. Обычно инфекции протекают латентно и бессимптомно, обостряются при стрессовых ситуациях. Лечение предполагает обязательное применение иммуностимулирующей терапии и макролидов. Мидекамицин может быть препаратом выбора.
Макролиды нашли применение и в гастроэнтерологии – при лечении хронических гастродуоденитов, ассоциированных с Н.
pylori
. Мидекамицин также активен в отношении
H.pylori
, что позволяет рассматривать вопрос о его включении в схемы эрадикационной терапии, если применение кларитромицина не представляется возможным.
Мидекамицин эффективен при лечении детей с пиодермиями, что также подтверждено результатами исследований [3, 10]. Мидекамицин применяется при коклюше у детей (среднетяжелая и тяжелая форма) и включается в комплекс лечебных мероприятий при дифтерии зева.
Высокая чувствительность к мидекамицину типичных пневмотропных и атипичных возбудителей, вызывающих инфекции дыхательных путей и урогенитального тракта у детей, удобство в применении, наличие двух детских лекарственных форм (таблетки и суспензия), кратность приема до двух раз в сутки, высокая эффективность и отсутствие выраженных нежелательных явлений позволяют рекомендовать антибиотик для широкого применения в педиатрической практике.