Кому, как не провизорам и фармацевтам, знать, что этанол — это типичный представитель одноатомных спиртов, способный вступать в различные химические реакции. Он взаимодействует со щелочными металлами, магнием, алюминием, карбоновыми, неорганическими кислотами и множеством других веществ, включая лекарственные. По некоторым данным, с различными нежелательными реакциями между алкоголем и ЛС связано до 25 % обращений в «неотложку» [1]. И вполне закономерно, что столь распространенные неблагоприятные события стали благодатной почвой для разных домыслов. Накануне череды праздников самое время найти ответы на самые спорные вопросы о взаимодействиях между лекарствами и алкоголем, а также развеять связанные с этим мифы.
Тезис № 1: Алкоголь несовместим с любыми антибиотиками
Статус: Миф
Действительно, ряд противомикробных средств блокирует ацетальдегидрогеназу, задерживая ферментную биотрансформацию этанола на этапе чрезвычайно токсичного уксусного альдегида. Его накопление в организме способствует развитию интоксикации, которая сопровождается тяжелыми ощущениями. По сути, эти препараты работают так же, как и знаменитый дисульфирам, применяемый для лечения алкогольной зависимости, который попросту вызывает отравление организма. Его типичные симптомы — затруднение дыхания, тахикардия, тошнота и рвота, снижение артериального давления, жар или озноб.
Однако действуют таким образом только несколько антимикробных ЛС, в частности: цефамандол, цефоперазон, хлорамфеникол, гризеофульвин, изониазид, метронидазол, орнидазол, нитрофурантоин и сульфаметоксазол.
Все остальные противомикробные не имеют строгих ограничений при комбинировании с этанолом, однако это вовсе не значит, что их совмещение помогает эффективно бороться с инфекцией.
Сравнение эффективности Ацикловира и Валвира
Эффективность у Ацикловира достотаточно схожа с Валвиром – это означает, что способность лекарственного вещества оказывать максимально возможное действие схоже.
Например, если терапевтический эффект у Ацикловира более выраженный, то при применении Валвира даже в больших дозах не получится добиться данного эффекта.
Также скорость терапии – показатель быстроты терапевтического действия у Ацикловира и Валвира примерно одинаковы. А биодоступность, то есть количество лекарственного вещества, доходящее до места его действия в организме, схожа. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Тезис № 2: Спиртное и нестероидные противовоспалительные средства несовместимы
Статус: Правда
НПВП — одни из самых популярных обезболивающих препаратов. Только в США на средства этой группы приходится 70 миллионов рецептов и 30 миллиардов безрецептурных продаж в год [2]. Их применяют в том числе и для купирования головной боли при алкогольной интоксикации. В то же время большинство НПВП способствуют развитию гастропатии и повышают риск желудочно-кишечных кровотечений. Алкоголь усиливает выраженность ЖК-побочных эффектов НПВП, увеличивая риск кровотечений, что доказано в клинических исследованиях [3].
Кроме того, при одновременном приеме с этанолом ацетилсалициловой кислоты, ибупрофена и индометацина повышается длительность кровотечения — показатель, который отражает эластичность сосудов, их способность к сокращению при травме [3]. Эта особенность еще более увеличивает риски кровотечений. Поэтому, отпуская пероральные и парентеральные НПВП во время новогодних каникул, не лишним будет напомнить посетителям о возможных лекарственных взаимодействиях с алкоголем.
Современные подходы к диагностике и лечению герпесвирусных инфекций
Герпеcвирусная инфекция относится к числу наиболее социально значимых заболеваний, что обусловлено высокой восприимчивостью человека к вирусам герпеса и ежегодным ростом числа больных герпесвирусными инфекциями как за рубежом, так и в России, опережающим естественный прирост населения [1, 4, 16]. Согласно данным серологического обследования около 90% всего населения планеты инфицировано одним или несколькими серотипами вируса простого герпеса (ВПГ). За последние 5 лет прирост зарегистрированных случаев по отдельным формам герпесвирусной инфекции составляет 90%, причем рост инфекции характерен в группе лиц в возрасте 20–40 лет. Рецидивирующими формами заболевания страдают от 25 до 30% инфицированных людей, у 30% инфекция обнаруживается в субклинической и латентной форме. Особенностями современного течения герпесвирусной инфекции являются длительно рецидивирующий характер заболевания, нередко атипичная клиническая картина, появление штаммов возбудителей, устойчивых к стандартным лекарственным препаратам [2, 12].
Анализ ежегодной заболеваемости в России показал, что генитальный герпес, по данным государственных кожно-венерологических учреждений, выявляется у 20% взрослого населения. За период 2000–2004 гг. показатель заболеваемости генитальным герпесом по Москве увеличился в 6 раз, по Московской области — в 2 раза [4]. Генитальный герпес встречается во всех популяционных группах, самая высокая заболеваемость зарегистрирована в возрастной группе 20–29 лет, однако имеется и второй пик, приходящийся на возраст 35–40 лет. Повышенному риску развития заболевания подвергаются лица, начинающие раннюю половую жизнь. Нередко генитальным герпесом заболевают молодые люди 15–19 лет, что, возможно, связано с недостаточной информированностью об урогенитальных инфекциях и их профилактике [11].
Одной из причин эпидемии заболевания мы считаем плохую диагностику субклинических или атипичных форм герпесвирусной инфекции. В таких случаях реактивация вируса наблюдается реже, чем при рецидивирующем течении заболевания с клиническими проявлениями. Установлено, что после первичного инфицирования вирус герпеса мигрирует от места инокуляции по периферическим нервам до спинальных и церебральных ганглиев, где и остается «спящим» и неуязвимым для противовирусных препаратов. Под влиянием провоцирующих факторов происходит реактивация вируса и его дальнейшая миграция по периферическим нервам. При этом происходит раздражение нервных окончаний, приводящее к продромальным ощущениям в виде покалывания, жжения или зуда, так называемым предшественникам везикулезных высыпаний. Однако возможна бессимптомная продукция вируса на слизистых оболочках, которая связана с недостаточностью местных механизмов иммунной защиты. Следовательно, вирус герпеса способен передаваться и в период клинической ремиссии рецидивирующей герпесвирусной инфекции. Такое хроническое вирусовыделение может стать причиной инфицирования полового партнера, новорожденных, развития неонатальной герпесвирусной инфекции [7].
Клиника герпесвирусной инфекции многообразна и зависит от нескольких факторов [12]:
- особенностей вируса ВПГ: типа, антигенности и вирулентности;
- пола, возраста и степени иммунокомпетентности пациента;
- стадии и фазы заболевания (обострение или ремиссии);
- тяжести течения и длительности инфекционного процесса;
- наличия сопутствующих заболеваний, влияющих на течение инфекции;
- наличия ранее проведенных терапевтических мероприятий.
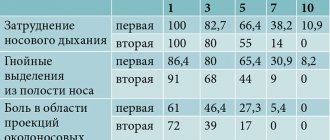
Первичный эпизод заболевания характеризуется обширными везикулезными и эрозивно-язвенными высыпаниями, тяжелыми общими клиническими симптомами и длительной репликацией вируса. У 80% пациентов типичным проявлениям первичной инфекции предшествуют локальные продромальные симптомы в виде парестезии, зуда, боли, жжения, регионарного лимфаденита, а также ухудшение общего состояния (головная боль, повышение температуры тела, озноб, миалгии, слабость, нарушения сна) [7]. Затем появляются высыпания на слизистой и коже в виде отдельных или сгруппированных везикулезных элементов величиной 2–3 мм на эритематозном фоне. Обычно сыпь обильная, пузырьки быстро вскрываются, оставляя после себя эрозии с неправильными очертаниями или язвенную поверхность. Как правило, высыпания имеют тенденцию к повторному появлению на том же месте.
Длительность острого периода заболевания колеблется от 8–10 до 18–22 дней. Клинические проявления нарастают в течение первой недели. В последующие 2 нед происходит бессимптомное слущивание поврежденного вирусом эпителия. Типичные высыпания простого герпеса во время первичного эпизода локализуются периорально в области красной каймы губ, крыльев носа, половых органов, ягодичной области. Также довольно часто первичный эпизод герпесвирусной инфекции может протекать с поражением слизистой ротоглотки в виде гингивита, глоссита, стоматита, герпетической ангины [4]. У иммунокомпрометированных пациентов (онкологические заболевания, ВИЧ-инфекция, прием глюкокортикостероидов, цитостатиков, лучевая терапия) возможны осложнения, такие как крестцовая радикулопатия, тяжелый асептический менингит или диссеминированная инфекция, требующие госпитализации.
Клинические проявления рецидива менее продолжительны по сравнению с первичным эпизодом герпесвирусной инфекции, длительность полной эпителизации составляет лишь 5–7 дней. С увеличением длительности заболевания и под воздействием терапии клиническая картина простого герпеса часто изменяется.
При типичном течении клиническая картина герпесвирусной инфекции в большинстве случаев позволяет поставить правильный диагноз без привлечения дополнительных лабораторно-инструментальных методов. Затруднения в дифференциальной диагностике могут возникать при атипичных формах простого герпеса или других заболеваниях, характеризующихся сходными кожными высыпаниями. Иногда приходится дифференцировать герпесвирусную инфекцию и чесотку, травматические поражения кожи и слизистых, контактный дерматит, герпетиформный дерматит Дюринга, стрептококковый импетиго, пузырчатку, буллезный пемфигоид, грибковые поражения кожи и слизистых, фиксированную токсидермию, болезни Дарье, Бехчета, Крона.
При атипичном течении высыпания простого герпеса в очаге поражения могут миновать отдельные стадии развития. Сохраняются лишь эрозия, папулезные элементы и отечные пятна на фоне эритемы. При данной форме герпесвирусной инфекции характерные очаги поражения на слизистых оболочках и коже могут отсутствовать, отмечаются лишь гиперемия и диффузный отек, на слизистой изредка возникают рецидивирующие болезненные трещины. Для генитального герпеса описана также рецидивирующая форма, для которой характерен лишь зуд, в ряде случаев субъективные ощущения отсутствуют [13].
Атипичный герпес в области гениталий может маскироваться под некоторые венерические заболевания, например под сифилис. Дифференциально-диагностическими признаками герпетических высыпаний в этом случае являются: полициклические очертания поражений, менее выраженная реакция регионарных лимфатических узлов, отсутствие инфильтрата в основании. Герпетические высыпания в области гениталий дифференцируют с герпетиформным шанкром при первичном сифилисе, сифилидами при вторичном сифилисе. При исследовании отделяемого отсутствует бледная трепонема.
Атипичная форма генитального герпеса нередко маскирована сопутствующей урогенитальной инфекцией и не всегда диагностируется врачами. Отмечено частое сочетание генитальной герпесвирусной инфекции с Chlamydia trachomatis, Ureaplasma urealyticum, Mycoplasma genitalium, Gardnerella vaginalis, Candida albicans, вирусом папилломы человека 16, 18 типов, цитомегаловирусом. Кроме того, сопутствующая урогенитальная микрофлора является благоприятным фоном для рецидивирования заболевания [7].
Особые затруднения в дифференциальной диагностике могут возникнуть при сочетании герпесвирусной инфекции и вышеперечисленных заболеваний. В таких случаях анамнез заболевания и диагностические тесты (исследования на выявление антигенов вируса и антител к нему) способствуют постановке правильного диагноза. Целью лабораторной диагностики является определение этиологического фактора (выявление вириона, генома или антигена вирусов) и динамическое наблюдение за течением патологического процесса (динамика специфических антител). Данные лабораторной диагностики часто используются для подтверждения диагноза герпесвирусной инфекции.
Современные методы идентификации ВПГ включают выявление вируса путем классического вирусовыделения на чувствительных клеточных культурах иммунофлюоресцентным методом (определение антител ИФА) и методом идентификации фрагментов нуклеиновых кислот вируса (полимеразная цепная реакция — ПЦР) [4]. Считаем, что среди множества лабораторных тестов для верификации ВПГ на коже и слизистых наиболее информативна ПЦР — выявление вирусов и вирионов. Преимуществами метода являются прямое определение возбудителя (выявление специфических участков ДНК), высокая специфичность (95–100%) и чувствительность (95–98%) — от 10 до 1000 геномных копий в пробе, высокая скорость получения результата анализа.
Для оценки активности вирусного процесса и адекватности противовирусного иммунного ответа наиболее доступным для широкой клинической практики является тест определения уровня специфических IgM и IgG к ВПГ 1 и 2 типов. Имеются особенности интерпретации данного теста. У ряда пациентов без клинических проявлений генитального герпеса встречается повышение только специфических IgG к ВПГ. Среди практикующих врачей бытует мнение, что это является свидетельством репликации вируса, и для снижения активности инфекционного процесса проводят противовирусную и иммуномодулирующую терапию. Такая тактика не совсем верна. В данных случаях для верификации собственно вирусного антигена необходимо дополнительное проведение ПЦР-теста. Отрицательная ПЦР к ВПГ 1 и 2 типов при повышении специфического IgG у пациентов без клинических проявлений герпесвирусной инфекции указывает на вирусоносительство и не требует дополнительного обследования и лечения. Мы настаиваем на этом положении, так как нередко первым этапом лабораторной диагностики является определение специфических антител к ВПГ 1 и 2 типов. Этим анализом многие практические врачи заменяют идентификацию собственно вируса герпеса и обосновывают назначение противовирусной терапии обнаружением высоких титров специфических антител к ВПГ 1 и 2 типов. Стоит отметить, что на сегодняшний день не существует клинически значимых титров специфических IgG к ВПГ, а уровень их превышения также клинически неинформативен. Мы считаем, что противовирусная терапия показана только пациентам с клиническими проявлениями генитальной герпесвирусной инфекции, а при их отсутствии — только при выявлении репликации вируса герпеса методом ПЦР.
Кроме того, при серологическом обследовании у части пациентов с дебютом клинических проявлений герпесвирусной инфекции возможны ложноотрицательные результаты. Нами была изучена уникальная группа больных, впервые инфицированных ВПГ с начальными клиническими проявлениями в виде генитального герпеса. В первые сутки заболевания мы констатировали формирование первичного раннего гуморального ответа у 86% пациентов в виде синтеза специфического IgM. На 7–14-е сутки у 26–47% больных был отмечен рост уровня специфического IgG на фоне снижения специфического IgM. Однако к 28-му дню заболевания у 38% пациентов не выявлено сероконверсии, т. е. не повышался уровень специфических IgM и IgG. У 86% этих пациентов поздний гуморальный иммунный ответ сформировался только через 2 мес. Полученные результаты показывают, что в период конверсии раннего гуморального ответа в поздний (к 28-му дню) у 38% пациентов формируется «серонегативная» зона. Именно в этот период возможны ложноотрицательные результаты исследования специфического гуморального иммунитета, которые не следует расценивать как отсутствие инфицирования ВПГ.
Таким образом, диагноз герпесвирусной инфекции и тактика терапии основываются на анамнестических, клинических данных и результатах лабораторного обследования.
Лечение больных с герпесвирусной инфекцией представляет определенные трудности из-за отсутствия противовирусных препаратов, способных полностью элиминировать ВПГ из организма, а также вследствие формирования нарушений в иммунной системе при высокой частоте рецидивов. Кроме того, причинами неэффективности лечения нередко являются недостаточность применяемых врачами терапевтических доз препаратов для контроля над тяжестью заболевания, непонимание механизмов действия ациклических нуклеозидов, а также отсутствие личностного контакта пациента с лечащим врачом.
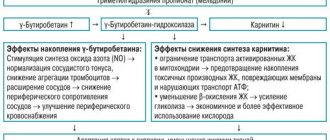
В настоящее время все методы лекарственной терапии и профилактики герпесвирусной инфекции можно объединить в три основные группы: химиотерапия (ациклические нуклеозиды), иммунотерапия и комбинированная терапия, включающая химио- и иммуномодулирующие препараты.
В 1981 г. был создан и внедрен в клиническую практику препарат ацикловир (Зовиракс). Механизм действия ацикловира основан на его высокой специфичности к вирусной тимидинкиназе, которая фосфорилирует ацикловир. ДНК-полимераза вируса ошибочно включает фосфорилированный ацикловир вместо естественного дезоксигуанозинтрифосфата в концевые участки новых вирусных ДНК, тем самым обрывая процесс репликации вируса на любой стадии, и новые генерации вирусов не образуются. В настоящее время это наиболее часто назначаемый противогерпетический препарат и его уже применили более 50 млн больных [15]. Помимо этого, синтезированы и широко используются в последнее время новые противовирусные препараты этой же группы — валацикловир (Валтрекс) и фамцикловир (Фамвир) [5]. Согласно проведенным исследованиям биодоступность противогерпетических препаратов из группы ациклических нуклеозидов возрастает следующим образом: ацикловир — 20%, валацикловир — 54% и фамцикловир — 77% [10].
Выделяют два основных способа применения противовирусных химиопрепаратов:
- эпизодическое назначение (по мере необходимости при обострениях герпесвирусной инфекции);
- пролонгированная или превентивная терапия.
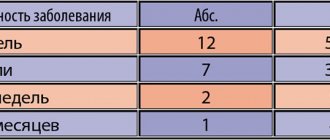
В первом случае препарат назначают коротким курсом в течение 7–10 дней. Во втором — пациенты принимают препарат ежедневно в течение нескольких месяцев или лет не только для купирования данного рецидива, но и для профилактики последующих рецидивов. Нами исследованы различные схемы применения ациклических нуклеозидов у пациентов с генитальной герпесвирусной инфекцией с высокой частотой рецидивов (таблица).
Явные преимущества высокодозовой терапии проявились при оценке продолжительности рецидива генитального герпеса на фоне лечения. Валтрекс и Фамвир в высоких дозах сократили сроки рецидива более чем в 2 раза по сравнению со стандартной терапией (с 3,9 до 1,7 дней). Эффективность ацикловира оказалась несколько ниже. Тем не менее все эти препараты существенно снизили сроки клинических проявлений рецидива по сравнению со стандартной схемой лечения. Проведенные нами исследования выявили неоспоримые преимущества высокодозовой схемы терапии, когда на ее фоне уже на 3-и сутки достоверно уменьшалась интенсивность зуда, жжения, отека и гиперемии в области высыпаний.
Проведенное исследование показало, что длительность ремиссии у больных с различными формами генитальной герпесвирусной инфекции зависит от схемы лечения. При стандартной и высокодозовой схеме терапии Ацикловиром, Валтрексом и Фамвиром при типичном течении заболевания период ремиссии колебался от 0,8 до 1,6 мес, при атипичной форме — от 0,7 до 1,7 мес. Статистически значимых различий по длительности ремиссии при данных схемах лечения не получено. В то же время пролонгированная схема терапии способствовала достоверному увеличению безрецидивного течения герпесвирусной инфекции. Так, при типичной форме заболевания после лечения Ацикловиром период ремиссии достиг 4,1 мес, Валтрексом — 10,5 мес, Фамвиром — 9,2 мес, при атипичной форме — соответственно 3,3 мес, 7,1 мес и 6,8 мес. Таким образом, максимальный безрецидивный период был получен при пролонгированном приеме Валтрекса и Фамвира.
В настоящее время практикующими врачами используются преимущественно стандартные схемы лечения противовирусными препаратами. Пролонгированная и высокодозовая схемы терапии практически не применяются для купирования и профилактики повторных рецидивов герпесвирусной инфекции. Возможно, препятствием для такой терапии служит недостаток информации о ее эффективности. Кроме того, пролонгированная терапия позволяет предупредить рецидивы генитального герпеса и тем самым оказывает положительное психологическое воздействие на больного. К сожалению, плохо информированные пациенты нередко отказываются от пролонгированной и высокодозовой терапии, выражая беспокойство по поводу безопасности ее применения и развития лекарственной резистентности.
Высокодозовая и пролонгированная схемы терапии улучшают качество жизни пациентов, которые на определенном этапе лечения начинают принимать непосредственное участие в контроле над заболеванием. Такую терапию следует назначать больным с высокой частотой рецидивов, поскольку повторное проявление заболевания является для них стрессом, который, в свою очередь, провоцирует иммуносупрессию и способствует развитию последующего рецидива.
Показано, что бессимптомное выделение вируса, как правило, встречается в первые годы после первичного инфицирования [15]. Поэтому при первом эпизоде герпесвирусной инфекции целесообразно проведение высокодозовой терапии, которая позволяет снизить риск передачи вируса. Как показывает практика, в это время пациенты отдают предпочтение быстрому и эффективному лечению. Кроме того, в этот период больные особенно нуждаются в консультации специалистов и психологической поддержке [9].
Образ жизни пациента определяет выбор тактики лечения генитального герпеса. Например, в периоды дальних поездок с переменой климата, экзаменов, стрессовых ситуаций предпочтительно назначение пациентам пролонгированной терапии, которая в данном случае является профилактической и предупреждает возможное развитие рецидива. Неотъемлемой частью терапии и профилактики распространения ВПГ является образовательная программа. Врач должен информировать больного об опасности распространения инфекции, перспективах лечения и необходимости сотрудничества.
У пациентов при высокой частоте рецидивов формируется так называемый вторичный иммунодефицит с нарушением гуморального и клеточного звеньев иммунитета, снижением количества и угнетением функциональной активности натуральных киллеров и клеток моноцитарно-макрофагального ряда, нарушением продукции интерферона [14]. Таким пациентам показано включение в схему лечения препаратов иммунокорригирующей направленности. В настоящее время уже накоплен достаточный опыт успешного применения интерферонов (Реаферон, Виферон и др.), индукторов интерферонов (Циклоферон, Амиксин, Кагоцел, Ридостин и др), иммуномодуляторов различного спектра действия (Полиоксидоний, Галавит, Иммуномакс, Ликопид и др.) при лечении рецидивирующей герпесвирусной инфекции [3, 6, 8]. Однако назначение препаратов, направленных на коррекцию нарушений в системе интерферона, стимуляцию клеточной противовирусной защиты и усиление специфического противогерпетического иммунитета, должно проводиться с учетом данных иммунологического обследования конкретного пациента.
В заключение обсудим четыре возможных варианта врачебной тактики в зависимости от результатов обследования пациентов в отношении герпесвирусной инфекции.
Вариант 1. Повышение уровня специфического IgG, отрицательный результат ПЦР-теста на ВПГ 1 и 2 типов у пациента без клинических проявлений герпесвирусной инфекции свидетельствуют о вирусоносительстве и не требуют дополнительного обследования и лечения. Проводится динамическое наблюдение за больным, назначается курс витаминов-антиоксидантов.
Вариант 2. В случае выявления ВПГ 1 и 2 типов при ПЦР-исследовании у пациента без клинических проявлений герпевирусной инфекции следует оценить уровень специфических IgM и IgG. Селективное повышение специфического IgM свидетельствует о первичном инфицировании. В этих случаях проводится стандартная противовирусная терапия, после которой выполняется контрольная ПЦР. Другие иммунологические обследования нецелесообразны. Повышение специфических IgG и IgM свидетельствует об усиленном иммунном ответе у реинфицированных больных. Им также проводится стандартная противовирусная терапия, после которой выполняется контрольная ПЦР. Также ведется динамическое наблюдение и применяются витамины-антиоксиданты.
Вариант 3. Повышение уровня специфических антител у больного с клиническими проявлениями герпесвирусной инфекции и низкой частотой рецидивов (2–4 раза в год) свидетельствует об усиленном иммунном ответе и не требует дальнейшего изучения противовирусного иммунитета. Таким пациентам рекомендуется стандартная противовирусная терапия. При выраженных клинических проявлениях показана высокодозовая терапия. Проводится динамическое наблюдение и курс витаминов-антиоксидантов.
Вариант 4. У больного с клиническими проявлениями герпесвирусной инфекции с высокой частотой рецидивов (более 6 раз в год) и повышенным уровнем специфических IgM и IgG выполняют иммунограмму. Оценивают субпопуляционный состав клеток, NK-активность и уровень α- и γ-интерферонов. При выявлении нарушений в противовирусной защите проводят либо пролонгированную терапию ациклическими нуклеозидами, либо стандартное противовирусное лечение в комбинации с иммуномодулирующими препаратами. Необходимы исключение провоцирующего фактора и назначение курса витаминов-антиоксидантов. Представленные варианты, возможно, не содержат всех возможных ситуаций обследования больных с герпесвирусной инфекцией, тем не менее они являются руководством к действию, доступным для практикующих врачей первичного звена.
Таким образом, индивидуальный подход к терапии с учетом результатов клинического и лабораторного обследования обеспечивает адекватный контроль течения герпесвирусной инфекции и дает преимущество перед стандартным лечением. Для широкого внедрения в клиническую практику необходимо, чтобы такие методы обследования и терапии были доступны всем слоям населения и соответствовали современному уровню медицинской помощи.
По вопросам литературы обращайтесь в редакцию.
А. Е. Шульженко, доктор медицинских наук И. Н. Зуйкова Институт иммунологии ФМБФ России, Москва
Тезис № 3: Во время лечения антидепрессантами следует избегать приема спиртных напитков
Статус: Правда
Алкоголь не рекомендуется совмещать со всеми антидепрессантами, хотя механизм лекарственного взаимодействия «этанол — препарат» и выраженность последствий бывают различными. Так, в сочетании с трициклическими АД (амитриптилин, мапротилин) этанол может способствовать гиперседации. Он нарушает метаболизм препаратов этой группы в печени, что приводит к повышению их концентрации в крови. Если к тому же у потребителя спиртного в анамнезе есть алкогольная болезнь печени, риски еще более увеличиваются, поскольку в таком случае замедляется расщепление антидепрессантов и, соответственно, повышается их уровень в кровотоке. Повышение дозы трициклических антидепрессантов в крови, в свою очередь, вызывает нарушение сердечного ритма, судороги, галлюцинации и другие тяжелые последствия вплоть до комы [3].
Гораздо менее опасна комбинация селективных ингибиторов обратного захвата серотонина и алкоголя. Препараты этой группы в целом имеют более высокий профиль безопасности, чем трициклические антидепрессанты, и реже вступают в лекарственные взаимодействия. Тем не менее, несмотря на отсутствие зарегистрированных реакций между ними и этанолом, применять их в комбинации всё же не рекомендуется. Это связано во многом с тем, что совмещение СИОЗС с алкоголем может способствовать обострению заболевания [4]. Кроме того, доказано, что при комбинации венлафаксина с этанолом могут снижаться память и когнитивные возможности [4].
Сравнение удобства применения Ацикловира и Валвира
Это и подбор дозы с учетом различных условий, и кратность приемов. При этом важно не забывать и про форму выпуска препарата, ее тоже важно учитывать при составлении оценки.
Удобство применения у Ацикловира примерно одинаковое с Валвиром. При этом они не являются достаточно удобными для применения.
Рейтинг препаратов составлен опытными фармацевтами, изучающий международные исследования. Отчет сгенерирован автоматически.
Дата последнего обновления: 2020-12-13 10:31:36
Тезис № 4: Если от спиртного разболелась голова, лучше принять парацетамол
Статус: Миф
Парацетамол метаболизируется с помощью фермента CYP2E с образованием гепатотоксичного метаболита N-ацетил-р-бензохинонимина. В норме он быстро инактивируется с помощью глутатиона. При потреблении алкогольных напитков, особенно хроническом, активность CYP2E1 увеличивается, что приводит к повышению выработки токсичного метаболита. К тому же на фоне длительного приема спиртного запасы глутатиона истощаются, что сопряжено с накоплением токсичного метаболита в крови и повышением риска развития печеночной недостаточности [5].
Вероятность лекарственного взаимодействия этанола и парацетамола увеличивается и при приеме более 4 граммов препарата в сутки. Американский регулятор FDA рекомендует тем, кто принимает более 3 алкогольных единиц в день (напомним, алкогольная единица составляет 30 мл 40 %-ного алкоголя, 100 мл вина или 250 мл пива), проконсультироваться с врачом перед приемом как парацетамола, так и безрецептурных анальгетиков [5]. Первостольникам же во время новогодних праздников важно обращать внимание потребителей на повышенную вероятность гепатотоксических реакций при совмещении со спиртным парацетамола и содержащих его комбинированных препаратов.
Тезис № 7: Алкоголь нельзя совмещать с некоторыми противодиабетическими препаратами
Статус: Правда
При сахарном диабете пить спиртные напитки вообще крайне нежелательно — это грозит резким падением уровня сахара в крови и развитием гипогликемии, что связано с нарушением высвобождения хранящихся в клетках печени углеводов на фоне алкогольной интоксикации. Риски гипогликемии у больных сахарным диабетом, принимающих спиртное, еще более увеличиваются из‑за возможных лекарственных взаимодействий этанола и некоторых препаратов сульфонилмочевины — в частности, глипизида [3].
Совмещение спиртных напитков с препаратом первой линии для лечения сахарного диабета 2‑го типа метформином может приводить к повышению уровня молочной кислоты в крови и развитию лактоацидоза. Вероятность его возникновения повышается при соблюдении низкокалорийной диеты, недостаточном питании и печеночной недостаточности. Поэтому метформин несовместим с алкоголем в составе как спиртных напитков, так и спиртосодержащих лекарственных средств [3].
В лекарственные взаимодействия с этанолом вступает и инсулин. Алкоголь может усиливать или ослаблять гипогликемический эффект препарата, что чревато развитием гипо- или гипергликемии и, соответственно, ухудшением контроля заболевания [7].
Тезис № 8: При похмелье можно принять обычные «порошки от простуды»
Статус: Миф
Противопростудные комбинированные средства содержат несколько компонентов, и вступать в лекарственные взаимодействия с этанолом могут как минимум два из них. Во-первых, в состав большинства препаратов этой группы входит парацетамол, причем иногда в дозе 1000 г. При его совмещении с алкоголем повышается риск гепатотоксических реакций. Во-вторых, многие противопростудные комбинированные препараты содержат антигистаминные компоненты 1‑го поколения. Алкоголь может потенцировать их угнетающий эффект на центральную нервную систему, способствуя развитию гиперседации и сонливости [3]. Поэтому не стоит рекомендовать препараты этой группы в качестве средств, облегчающих симптомы похмелья.
Источники
- Alcohol-medication interactions. Alberta Health Services. – [Электронный ресурс] – URL: https://www.albertahealthservices.ca/assets/healthinfo/AddictionsSubstanceAbuse/hi-asa-beyond-abcs-a… (Дата обращения 09.12.2019).
- Alcohol-medication interactions. Alberta Health Services. – [Электронный ресурс] – URL: https://www.albertahealthservices.ca/assets/healthinfo/AddictionsSubstanceAbuse/hi-asa-beyond-abcs-a… (Дата обращения 09.12.2019).
- Green G. A. Understanding NSAIDs: from aspirin to COX-2 //Clinical cornerstone. 2001; 3 (5): 50–59.
- Weathermon R., Crabb D. W. Alcohol and medication interactions //Alcohol research. 1999; 23 (1): 40.
- Adams W. L. Interactions between alcohol and other drugs //International journal of the addictions. 1995; 30 (13–14): 1903–1923.
- Noureldin M. et al. Drug-alcohol interactions: a review of three therapeutic classes //US Pharm. 2010; 35 (11): 29–40.
- Moore A. A., Whiteman E. J., Ward K. T. Risks of combined alcohol/medication use in older adults //The American journal of geriatric pharmacotherapy. 2007; 5 (1): 64–74.
- По данным ГРЛС на 12.12.2019.