Скорочений виклад
J. G. O’Brien, S. A. Chennubhotla, R. V. Chennubhotla Am Fam Physician 2005;71:2111-7, 2118
1Див. також статтю Внутрішньоклітинна та позаклітинна гіпергідратація та дегідратація: етіологія, патофізіологія, діагностика, лікування. – Медицина світу. – 1999. – Т. VIІ. – Ч. 3. – С. 460-469; Т. VII – Ч. 4. – С. 523-530.
Набряки часто трапляються у клінічній практиці, проте ефективне їх лікування розроблено відносно недавно. Завжди слід визначати етіологію набряків: вони можуть викликатися захворюванням, небезпечним для життя, наприклад застійною серцевою недостатністю, або якимсь доброякісним станом, зокрема тривалим перебуванням у сидячому положенні. Набряки можуть обмежуватися однією кінцівкою або бути генералізованими та масивними. Вони звичайно виникають унаслідок дисбалансу обміну рідини, включаючи порушення гемодинаміки на рівні капілярів, які сприяють затримці води та натрію нирками та переміщенню рідини з судинного русла в інтерстицій. Найчастіша етіологія набряків: венозна недостатність, підвищена проникність стінки капілярів та зростання об’єму плазми крові внаслідок затримки натрію та води.
ПАТОФІЗІОЛОГІЯ
Набряки виникають тоді, коли зростає величина фільтрації під впливом підвищення гідравлічного тиску в капілярах чи інтерстиціального онкотичного тиску, збільшення проникності капілярів або зниження онкотичного тиску плазми крові. Нирки відіграють центральну роль у підтримці балансу рідини в організмі, контролюючи величину об’єму позаклітинної рідини за допомогою зміни екскреції натрію та води. Первинним регулятором об’єму рідини в організмі є антидіуретичний гормон, який виділяється у відповідь на зміну ОЦК, тонусу судин та артеріального тиску. Натрій та інші аніони — основні розчинені компоненти позаклітинної рідини, вміст яких коливається у вузьких межах. Надходження хлориду натрію в організм загалом еквівалентне його виведенню протягом кількох днів; якщо надходження підвищується — через певний період компенсаторно зростає його екскреція. Таким чином об’єм позаклітинної рідини підтримується на постійному рівні, незважаючи на значні коливання надходження рідини в організм.
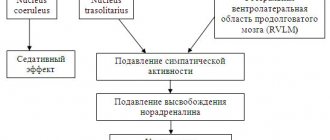
Для того, щоб зрозуміти роль затримки натрію для підтримання об’єму плазми крові, важливо зрозуміти концепцію ефективного об’єму артеріальної крові (ЕОАК). ЕОАК визначається гомеостатичними механізмами підтримки ОЦК і, у свою чергу, регулює реабсорбцію натрію в нирках. ЕОАК корелює з об’ємом позаклітинної рідини. У здорових осіб при надходженні натрію в організм підвищується об’єм позаклітинної рідини і ЕОАК, відповідно швидко зростає натрійурез і таким чином відновлюється нормальна величина об’єму рідини. При дегідратації рівень ЕОАК та позаклітинної рідини знижений, активізується затримка натрію в організмі через ренін-ангіотензин-альдостероновий механізм, що призводить до відновлення ОЦК. При зниженні функції нирок порушується розподіл рідини в організмі. При розвитку набряку зниження рівня ЕОАК активує рецептори об’єму/тиску, включаючи барорецептори низького тиску у венозній системі, барорецептори високого тиску у великих судинах, ниркові та печінкові рецептори.
У пацієнтів з первинною затримкою натрію пригнічується аферентна стимуляція. У міру зростання об’єму позаклітинної рідини появляються набряки, а об’єм ЕОАК — знижується. Унаслідок цього стимулюються еферентні рефлекторні шляхи, зумовлюючи затримку натрію, активацію симпатичної нервової системи, стимуляцію ренін-ангіотензин-альдостеронової системи та виділення вазопресину.
Незважаючи на те, чи викликаний набряк зменшенням серцевого викиду чи іншими причинами, він утримується через те, що компенсаторні механізми намагаються підтримувати об’єм плазми крові.
Диуретики
Сохранение водно-солевого баланса в организме — важнейшее условие поддержания стабильных показателей артериального давления. Почечные нефроны регулируют объем жидкости и содержание электролитов в организме посредством секреции и реабсорбции. Водно-солевой баланс может нарушаться при ряде состояний, в том числе при гипертонической болезни, сердечной или почечной недостаточности, а также при нефротическом синдроме, циррозе и др.
Нормализовать водно-солевое равновесие позволяют диуретики, увеличивающие скорость потока мочи и экскреции Na+ и сопутствующего аниона, обычно Cl-. Основной детерминантой объема внеклеточной жидкости в организме является NaCl, и большинство диуретиков уменьшают объем внеклеточной жидкости путем снижения общего содержания NaCl в организме [1].
Сегодня для лечения артериальной гипертензии применяются как тиазидные и тиазидоподобные, так и петлевые диуретики.
Принципи лікування
Лікування набряків полягає в боротьбі з первинним захворюванням (по можливості), обмеженні прийому натрію з їжею для мінімізації затримки рідини та, як звичайно, застосуванні сечогінних. Тому важливо встановити клінічний діагноз та по можливості радше застосовувати нефармакологічні методи лікування, ніж відразу призначати діуретики.
Не всі пацієнти з набряками потребують медикаментозної терапії; у деяких хворих достатньо обмежити вживання натрію до рівня, нижчого від об’єму натрійурії, та піднімати нижні кінцівки вище від рівня лівого передсердя. Проте в більшості пацієнтів доводиться додавати сечогінні до нефармакологічних заходів, з яких особливо ефективне тривале обмеження вживання солі. Вибір діуретика, способу введення та дозування залежить від первинного захворювання, важкості перебігу та ургентності проблеми. Важливо знати фармакокінетику та фармакодинаміку різних препаратів.
Діуретики діють на різні структури нирки (таблиця 1). Петлеві діуретики (фуросемід, буметанід та торсемід) блокують транспорт хлориду натрію і калію у висхідній частині петлі Генле, тоді як тіазидові сечогінні — електронейтральний транспорт хлориду натрію в дистальних звивистих канальцях. Амілорид та тріамтерен блокують апікальні натрієві канали в кіркових збірних трубочках. Ці препарати тісно зв’язуються з альбуміном. Усі діуретики, крім спіронолактону, потрапляють у просвіт ділянки нефрона, де проявляють свою дію, з первинною сечею.
Таблиця 1. Фізіологічна класифікація діуретиків (за D. H. Ellison, 1994)
| Діуретики, які діють на проксимальні звивисті канальці | Петлеві діуретики | Діуретики, які діють на дистальні звивисті канальці | Діуретики, які діють на кіркові збірні трубочки |
| Інгібітори карбоангідрази: ацетазоламід (діакарб) Інгібітори фосфодіестерази*: теофілін | Інгібітори транспорту хлориду натрію і калію: буметанід, етакринова кислота, фуросемід | Інгібітори транспорту хлориду натрію: хлорталідон, гідрохлортіазид, метолазон | Антагоністи альдостерону: спіронолактон Блокатори натрієвих каналів: амілорид, тріамтерен |
| * Механізм, за допомогою якого інгібітори фосфодіестерази посилюють екскрецію хлориду натрію з сечею, достеменно невідомий і може включати дію на гемодинаміку та ниркові канальці (можливо, медіатором є цАМФ). | |||
Після орального прийому всмоктування фуросеміду в середньому досягає 50% (коливається в межах 10–80%). Всмоктування буметаніду і торсеміду ліпше і сягає 80–100%. Тіазидові діуретики, такі як хлортіазид та гідрохлортіазид, можуть виділятися з сечею в незміненому вигляді; інші препарати (бендрофлюметазид та індапамін) метаболізуються в печінці. Частота прийому сечогінних залежить від часу напіввиведення з плазми крові: тіазидові діуретики з тривалим часом напіввиведення можна призначати один або два рази на день.
Петлеві діуретики мають коротший час напіввиведення (коливається від 1 години в буметаніду до 3–4 годин в торсеміду), тому їх доводиться приймати частіше, ніж тіазидові похідні. Дія петлевих діуретиків швидко припиняється, після чого нирки відразу починають реабсорбцію натрію, що нівелює дію сечогінних препаратів, — цей процес називається постдіуретичною затримкою хлориду натрію. Якщо хворий приймає з їжею велику кількість хлориду натрію, а час напіввиведення сечогінного короткий (це стосується петлевих діуретиків), то постдіуретична затримка хлориду натрію повністю компенсує попередню втрату натрію. Тому пацієнтам, які приймають петлеві діуретики, важливо обмежувати споживання натрію.
Тиазидные и тиазидоподобные диуретики
Механизм действия
Тиазидные и тиазидоподобные мочегонные средства действуют главным образом в кортикальном сегменте петли нефрона, на участке ингибирования реабсорбции катионов (калия, натрия, магния). Они блокируют транспортный белок, обеспечивающий перенос натрия и хлора в клетки канальцевого эпителия, вследствие чего увеличивается выведение этих электролитов с мочой. Выведение же ионов кальция, напротив, снижается [2]. Это сопровождается усилением диуреза и уменьшением объема циркулирующей крови [3].
У больных пожилого возраста более эффективны тиазидные и тиазидоподобные средства, чем β-адреноблокаторы и ингибиторы АПФ [3].
Даже в низких дозах они обладают довольно высокой антигипертензивной активностью, не уступающей эффекту антагонистов кальция, α1‑адреноблокаторов [4].
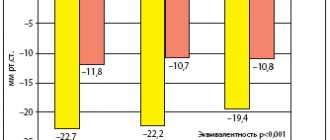
По данным исследований, на фоне регулярного приема тиазидных и тиазидоподобных диуретиков систолическое артериальное давление (АД) снижается в среднем на 10–20 мм рт. ст., а диастолическое — на 5–15 мм рт. ст. Кроме того, препараты этой группы снижают периферический сосудистый тонус [2].
Показания и свойства
Препараты этой группы применяются как в качестве монотерапии, так и в комбинации с другими гипотензивными средствами при артериальной гипертензии. Кроме того, их назначают при хронической сердечной недостаточности, нарушениях работы почек, предменструальном синдроме (для уменьшения сопутствующих ПМС отеков).
Тиазиды и тиазидоподобные диуретики, как и большинство других классов современных антигипертензивных ЛС, проявляют комплексный сердечно-сосудистый эффект [3]:
- снижают АД;
- предотвращают развитие сердечно-сосудистых осложнений;
- уменьшают сердечно-сосудистую смертность.
Влияние на сердечно-сосудистые риски обусловлено способностью препаратов этой группы обеспечивать обратное развитие гипертрофии левого желудочка. Еще одно положительное их свойство — повышение эффективности антигипертензивных препаратов остальных четырех фармакологических групп.
При приеме некоторых препаратов этой группы увеличивается уровень мочевой кислоты, незначительно — глюкозы и атерогенных липидов [2].
Отдельные представители
- Гидрохлоротиазид относится к числу самых изученных и популярных диуретиков, применяющихся для лечения артериальной гипертензии. Эффективность и высокий профиль безопасности были доказаны в длительных рандомизированных исследованиях, поэтому именно этот диуретик является одним из препаратов выбора для длительного лечения гипертензии [4].
- Индапамид, в отличие от других тиазидных (и тиазидоподобных) диуретиков блокирует кальциевые каналы мышечной стенки артерий, снижая периферическое сосудистое сопротивление и оказывая прямое сосудорасширяющее действие [2, 5]. Индапамид доказал значительные органопротективные эффекты — регрессию гипертрофии левого желудочка, защиту почек. По влиянию на уровень систолического давления значительно превосходит гипотиазид [5]. Кроме того, препарат не влияет на уровень глюкозы и подходит для применения при сахарном диабете [2].
Переносимость
Тиазиды и тиазидоподобные диуретики в низких дозах хорошо переносятся и не вызывают существенных изменений углеводного и липидного обмена. Изредка, как правило у мужчин, на фоне приема препаратов может развиться подагра [4]. Кроме того, для тиазидных диуретиков свойственно неблагоприятное влияние на эректильную функцию.
О чем предупредить клиента?
- На фоне лечения может нарушаться электролитный баланс, поэтому при появлении сухости во рту, жажды, нарушения сердечного ритма, необычной усталости на фоне лечения следует как можно быстрее связаться с лечащим врачом [6].
- При совместном приеме с алкоголем может возникать ортостатическая гипотензия (резкое снижение давления при перемене положения тела с горизонтального на вертикальное) [6].
- В начале лечения препаратами этой группы не рекомендуется водить автомобиль и выполнять работы, требующие повышенного внимания. Длительность этого периода индивидуальна [6].
- Тиазидные и тиазидоподобные диуретики могут способствовать развитию эректильной дисфункции. Если клиент приобретает препараты этой группы (в том числе и в составе комбинированных средств) и ингибиторы ФДЭ-5, уместно предупредить его о возможном негативном влиянии первых на сексуальную функцию.
Причини неефективності лікування діуретиками
Резистентність до дії діуретиків — неможливість досягнути негативного балансу натрію в організмі, незважаючи на застосування високих доз сечогінних (наприклад, фуросеміду в добовій дозі 240 мг). Цей стан слід виключати у хворих з персистуючими набряками, які отримують адекватне лікування діуретиками, обмежують фізичну активність та вживання натрію з їжею (тобто менш як 2 г/день).
Резистентність до дії діуретиків може посилюватися при супутньому призначенні НСПЗП, які можуть інгібувати сечогінну дію |
Для боротьби з резистентністю до дії діуретиків важливо знати фармакокінетику різних сечогінних препаратів. Буметанід, на відміну від фуросеміду, після орального прийому всмоктується краще. Адаптації епітелію дистальних звивистих канальців до хронічного застосування діуретиків можна уникнути, додаючи ще один сечогінний препарат, який діє на іншу ділянку нефрона. Частіше застосування короткодіючих сечогінних або призначення довгодіючих діуретиків обмежує реабсорбцію натрію, яка може виникати при припиненні сечогінної дії препарату. Пацієнти потребують ретельного спостереження для вчасного виявлення побічних ефектів, таких як гіпокаліємія та гіповолемія. У пацієнтів із резистентністю до діуретиків, яких лікують у відділенні інтенсивної терапії, може виникнути потреба у тривалій внутрішньовенній інфузії петлевих діуретиків.
У таблиці 2 подано інші потенційні причини неефективності лікування діуретиками. Проблема може полягати не в справжній резистентності до препаратів, а в недотриманні режиму лікування; це особливо стосується пацієнтів похилого віку, які отримують багато препаратів і належать до групи ризику розвитку нетримання сечі. Такі хворі можуть обмежувати вживання сечогінних, щоб залишатися сухими. Резистентність до сечогінних може посилюватися від супутнього призначення НСПЗП, які можуть інгібувати дію діуретиків. Відміна НСПЗП може нівелювати резистентність до сечогінних.
Таблиця 2. Причини неефективності лікування петлевими діуретиками (за Dormans T. P. et al., 1998)
Порушення комплаєнсу пацієнта
Справжня резистентність до дії діуретиків
|
Інша потенційна причина неефективності лікування — розвиток толерантності до діуретиків. Короткотермінову толерантність слід запідозрити тоді, коли після введення першої дози починає спостерігатися зменшення відповіді на препарат. Вважають, що внаслідок зменшення ОЦК відбувається компенсаторна реакція, щоб уникнути подальшої втрати рідини. Довготермінова толерантність трапляється у хворих, які тривалий час отримують петлеві діуретики, — внаслідок тривалого контакту з розчиненими у сечі сполуками відбувається гіпертрофія дистальних сегментів нефронів, які реабсорбують більше натрію і таким чином зменшують загальний діурез. Підвищення дози петлевого діуретика при довготерміновій толерантності навряд чи поліпшить діурез, тоді як додаткове призначення тіазидового похідного, який діє на іншу ділянку нефрона, призведе до синергічного та швидкого підвищення діурезу. Якщо спостерігається зниження ефективності інших діуретиків, також буває корисно додати діакарб, який діє на проксимальні звивисті канальці.
Петлевые диуретики
Механизм действия
Действующие на уровне петли Генле диуретики являются наиболее сильнодействующими представителями этого класса препаратов, поскольку через этот сегмент нефрона реабсорбируется 20–30 % всего профильтрованного натрия. Уменьшая объем циркулирующей крови, петлевые диуретики снижают нагрузку на миокард, уменьшают застойные явления в легких и расслабляют стенку сосудов. Им свойственны быстрое начало действия и мощный краткосрочный эффект [7].
Показания и свойства
Область применения петлевых диуретиков, как правило, ограничена неотложными ситуациями. Их назначают при отечном синдроме различного происхождения. При артериальной гипертензии препараты этого ряда используются при гипертонических кризах, устойчивости к тиазидным диуретикам, а также при сопутствующей тяжелой почечной недостаточности [7]. Исключение может составлять современный петлевой диуретик торасемид.
Отдельные представители
- Фуросемид — мощный петлевой диуретик. Расширяет сосуды, увеличивает почечный кровоток, обладает антиагрегационной активностью. Применяется при острых состояниях, редко — для лечения гипертонической болезни [6]. Препарат «резервируют» для пациентов, устойчивых к традиционной антигипертензивной терапии.
- Торасемид — петлевой диуретик, который характеризуется менее выраженным пиковым эффектом и большей продолжительностью действия по сравнению с фуросемидом. Антигипертензивный эффект доказан в ряде клинических исследований. Применяют как для долгосрочного лечения гипертонии, так и в составе комбинированной терапии хронической сердечной недостаточности [7]. Тем не менее, в современных руководствах по лечению АГ препарат не упоминается в качестве средства первой линии терапии [3].
Переносимость
Петлевые диуретики могут способствовать резкому снижению давления и развитию ортостатической гипотензии.
О чем предупредить клиента?
- На фоне приема петлевых диуретиков может происходить чрезмерная потеря жидкости и/или электролитов. Важно рассказать покупателю, что при появлении сухости во рту, повышенной жажды, головокружения следует как можно быстрее связаться с лечащим врачом.
- Петлевые диуретики не рекомендуется применять водителям транспортных средств и людям, работа которых связана с повышенной концентрацией внимания.
- Препараты этой группы не следует принимать на ночь из‑за мощного мочегонного эффекта.
Застійна серцева недостатність
У пацієнтів із застійною серцевою недостатністю середнього або важкого ступеня активація ренін-ангіотензинової системи спричинює вазоконстрикцію аферентних та еферентних артеріол нирок. Нейрогуморальна реакція включає виділення альдостерону наднирниками; підвищення тонусу симпатичної нервової системи, яке зумовлює підвищення реабсорбції натрію у проксимальних канальцях; секрецію антидіуретичного гормону, який призводить до підвищення реабсорбції води в збірних канальцях і внаслідок цього — до гіпонатріємії.
Завдання лікування хворих з застійною серцевою недостатністю — полегшення симптоматики, поліпшення якості життя, затримка прогресування захворювання та зниження смертності. |
Незважаючи на широке застосування, поліпшення виживання у хворих із застійною серцевою недостатністю не доведено, за винятком спіронолактону — згідно з дослідженням Pitt B. et al. (1999), цей препарат знижував хворобливість та смертність у хворих з серцевою недостатністю III та IV класу (за класифікацією NYHA). У всіх інших великих дослідженнях виживання пацієнтів з серцевою недостатністю (Packer M. et al., 1992) сечогінні застосовувалися в комбінації з іншими препаратами і забезпечували більше полегшення симптоматики. Перед тим, як викликати підвищення діурезу, через декілька хвилин після внутрішньовенного введення петлеві діуретики зменшують тиск заклинювання в легеневих капілярах та підвищують ємність венозного русла. Петлеві діуретики ефективні в режимі монотерапії при лікуванні серцевої недостатності середнього або важкого ступеня. У більшості хворих з серцевою недостатністю до певної міри наявна ниркова недостатність унаслідок первинного захворювання, преренальної азотемії або вікового зниження функції нирок. Враховуючи наявність конкуренції з ендогенними органічними іонами за місця зв’язування в канальцях нирок, у пацієнтів з серцевою недостатністю, як звичайно, доводиться призначати петлеві діуретики у вищих дозах.
Цироз печінки2
2Див. також статтю Асцит як ускладнення цирозу печінки.
– Медицина світу. – 1998. – Т. V. – Ч. 1. – С. 4-11 та
Асцит: новий погляд на класичну проблему.
– Медицина світу. – 2004. – Т. XVI. – Ч. 2. – С. 77–83. (Прим. перекл.)
Для лікування асциту з набряками, пов’язаними з цирозом, можна застосовувати більшість принципів призначення сечогінних та обмеження прийому натрію з їжею. Асцит — часте ускладнення цирозу печінки, при якому погіршується прогноз. Важкість перебігу асциту поділяють на три стадії: при першій стадії асцит діагностується тільки за допомогою УЗД; при другій — наявне помірне симетричне збільшення живота; при третій — значне збільшення живота. Для виявлення етіології можна взяти пробу асцитичної рідини. Фактично універсальна рекомендація в цій ситуації — обмеження вживання натрію та води.
При асциті ІІ або ІІІ ступеня для боротьби з гіперальдостеронізмом звичайно необхідно призначити спіронолактон у дозі 100–200 мг на день під час їди. За допомогою щоденного зважування можна проводити моніторинг результатів лікування. Втрата ваги не повинна перевищувати 0,5 кг на день у хворих без периферичних набряків та 1,0 кг при наявності набряків. Якщо немає реакції на добове застосування 100 мг спіронолактону, можна додати петлевий діуретик у низькій дозі. При надмірно агресивному лікуванні діуретиками можливе загострення гепаторенального синдрому. Побічні прояви від застосування спіронолактону включають гіперкаліємію, метаболічний ацидоз та гінекомастію, які звичайно минають після зниження дози або відміни препарату.
Лікуванням вибору у хворих з асцитом ІІІ ступеня є парацентез із призначенням сечогінних та обмеженням вживання натрію. Навіть якщо об’єм рідини перевищує 5 літрів, рекомендується евакуювати її за одну процедуру. Для профілактики ниркових ускладнень після парацентезу необхідно провести інфузійну терапію синтетичним плазмозамінником або альбуміном, особливо після евакуації більш як 5 л рідини. У пацієнтів з рефрактерним асцитом слід розглянути показання для проведення трансюгулярного внутрішньопечінкового портосистемного шунтування (ТВПШ). Під час рандомізованого дослідження M. Rossle et al. (2000) встановлено, що ТВПШ має переваги над парацентезом великого об’єму рідини щодо ліквідації асциту та продовження виживання (58 на противагу 32% у пацієнтів, які залишилися живими протягом 2 років). Багато хворих з асцитом та цирозом стають кандидатами на пересадку печінки.
Тиазидные диуретики в лечении артериальной гипертензии
В июне 2007 г. на Европейском конгрессе по гипертонии в Милане (Италия) были обнародованы новые европейские рекомендации по лечению артериальной гипертензии (АГ). Особое внимание кардиологов было направлено на место отдельных классов препаратов в схемах лечения АГ.
Было предложено 6 рациональных комбинаций антигипертензивных препаратов [1]:
- тиазидный диуретик + ингибитор ангиотензинпревращающего фермента (АПФ);
- тиазидный диуретик + блокатор рецепторов к ангиотензину;
- антагонист кальция + ингибитор АПФ;
- антагонист кальция + блокатор рецепторов к ангиотензину;
- антагонист кальция + тиазидный диуретик;
- бета-адреноблокатор + антагонист кальция дигидропиридинового ряда.
Исходя из вышеперечисленного, можно сделать вывод о том, что чаще всего в комбинациях фигурируют антагонисты кальция (4 раза) и тиазидные диуретики (3 раза).
Тиазидные диуретики давно применяются в качестве средств для лечения АГ. В Европейских рекомендациях 2007 г. целевые группы, которым предпочтительно назначение диуретиков, включают в себя пожилых пациентов с систолической АГ, а также с сердечной недостаточностью [1].
Однако применение средних и высоких доз тиазидных диуретиков в настоящее время считается нежелательным: так, гидрохлоротиазид в дозе 100 мг/сут увеличивает риск внезапной смерти, а в дозах 50–100 мг/сут не предупреждает развития ишемической болезни сердца (ИБС). В этой связи рекомендуемые дозы тиазидных диуретиков в настоящее время составляют 12,5–25 мг/сут, при назначении которых не всегда достигается адекватный диуретический и антигипертензивный эффект [2]. Кроме того, ограничение доз тиазидных диуретиков связано также с их негативным влиянием на углеводный, жировой и пуриновый обмен [3]. Поэтому в Европейских рекомендациях 2007 г. к числу абсолютных противопоказаний к применению тиазидных диуретиков отнесли подагру, а относительных — метаболический синдром и нарушение толерантности к глюкозе. Кроме того, сделан особый акцент на том, что высокие дозы диуретиков нельзя назначать беременным из-за возможности снижения объема циркулирующей крови (ОЦК) и ухудшения кровоснабжения плода. Однако при этом не следует забывать о том, что диуретики способны отсрочить развитие хронической сердечной недостаточности у пациентов с АГ (Davis B. R., 2006).
Таким образом очевидно, что сферы применения тиазидных диуретиков при лечении АГ довольно ограничены. В этой связи особый интерес представляет собой тиазидоподобный диуретик индапамид.
Индапамид обладает двойным действием, за счет чего имеет кратковременный и долгосрочный антигипертензивный эффект. Краткосрочное действие связано с влиянием препарата на проксимальный отдел дистальных канальцев нефрона и представляет собой натрийуретический эффект, характерный для представителей класса диуретиков в целом. Что касается долгосрочного антигипертензивного эффекта, то он уникален именно для индапамида и возникает благодаря прямому вазодилятирующему действию на гладкомышечные клетки сосудистой стенки [4].
Антигипертензивное действие индапамида-ретард 1,5 мг сравнивалось с амлодипином (5 мг/сут) и гидрохлоротиазидом (25 мг/сут) при участии в исследовании 605 пациентов с АГ, получавших лечение вышеперечисленными препаратами в течение 3 месяцев. Число пациентов, ответивших на монотерапию, было несколько выше в группе индапамида-ретард (75,3%), по сравнению с группой амлодипина (66,9%) и гидрохлоротиазида (67,3%). В подгруппе пациентов с изолированной систолической АГ наблюдалась аналогичная тенденция: число ответивших в группе индапамида-ретард составило 84,2%, в то время как в группе амлодипина — 80%, гидрохлоротиазида — 71,4% [5].
В многоцентровом исследовании LIVE (Left ventricle hypertrophy: Indapamide Versus Enalapril) проводилось изучение влияние терапии индапамидом и эналаприлом на регрессию массы миокарда левого желудочка (ММЛЖ). 505 пациентам (255 — группа индапамида; 250 — группа эналаприла) с мягкой и умеренной АГ в течение 1 года назначался индапамид-ретард 1,5 мг/сут или эналаприл в дозе 20 мг 1 раз в сутки. Терапия индапамидом приводила к достоверному снижению ММЛЖ (p < 0,001), в группе эналаприла подобных результатов получено не было. Индапамид также в большей степени снижал выраженность гипертрофии левого желудочка (ГЛЖ), чем эналаприл (p < 0,049) [6, 7].
Тиазидные диуретики очень давно назначались в комбинации с ингибиторами АПФ: многие фармацевтические компании даже разработали фиксированные комбинации данных составляющих. В большом числе исследований также хорошо себя показала комбинация индапамида с периндоприлом. Однако работ по эффективности комбинаций индапамида с другими классами препарата не так много.
В этой связи нам показалась интересной работа Hashimoto J. и соавт. [8], которые добавляли индапамид в дозе 1 мг 76 пациентам, получавшим ингибиторы АПФ, блокаторы рецепторов к ангиотензину и антагонисты кальция в качестве монотерапии, но достичь целевых цифр артериального давления (АД) у которых на этом лечении не удалось. В течение 4-недельной комбинированной терапии в данных трех группах оценивалась динамика уровня суточного мониторирования АД, измерения АД в домашних условиях и случайного измерения АД. Во всех группах было отмечено достоверное снижение систолического АД (САД) и диастолического АД (ДАД). Снижение САД в вечернее время и пульсового АД было достоверно более выражено в группе «блокатор ангиотензиновых рецепторов + индапамид», по сравнению с группой «антагонист кальция + индапамид». Таким образом, добавление к антигипертензивной терапии индапамида приводило к дополнительному гипотензивному эффекту, продолжительность которого составляла 24 часа.
До недавнего времени считалось, что лишь три класса препаратов обладают нефропротективным действием: ингибиторы АПФ, блокаторы рецепторов к ангиотензину и антагонисты кальция (преимущественно фенилалкиламины). Нефропротективный эффект тиазидоподобных диуретиков был продемонстрирован в ходе исследования NESTOR [9]. У 570 больных с АГ и сахарным диабетом 2 типа проводилось сравнительное изучение влияния индапамида-ретард 1,5 мг и эналаприла 10 мг на выраженность микроальбуминурии (МАУ) на фоне годичной терапии. Было отмечено уменьшение МАУ на 37% в группе эналаприла и на 45% в группе индапамида-ретард. Таким образом, нефропротективный эффект индапамида ретард 1,5 мг оказался сопоставимым и даже несколько превышающим таковой у эналаприла.
В другом исследовании изучалось влияние индапамида-ретард в дозе 1,5 мг, назначенного на 3 месяца, в сравнении с плацебо на показатели суточного мониторирования АД, углеводный и липидный обмен у пациентов с сахарным диабетом 2 типа [10]. Было выявлено достоверное снижение среднесуточных показателей АД в группе индапамида, по сравнению с плацебо. Кроме того, не было показано влияния проводимой терапии на электролиты, креатинин, липидный спектр, мочевую кислоту, печеночные трансаминазы, уровень инсулина, гликозилированного гемоглобина и результаты глюкозотолерантного теста.
Учитывая, что диуретики уже давно зарекомендовали себя как препарат выбора для лечения пожилых пациентов, особенно имеющих изолированную систолическую АГ (ИСАГ). В многоцентровое исследование X-CELLENT было включено 1758 пациентов с систолодиастолической АГ или ИСАГ, которые затем были рандомизированы в 4 группы, в которых назначалась монотерапия индапамидом-ретард 1,5 мг/сут, амлодипином 5 мг/сут, кандесартаном цилексетилом 8 мг/сут и плацебо в течение 3 месяцев. По сравнению с группой плацебо, во всех группах было отмечено достоверное снижение АД. Преимуществом индапамида у пациентов с ИСАГ оказалось практически отсутствие влияния препарата на нормальные показатели ДАД при снижении САД; остальные препараты снижали как САД, так и ДАД. Кроме того, в данной группе пациентов индапамид-ретард снижал среднесуточное САД в большей степени, чем амлодипин. Переносимость всех трех видов терапии была хорошей [11].
Как мы указывали выше, доза гидрохлоротиазида 12,5–25 мг/сутки считается метаболически нейтральной. В работе А. А. Семенкина и соавт. проводилось сравнительное изучение антигипертензивной эффективности и метаболического воздействия индапамида-ретард (1,5 мг/сутки) и гидрохлоротиазида (25 мг/сут). Несмотря на сопоставимое антигипертензивное действие, в группе пациентов, получавших гидрохлоротиазид, через 3 месяца было отмечено достоверное увеличение уровня триглицеридов на 15,3% (p < 0,05) и глюкозы на 12,2% (p < 0,05), а также достоверное ухудшение эндотелий-зависимой вазодилятации на 17% (p < 0,05) [12].
Интересным представляется потенциальное расширение показаний для использования индапамида, в частности, его использование при лечении хронической сердечной недостаточности, сопровождающейся отечным синдромом. В одном недавно проведенном исследовании у больных с упорными периферическими отеками индапамид в дозе 2 мг добавлялся к фуросемиду (40–120 мг/сут), что приводило к достоверно большему диуретическому эффекту при отсутствии значимого влияния на уровень калия и креатинина плазмы [13].
Таким образом, оригинальный индапамид более чем убедительно доказал в ходе исследований свою антигипертензивную эффективность и органопротективные свойства. В попытке совместить невысокую стоимость с высоким качеством препарата для обеспечения большей части пациентов АГ препаратами адекватного действия особый интерес представляют современные дженерики индапамида и, в частности, препарат «Равел СР», выпускаемый в дозе 1,5 мг. Препарат успешно зарекомендовал себя после проведенного в Словении в 2005–2006 гг. исследования [4], в ходе которого изучалась его антигипертензивная эффективность и переносимость. Препарат был назначен 1419 пациентам (58,1% — женщины, средний возраст 61,9 ± 11,6 лет), у которых было отмечено снижение уровня САД на 14,1%, а ДАД на 11,1%. Развитие нежелательных явлений на фоне приема Равела СР было отмечено лишь у 2,5% пациентов (наиболее частыми были сухость в полости рта и головокружение — по 0,42%, а 1 пациенту потребовалась коррекция уровня калия из-за развития гипокалиемии без отмены препарата).
Изучение эффективности и переносимости Равела СР проводилось также и в отечественных исследованиях. С. В. Недогода и соавт. [14] сравнивали терапию Равелом СР 1,5 мг/сут и гидрохлоротиазидом 25 мг у пациентов с АГ и ожирением. Пациенты 1-й группы в течение 6 месяцев получали Равел СР, пациентам 2-й группы в течение первых 3 месяцев назначался гидрохлоротиазид в дозе 25 мг/сут, а затем их переводили на Равел СР (3 месяца). Результаты исследования показали, что на фоне приема Равела СР достижение цифр целевого АД происходило на 15% чаще, чем на гидрохлоротиазиде. Было отмечено, что только на терапии Равелом СР происходило улучшение эластичности сосудов (при оценке скорости пульсовой волны) и уменьшение гипертрофии миокарда, а также улучшение показателей углеводного и липидного обмена.
Интерес представляют также результаты программы БОЛЕРО (Базовое лечение и антигипертензивный эффект: препарат «Равел СР» у пациентов с артериальной гипертонией), направленной на изучение антигипертензивной эффективности медленно высвобождающейся формы препарата и его влияния на качество жизни. Было показано, что применение индапамида-ретард в течение 2 месяцев приводило к снижению САД и ДАД у мужчин на 18%, а у женщин на 15%. На фоне лечения происходило снижение сердечно-сосудистого риска в одинаковой степени у мужчин и женщин, а улучшение качества жизни было более заметным в группе женщин [15].
Появление каждого нового высококачественного и безопасного дженерика — это шаг к тому, чтобы российские пациенты демонстрировали более высокую приверженность лечению АГ. В настоящее время пациенты с АГ в РФ, имеющие целевой уровень АД, не превышают 5–15% от популяции, в то время как в Западной Европе таких пациентов более 30%. Препарат «Равел СР» (индапамид-ретард) 1,5 мг как антигипертензивный препарат, обладающий мягким диуретическим эффектом, имеет все возможности, чтобы расширить границы применения диуретиков, очерченные современными рекомендациями по лечению АГ.
По вопросам литературы обращайтесь в редакцию.
Д. А. Напалков, кандидат медицинских наук ММА им. И. М. Сеченова, Москва
Нефротичний синдром3
3Див також статтю Набряки нижніх кінцівок: діагностична орієнтація
. – Медицина світу. – 1999. – Т. VI. – Ч. 1. – С. 27-31. (Прим. перекл.)
Нефротичний синдром рідше викликає набряки і характеризується вираженою протеїнурією, гіпоальбумінемією, гіперліпідемією та набряками. Продовжується дискусія щодо того, чи набряки виникають унаслідок зниження онкотичного тиску, чи від наявності надмірної кількості натрію, що призводить до затримки води; нині більшість дослідників схиляється до другої гіпотези. Лікування включає обмеження вживання натрію з їжею та комбінацію петлевих діуретиків, антагоністів альдостерону та препаратів для лікування первинного захворювання.
Хронічна венозна недостатність4
4Див також статтю Варикозні вени: не тільки косметична проблема
. – Медицина світу. – 2000. – Т. VIII. – Ч. 3. – С. 130—136; Ч. 4. – С. 201—203. (Прим. перекл.)
Венозна недостатність — часта етіологія набряків нижніх кінцівок. При появі набряку, особливо одностороннього, необхідно виключити тромбоз глибоких вен нижньої кінцівки. До ускладнень довготривалого набряку ноги належать застійний дерматит, виразкування та целюліт. Ефективність діуретиків обмежена. Надання нозі підвищеного положення вище рівня серця та застосування щільних панчіх може зменшити венозну недостатність та набряк.
Набряки, зумовлені дією ліків
Набряки стоп зумовлює багато медикаментів, особливо вазодилятатори, естрогени, НСПЗП та блокатори кальцієвих каналів. Серед блокаторів кальцієвих каналів набряки найчастіше викликають похідні дигідропіридину5. Вираженість набряку залежить від дози і з часом зростає. Оскільки медикаментозні набряки виникають внаслідок капілярної гіпертензії, для їх лікування ефективні інгібітори АПФ та блокатори ангіотензинових рецепторів, а не сечогінні.
5До цієї групи належать амлодипін, фелодипін, ісрадипін, ніфедипін, німодипін, нітрендипін, лацидипін, ріодипін. (Прим. перекл.)
Бета-адреноблокаторы
Бета-адреноблокаторы (БАБ) на протяжении многих лет применяются в качестве первой линии терапии артериальной гипертензии.
Механизм действия
В основе действия препаратов этой группы лежит блокада β1- и β2‑адренорецепторов, расположенных в различных органах. В зависимости от селективности блокады, которая определяется по отношению β1/β2, БАБ делятся на селективные и неселективные. Последние (пропранолол, пиндолол, соталол) сегодня практически не применяются в кардиологии [8].
Современные кардиоселективные БАБ (метопролол, бисопролол, бетаксолол и другие) проявляют комплекс сердечно-сосудистых эффектов [8]. Они снижают частоту сердечных сокращений и уменьшают активность ренин-ангиотензин-альдостероновой системы за счет блокады синтеза ренина в почках. Таким образом они проявляют антиангинальный и антиаритмический эффекты, а также снижают АД.
Показания и свойства
Препараты этой группы показаны для длительного лечения АГ с сопутствующей стенокардией, а также для лечения после перенесенного инфаркта миокарда и при некоторых видах аритмии.
Однако БАБ имеют и существенный недостаток: они не влияют на частоту развития сердечно-сосудистых событий и жесткость артерий, а также не оказывают благоприятного влияния на состояние органов-мишеней [8].
Отдельные представители
- Бисопролол — один из наиболее популярных селективных β1‑адреноблокаторов. Обеспечивает контролируемое снижение давления, зависящее от дозы. Благодаря высокой селективности может применяться у особых групп пациентов — больных диабетом и пациентов с нарушением липидного обмена [9].
- Карведилол — препарат, выделяющийся из ряда селективных БАБ. Проявляет дополнительный вазодилатирующий эффект. Он блокирует β1- и β2‑рецепторы, а также (незначительно) α1‑рецепторы периферических артерий, способствуя снижению периферического сосудистого сопротивления и более выраженному снижению АД по сравнению с другими представителями этой группы.
- Небиволол — БАБ нового поколения, обладающий высокой селективностью в отношении β1‑адренорецепторов. Оказывает непосредственное сосудосуживающее действие за счет стимуляции выработки эндотелием сосудов оксида азота. Переносится значительно лучше, чем другие БАБ [9].
Переносимость
БАБ могут проявлять ряд побочных эффектов, негативно влияющих на качество жизни. Среди них:
- нарушение сердечного ритма;
- неврологические реакции — депрессия, бессонница;
- диспепсические явления — тошнота, рвота, запор или диарея.
У 1 пациента мужского пола из 199‑ти на фоне приема препаратов этой группы развивается эректильная дисфункция [8].
О чем предупредить клиента?
Посетители, изучив инструкцию по применению и ознакомившись с внушительным перечнем побочных эффектов, могут засомневаться, стоит ли принимать такой «вредный» препарат. Задача первостольника — объяснить, что при наличии показаний (артериальной гипертензии на фоне ишемической болезни сердца, нарушений ритма сердца, сердечной недостаточности, мигрени, беременности, глаукомы) польза от приема БАБ значительно выше, чем потенциальный риск побочных эффектов. К тому же, по данным исследований, лишь 3–5 % больных не могут принимать препараты этой группы из‑за развивающихся неблагоприятных реакций [8].
Лімфедема6
6Див. також статтю Лімфедема
. – Медицина світу. – 2004. – Т. XVII. – Ч. 2. – С. 77–86. (Прим. перекл.)
Терміном “лімфедема” називають сукупність станів, які характеризуються надмірним реґіонарним накопиченням багатої на білок рідини в інтерстиції. Розрізняють первинну і вторинну лімфедему (у світі остання трапляється набагато частіше і викликається філяріозом). У США найчастіше трапляється лімфедема після видалення аксилярних лімфовузлів (до 80% пацієнтів після цієї операції).
На наявність лімфедеми вказує симптом Стеммера — неможливість взяти шкіру у складку на дорзальній поверхні пальців ноги |
Віддиференціювати лімфедему від інших форм набряків буває важко, особливо на ранніх стадіях. На наявність лімфедеми вказує симптом Стеммера, набряк дорзальної поверхні стопи з “квадратним” виглядом пальців. Для підтвердження діагнозу можна провести КТ або ЯМР (чутливість ЯМР вища, ніж КТ). Лімфедему можна відрізнити від інших видів набряку за наявністю характерної “сотової” структури підшкірної жирової клітковини.
Показанням для лікування є збільшення окружності руки на 2 см порівняно з передопераційним періодом. Корисно тривалий час уникати носіння стискаючого одягу, ретельно доглядати за шкірою, уникати вимірювання артеріального тиску та стискання ураженої кінцівки. Ефективним може бути виконання фізичних вправ, догляд за шкірою, носіння компресійних панчіх або рукавиць, комплексна протинабрякова фізіотерапія, двофазний процес спеціального мануального масажу та дренування лімфовузлів. На початкових стадіях хвороби діуретики можуть бути ефективними; проте потім вони допомагають рідко. Хірургічне лікування малоефективне, хоча може забезпечити зменшення об’єму кінцівки у хворих з важкою формою слонової хвороби.
Підготував Богдан Борис