Несмотря на большой арсенал антигипертензивных средств, 20–30 % больных не удается контролировать артериальное давление (АД) даже на фоне приема комбинации из 3–4 лекарственных препаратов основных групп [1]. При существующих различиях в подходах к комбинированной терапии артериальной гипертензии (АГ) в разных клинических рекомендациях как наиболее рациональные часто рассматриваются сочетания ингибиторов ренин-ангиотензиновой системы с блокаторами кальциевых каналов или тиазидными диуретиками [2–4]. В патогенезе АГ важную роль играет активация симпатической нервной системы (СНС). Среди групп, позволяющих уменьшать проявления активации СНС, к препаратам первого ряда относятся β-адреноблокаторы. Однако для значительной части больных назначение препаратов этой группы невозможно из-за наличия противопоказаний и неблагоприятных метаболических эффектов. К другой возможности подавить активацию центральных симпатических ядер относится возможность использовать препараты центрального действия. В настоящее время достаточно широко используются препараты 2-го поколения, одним из которых является моксонидин (Физиотенз, Эбботт).
Особенности механизма действия и фармакокинетики моксонидина
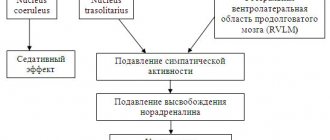
Препараты центрального действия 2-го поколения являются селективными агонистами имидазолиновых рецепторов. Эти рецепторы участвуют в центральной регуляции тонуса СНС. Имидазолиновые рецепторы 1-го типа (I1) локализуются в центральной нервной системе (ЦНС; в ядрах ретикулярной формации) и участвуют в механизме отрицательной обратной связи. На периферии (например, в почках, поджелудочной железе, жировой ткани, сердце) обнаружены рецепторы имидазолина 2-го типа. Активация I1-рецепторов приводит к снижению АД и уменьшению частоты сердечных сокращений (ЧСС) [5]. Для моксонидина характерно выраженное антигипертензивное действие, сопровождающееся незначительным седативным эффектом. Умеренный натрийуретический эффект, вероятно, связан со стимуляцией I1-рецепторов почек и может вносить свой вклад в системный гипотензивный эффект. Центральные I1-рецепторы гипоталамической области вовлечены и в регуляцию уровня гликемии крови.
Физиологическая роль I1- и α-адренергических рецепторов ЦНС до конца не уточнена. В экспериментах на животных, находящихся в условиях гипоксии, было показано, что активация этих рецепторов связана с функционированием системы антиоксидантной защиты. Применение агонистов этих рецепторов – клонидина и моксонидина, оказывается церебропротективным и помогает тормозить прогрессирование сосудистой деменции [6]. Аналогично в эксперименте на животных было показано, что применение моксонидина позволяет уменьшать риск повреждения почек при ишемии [7].
Инфузия моксонидина даже в маленькой дозе у спонтанно гипертензивных крыс приводила к улучшению барорецепторной регуляции АД. Инфузия специфического блокатора этих рецепторов йохимбина угнетала барорецепторную чувствительность [8]. В эксперименте на крысах было показано, что при внутривенном введении моксонидина происходит увеличение диуреза и натрийуреза. Совместное использование с а-адреноблокатором празозином уменьшало диуретический эффект моксонидина, что позволило предположить, что активация центральных I1-рецепторов ведет в активации α1-адренорецепторов, которые и опосредуют увеличение диуреза [9].
В ткани предсердий I1-рецепторы опосредуют увеличение синтеза натрийуретических пептидов. Это было показано в эксперименте на крысах с изолированным кровообращением предсердий. Моксонидин повышал уровень предсердного натрийуретического пептида, а центральный а-агонист клонидин – нет. Это может быть одним из дополнительных компонентов антигипертензивного действия моксонидина [10].
Исследования фармакокинетики моксонидина показали, что препарат достаточно быстро и полно всасывается в желудочно-кишечном тракте (ЖКТ). Максимальная концентрация моксонидина в крови создается через 0,5–2,0 часа после приема. Основной путь выведения – с мочой и лишь в незначительном количестве – через ЖКТ. Моксонидин в организме подвергается как окислению, так и реакции метаболизма II фазы (коньюгации с цистеином) [11]. Основным показанием к назначению моксонидина является АГ. Для лечения АГ препарат назначают в дозе 0,2–0,6 мг/сут. При однократном применении моксонидин позволяет контролировать АД на протяжении всех суток, что подтверждается данными суточного мониторирования. Соотношение остаточного и пикового эффектов при лечении этим препаратом составляет 0,7 [12]. В исследовании на животных было показано, что прекращение введения моксонидина не приводило к развитию феномена «рикошета» и повышению АД в отличие от препаратов центрального действия 1-го поколения (клонидина и др.), для которых была свойственна «рикошетная» гипертензия [13].
Симпатолитические эффекты моксонидина приводят к изменениям в центральной гемодинамике. Это было продемонстрировано в исследовании группы из 22 больных АГ, гипертрофией миокарда левого желудочка, положительным тестом с физической нагрузкой и отсутствием значимых стенозов коронарных артерий. Через 2 часа после приема 0,4 мг моксонидина АД снизилось на 28/10 мм рт. ст., ЧСС уменьшилась на 5 уд/мин. Снизилось давление в малом круге кровообращения – среднее давление в легочной артерии уменьшилось на 17 %, давление заклинивания легочных артерий – на 26 %. Уменьшились давление в левом желудочке, его работа и потребность в кислороде. Общий коронарный резерв вырос на 12 %. Концентрация норадреналина в крови уменьшилась на 30 %, в эндотелии – на 20 % [14].
Антигипертензивная эффективность моксонидина: реальная практика и данные клинических исследований
В реальной клинической практике моксонидин применяется чаще всего как компонент комбинированной терапии. В одном из когортных исследований проанализировали частоту назначения 990 больным АГ и основные показания к лечению моксонидином. Препарат использовали 4,5 % больных. Две трети больных получали моксонидин в связи с резистентной к обычной антигипертензивной терапии АГ. Еще 33 % больных отметили непереносимость антигипертензивных препаратов первого ряда. Они получали препарат в монотерапии [15].
В группе из 748 больных в открытом исследовании оценили особенности применения моксонидина при лечении АГ в сочетании с метаболическим синдромом (МС): 81,1 % больных получали его в составе комбинированной терапии. Наиболее часто моксонидин назначали в дозе 0,4 мг/сут, 98 % больных закончили 6 месяцев лечения. Серьезных побочных эффектов при применении препарата не наблюдалось, АД снижалось достоверно, при этом неблагоприятных метаболических эффектов не зарегистрировано [16].
В открытом исследовании было показано, что у пациентов с АГ 1-й и 2- степеней 62 % оказалась эффективной доза моксонидина 0,2 мг/сут, еще 36 % пациентов нормализация АД была достигнута при приеме препарата в дозе 0,4 мг/сут. В этом исследовании было показано, что максимальное снижение АД достигается на 3-й неделе от начала терапии, а затем эффект сохраняется на прежнем уровне на протяжении года наблюдения. Очевидным преимуществом препарата, таким образом, оказалось то, что толерантность к препарату не развивается даже при длительном применении [17].
Моксонидин в лечении АГ изучался более чем в 70 исследованиях. Всего в исследованиях II и III фаз участвовали более 1500 больных. При этом переносимость препарата была хорошей. Только 9 % больных отмечали сухость во рту, 5–8 % – сонливость, 6 % – головные боли. Отказывались от приема препаратов из-за побочных эффектов не более 4 % больных. Прием моксонидина не ухудшал течения сахарного диабета и хронической обструктивной болезни легких. В постмаркетинговых исследованиях отмечено два случая аллергических реакций. Таким образом, моксонидин обладал хорошим профилем безопасности [18].
Был проведен ряд исследований, касающихся сравнения эффективности моксонидина с антигипертензивными препаратами других групп. Показано, что моксонидин обладает сравнимой антигипертензивной активностью с препаратами первого ряда в лечении АГ, ингибиторами ангиотензинпревращающего фермента, β-адреноблокаторами и диуретиками [19–21].
В настоящее время моксонидин является препаратом, который используется прежде всего в комбинированной терапии, однако этот препарат имеет ряд органопротективных свойств, а также благоприятных метаболических эффектов, которые позволяют сформулировать дополнительные показания к его использованию.
Органопротективные свойства моксонидина
Влияние на состояние эндотелия рассматривается как одна из важнейших суррогатных конечных точек в оценке эффективности антигипертензивной терапии. Влияние моксонидина на функцию эндотелия оценивалось в нескольких небольших исследованиях. В группе из 26 пациентов с ожирением и АГ было показано, что терапия моксонидином в сочетании с гипокалорийной диетой в течение 3 месяцев приводит к улучшению чувствительности тканей к инсулину и улучшает состояние эндотелия сосудов по сравнению с группой больных, получавших только гипокалорийную диету. При терапии моксонидином отмечен достоверный прирост степени эндотелийзависимой вазодилатации в тесте с реактивной гиперемией по сравнению с группой контроля [22]. В небольшой группе больных АГ с признаками инсулинорезистентности (ИР; индекс HOMA – Homeostasis Model Assessment > 2,77) сравнили эффективность моксонидина и амлодипина. Препараты оказали сравнимое гипотензивное действие. В группе моксонидина отмечено более выраженное снижение уровня триглицеридов. Динамика уровней мочевой кислоты, глюкозы, инсулина, липопротеидов высокой и низкой плотности, биомаркера YKL (tyrosine – Y, lysine – K, leucin – L)-40, являющегося маркером дисфункции эндотелия и формирования атеросклеротического поражения стенки сосуда, достоверно не различалась у больных, получающих препараты разных групп [23].
В группе из 56 больных эссенциальной АГ и микроальбуминурией была изучена эффективность применения моксонидина в монотерапии. Больные получали препарат в дозе 0,3–0,4 мг/сут в течение 6 месяцев. На фоне терапии моксонидином достоверно снижалось АД, уменьшалась выраженность альбуминурии. Кроме того, отмечено уменьшение концентрации тромбомодулина плазмы крови и снижение уровня ингибитора активатора плазминогена. Динамику уровней этих маркеров авторы исследования связывают с нормализацией состояния эндотелия на фоне лечения [24].
В проспективном рандомизированном исследовании сравнили клиническую и фармакоэкономическую эффективность лечения пациентов с хронической болезнью почек моксонидином и нитрендипином. В исследование включены больные АГ и нетерминальной хронической почечной недостаточностью. За 3 года наблюдения в группе больных, получавших нитрендипин, терминальная хроническая почечная недостаточность развилась у 38 % больных, в группе моксонидина – у 7 %. Общая стоимость лечения моксонидином в этой группе больных оказалась в 4 раза ниже по сравнению с лечением нитрендипином [25].
Моксонидин может способствовать регрессу гипертрофии левого желудочка (ГЛЖ). Это было показано при лечении моксонидином больных АГ в течение 6 месяцев, причем фракция выброса существенно не изменилась [19]. Уменьшение ГЛЖ было подтверждено и в экспериментальных исследованиях. Механизм воздействия моксонидина на сердечную мышцу может быть связан с активацией имидазолиновых рецепторов, локализующихся в сердце, и с воздействием препарата на регуляцию процессов апоптоза и стабилизации ДНК [26].
Применение моксонидина может позволить уменьшить частоту и продолжительность пароксизмов мерцательной аритмии. Это было показано в исследовании перекрестного дизайна в группе из 56 больных пароксизмальной мерцательной аритмией. Больные получали лечение моксонидином или плацебо в течение 6 недель. Контроль эффективности терапии проведен с использованием 48-часового мониторирования электрокардиограммы. На фоне лечения моксонидином отмечено достоверное снижение диастолического АД и уменьшение средней продолжительности мерцательной аритмии за сутки с 28 до 16 минут. Антиаритмический эффект моксонидина связан с его симпатолитической активностью [27].
Применение моксонидина особыми группами больных
В качестве дополнительного показания к назначению моксонидина чаще всего рассматривается МС. Применение препарата способствует активации липолиза жировой ткани и снижению массы тела. Это было показано в большом открытом исследовании CAMUS, где 4005 больных АГ в сочетании с ожирением или МС получали моксонидин в виде монотерапии и в составе комбинированной терапии. За 8 недель исследования на фоне терапии моксонидином было отмечено снижение массы тела пациентов в среднем на 1,4 кг. У пациентов с ожирением на момент включения в исследование снижение массы тела было более выраженным [28]. ИР и гиперинсулинемия – это ведущие компоненты патогенеза МС. Способность моксонидина влиять на чувствительность тканей к инсулину изучалась в нескольких исследованиях. В исследовании с участием 99 больных АГ и сахарным диабетом сравнили эффективность моксонидина в монотерапии и комбинации моксонидина и ирбесартана. Больные, включенные в лечение, не получали антигипертензивной и сахароснижающей терапии. Сначала в течение 3 месяцев все больные получали моксонидин в дозе 0,2 мг, затем части больных эту дозу удвоили, а второй половине больных к терапии добавили ирбесартан в дозе 150 мг/сут. Проведен контроль АД, углеводного и липидного обменов. Оба режима лечения вызвали достоверное снижение АД, однако только при применении моксонилина в дозе 0,4 мг/сут произошло снижение уровня глюкозы крови и гликированного гемоглобина. Улучшен индекс инсулинчувствительности. Отмечено достоверное увеличение уровня холестерина липопротеидов высокой плотности [29].
В группе из 77 пациентов с ожирением и АГ изучили влияние терапии моксонидином на индекс чувствительности к инсулину. Больные получали терапию моксонидином или плацебо в течение 8–9 недель. Оказалось, что в целом моксонидин вызывал достоверное увеличение индекса чувствительности тканей к инсулину, особенно выраженное у больных, имевших признаки ИР [30].
Показано, что моксонидин способствует снижению уровня глюкозы крови больных МС и улучшению чувствительности тканей к инсулину в отличие от препаратов центрального действия 1-го поколения (альфа-метилдопы и клонидина) [31].
При сравнении эффективности лечения моксондином в дозе 0,2–0,6 мг/сут и метопрололом в дозе 50–150 мг/сут оказалось, что снижение систолического и диастолического АД на фоне лечения этими препаратами одинаково. Однако в группе моксонидина к концу терапии оказался ниже уровень глюкозы крови натощак и отмечено нарастание индекса инсулинчувствительности. В группе метопролола индекс инсулинчувствительности снизился, а уровень глюкозы натощак оказался выше, чем при лечении моксонидином [32].
Хороший профиль переносимости, отсутствие значимых фармакокинетических взаимодействий создают условия для применения моксонидина в лечении АГ у пожилых больных.
В группе из 14 больных старческого возраста с АГ, резистентной к лечению тремя препаратами, изучена эффективность моксонидина в комбинированной терапии. Контроль АД осуществлен по данным клинического измерения и суточного мониторирования АД. Моксонидин назначали в дозе 0,2–0,4 г/сут. На фоне добавления этого препарата к лечению, по данным клинического контроля АД, зарегистрирована достоверная динамика и систолического (снижение со 195,9 ± 19,6 до 174 ± 17,8 мм рт. ст.), и диастолического АД (снижение со 103,6 ± 9,5 до 99,0 ± 12,4 мм рт. ст.). По данным суточного мониторирования, систолическое АД в дневное время снизилось на 15,4 мм рт. ст., диастолическое – на 7,4. В ночное время достоверно снижалось только систолическое АД (на 9,3 мм рт. ст.). Таким образом, 11 из 14 больных отметили очень хорошую переносимость моксонидина [33].
Седативное и симпатолитическое действия моксонидина позволяют рекомендовать препарат для лечения АГ у женщин в пери- и постменопаузах. Моксонидин может помочь купированию климактерической симптоматики у женщин. Это было показано в рандомизированном исследовании с участием 112 женщин в постменопаузе, не получавших заместительной гормональной терапии, страдавших АГ и ожирением. Больные получали атенолол или моксонидин. Оба препарата достоверно снижали АД и способствовали купированию сердцебиения, приливов, одышки, бессонницы. Различий между группами по влиянию на клиническую симптоматику не было [34]. Только моксонидин способствовал повышению чувствительности тканей к инсулину. Эта закономерность прослеживалась у женщин с исходной ИР и была более выраженной среди женщин, достигших хорошего контроля АД на фоне терапии моксонидином [35]. Терапия моксонидином способствовала уменьшению площади под кривой теста глюкозотолерантности и достоверному снижению уровня инсулина плазмы крови [36].
При сравнении влияния тех же препаратов на уровень воспалительных цитокинов у женщин в постменопаузе оказалось, что и атенолол, и моксонидин способствуют снижению активности фактора некроза опухоли. Однако при лечении атенололом происходило еще и снижение активности адипонектина. На его уровень моксонидин существенно не влиял. Таким образом, использование моксонидина оказалось предпочтительным [37].
В другом исследовании в группе из 55 женщин с АГ без сахарного диабета было показано, что терапия моксонидином позволяет достоверно снижать АД и уменьшать уровни глюкозы, холестерина, триглицеридов, альбуминурии и индекса ИР. При этом уровень адипонектина вырос. Была показана значимая отрицательная корреляция между динамикой индекса ИР и адипонектина [38].
Таким образом, моксонидин – это препарат с доказанной антигипертензивной эффективностью, удобным режимом приема и хорошей переносимостью. Препарат может быть рекомендован как один из возможных компонентов комбинированной терапии больных резистентной АГ или при наличии противопоказаний к назначению препаратов основных групп. Данные о влиянии моксонидина на чувствительность тканей к инсулину и отсутствие у препарата неблагоприятных метаболических эффектов позволяют рассматривать сахарный диабет, ожирение и МС как дополнительные показания к назначению этого препарата. Моксонидин может использоваться и для лечения АГ у пожилых больных, а также у женщин в постменопаузе. Препарат обладает и органопротективными свойствами – уменьшает выраженность микроальбуминурии, улучшает функцию эндотелия, способствует уменьшению ГЛЖ и профилактике пароксизмов мерцательной аритмии.
Препарат центрального действия моксонидин в лечении артериальной гипертензии
По данным эпидемиологических исследований, распространенность артериальной гипертензии (АГ) среди взрослого населения в развитых странах мира колеблется от 20% до 40% и увеличивается с возрастом [3]. Повышенное АД обнаруживается более чем у 50% мужчин и женщин старше 60 лет [4]. Актуальность проблемы поддерживается возрастающими процессами урбанизации общества, создающими предпосылки для возникновения факторов риска, таких как стресс, гиподинамия, ожирение, вредные привычки и нарушенная экология. Повышенное АД является одним из главных факторов риска развития мозгового инсульта, ишемической болезни сердца (ИБС) и других сердечно-сосудистых заболеваний атеросклеротического происхождения, с которыми связано более 50% всех случаев смерти [5]. Согласно современным национальным рекомендациям [6], рекомендациям Европейского общества по артериальной гипертонии и Европейского общества кардиологов [7], тактика лечения эссенциальной АГ зависит от уровня АД и степени риска кардиоваскулярных осложнений. Основной целью лечения является максимальное снижение риска развития сердечно-сосудистых осложнений и смерти от них. Основными задачами – нормализация уровня АД с целью предупреждения осложнений при отсутствии или минимальном уровне нежелательных лекарственных реакций, коррекция всех модифицируемых факторов риска (курение, дислипидемия, гипергликемия, ожирение), предупреждение, замедление темпа прогрессирования и/или уменьшение поражения органов-мишеней, а также лечение ассоциированных и сопутствующих заболеваний – ИБС, сахарного диабета (СД) и т. д. [6, 7]. При лечении больных АГ величина АД должна быть менее 140/90 мм рт. ст., что является ее целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском сердечно-сосудистых осложнений необходимо снизить АД до 140/90 мм рт. ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости, рекомендуется снижение АД до 130/80 мм рт. ст. и менее. У больных ИБС уровень АД необходимо снижать до целевого значения 130/85 мм рт. ст. У больных с СД и/или заболеванием почек целевой уровень АД должен составлять менее 130/85 мм рт. ст. [6]. Единых рекомендаций относительно того, с каких именно средств следует начинать лечение больного, нет. Выбор лекарственного средства зависит от многих факторов, в т. ч. от возраста, пола и наличия сопутствующих заболеваний. В настоящее время для лечения АГ рекомендованы 5 основных классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов AT1 (БРА), антагонисты кальция (АК), β-адреноблокаторы (БАБ), диуретики. В качестве дополнительных классов для комбинированной гипотензивной терапии могут использоваться α-адреноблокаторы, агонисты имидазолиновых I1-рецепторов и прямые ингибиторы ренина [6, 7].
Агонисты имидазолиновых рецепторов (моксонидин, рилменидин) являются современными лекарственными средствами с центральным механизмом действия – снижают активность сосудодвигательного центра продолговатого мозга. Также к гипотензивным средствам центрального действия относят клонидин, гуанфацин, метилдопу [1, 2]. Моксонидин (Моксарел, ЗАО «Вертекс», Россия) – высокоселективный агонист имидазолиновых I1-рецепторов, расположенных в ростральном вентролатеральном отделе продолговатого мозга. Стимуляция этих рецепторов снижает симпатический поток и, соответственно, АД путем уменьшения резистентности сосудов. Кроме того, снижается активность сосудодвигательного центра, уменьшаются сердечный выброс, периферическая симпатическая активность. Прием моксонидина приводит к снижению системного сосудистого сопротивления и АД. Моксонидин снижает уровень ренина, ангиотензина II и альдостерона в плазме крови [20]. После приема внутрь пиковая концентрация достигается в пределах 1 ч. Период полувыведения в плазме составляет 2 ч и увеличивается при почечной недостаточности. Несмотря на относительно короткий период полувыведения, АД эффективно регулируется однократным приемом препарата в сутки. Антигипертензивный эффект длится значительно дольше, что связано с задержкой препарата в центральной нервной системе. Симпатоингибирующий эффект моксонидина, вероятно, опосредуется практически полностью его влиянием на I-рецепторы. Моксонидин отличается от других симпатолитических гипотензивных средств более низким сродством к центральным α2-адренорецепторам, что объясняет меньшую вероятность развития седативного эффекта и сухости во рту, по сравнению с клонидином. Антигипертензивная эффективность моксонидина при эссенциальной АГ доказана в масштабных двойных слепых плацебо-контролируемых рандомизированных исследованиях и сравнима с таковой большинства других антигипертензивных препаратов [8].
Прием пищи не оказывает влияния на фармакокинетику препарата. Препарат хорошо всасывается из желудочно-кишечного тракта и почти полностью абсорбируется в его верхних отделах. Абсолютная биодоступность составляет приблизительно 88%. Максимальная концентрация в крови регистрируется через 0,5–3 ч. Связь с белками плазмы крови составляет 7,2%. 90% препарата выводится почками, в основном (70%) в неизмененном виде. Период полувыведения (Т1/2) моксонидина и метаболита составляет 2,5 и 5 ч соответственно. Несмотря на короткий период полужизни (около 3 ч), он контролирует АД в течение суток [9]. Моксонидин эффективен при монотерапии АГ, однако оптимально его назначение в составе комбинированной терапии, например, с иАПФ, сартанами (БРА), тиазидными диуретиками и другими основными гипотензивными средствами. Сочетание моксонидина с другими гипотензивными средствами усиливает их антигипертензивный эффект. Моксонидин при добавлении к терапии БРА II (эпросартан) нормализует АД и симпатическую гиперактивность у гипертензивных нормоволемических пациентов с хронической почечной недостаточностью. Моксонидин по антигипертензивной эффективности не уступает диуретикам, БАБ, АК и иАПФ, а по переносимости достоверно превосходит прежние препараты центрального действия. Он более безопасен, чем клонидин, пропранолол, каптоприл, нифедипин. Моксонидин улучшает на 21% индекс чувствительности к инсулину (в сравнении с плацебо) у пациентов с ожирением, инсулинорезистентностью и умеренной степенью АГ. Седативный эффект выражен значительно меньше, чем у других препаратов центрального действия. Препарат потенцирует эффекты средств, угнетающих ЦНС, – этанола, транквилизаторов, барбитуратов. Моксонидин способен умеренно улучшать ослабленные когнитивные функции у пациентов, получающих лоразепам. Назначение моксонидина совместно с бензодиазепинами может сопровождаться усилением седативного эффекта последних [1, 6, 8–10, 13–19].
В исследование TOPIC (Trial Of Physiotens In Combination), проведенное в Великобритании на 138 клинических базах, были включены 566 пациентов с АГ в возрасте 18–80 лет. При назначении моксонидина в дозе 0,2 или 0,4 мг/сут надежный контроль при монотерапии был достигнут у 294 (52%) пациентов, у остальных – при комбинированной терапии (в сочетании с амлодипином или эналаприлом). В ходе исследования препарат зарекомендовал себя как эффективный и хорошо переносимый и в условиях монотерапии, и комбинированной терапии [10, 11]. При применении моксонидина у пациентов с АГ наблюдается двойной механизм действия – препарат обеспечивает как краткосрочный (в основном за счет воздействия на симпатические центры головного мозга), так и долгосрочный (за счет подавления выброса ренина и улучшения экскреторной функции почек) контроль АД. Так, разовая пероральная доза моксонидина (0,4 мг) вызвала статистически достоверное снижение АД у пациентов с АГ в среднем со 176/105 мм рт. ст. до 158/95 мм рт. ст. [10, 11].
Для лечения больных с мягкой и умеренной АГ рекомендована начальная доза Моксарела (моксонидина) 0,2 мг/сут. Если реакция на лечение неудовлетворительная, через 2 нед. дозу удваивают. Дозы 0,2–0,4 мг/сут в большинстве случаев было достаточно для поддержания АД на удовлетворительном уровне. Высокая антигипертензивная эффективность моксонидина подтверждена при лечении пациентов с неосложненным гипертоническим кризом. Так, при сублингвальном назначении моксонидина в дозе 0,4 мг эффективное снижение АД при хорошей переносимости препарата достигалось у 90% пациентов. Существенное снижение систолического АД и диастолического АД после однократного приема препарата отмечается уже через 20 мин и достигает максимума через 1,5 ч [1, 2, 10, 12]. Моксарел (моксонидин) занимает особое место в терапии АГ, сочетающейся с ожирением. За счет активации имидазолиновых I1-рецепторов он способствует снижению гидролиза жиров, уменьшению свободных жирных кислот, усилению метаболизма глюкозы и повышению чувствительности к инсулину, снижению уровня триглицеридов, повышению липопротеидов высокой плотности и снижению уровня ингибитора активатора плазминогена-1. В исследованиях получены данные о влиянии моксонидина на уменьшение инсулинорезистентности у пациентов с избыточным весом и нарушением толерантности к глюкозе. Так, в сравнительном исследовании ALMAZ была проведена оценка влияния моксонидина и метформина на гликемический контроль у пациентов с избыточным весом, мягкой АГ, инсулинорезистентностью и нарушением толерантности к глюкозе. Критериями включения пациентов в исследование были: возраст старше 40 лет, индекс массы тела (ИМТ) >27 кг/м2, глюкоза натощак >6,1 ммоль/л. Исследование ALMAZ показало, что моксонидин понижал уровень глюкозы натощак, снижал вес пациентов, повышал скорость утилизации глюкозы, снижал инсулинорезистентность. На фоне моксонидина уровень глюкозы натощак снижался менее выраженно, чем на фоне метформина, но достоверно снижался уровень инсулина, в то время как метформин на него не влиял, а ИМТ снижался равнозначно на фоне обоих препаратов. Оба препарата статистически достоверно повышают чувствительность к инсулину после нагрузки глюкозой. Моксонидин оказывает влияние на уровень инсулина в крови, метформин регулирует уровень глюкозы, что сопровождается снижением гликозилированного гемоглобина. Оба препарата статистически достоверно снижают массу тела, оставаясь метаболически нейтральными к липидам [21–26].
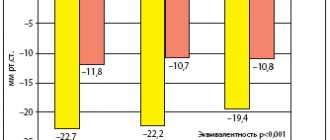
Длительная терапия моксонидином пожилых больных с АГ 1–2 степени обеспечивает оптимальное снижение АД в дневное и ночное время при хорошей переносимости препарата (низкая частота и незначительная выраженность побочных эффектов), приводит к достоверному уменьшению гипертрофии левого желудочка, снижению индекса массы миокарда левого желудочка. Монотерапия моксонидином в течение 24 нед. оказывает положительное влияние на когнитивные функции (память и мышление), что свидетельствует об улучшении функционирования лобных долей головного мозга. В области интеллектуальной деятельности наблюдалась положительная динамика – повысились возможности больных в выполнении действий, требующих более высокого уровня обобщения в наглядно-образной и зрительно-логической сферах. Кроме того, на фоне лечения выявлены положительные изменения памяти – возросла продуктивность запоминания [27]. Для пациентов с метаболическим синдромом важно также отметить нефропротективный эффект моксонидина. Длительное применение моксонидина вызывает достоверное снижение микроальбуминурии, концентраций свободного тромбомодулина и ингибитора активатора плазминогена в крови. По результатам постмаркетингового обзорного исследования, моксонидин эффективно снижает АД у больных c метаболическим синдромом и одновременно способствует уменьшению массы тела у пациентов с ожирением. После 8 нед. лечения у пациентов было зарегистрировано снижение массы тела в среднем на 1,4 кг, при этом наиболее выраженное снижение было отмечено у больных с ожирением. Частота использования комбинированной антигипертензивной терапии составила 81,1% среди больных с метаболическим синдромом и 63,3% – по группе в целом. Было выявлено значительное снижение систолического (26,9±15,1 мм рт. ст., 95% ДИ 26,4–27,3) и диастолического (13,2±9,5 мм рт. ст., 95% ДИ 12,9–13,5) АД. Высокая эффективность моксонидина (снижение диастолического артериального давления до уровня <90 мм рт. ст. и/или снижение диастолического артериального давления >10 мм рт. ст.) была зарегистрирована у 94% пациентов. Сходным образом положительный эффект наблюдался у большого числа пациентов с метаболическим синдромом – 94%, ожирением – 93%, СД – 94% и получавших монотерапию – 95% [28–31].
Выводы. Моксарел (моксонидин) является препаратом выбора из гипотензивных средств с центральным механизмом действия и характеризуется высокой антигипертензивной эффективностью и переносимостью у пациентов с избыточной массой тела, ожирением, метаболическим синдромом или без него, а также обладает дополнительными метаболическими свойствами и оказывает благоприятное действие на массу тела. Моксонидин хорошо переносится, мало взаимодействует с другими препаратами и у большинства пациентов может использоваться однократно в сутки. Моксарел (моксонидин) показан для лечения больных мягкой и умеренной АГ, и в особенности в качестве дополнительного лекарственного средства, – при лечении пациентов с метаболическим синдромом.
Литература 1. Клиническая фармакология и фармакотерапия / Под ред. В.Г. Кукеса, А.К. Стародубцева. М.: ГЭОТАР-Медиа, 2012. 832 с. 2. Клиническая фармакология: национальное руководство (Серия «Национальные руководства»). М.: ГЭОТАР-Медиа, 2014. 976 с. 3. Оганов Р.Г., Тимофеева Т.Н., Колтунов И.Е. и др. Эпидемиология артериальной гипертонии в России. Результаты федерального мониторинга 2003–2010 гг. // Кардиоваскулярная терапия и профилактика. 2011. № 1. С. 9–13. 4. ABC Of Hypertension / Ed. by D. Gareth Beevers, Gregory H. Lip and Eoin O’Brien. 5th ed. Malden, Mass.: BMJ Books, 2007. P. 88. 5. Ezzati M., Lopez A.D., Rodgers A. et al. Selected major risk factors and global and regional burden of disease // Lancet. 2002. Vol.360(9343). P.1347–1360. 6. Диагностика и лечение артериальной гипертензии. Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов. Четвертый пересмотр // Системные гипертензии. 2010. № 3. С. 5–26. 7. ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension // J. Hypertens. 2013. Vol. 31. P. 1281–1357. 8. Neumann J., Ligtenberg G., Oey L. et al. Моксонидин нормализует симпатическую гиперактивность у пациентов с ХПН, получающих эпросартан // J. Amer. Soc. Nephrol. 2004. Vol.15. P. 2902–2907. 9. Инструкция (ТКФС) препарата Моксарел. 10. Гапонова Н.И., Абдрахманов В.Р., Бараташвили В.Л., Терещенко С.Н. Анализ эффективности и безопасности применения моксонидина у пациентов с артериальной гипертензией и гипертоническими кризами // Практическая медицина. Кардиология. 2011. 04. 11. Waters J., Ashford J., Jager B.A. et al. Use of moxonidine as unitial therapy and in combination in the treatment of essential hypertension: results of the TOPIC (Trial of Physiotens in Combination) study // J. Clin Basic Cardiol. 1999. Vol. 2. P. 219–224. 12. Руксин В.В., Гришин О.В. Неотложная помощь при повышении артериального давления, не угрожающем жизни // Кардиология. 2011. № 2. С. 45–51. 13. Frei M., Küster l., Gardosch von Krosigk P-P. et al. Moxonidine and hydrochlorothiazide in combination: a synergistic antihypertensive effect // J. Cardiovasc. Pharmacol. 1994. Vol. 24. P. 25–28. 14. Prichard B.N.C, Simmons R., Rooks M.J. et al. A double-blind comparison of moxonidine and atenolol in the management of patients with mild – to moderate hypertension // J. Cardiovasc. Pharmacol.1992. Vol. 20. P. 45–49. 15. Wolf R. The treatment of hypertensive patients with a calcium antagonist or moxonidine: a comparison // J. Cardiovasc. Pharmacol. 1992. Vol. 20. P. 42–44. 16. Lotti G., Gianrossi R. Moxonidin vs. captopril in mild to moderate hypertension (German) // Fortschr. Med. 1993. Vol. 111 (27). P. 429–432. 17. Kraft K., Vetter H. Twenty – four – hour blood pressure profiles in patients with mild – to – moderate hypertension; moxonidine versus captopril // J. Cardiovasc. Pharmacol. 1994. Vol. 24 (Suppl. 1). S. 29–S33. 18. Küppers H.E., Jäger B.A., Luszick J.H. et al. Placebo-controlled comparison of the efficacy and tolerability of once – daily moxonidine and enalapril in mild – to moderate essential hypertension // J. Hypertens. 1997. Vol.15. P. 93–97. 19. Prichard B.N.C., Kuster L.J., Hughes P.R. et al. Dose relation of blood pressure reduction with moxonidine: findings from three placebo – and active – controlled randomized studies // J. Clin. Basic. Cardiol. 2003. Vol. 6. P. 49–51. 20. Sanjuliani A.E., Genelhu de Abreu V., Ueleres Braga J., Francischetti E.A. Effects of moxonidine on the sympathetic nervous system, blood pressure, plasma renin activity, plasma aldosterone, leptin and metabolic profile in obese hypertensive patients // J. Clin Basic Cardial. 2004. Vol. 7. P. 19–25. 21. Метаболический синдром. М.: «МЕДпрес-информ», 2007. 22. Мкртумян А.М., Бирюкова Е.В. Основной подход к фармакотерапии метаболического синдрома // Consilium medicum. 2006. Т. 8, № 5. C.54–57. 23. Мычка В.Б., Чазова И.Е. Метаболический синдром. Возможности диагностики и лечения. (Подготовлено на основе рекомендаций экспертов ВНОКпо диагностике и лечению метаболического синдрома), 2008. C. 1–16. 24. Чазова И.Е., Алмазов В.А., Шляхто Е.В. Моксонидин улучшает гликемический контроль у пацинтов с артериальной гипертонией и избыточной массой тела в сравнении с метформином: исследование ALMAZ // Diabetes, Obesity and Metabolism. 2006. Vol. 8. P. 456–465. 25. Scarpello J.H., Howlett H.C. Metformin therapy and clinical uses // Diab. Vase. Dis. Res. 2008. Vol. 5. P. 157–167. 26. Шилов А.М., Авшалумов А.Ш., Синицина Е.Н., Еремина И.В. Коррекция факторов риска у пациентов с избыточной массой тела, сочетающейся с инсулинорезистентностью и артериальной гипертонией // РМЖ. 2011. Т. 19, № 2. С.1–7. 27. Мартынов А.И., Остроумова О.Д., Корсакова Н.К. и др. Влияние препарата моксонидин (физиотенз) на состояние сердечно-сосудистой системы и головного мозга у пожилых больных с артериальной гипертонией // Российский кардиологический журнал. 2002. № 4. 28. Hausberg M., Tokmak F., Pavenstadt H. Et al. Effects of moxonidine on sympathetic nerve activity in patients with end-stage renal disease // J. Hypertens. 2010. Jul 14. 29. Krespi P.G., Makris T.K., Hatzizacharias A.N. et al. Moxonidine effect on microalbuminuria, thrombomodulin, and plasminogen activator inhibitor-1 levels in patients with essential hypertension // Cardiovasc. Drugs Ther. 1998.Vol.12(5). P. 463–467. 30. Алексанян Л.А., Полосьянц О.Б. Моксонидин в современном лечении кардиоваскулярных заболеваний // РМЖ. 2010. № 18. 31. Sharma A.M., Wagner T., Marsalek P. Моксонидин в лечении больных с избыточной массой тела и ожирением, страдающих метаболическим синдромом: результаты постмаркетингового обзорного исследования (CAMUS) // Обзоры клинической кардиологии. 2007. № 10.