Налидиксовая кислота
Наименование: Налидиксовая кислота (Acidumnalidixicum) Фармакологическое действие: Является синтетическим антибактериальным препаратом. Эффективна при инфекциях, вызванных грамотрицательными бактериями, кишечной, дизентерийной и брюшнотифозной палочками, протеем (видом микроорганизмов, которые в определенных условиях могут вызывать инфекционные заболевания тонкого кишечника и желудка), палочкой клебсиеллы (Фридлендера — бактерий-возбудителей воспаления легких и местных гнойных процессов). Действует бактериостатически и бактерицидно (препятствует размножению и уничтожает бактерии). Эффективна в отношении штаммов, устойчивых к антибиотикам и сульфаниламидам. Малоэффективна в отношении грамположительных кокков (стафилококки, стрептококки, пневмококки) и патогенных анаэробов (способных существовать в отсутствии кислорода бактерий, вызывающих заболевания человека). Препарат хорошо всасывается из желудочно-кишечного тракта. Около 80% выделяется с мочой в неизмененном виде. Период полувыведения (время, за которое выводится 1/2 дозы препарата) составляет примерно 8 ч, однако при почечной недостаточности достигает 20 ч и более.
Показания к применению: Применяют главным образом при инфекциях мочевых путей: цистите (воспалении мочевого пузыря), пиелите (воспалении почечной лоханки), пиелонефрите (воспалении ткани почки и почечной лоханки), — вызванных чувствительными к препарату микроорганизмами. Наиболее эффективен при острых инфекциях. Назначают также для профилактики инфекций при операциях на почках и мочевом пузыре. Рекомендуется при энтероколитах (воспалении тонкой и толстой кишки), холециститах (воспалении желчного пузыря), воспалении среднего уха и других заболеваниях, вызванных чувствительными к препарату микроорганизмами, в том числе устойчивыми к другим антибактериальным средствам.
Способ применения: Взрослые принимают внутрь по 0,5 г (1 капсула или 1 таблетка), а при более тяжелых инфекциях — по 1 г 4 раза в день. Курс лечения не менее 7 дней. При длительном лечении применяют по 0,5 г 4 раза в день. Детям назначают из расчета 60 мг/кг, распределив суточную дозу на 4 равные части.
Побочные действия: Обычно налидиксовая кислота хорошо переносится; однако возможны тошнота, рвота, понос, головная боль, головокружение. Могут возникать аллергические реакции (дерматиты /воспаление кожи/, повышение температуры тела, эозинофилия /увеличение числа эозинофилов в крови/), а также повышаться чувствительность кожи к солнечному свету (фотодерматозы). У больных с нарушением мозгового кровообращения, паркинсонизмом, эпилепсией могут появиться судороги. В связи с возможностью судорожных реакций следует остерегаться передозировки препарата у детей. Выраженные побочные реакции требуют временной или полной отмены препарата.
Противопоказания: Нарушение функции печени, угнетение дыхательного центра. Большая осторожность необходима при недостаточной функции почек. Нельзя назначать женщинам в первые 3 мес. беременности и детям до 2 лет. Не следует применять препарат одновременно с нитрофуранами, так как при этом уменьшается антибактериальный эффект.
Форма выпуска: В капсулах или таблетках по 0,5 г.
Условия хранения: Список Б. В сухом, защищенном от света месте.
Синонимы: Невиграмон, Неграм, Цистидикс, Награм, Налидин, Нилидиксан, Налидиксин, Налиграм, Наликс, Налурин, Наксурил, Нограм, Нотрицел, Специфин, Уродиксин, Урограм, Уронег, Винтомилон.
Внимание! Описание препарата «Налидиксовая кислота» на данной странице является упрощённой и дополненной версией официальной инструкции по применению. Перед приобретением или использованием препарата вы должны проконсультироваться с врачом и ознакомиться с утверждённой производителем аннотацией. Информация о препарате предоставлена исключительно с ознакомительной целью и не должна быть использована как руководство к самолечению. Только врач может принять решение о назначении препарата, а также определить дозы и способы его применения.
Невиграмон
ИНСТРУКЦИЯ по медицинскому применению препарата Невиграмон (NEVIGRAMON (R))
Общая характеристика:международное и химическое названия: Nalidixic acid — 1-этил-7-метил-4-оксо-1,4-дигидро-1,8-нафтиридин-3-карбоновая кислота основные физико-химические свойства: непрозрачные твердые желатиновые капсулы с корпусом и крышкой желтого цвета 1 таблетка содержит 500 мг налидиксовой кислоты Вспомогательные вещества: кремния диоксид водный, стеариновая кислота, хинолин желтый, сансет желтый, титана диоксид, желатин. Форма выпуска. Капсулы. Фармакологическая группа. Уроантисетикы и противомикробные средства. Производные хинолонов. Код АТС J01MB02.
Фармакотерапевтические свойства. Фармакологические. Налидиксовая кислота имеет выраженной антибактериальной активностью в отношении грамположительных бактерий, включая Proteus mirabilis, P.morganii, P. vulgaris, P. rettgeri, Escherichia coli, Enterobacter (Aerobacter), Klebsiella. Штаммы Pseudomonas обычно устойчивы к действию препарата. Налидиксовая кислота действует путем селективного подавления бактериального синтеза ДНК. Налидиксовая кислота оказывает бактерицидное действие при любом рНсечи. В низких концентрациях налидиксовая кислота влияет только напролиферуючи микроорганизмы путем подавления репликации ДНК. При длительном воздействии она ингибирует также бактериальный синтез РНК и белка. Минимальная подавляемых концентрация (МПК) налидиксовой кислоты составляет 5-75 мкг / мл. В высших концентрациях бактерицидное действие налидиксовой кислоты осуществляется путем дезинтеграции молекул ДНК. Фармакокинетика. Налидиксовая кислота быстро всасывается из желудочно-кишечного тракта, частично метаболизируется в печени и быстро выводится почками. Изменена налидиксовая кислота определяется в моче вместе с ее активным метаболитом, гидрокси-налидиксовой кислотой, которая имеет такую ??же антибактериальную активность, как и налидиксовая кислота. Гидрокси-налидиксовая кислота составляет 30% биологически активного препарата в крови и 85% — в моче. Максимальный уровень активного препарата в сыворотке в среднем составляет 20-50 мкг / мл через 2 часа после приема натощак 1 г налидиксовой кислоты здоровыми лицами. Период полувыведения составляет 6-7 часов. Около 93% налидиксовоикислоты и 63% гидрокси-налидиксовой кислоты связываются с белками плазмы. Максимальный уровень активного препарата в моче после приема однократной дозы 1 г составляет в среднем около 150-250 мкг / мл. Подщелачивание мочи увеличивает концентрацию неизмененного препарата в моче. Примерно 4% налидиксовой кислоты выводится с калом. Налидиксовая кислота проникает через плаценту, небольшие количества появляются в материнском молоке. Показания. Лечение инфекций мочевыводящих путей, вызванных грамотрицательных микроорганизмов, чувствительными к налидиксовоикислоты. Лечение бактериальной дизентерии. Способ применения и дозы. Невиграмон рекомендуется принимать натощак, преимущественно за час до еды. Взрослые. Средняя доза составляет 4 г (по 2 капсулы 4 раза в сутки) не менее 7 дней. Если применение препарата необходимо продолжить, доза может быть снижена до 1 капсулы 4 раза в сутки. Дети старше 12 лет (массой более 40 кг). Рекомендуемая суточная доза составляет 50 мг / кг массы тела (4 раза по 1 капсуле). Больные с почечной недостаточностью. Больным с клиренсом креатинина 20 мл / мин и ниже дозу уменьшают наполовину (см. «Особые указания»).
Побочное действие.Со стороны центральной нервной системы могут наблюдаться сонливость, головная боль, головокружение. В редких случаях — токсический психоз, кратковременные судороги. Конвульсии обычно наблюдаются после передозировки у больных с эпилепсией, церебральным артериосклерозом. Паралич шестого черепного нерва, который быстро проходит после отмены препарата. Зрение. Редко может наблюдаться обратимое субъективное нарушение зрения (обычно в течение первых нескольких дней приема препарата после приема каждой дозы): ощущение чрезмерной яркости света, восприятия цвета, затрудненность фокусировки, снижение остроты зрения, диплопия. Обычно эти явления быстро проходят после снижения дозы или отмены препарата. Со стороны желудочно-кишечного тракта. Боль в животе, тошнота, рвота, понос. Аллергические реакции. Сыпь, зуд, крапивница, эозинофилия, артралгия с туго подвижностью и отеком суставов. Редко — ангио невротичнийнабряк, анафилактический шок и анафилактоидные реакции. Со стороны кожных покровов. Реакции светочувствительности: эритема и волдыри на экспонированной поверхности кожи, которые обычно полностью проходят в течение от двух недель до двух месяцев после отмены невиграмон. Волдыри могут продолжать появляться при экспозиции солнечным светом или при небольших повреждениях поверхности кожи в течение трех месяцев после отмены препарата. Другие. Редко — холестаз, парестезии, метаболический ацидоз, тромбоцитопения, лейкопения или гемолитическая анемия, иногда сопровождается дефицитом глюкозо-6-фосфат дегидрогеназы. Противопоказания. Повышенная чувствительность к налидиксовой кислоты абоподибних к ней соединениям. Конвульсии, болезнь Паркинсона, тяжелый церебральный артериосклероз в анамнезе. Почечная и печеночная недостаточность. Дефицит глюкозо-6-фосфат-дегидрогеназы. Порфирия. Дети до 12 лет. Первый триместр беременности. Лактация.
Передозировки. У больных, которые приняли дозу, превышающую рекомендованную, могут наблюдаться токсический психоз, судороги, повышенное внутренне черепной давление или метаболический ацидоз, тошнота, рвота и летаргия. Эти явления кратковременные (двиабо 3:00), так как препарат быстро выводится из организма. Если препарат уже абсорбировавшийся, рекомендуется повышенное потребление жидкости; необходимо иметь в распоряжении кислород и средства искусственной респирации. В слишком тяжелых случаях может потребоваться проведение анти конвульсивной терапии.
Особенности применения.Пре пубертатный период. Невиграмон вызывает эрозии в хрящах несущих суставов и другие признаки артропатии у большинства животных изученных видов, достигших половой зрелости. Поэтому следует с осторожностью назначать Невиграмон хворимпре пубертатного возраста. При обнаружении артралгии применения невиграмон необходимо прекратить. Следует соблюдать осторожность при назначении невиграмон больным, страдающим заболеваниями печени (см. «Побочное действие») и тяжелой почечной недостаточности. Таким больным может потребоваться снижение дозы (см. «Способ применения и дозы»). При необходимости применения невиграмон более двух недель рекомендуется проводить анализ крови, контролировать функцию печени и почек. Больных следует предупредить о необходимости избегать излишнего воздействия солнечного света, с появлением реакций светочувствительности применения Невиграмонуслид прекратить. С появлением у больного симптомов повышенного внутричерепного давления, психоза или других токсических явлений, применение невиграмон следует прекратить. Если применение невиграмон не дает ожидаемого результата, необходимо провести анализ на чувствительность микроорганизмов. Бактериальная резистентность доНевиграмону обычно развивается в течение первых 48 часов применения препарата. Отмечалась перекрестная резистентность между невиграмон и другими производными хинололу, такими как оксолиновая кислота и циноксацин.
Влияние на способность управлять автомобилем и выполнять работы, требующие повышенного внимания, незначительный.
Беременность. Безопасность применения невиграмон во время беременности не установлена. Поэтому применять препарат во время беременности можно только в том случае, когда ожидаемая польза превышает потенциальный риск, особенно в течение первого триместра беременности (Невиграмон проникает через плацентарный барьер и, как исследованы на животных, встраивается в хрящевую ткань, развивается,) и на последнем месяца беременности, так как у младенца может проявляться высокий уровень препарата в крови.
Лактация. Препарат проникает в грудное молоко, поэтому застосуванняНевиграмону при лактации противопоказано.
Взаимодействие с другими лекарственными средствами. Невиграмон может усиливать действие пероральных антикоагулянтов, таких как варфарин или бис-гидроксикумарин — невиграмон занимает значительное количество мест их связывания с белками плазмы. При одновременном применении невиграмон и пероральных антикоагулянтов необходимо контролировать ватипротромби новое время или INR (международный нормализует чей показатель), может возникнуть необходимость изменения дозы антикоагулянта. Поскольку для проявления антибактериального действия невиграмон необходимо размножения бактериальных клеток, его действие может подавляться в присутствии других антибактериальных средств, особенно бактериостатических, таких как тетрациклин, левомицетин или нитрофурантоин (последний является антагонистомНевиграмону in vitro). Пробенецид подавляет секрецию невиграмон в почечных канальцах и может снижать его эффективность в отношении инфекций мочеполовой системы, при этом увеличивается развитие системных побочных явлений. Одновременное применение невиграмон и мелфалана супроводжуетьсягастроинтестинальною токсичностью. Результаты лабораторных анализов. Если для анализа мочи больных, принимающих Невиграмон, используются методы, основанные на восстановлении меди (например, использование растворов Бенедикта или Фелинга) может быть получена ошибочная положительная реакция на глюкозу. Поэтому рекомендуется применять специфические методы на основе глюкозо-оксидазы. Неправильные значения могут быть получены при определении 17-кето икето генных стероидов в моче при проведении анализов, основанных на вимириванилилминдальнои кислоты в моче. В таких случаях рекомендуется использовать тест Портера-Зильбера для 17-гидрокортикостероидив.
Условия хранения. Хранить при комнатной температуре (от 15 ° С до + 25 ° С), в защищенном от света месте. Срок годности — 5 лет.
Гемифлоксацин: 10 лет клинического применения в терапии инфекций нижних дыхательных путей
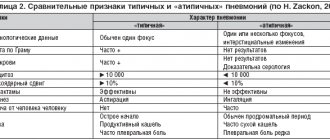
История рождения класса хинолоновых антибиотиков ведет свое начало с 1960-х гг., когда в процессе синтеза хлорохина была получена налидиксовая кислота (рис. 1). На протяжении двух 10-летий налидиксовая кислота и ее производные (пипемидиевая и оксолиниевая кислоты), обладающие активностью в отношении грамотрицательных микроорганизмов, с успехом использовались для лечения инфекций мочевыводящих путей. Вторая волна развития хинолонов (1980-е гг.) связана с появлением фторированных соединений с более высокой активностью в отношении грамотрицательных и грамположительных бактерий, внутриклеточных микроорганизмов, обладающих улучшенной фармакокинетикой, наличием форм для парентерального введения (ципрофлоксацин, офлоксацин, флероксацин, ломефлоксацин, норфлоксацин) [2]. Следующий этап развития хинолонов (1990-е гг.) связан с появлением ди- и трехфторированных соединений, обладающих усиленной активностью в отношении грамположительных бактерий (особенно Streptococcus pneumoniae) и внутриклеточных возбудителей. Данное качество обусловило название этих препаратов – «респираторные» фторхинолоны, относящиеся, согласно современной классификации, к III (спарфлоксацин, левофлоксацин) и IV (моксифлоксацин, гатифлоксацин, гареноксацин) поколениям хинолонов. В 1999 г. исследовательская группа лаборатории LG Life Sciences (Южная Корея) путем присоединения аминометиловой группы в положении С7 пирролидинового кольца (рис. 2) синтезировала новый препарат, отнесенный к IV поколению хинолоновых антибиотиков [4]. Как оказалось, данная формула обеспечила уникальные свойства гемифлоксацина, характеризующегося наибольшей антипневмококковой активностью среди всех представителей данного класса антимикробных препаратов. Механизм действия гемифлоксацина бактерицидный и аналогичен механизму действия других фторхинолонов. В его основе лежит нарушение процессов репликации, репарации и транскрипции бактериальной ДНК посредством ингибирования ферментов ДНК-гиразы (топоизомеразы II) и топоизомеразы IV, необходимых для роста бактерий. Отличительной особенностью «респираторных» фторхинолонов является высокая эффективность в отношении всех потенциальных возбудителей ВП. При этом гемифлоксацин, как уже было отмечено, обладает наивысшей активностью в отношении S. pneumoniae. Это продемонстрировано в целом ряде исследований, по результатам которых его минимальная подавляющая концентрация для 90% исследуемых штаммов (МПК90) в отношении пневмококка составляет 0,015–0,03 мкг/мл [5–7]. У левофлоксацина данный показатель равен 1–2 мкг/мл, у моксифлоксацина – 0,12–0,25 мкг/мл (табл. 1). Гемифлоксацин активен также в отношении S. pneumoniae, устойчивых к пенициллину и макролидам, и большинства штаммов, устойчивых к офлоксацину и левофлоксацину. Активность гемифлоксацина в отношении «атипичных» возбудителей (Mycoplasma pneumoniae, Chlamydophila pneumoniae, Legionella pneumophila) сравнима с активностью других «респираторных» фторхинолонов. Основным механизмом развития резистентности к фторхинолонам являются мутации в генах ДНК-гиразы и ДНК-топоизомеразы IV. Важно, что для классических фторхинолонов для развития резистентности может оказаться достаточно одной мутации генов, кодирующих ту или иную субъединицу топоизомеразы IV, тогда как для «респираторных» фторхинолонов требуются дополнительные мутации в генах ДНК-гиразы. Применение гемифлоксацина за счет наибольшей пневмококковой активности характеризуется минимальной вероятностью одиночной и двойной последовательной мутации, что было показано на экспериментальной модели пневмококковой пневмонии [9]. Резистентность пневмококка к «респираторным» фторхинолонам во всем мире, за исключением ряда стран Юго-Восточной Азии, остается невысокой [10]. В Европе более 97% штаммов S. pneumoniae чувствительны к «респираторным» фторхинолонам [11], в России, согласно результатам исследования ПеГАС-III (табл. 2), отсутствуют резистентные штаммы пневмококка к лево–, мокси- и гемифлоксацину [12]. Штаммы гемофильной палочки, устойчивые к «респираторным» фторхинолонам, на территории РФ также не выделялись. Все «респираторные» фторхинолоны имеют длительный период полувыведения, что позволяет принимать их 1 р./сут, характеризуются высокой биодоступностью и быстрой абсорбцией. Антимикробное действие фторхинолонов зависит от создаваемых концентраций антибиотика, при этом наилучшим фармакодинамическим параметром, коррелирующим с эрадикацией бактерий, является отношение AUC (не связанной с белками фракции антибиотика) к МПК. Надежный предиктор эрадикации S. pneumoniae – отношение свободной AUC/МПК ≥25. У левофлоксацина, моксифлоксацина и гемифлоксацина этот показатель составляет 40, 96 и 97–127 соответственно (табл. 3) [7, 13]. «Респираторные» фторхинолоны обладают хорошей тканевой пенетрацией, создавая в альвеолярных макрофагах, слизистой бронхов и жидкости, выстилающей эпителий дыхательных путей, концентрации, существенно превосходящие МПК чувствительных к ним возбудителей респираторных инфекций. Гемифлоксацин характеризуется лучшим проникновением, нежели другие фторхинолоны, в альвеолярные макрофаги и слизистую бронхов (табл. 4). Элиминация антибиотика осуществляется преимущественно через кишечник (>60%), и лишь 27–30% гемифлоксацина выводятся из организма в неизмененном виде через почки, т.е. элиминация антибиотика осуществляется преимущественно неренальными путями. Однако у пациентов с тяжелой почечной недостаточностью (клиренс креатинина ≤29 мл/мин) необходима коррекция дозы гемифлоксацина. Препарат не метаболизируется системой цитохрома Р450, что определяет отсутствие клинически значимых лекарственных взаимодействий, в частности, с теофиллином, варфарином, дигоксином, оральными контрацептивами. Прием пищи практически не изменяет фармакокинетику препарата, поэтому его можно принимать вне зависимости от еды. Стоит отметить, что при параллельном назначении пациенту сульфата железа или сукральфата их необходимо принимать за 4 ч до или спустя 2 ч после приема гемифлоксацина. Учитывая тот факт, что клиническое применение некоторых антибиотиков фторхинолонового ряда (грепафлоксацин, тровафлоксацин, клинафлоксацин и др.) сопровождалось высокой частотой серьезных нежелательных явлений (НЯ), «респираторные» фторхинолоны находятся под пристальным вниманием исследователей и практических врачей. Однако достаточное число исследований, длительный срок использования указанных препаратов в клинической практике позволяют отметить, что левофлоксацин, моксифлоксацин и гемифлоксацин характеризуются благоприятным профилем безопасности. В сравнительном обзоре P. Ball et al. проведен анализ безопасности гемифлоксацина в сравнении с другими антибактериальными препаратами, применяемыми в лечении инфекций респираторного тракта (табл. 5) [14]. Частота серьезных НЯ при применении гемифлоксацина была сравнимой с частотой НЯ при использовании макролидов, β-лактамов и других фторхинолонов. Основной проблемой для гемифлоксацина было появление макулопапулезной кожной сыпи при длительных курсах его приема женщинами моложе 40 лет и женщинами в постменопаузальном периоде, находящимися на заместительной гормональной терапии. В этой связи не рекомендуется его применение данной категорией пациентов курсами более 7 дней. Частота других НЯ (тошнота, диарея, головная боль и др.) была сравнимой. Умеренное и обратимое повышение концентрации печеночных трансаминаз, превышающее в 1,5–3 раза верхнюю границу нормы, наблюдается у 1–5% больных, получающих терапию «респираторными» фторхинолонами. В то же время серьезные гепатотоксические побочные реакции при применении лево-, мокси- и гемифлоксацина встречаются редко [15]. Напротив, в отношении тяжелых поражений печени показательным является пример тровафлоксацина. Именно при его применении встречались непредсказуемые реакции, приводившие в ряде случаев к смертельному исходу или требовавшие трансплантации печени. Частота тяжелых печеночных реакций при применении тровафлоксацина составляет в среднем 58 на 10 млн назначений, в связи с чем лицензия на его использование была отозвана. В то же время, по данным FDA, частота тяжелых поражений печени при использовании моксифлоксацина и левофлоксацина не превышает 6,6 и 2,1 случая на 10 млн назначений соответственно. Данных о подобных случаях при приеме гемифлоксацина не отмечено. Все фторхинолоны в той или иной степени способны влиять на интервал QT, что является групповым свойством данной группы антимикробных препаратов (табл. 6) [16]. Так, грепафлоксацин был отозван с фармацевтического рынка на основании 3 сообщений о развитии пируэнтной желудочковой тахикардии без летального исхода и 7 сообщений о летальных исходах вследствие сердечных нарушений, связь которых с препаратом расценивалась как возможная. Наиболее выраженный отрицательный эффект на проводящую систему сердца оказывает спарфлоксацин, клинические проявления кардиотоксичности также регистрировались при применении офлоксацина, гатифлоксацина и других фторхинолонов. Необходимо отметить, что практически во всех случаях клинически значимое удлинение интервала QT при приеме фторхинолонов наблюдалось у пациентов с факторами риска (лекарственные взаимодействия с другими препаратами, удлиняющими интервал QT, женский пол, пожилой возраст, сопутствующая патология сердца, генетическая предрасположенность и электролитные нарушения). Учитывая возможный риск данного осложнения, «респираторные» фторхинолоны не рекомендуется применять у больных с врожденным или приобретенным удлинением интервала QT; при гипокалиемии; с клинически значимой брадикардией; с клинически значимой сердечной недостаточностью со сниженной фракцией выброса; с желудочковыми аритмиями в анамнезе. Препараты не следует применять одновременно с другими лекарственными средствами, способными удлинять интервал QT, антиаритмическими препаратами IА класса (хинидин, прокаинамид) или класса III (амиодарон, соталол). Высокая клиническая эффективность гемифлоксацина при инфекциях нижних дыхательных путей (ВП, ОХБ, хронической обструктивной болезни легких (ХОБЛ)) доказана в целом ряде клинических исследований. Обращает на себя внимание тот факт, что практически во всех работах применение гемифлоксацина сравнивалось с режимами терапии, использующими парентеральные антибиотики. Так, Н. Lode et al. (2002) продемонстрировали сопоставимую клиническую и бактериологическую эффективность пероральной монотерапии гемифлоксацином и комбинированной ступенчатой терапии (цефтриаксон → цефуроксим ± макролид) в лечении госпитализированных пациентов с ВП [17]. Оба режима терапии показали сопоставимо высокую клиническую эффективность – 92,2% в группе, получавшей гемифлоксацин, и 93,4% у пациентов, получавших ступенчатое лечение (цефтриаксон → цефуроксим ± макролид), а также бактериологическую эффективность, которая составила 92 и 89,9% соответственно. В многоцентровом двойном слепом исследовании, включившем 571 пациента с нетяжелой ВП, гемифлоксацин, применяемый по 320 мг 1 р./сут внутрь в течение 7–14 дней (2/3 больных получали антибиотик всего 7 дней), продемонстрировал высокую клиническую эффективность – 95,8%, сравнимую с эффективностью тровафлоксацина, применяемого по 200 мг 1 р./сут внутрь при лечении ВП – 93,6% [18]. В исследовании P. Leophonte et al. (2002) изучались эффективность и безопасность гемифлоксацина (320 мг 1 р./сут внутрь в течение 7 дней) в сравнении с высокодозной терапией амоксициллином/клавуланатом (1000/125 мг 3 р./сут внутрь в течение 10 дней) в лечении больных с предполагаемой пневмококковой ВП [19]. Оба режима терапии оказались эффективны как на момент окончания терапии (95,3 и 90,1% соответственно), так и спустя 21–28 дней от начала исследования – 88,7% (гемифлоксацин) и 87,6% (амоксициллин/клавуланат). Бактериологическая эффективность гемифлоксацина и амоксициллина/клавуланата после окончания терапии составила 96,3 и 91,8% соответственно. В российском исследовании гемифлоксацин продемонстрировал высокую клиническую (96,7%) и бактериологическую (83,4%) эффективность при лечении госпитализированных пациентов с ВП, что оказалось сопоставимо с терапией сравнения (амоксициллин/клавуланат в/в с последующим переходом на амоксициллин/клавуланат внутрь ± кларитромицин) [20]. В исследовании R. Wilson et al. (2003) изучалась эффективность гемифлоксацина в сравнении с терапией цефтриаксон → цефуроксим у пациентов с обострением ХОБЛ (I тип по Anthonisen), требующим лечения в условиях стационара [21]. Оказалось, что применение перорального гемифлоксацина демонстрирует высокую клиническую эффективность – 92% (анализ на 2–4-й день после окончания терапии), превосходящую эффективность парентерального применения цефтриаксона с переходом на пероральный прием цефуроксима – 88,2% (ITT популяция). При этом длительность госпитального периода при использовании гемифлоксацина была существенно меньше, нежели в группе сравнения. В исследовании GLOBE оценивались сравнительная эффективность и безопасность гемифлоксацина (320 мг/сут в течение 5 дней) и кларитромицина (1000 мг/сут в течение 7 дней) у пациентов с обострением ХОБЛ. Авторами было показано, что прием гемифлоксацина характеризовался достоверным снижением частоты развития последующих обострений по сравнению с приемом кларитромицина [22]. И, наконец, в настоящее время мы обладаем результатами метаанализа, выполненного китайскими учеными и включившего 10 рандомизированных клинических исследований (РКИ), изучавших сравнительную эффективность гемифлоксацина в терапии ВП и ОХБ/ХОБЛ (3940 пациентов) (табл. 7) [23]. В 5 исследованиях гемифлоксацин сравнивался с другими хинолонами (левофлоксацин, тровафлоксацин). 5 РКИ посвящено сравнению гемифлоксацина с β-лактамами и/или макролидами (амоксициллин/клавуланат, кларитромицин, цефтриаксон (в/в)/цефуроксим (per os). При анализе эффективности режимов терапии показано, что гемифлоксацин демонстрирует более высокую терапевтическую эффективность при лечении пациентов как с ВП, так и обострением ХОБЛ, нежели антибиотики сравнения (рис. 3). Смертность от всех причин в период исследования оценивалась в 8 РКИ. Между гемифлоксацином и антибиотиками сравнения не было выявлено никакой значительной разницы для этого показателя. В 9 РКИ оценивалась микробиологическая эффективность. По данным метаанализа, не было отмечено значительной разницы между гемифлоксацином и антибиотиками сравнения. Также не наблюдалось значимых различий между антибиотиками сравнения в эрадикации S. pneumoniae (182 изолята), H. influenzae (160 штаммов), M. catarrhalis (90) и атипичных патогенов (M. pneumoniae, C. pneumoniae и штаммов Legionella spp.). В сравнении с другими фторхинолонами (рис. 4) гемифлоксацин демонстрирует более высокую клиническую эффективность, тогда как существенных различий между β-лактамами и макролидами не наблюдалось (рис. 5). Стоит отметить, что отсутствие различий, вероятно, связано с использованием в ряде РКИ парентеральных форм антибиотиков цефалоспоринового ряда, высокодозной терапии «защищенными» аминопенициллинами. Данные о НЯ, вероятно, связанных с проведением антибиотикотерапии, были получены во всех РКИ, включенных в метаанализ. Не было выявлено существенных различий между гемифлоксацином и другими хинолонами в общей частоте развития НЯ (рис. 6). Отмечено, что у пациентов, которые получили гемифлоксацин, несколько чаще возникали такие НЯ, как диарея и сыпь. При сравнении с β-лактамами и/или макролидами применение гемифлоксацина ассоциировалось с более низким числом побочных эффектов. В отношении возникновения макулопапулезной сыпи назначение гемифлоксацина сопровождалось более высокой частотой возникновения данного НЯ, однако статистически значимой разницы получено не было. Завершая настоящий обзор, хотелось бы отметить, что более чем 10-летний успешный опыт эффективного и безопасного клинического применения гемифлоксацина, целый ряд доказательств его эффективности, включая цитируемый метаанализ, позволили гемифлоксацину занять важное место в современных режимах антибактериальной терапии ВП и ОХБ/ХОБЛ. Так, в национальных рекомендациях по ведению пациентов с ВП гемифлоксацин наряду с левофлоксацином и моксифлоксацином рекомендован к применению у больных с нетяжелой пневмонией, имеющих факторы риска1 терапевтической неудачи [29]. «Респираторные» фторхинолоны (левофлоксацин, моксифлоксацин и гемифлоксацин) являются препаратами выбора при осложненном2 ОХБ/ХОБЛ [30]. 1 Наличие сопутствующих заболеваний: ХОБЛ, сахарный диабет, застойная сердечная недостаточность, хроническая почечная недостаточность, цирроз печени, хронический алкоголизм, наркомания, истощение и/или прием за последние 3 мес. антимикробных препаратов более 2 дней. 2 Наличие ≥1 признака: возраст ≥60 лет; ОФВ1<50%; ≥4 обострений в год; сопутствующие заболевания; оксигенотерапия на дому; длительный прием стероидов внутрь; госпитализация по поводу предшествующего обострения ХОБЛ за последние 12 мес.
Литература 1. US FDA panel backing for Factive. SCRIP 2003; 2830: 22. Электронный ресурс https://www.antibiotic.ru/index.php?article=174. 2. Anderson M., MacGowan A. Development of the quinolones // JАС. 2003. Vol. 51. Suppl. 1. Р. 1–11. 3. Ball P. Quinolone generations: natural history or natural selection? J. Antimicrob. Chemother. 2000. Vol. 46. Р. 17–24. 4. Chang Yong Hong. Discovery of gemifloxacin (Factive, LB2o304a): a quinolone of a new generation // Farmaco. 2001. Vol. 56. Р. 41–44. 5. Hoban D., Bouchillon S., Johnson J. et al. Comparative in vitro activity of gemifloxacin, ciprofloxacin, levofloxacin and ofloxacin in a North American surveillance study. Diagn Microb Infect Dis. 2001. Vol. 40. Р. 51–57. 6. Koeth L., Jacobs M., Bajaksouzian S. et al. Comparative in vitro activity of gemifloxacin to other fluoroquinolones and non-quinolone agents against Streptococcus pneumoniae, Haemophilus influenzae and Moraxella catarrhalis in Unated States in 1999-2000 // Intern J Antimicrob Agents. 2002. Vol. 19. Р. 33–37. 7. Blondeau J., Missaghi B. Gemifloxacin: a new fluoroquinolone // Expert Opin Pharmacother. 2004. Vol. 5. Р. 1117–1152. 8. Hoshino K., Inoue K., Murakami Yo. et al. In Vitro and In Vivo Antibacterial Activities of DC–159a, a New Fluoroquinolone // Antimicrobial Agents and Chemotherapy. 2008. Vol. 52 (1) Р. 65–76. 9. Синопальников А.И. Гемифлоксацин в лечении инфекций нижних дыхательных путей у взрослых // Клиническая микробиология и антимикробная химиотерапия. 2006. № 3. Т. 8. С. 260–269. 10. Козлов Р.С., Веселов А.В. Респираторные фторхинолоны / Внебольничные инфекции дыхательных путей: диагностика и лечение. М.: ООО «М-Вести», 2008. С. 88–105. 11. Jones M., Draghi D., Thornsberry C., Sahm D. A current perspective on S. pneumoniae and H. influenzae resistance trends in Europe: GLOBAL Surveillance Study, 2005. Proceedings of 16th ECCMID, 2006. Abst.rp.1629. 12. Козлов Р.С., Сивая О.В., Кречикова О.И., Иванчик Н.В. и соавт. Динамика резистентности Streptococcus pneumoniae к антибиотикам в России за период 1999–2009 гг. (Результаты многоцентрового проспективного исследования ПеГАС) // Клиническая микробиология и антимикробная химиотерапия. 2010. № 12 (4). С. 329–341. 13. Zanel G., Noreddin A. Pharmacokinetics and pharmacodynamics of the new fluoroquinolones: focus on respiratory infections // Curr Opin Pharmacol. 2001. Vol. 1. Р. 459–463. 14. Ball P., Mandell L., Patou G. et al. A new respiratory fluoroquinolone, oral gemifloxacin: a safety profile in context // Int J Antimicrob Agents. 2004. Vol. 23. Р. 421–429. 15. Leitner J., Graninger W., Thalhammer F. Hepatotoxicity of antibacterials: Pathomechanisms and clinical // Infection. 2010. Vol. 38 (1). Р. 3–11. 16. Iannini P. Quinolone-induced QT interval prolongation: a not-so-unexpected class effect // J Antimicrob Chemother. 2001. Vol. 47 (6). Р. 893–894. 17. Lode H., File T.M., Mandell L. et al. Oral gemifloxacin versus sequental therapy with intravenosus ceftriaxone/oral cefuroxime with or without a macrolide in the treatment of patients hospitalized with community-acquired pneumoniae: a randomized, open-label, multicenter study of clinical efficacy and tolerability // Clin Therapeut. 2002. Vol. 24. Р. 1915–1936. 18. File T., Schlemmer B., Garau J. et al. Efficacy and safety of gemifloxacin in the treatment of community-acquired pneumonia: a randomized, double-blind comparisoin with trovafloxacin // JAC. 2001. Vol. 48. Р. 67–74. 19. Leophonte P., File T.M., Feldman C. Gemifloxacin once daily for 7 days compared to amoxicillin/clavulanic acid thrice daily for 10 days for the treatment of community-acquired pneumonia of suspected pneumococcal origin // Respir Med. 2004. Vol. 98. Р. 708–720. 20. Синопальников А.И., Зайцев А.А. Гемифлоксацин: новые возможности антибактериальной терапии внебольничной пневмонии у взрослых // Российские медицинские вести. 2007. № 1. С. 4–12. 21. Wilson R., Langan C., Ball P. et al. Oral gemifloxacin once daily for 5 days compared with sequential therapy with i.v. ceftriaxone/oral cefuroxime (maximum of 10 days) in the treatment of hospitalized patients with acute exacerbations of chronic bronchitis // Respir Med. 2003. Vol. 97. Р. 242–249. 22. Wilson R., Schentage J.J., Ball P. et al. A comparison of gemifloxacin and clarithromycin in acute exacerbations of chronic bronchitis and long-term clinical outcomes // Clin Therapeut. 2002. Vol. 24. Р. 639–652. 23. Zhang L., Wang R., Matthew F., Chen L., Liu Y. Gemifloxacin for the treatment of community-acquired pneumonia and acute exacerbation of chronic bronchitis: a meta-analysis of randomized controlled trials // Chin Med J (Engl). 2012. Vol. 125 (4). Р. 687–695. 24. Yao Z. A study of the effectiveness of gemifloxacin on chronic obstructive pulmonary disease // PractClin Med. 2008. Vol. 9. Р. 36–37. 25. Shi H., Huang Z., Huang Y. et al. Gemifloxacin versus levofloxacin in treatment of lower respiratory tract infection: a randomized controlled trial // Chin J New Drugs Clin Rem (Chin). 2007 Vol. 26. Р. 678–680. 26. Sethi S., Fogarty C., Fulambarker A. A randomized, double-blind study comparing 5 days oral gemifloxacin with 7 days oral levofloxacin in patients with acute exacerbation of chronic bronchitis // Respir Med. 2004. Vol. 98. Р. 697–707. 27. Ball P., Wilson R., Mandell L. et al. Efficacy of gemifloxacin in acute exacerbations of chronic bronchitis: a randomised, double-blind comparison with trovafloxacin // J Chemother. 2001. Vol. 13. Р. 288–298. 28. File T., Schlemmer B., Garau J. et al. Gemifloxacin versus amoxicillin/clavulanate in the treatment of acute exacerbations of chronic bronchitis. The 070 Clinical Study group // J Chemother. 2000. Vol. 12. Р. 314–325. 29. Чучалин А.Г., Синопальников А.И., Козлов Р.С. и соавт. Внебольничная пневмония у взрослых. Практические рекомендации по диагностике, лечению и профилактике. М., 2010. 82 с. 30. Синопальников А.И., Козлов Р.С., Романовских А.Г., Рачина С.А. Инфекционное обострение ХОБЛ: практические рекомендации по диагностике, лечению и профилактике // Российские медицинские вести. 2006. Вып. XI (№ 1). С. 4–18.