Фармакологические свойства препарата Лефлуномид
базисный противоревматический препарат, обладающий антипролиферативными, иммунодепрессивными и противовоспалительными свойствами. Активный метаболит лефлуномида — А771726 ингибирует фермент дегидрооротатдегидрогеназу и проявляет антипролиферативную активность. А771726 in vitro тормозит вызванную митогенами пролиферацию и синтез ДНК Т-лимфоцитов. Антипролиферативная активность А771726 проявляется, по-видимому, на уровне биосинтеза пиримидина, поскольку добавление в клеточную культуру уридина устраняет тормозящее действие метаболита А771726. С использованием радиоизотопных лигандов показано, что А771726 избирательно связывается с дегидрооротатдегидрогеназой, чем объясняется его свойство угнетать этот фермент и пролиферацию лимфоцитов на стадии G1. Пролиферация лимфоцитов является одним из ключевых этапов развития ревматоидного артрита. Одновременно А771726 тормозит экспрессию рецепторов к интерлейкину-2 и антигенов ядра Ki-67 и PCNA, связанных с клеточным циклом. Терапевтический эффект обычно проявляется через 4–6 нед и может нарастать в дальнейшем в течение 4–6 мес. Лефлуномид быстро превращается в активный метаболит — А771726 (первичный метаболизм осуществляется в кишечнике и печени). В плазме, моче или кале обнаруживаются следовые количества неизмененного лефлуномида. Единственным определяемым метаболитом является А771726, ответственный за основные свойства препарата in vivo. При приеме внутрь абсорбция составляет 82–95%. Максимальная концентрация А771726 достигается через 1–24 ч после однократно принятой дозы. Прием пищи не влияет на абсорбцию препарата. В дозе 5–25 мг фармакокинетические параметры А771726 имеют линейную зависимость. В дозе 20 мг в сутки средние плазменные концентрации А771726 при равновесном состоянии имели значение 35 мкг/мл. А771726 быстро связывается с альбуминами. Несвязанная фракция А771726 — 0,2%. Связь с белками А771726 более вариабельна и несколько снижается у больных ревматоидным артритом или с ХПН. Лефлуномид метаболизируется до одного главного (А771726) и нескольких второстепенных метаболитов, включая 4-трифторметилаланин. Выводится А771726 медленно, клиренс составляет 31 мл/ч. Период полувыведения — 2 нед. У больных с ХПН период полувыведения удлиняется.
Псориатический артрит (ПА) – хроническое воспалительное заболевание суставов, позвоночника и энтезисов, обычно ассоциирующееся с псориазом, относится к группе серонегативных спондилоартропатий. Данные о частоте встречаемости ПА среди больных псориазом широко варьируются – от 7 до 30 %, что связано с особенностями популяционных исследований, а также отсутствием в течение длительного времени единых диагностических критериев.
Клиническая картина ПА
Клинически ПА имеет черты как ревматоидного артрита (РА), так и анкилозирующего спондилоартрита (АСА). Обычно ПА начинается в возрасте от 30 до 55 лет, причем мужчины и женщины болеют с одинаковой частотой. Исключение составляет изолированный псориатический спондилоартрит, который в два раза чаще встречается у мужчин. У большинства пациентов (75 %) псориаз предшествует артриту на срок от нескольких месяцев до нескольких лет. У 10–15 % больных артрит развивается раньше псориаза, а у 11–15 % – одновременно с поражением кожи [1, 2].
Поражение позвоночника (спондилит) сближает ПА с АСА: изменения локализуются в илиосакральных сочленениях, связочном аппарате позвоночника с формированием синдесмофитов и паравертебральных оссификатов. Однако в отличие от АСА при ПА рентгенологические изменения в крестцово-подвздошных сочленениях редко достигают стадии анкилоза и подвижность позвоночника долгое время остается вполне удовлетворительной.
Ранее ПА считали “благоприятным” с точки зрения течения и прогноза воспалительным заболеванием суставов. Однако в последние годы установлено, что при ПА, как и при РА, суставной синдром имеет тенденцию к прогрессированию, развитию деструктивных изменений, что приводит к значительным нарушениям функциональных возможностей больных, особенно в случае мутилирующего (обезображивающего) артрита или ишемического некроза крупных (опорных) суставов. Кроме того, при этом заболевании выявлено повышение смертности по сравнению с общей популяцией и снижение качества жизни больных. Стандартный показатель смертности (SMR) среди лиц, страдающих ПА, выше, чем в популяции, – на 59 % у женщин и на 65 % у мужчин [3]. Отрицательное влияние на качество жизни оказывают как псориаз, так и артрит. Пациенты испытывают серьезные психологические и физические трудности не только из-за обширного поражения кожи, но и в связи с вынужденным ограничением повседневной активности в результате артрита. Основные клинические проявления псориаза и ПА представлены на рис. 1 и .
Общие принципы лечения ПА
Идеальным средством лечения ПА можно считать препарат, оказывающий положительное воздействие как на кожу, так и на артрит.
Согласно рекомендациям Британского общества ревматологов (2005), лечение ПА складывается из двух основных направлений – стандартной терапии и применения биологических агентов [4]. Цель терапии ПА состоит в уменьшении воспаления в суставах, позвоночнике и энтезисах, замедлении рентгенологического прогрессирования, улучшении показателей качества жизни пациентов.
Лечение биологическими агентами основано на парентеральном (внутривенном или подкожном) введении препаратов, оказывающих блокирующее действие на фактор некроза опухоли альфа (ФНО-альфа). К их числу в первую очередь относятся моноклональные антитела к ФНО-альфа инфликсимаб (Ремикейд) и адалимумаб (Хумира), которые быстро и эффективно воздействуют на основные клинические проявления ПА, однако их широкое применение в клинической практике пока ограничено высокой стоимостью лечения. Поэтому первым и обязательным этапом в лечении ПА остается применение базисных противовоспалительных препаратов (БПВП).
Стандартное лечение ПА включает использование нестероидных противовоспалительных средств (НПВС), в основном традиционных – диклофенака или препаратов индольной группы, например индометацина, в средних терапевтических дозах (данных о предпочтительности селективных ингибиторов циклооксигеназы-2 при ПА нет), и внутрисуставное введение глюкокортикоидов (ВСГК). БПВП – сульфасалазин, метотрексат, циклоспорин А и лефлуномид (ЛФ) – назначают по отдельности или в комбинации.
Мета-анализ результатов плацебо-контролируемых, когортных и наблюдательных исследований по оценке эффективности и переносимости препаратов для стандартной терапии ПА показал, что возможности их применения в терапии этого заболевания ограничены. НПВС и ВСГК вызывают уменьшение симптомов артрита, но у части пациентов положительный эффект сохраняется лишь короткое время. Среди БПВП наиболее клинически эффективными считают циклоспорин А и парентеральный метотрексат в высоких дозах – 1–3 мг/кг каждые 10 дней (уровень доказательности В), а также сульфасалазин и ЛФ (уровень доказательности А) [5–7].
Исследования лефлуномида при ПА
Лефлуномид – противовоспалительный иммуномодулирующий препарат, который первоначально был разработан для лечения РА [8]. С 2005 г. ЛФ рекомендован для лечения ПА в России. Использование ЛФ в терапии ПА объясняется признанием ключевой роли Т-клеток в патогенезе этого заболевания.
Активация Т-лимфоцитов происходит в результате распознавания антигена и при участии рецепторных взаимодействий СD28-CD80/CD86, что вызывает сложный каскад иммунных реакций, в результате которых продуцируются различные группы цитокинов (интерлейкинов, интерферонов, ФНО, колониестимулирующих факторов, хемокинов, факторов роста). Основная роль отводится ФНО-альфа – ключевому провоспалительному цитокину, который регулирует процессы воспаления в коже и синовии посредством разнообразных механизмов, таких как экспрессия генов, миграция, дифференциация, пролиферация клеток, апоптоз. Обнаружено, что при псориазе кератоциты получают сигнал к гиперпролиферации при высвобождении Т-лимфоцитами различных хемокинов и цитокинов, включая ФНО-альфа. При этом в псориатических бляшках, синовиальной жидкости и синовии обнаруживают высокий уровень ФНО-альфа, интерлейкина-1, матричной металлопротеиназы [9].
Активный метаболит ЛФ А77 1726 (малононитриламид) тормозит пролиферацию активированных Т- и В-клеток, главным образом через блокирование тирозинкиназы и дегидрооротатдегидрогеназы, которые вовлечены в биосинтез de novo пиримидиновых нуклеотидов. К другим биологическим эффектам ЛФ относят уменьшение синтеза матричной металлопротеиназы, продукции иммуноглобулинов
В-клетками, способность снижать экспрессию циклооксигеназы-2 макрофагами, ингибировать активацию нуклеарного фактора kB (NF-kB), нарушать процесс гликозилирования молекул адгезии, тормозя межклеточные контакты и замедляя миграцию клеток в очаг воспаления. А77 1726 подавляет продукцию ФНО-альфа и интерлейкина-1b, пролиферацию эпидермальных клеток через индукцию регулятора негативного клеточного цикла р53. Подробно механизмы действия ЛФ освещены в предыдущих публикациях и обзорах других авторов [10, 11].
Первые сообщения о применении ЛФ при ПА появились в 2001 г. К этому времени препарат активно использовался при РА, и его роль в лечении ПА была неясна. В связи с этим исследования в отношении эффективности и безопасности ЛФ при ПА вначале носили открытый наблюдательный характер и проводились на небольших группах пациентов.
Liang C. и Barr W. наблюдали 12 пациентов с полиартикулярной (ревматоидоподобной) формой ПА и неэффективностью предшествующей терапии БПВП (метотрексатом, сульфасалазином, ауронафином, азатиоприном) в течение от 8 до 24–31 месяца. ЛФ назначали в дозе 100 мг/сут в течение 3 дней (нагрузочная доза), далее по 20 мг/сут ежедневно. Два пациента продолжили прием преднизолона по 10 мг/сут.
Оценку эффективности терапии проводили на 2-м и 3-м месяцах лечения и после окончания приема ЛФ на основании изменения следующих показателей:
- число болезненных и число припухших суставов;
- сила сжатия кисти;
- оценка активности ПА пациентом и врачом по визуальной аналоговой шкале (ВАШ; 0–100 мм);
- оценка врачом влияния лечения на псориаз кожи и артрит по шкале от 0 до 3 (0 – нет эффекта, 1, 2 и 3 – слабое, среднее и заметное улучшение соответственно).
У большинства больных (восемь человек) отмечалось уменьшение числа болезненных и припухших суставов, увеличение силы сжатия кисти, снижение активности заболевания по ВАШ с одновременным ослаблением симптомов псориаза, причем у семерых и них ранее не отмечалось эффекта от приема минимум трех БПВП. В основном ЛФ хорошо переносился больными. Среди нежелательных явлений наиболее значимыми можно считать следующие: у одного больного появились симптомы сенсорной нейропатии нижних конечностей, у одной пациентки на фоне одновременного приема ЛФ и заместительной гормональной терапии развилось маточное кровотечение (в обоих случаях лечение было прекращено). У четверых пациентов из-за появления признаков токсичности прием препарата был временно приостановлен и возобновлен в меньшей дозе (10 мг/сут) после их исчезновения. Также препарат отменялся из-за повышения уровня трансаминаз крови (один больной), развития алопеции (один больной), диареи (двое). У половины больных никаких нежелательных явлений не наблюдалось [12, 13].
Scarpa R. и соавт. (2001) провели пилотное исследование эффективности ЛФ в стандартной дозе у шести пациентов с полиартикулярной формой ПА в течение 3 месяцев. На фоне лечения отмечалось значимое уменьшение количества болезненных и припухших суставов, снижение СОЭ и уровня С-реактивного белка (СРБ), однако площадь поражения кожи осталась прежней. Нежелательных эффектов на функцию печени не отмечалось [14].
Reich K и соавт. (2002) сообщили об успешном применении ЛФ у больной с длительным анамнезом (более 44 лет) распространенного псориаза и остеолитической полиартикулярной формы ПА (более 15 лет) с отсутствием эффекта от предшествующего лечения БПВП (циклоспорином А 2 мг/кг в течение 6 месяцев, метотрексатом 7,5 мг/нед в течение 9 лет и сульфасалазином 2 г/сут в течение 2 месяцев). ЛФ в дозе 10мг/сут применяли в составе комбинированной схемы, включавшей также преднизолон 10 мг/сут и сульфасалазин 2 г/сут, что привело к быстрому (через 3 недели) уменьшению числа болезненных, припухших суставов и площади псориатического поражения кожи без ухудшения функции печени и почек [10].
Cuchacovich M. и Soto L. (2002) показали способность ЛФ задерживать при ПА рентгенологическое прогрессирование и вызывать ремодуляцию кости. Это представляется особенно важным, т. к. отмечено, что при ПА ни один из известных БПВП не способен препятствовать разрушению суставных поверхностей [15].
Наиболее значимым считают международное многоцентровое плацебо-контролируемое рандомизированное исследование по оценке эффективности и безопасности ЛФ в лечении ПА и псориаза, проведенное в 2004 г. (Treatment of Psoriatic Arthritis Study – TOPAS). В него были включены 190 человек с активным ПА и кожным псориазом. Активность процесса определялась на основании числа болезненных и припухших суставов, а также площади псориатического поражения кожи (более 3 болезненных и припухших суставов, более 3 % соответственно) [16, 17].
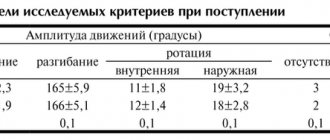
Результаты исследования были проанализированы у 186 человек (91 – в группе плацебо, 95 – в группе ЛФ). У большинства пациентов отмечалась предшествующая неэффективность одного, у нескольких больных четырех БПВП, включая метотрексат. В то же время почти половина включенных в исследование пациентов никогда не принимали БПВП. ЛФ назначали в нагрузочной дозе 100 мг/сут в течение 3 дней, далее по 20 мг/сут до 24 недель. Все пациенты были сопоставимы по полу, возрасту, расе, длительности заболевания. Частота отдельных клинических вариантов ПА была одинакова в обеих группах, кроме мутилирующего ПА, который чаще встречался в группе плацебо (см. таблицу).
Первичная оценка эффективности лечения проводилась через 24 недели на основании критериев PsARC. Вторичная – в те же сроки на основании критериев ACR 20, определения динамики показателей HAQ (индекс качества жизни) и HAQ DI (дерматологический индекс качества жизни), индекса PASI (изменение целевой бляшки – target lesion) и отдельных параметров PsARC и ACR [1, 18].
Оригинальные критерии PsARC (Psoriatic Arthritis Response Criteria) предложены Сlegg D. и соавт. (1996) в исследовании по сравнительной оценке эффективности сульфасалазина и плацебо при ПА. В указанные критерии входят счет болезненных и припухших суставов, общая оценка активности ПА врачом и пациентом по
5-балльной шкале Likert [2, 6, 13]:
- счет болезненных суставов из 76 по 4-балльной шкале (от 0 до 3; максимально – 228 баллов);
- счет припухших суставов из 74 по 4-балльной шкале (от 0 до 3; максимально – 222 балла);
- общая оценка активности ПА врачом по 5-балльной шкале Likert: “отлично”, “хорошо”, “удовлетворительно”, “плохо”, “очень плохо”;
- общая оценка активности ПА больным по 5-балльной шкале Likert – “отлично”, “хорошо”, “удовлетворительно”, “плохо”, “очень плохо”.
Критерии ACR, модифицированные для ПА:
- количество болезненных суставов из 76;
- количество припухших суставов из 74;
- общая оценка активности ПА врачом по ВАШ (мм);
- общая оценка активности ПА пациентом по ВАШ (мм);
- оценка интенсивности боли в суставах за последнюю неделю пациентом по ВАШ (мм);
- HAQ (Health Assessment Questionnaire);
- уровни СРБ/СОЭ.
В исследовании TOPAS применялись критерии ACR 20: уменьшение на 20 % числа болезненных и припухших суставов и любых 3 из 5 последних показателей ACR.
Среди больных, получавших ЛФ, через 24 недели по критериям PsARC на терапию ответили достоверно больше пациентов, чем в группе плацебо: 59 (56/95) против 30 % (27/91).
По критериям ACR 20 через 24 недели в группе ЛФ на лечение ответили 36,3 % (29/80) больных, а в группе плацебо – 20 % (16/80). В группе ЛФ по сравнению с группой плацебо отмечалось значимое улучшение и по другим показателям вторичной оценки эффективности (компонентам ACR и PsARC): количеству припухших суставов (-4,4 ± 8,6 против -2,7 ± 9,7), счету припухших суставов (-6,8 ± 16,8 против -4,2 ± 13,6), количеству болезненных суставов (-5,6 ± 10,9 против -3,0 ± 12,3), счету болезненных суставов (-9,1 ± 21,0 против -4,6 ± 19,6). Также у больных, принимавших ЛФ, регистрировалось значимое улучшение показателей качества жизни: изменение счета HAQ составило -0,19 ± 0,51, в группе плацебо – -0,05 ± 0,46. Количество больных, отметивших улучшение при оценке активности заболевания по ВАШ, составило в группе ЛФ 52,6 %, а в группе плацебо 34,1 %.
Лечение ЛФ приводило к значимому уменьшению выраженности и активности псориаза: изменение индекса PASI в основной группе по сравнению с началом терапии составило -2,1 ± 5,9, а при применении плацебо – только -0,6 ± 6,1 (р = 0,003). Количество больных со снижением индекса PASI на 50 и 75 % на фоне лечения ЛФ составило 30,4 и 17,4 %, а в группе плацебо – 18,9 и 7,8 % соответственно.
В целом ЛФ удовлетворительно переносился больными. Нежелательные явления, потенциально связанные с приемом препарата, были зарегистрированы у 61 (63,5 %) пациента в группе ЛФ и у 37 (40,2 %) – в группе плацебо. Случаев респираторных инфекций или смерти больных зарегистрировано не было. Серьезные нежелательные явления наблюдались у 13,5 % пациентов в группе ЛФ и у 5,4 % – в группе плацебо. Наиболее частыми побочными реакциями были повышение уровней АЛТ и/или АСТ и нейтропения. Реже встречались диарея, головная боль, тошнота.
Исследование, проведенное в Институте ревматологии РАМН, посвящено оценке эффективности и переносимости ЛФ при ПА. Опубликованы результаты предварительного анализа данных 63 больных [19].
В исследование включены пациенты с активным ПА, что определялось наличием не менее пяти болезненных и пяти припухших суставов. Большинство больных, а именно 85 %, ранее принимали один или более БПВП (сульфасалазин, циклоспорин А, метотрексат). Пациенты получали ЛФ по стандартной схеме: нагрузочная доза по 100 мг/сут в течение 3 дней, далее по 20 мг/сут. Длительность лечения составляла 24 недели, оценка эффективности и переносимости терапии проводилась каждый месяц. Определяли количество болезненных и припухших суставов, проводили оценку активности ПА пациентом и врачом по ВАШ, оценку интенсивности боли пациентом по ВАШ, оценку активности ПА и псориаза пациентом и врачом по шкале Likert, определяли индекс PASI, пациенты самостоятельно заполняли опросник HAQ. Отмечено значимое уменьшение практически всех указанных параметров уже после первого месяца лечения. Показатели выраженности боли и оценки активности ПА больным улучшились начиная со 2-го и 3-го месяца лечения и в дальнейшем существенно не менялись вплоть до конца исследования. К моменту завершения лечения по критериям PsARC на терапию ЛФ ответили 58 % (36/62) больных, по критериям ACR – 55 % (34/62).
В исследовании впервые проанализирован ответ на терапию ЛФ у больных с различной давностью заболевания: менее 3 лет (10 пациентов), от 3 до 10 лет (29), более 10 лет (24). Оказалось, что у больных с небольшой давностью ПА положительная динамика отмечалась только в отношении числа припухших суставов и счета HAQ, в двух других группах через 6 месяцев наблюдалось значимое улучшение практически всех исследуемых показателей. Количество пациентов, ответивших на лечение ЛФ по критериям PsARC и ACR, было в указанных группах одинаковым и не зависело от длительности ПА.
Уровень CPБ (мг/л) достоверно снизился уже к третьему месяцу применения ЛФ. Данная тенденция сохранилась и к 6-му месяцу терапии. Показатель СОЭ существенно не менялся в течение всего срока наблюдения, несмотря на улучшение всех основных показателей клинической активности ПА. Этот факт подтверждает существующее мнение о диссоциации при этом заболевании клинической и лабораторной активности, а также отсутствии адекватных для ПА методов оценки последней.
Интересные данные получены в отношении влияния ЛФ на выраженность псориаза. В отличие от исследования TOPAS анализ динамики PASI не выявил положительного влияния ЛФ на тяжесть и распространенность псориаза, более того, у 14 (22 %) больных зарегистрировано обострение кожного процесса.
Качество жизни оценивали на основании изменения общего счета HAQ через 3 и 6 месяцев от начала терапии. У 30 (48 %) пациентов на фоне лечения отмечалось уменьшение общего счета HAQ на 0,5, что считается клинически значимым.
Переносимость терапии ЛФ в целом была удовлетворительной. Частота и выраженность побочных явлений не отличались от таковых, описанных другими авторами. Нежелательные реакции как причина преждевременной отмены ЛФ зарегистрированы у 13 (21 %) пациентов. К их числу относились аллергический дерматит, тяжелое обострение псориаза, сопровождавшееся изъязвлением бляшек и присоединением вторичной инфекции, повышение более чем в 2 раза уровня печеночных ферментов, фурункулез, усиление выпадения волос, оссалгии.
Представленные выше результаты контролируемых, неконтролируемых и наблюдательных исследований свидетельствуют о том, что ЛФ способствует ослаблению симптомов ПА и псориаза, улучшает качество жизни пациентов, включая те случаи, когда предшествующее применение БПВП было неэффективным. Положительное воздействие как на проявления воспаления в суставах, так и на кожу позволяет ЛФ занимать достойное место в базисной противовоспалительной терапии ПА.
Противопоказания к применению препарата Лефлуномид
Гиперчувствительность к лефлуномиду, печеночная недостаточность, тяжелый иммунодефицит (в том числе СПИД), нарушение костномозгового кроветворения (анемия, лейкопения или тромбоцитопения, не связанные с ревматоидным артритом), тяжелые инфекции, умеренная или тяжелая почечная недостаточность, тяжелая гипопротеинемия (в том числе при нефротическом синдроме), период беременности и кормления грудью, женщины репродуктивного возраста (не использующие контрацептивы в период лечения лефлуномидом и пока плазменный уровень активного метаболита выше 0,02 мг/л), возраст до 18 лет.
Побочные эффекты препарата Лефлуномид
Со стороны сердечно-сосудистой системы: повышение АД. Со стороны ЖКТ: диарея, тошнота, рвота, анорексия, эрозивно-язвенные поражения слизистой оболочки полости рта (афтозный стоматит, изъязвление губ), абдоминальная боль, повышение активности печеночных трансаминаз, особенно АлАТ, реже γ-глутаминтрансферазы, ЩФ, гипербилирубинемия, гепатит, холестастатическая желтуха, печеночная недостаточность, острый некроз печени. Со стороны опорно-двигательного аппарата: тендовагинит; разрыв связок. Со стороны кожных покровов: усиленное выпадение волос, экзема, сухость кожи. Аллергические реакции: сыпь (в том числе макулопапулезная сыпь), зуд кожи; крапивница, мультиформная эритема, злокачественная экссудативная эритема (синдром Стивенса — Джонсона), токсический эпидермальный некролиз (синдром Лайелла); анафилактические/анафилактоидные реакции. Со стороны органов кроветворения: лейкопения, анемия, незначительная тромбоцитопения (тромбоциты менее 100 000/мкл), эозинофилия, панцитопения; менее 0,01% — агранулоцитоз. Лабораторные показатели: незначительная гиперлипидемия, гипоурикемия, повышение активности ЛДГ и КФК, незначительная гипофосфатемия. Прочие: обратимое снижение концентрации спермы, общего количества сперматозоидов и их подвижности; менее 0,01% — развитие тяжелых инфекций и сепсиса.
Особые указания по применению препарата Лефлуномид
Препарат должен назначаться после тщательного медицинского обследования специалистами, имеющими необходимый опыт лечения ревматоидного артрита. Режим дозирования препарата при ХПН легкой степени не определен. Перед началом лечения необходимо помнить о возможном увеличении количества побочных эффектов у пациентов, получавших ранее базисные препараты для лечения ревматоидного артрита, обладающие гепато- и гематотоксическими действиями. Активный метаболит лефлуномида — А771726 характеризуется длительным периодом полувыведения — 1–4 нед. Могут возникнуть серьезные нежелательные эффекты (например гепатотоксичность, гематотоксичность или аллергические реакции), даже при прекращении лечения лефлуномидом. Поэтому при возникновении подобных случаев токсичности или при переходе к приему другого базисного препарата (например метотрексата) после лечения лефлуномидом необходимо проводить процедуру «отмывания»: колестирамин — 8 г 3 раза в сутки в течение 11 дней; в качестве альтернативы — 50 г активированного угля, измельченного в порошок, 4 раза в сутки в течение 11 дней. Сообщалось о редких случаях развития тяжелого поражения печени, в отдельных случаях с летальным исходом, при лечении лефлуномидом, большинство которых наблюдалось в первые 6 мес лечения. Хотя не установлена причинная взаимосвязь этих нежелательных явлений с лефлуномидом, и в большинстве случаев имелось несколько факторов риска, необходимо точно выполнять рекомендации по наблюдению пациентов в процессе лечения. Необходим контроль активности АлАТ перед началом терапии, а затем каждый месяц в течение первых 6 мес лечения, с последующим контролем 1 раз каждые 2–3 мес. Рекомендации по коррекции режима дозирования или прекращению приема препарата в зависимости от выраженности и стойкости повышения уровня АлАТ: при подтвержденном превышении верхней границы нормы АлАТ в 2–3 раза — снижение дозы с 20 до 10 мг/сут (возможно продолжение приема лефлуномида при условии тщательного контроля этого показателя); если 2-, 3-кратное превышение верхней границы нормы АлАТ сохраняется или если имеется подъем уровня АлАТ, превышающий верхнюю границу нормы более чем в 3 раза, прием лефлуномида должен быть прекращен и начата процедура «отмывания». В период лечения рекомендуется воздержаться от приема этанола (повышение риска гепатотоксичности). Полный клинический анализ крови, включая определение лейкоцитарной формулы и количества тромбоцитов, необходимо проводить до начала лечения, а также каждые 2 нед в течение первых 6 мес лечения и каждые 8 нед после завершения лечения. У больных с ранее имевшей место анемией, лейкопенией и/или тромбоцитопенией, а также у больных с нарушениями функции костного мозга или с риском развития таких нарушений возрастает опасность возникновения гематологических нарушений. При возникновении подобного рода явлений следует использовать процедуру «отмывания» для снижения уровня А771726 в плазме крови. При развитии тяжелой гематотоксичности необходимо прекратить прием лефлуномида и любого другого сопутствующего препарата, угнетающего костномозговое кроветворение, и начать процедуру «отмывания». В случае развития язвенного стоматита следует прекратить прием лефлуномида. Сообщалось об очень редких случаях возникновения синдрома Стивенса — Джонсона или токсического эпидермального некролиза у пациентов, получавших лефлуномид. В случае возникновения кожных и/или слизистых реакций необходимо отменить прием лефлуномида и любого другого связанного с ним препарата и немедленно начать процедуру «отмывания» (в подобных случаях оно имеет существенное значение), повторное назначение противопоказано. Препараты, подобные лефлуномиду и обладающие иммунодепрессивными свойствами, повышают риск развития различных инфекций. Возникшие инфекционные заболевания протекают, как правило, тяжело и требуют раннего и интенсивного лечения. При возникновении тяжелого инфекционного заболевания необходимо прервать лечение лефлуномидом и начать процедуру «отмывания». Необходимо тщательно наблюдать за больными с выраженной туберкулиновой реактивностью из-за риска реактивации туберкулеза. Перед началом лечения лефлуномидом и периодически после его начала следует контролировать уровень АД. Отсутствуют экспериментальные данные о риске фетотоксичности при использовании лефлуномида мужчинами. Для максимального уменьшения возможного риска мужчинам при планировании потомства необходимо прекратить прием лефлуномида и использовать колестирамин по 8 г 3 раза в сутки в течение 11 дней или 50 г измельченного в порошок активированного угля 4 раза в день в течение 11 дней. Мужчины, получающие лечением лефлуномидом, должны быть предупреждены о возможном фетотоксическом действии препарата и о необходимости использовать адекватные средства контрацепции. Необходимо убедиться в отсутствии беременности до начала лечения лефлуномидом. В случае подозрения на наступление беременности необходимо незамедлительно сообщить об этом врачу. Врач должен обсудить с больной возможный риск, которому подвергается данная беременность. Быстрое снижение уровня содержания активного метаболита в крови с помощью процедуры «отмывания» препарата при подозрении на беременность поможет снизить риск, которому подвергается плод. В случае если женщина, принимающая лефлуномид, хочет забеременеть, рекомендуется следовать одной из ниже указанных процедур, чтобы удостовериться в том, что плод не подвержен воздействию токсичных концентраций А771726 (контрольная концентрация ниже 0,02 мг/л). Период ожидания: допускается, что концентрация А771726 в плазме крови может быть выше 0,02 мг/л в течение длительного периода. Предполагается, что концентрация может стать ниже 0,02 мг/л через 2 года после прекращения лечения лефлуномидом. После этого необходимо измерить концентрацию А771726 в плазме крови как минимум через 14 дней. Если величина обоих измерений ниже 0,02 мг/л, риск тератогенного действия отсутствует. Далее следует процедура «отмывания». Независимо от выбранной процедуры «отмывания» необходимо провести проверку двумя отдельными тестами с интервалом как минимум в 14 дней. Оплодотворение возможно через 1,5 мес после установления концентрации активного метаболита ниже 0,02 мг/л. Необходимо воздерживаться от зачатия в течение 2 лет после прекращения лечения лефлуномидом. Если период ожидания примерно в 2 года при надежной контрацепции кажется необоснованным, можно провести процедуру «отмывания» в профилактических целях. Возможно снижение контрацептивной активности пероральных противозачаточных средств в результате процедуры «отмывания» с колестирамином или активированным углем. Рекомендуется использовать альтернативные методы контрацепции. В эксперименте показано, что лефлуномид и его метаболиты проникают в грудное молоко.
Купить Лефлуномид Канон таблетки покрытые оболочкой 20мг №30 в аптеках
Инструкция по применению
Лефлуномид таб п.о 20мг №30
Лекарственные формы таблетки 10мг таблетки 20мг Синонимы Арава Лефлайд Лефлуномид Элафра Группа Противовоспалительные средства разных групп Международное непатентованное названиеЛефлуномид Состав Активное вещество: лефлуномид 10 мг. Производители Канонфарма продакшн (Россия) Фармакологическое действиеФармакодинамика Лефлуномид принадлежит к классу базисных противоревматических препаратов и обладает антипролиферативными, иммуномодулирующими, иммуносупрессивными и противовоспалительными свойствами. Активный метаболит лефлуномида А771726 ингибирует фермент дегидрооротатдегидрогеназу и обладает антипролиферативной активностью. А771726 в условиях in vitro тормозит вызванную митогенами пролиферацию и синтез дезоксирибонуклеиновой кислоты (ДНК) Т-лимфоцитов. Антипролиферативная активность А771726 проявляется, по-видимому, на уровне биосинтеза пиримидина, поскольку добавление в клеточную культуру уридина устраняет тормозящее действие метаболита А771726. С использованием радиоизотопных лигандов показано, что А771726 избирательно связывается с ферментом дегидрооротатдегидрогеназой, чем объясняется его свойство тормозить этот фермент и пролиферацию лимфоцитов на стадии G1. Пролиферация лимфоцитов является одним из ключевых этапов развития ревматоидного артрита. Одновременно А771726 тормозит экспрессию рецепторов к интерлейкину-2 (СВ-25) и антигенов ядра Ki-67 и PCNA, связанных с клеточным циклом. Терапевтическое действие лефлуномида было показано на нескольких экспериментальных моделях аутоиммунных заболеваний, включая ревматоидный артрит. Лефлуномид уменьшает симптомы и замедляет прогрессирование поражения суставов при активной форме ревматоидного артрита. Терапевтический эффект обычно проявляется через 4 — 6 недель и может нарастать в дальнейшем на протяжении 4 — 6 месяцев. Фармакокинетика Лефлуномид быстро превращается в свой активный метаболит А771726 (первичный метаболизм в кишечной стенке и печени). В плазме, моче или кале были замечены лишь следовые количества неизмененного лефлуномида. Единственным определяемым метаболитом является А771726, ответственный за основные свойства препарата in vivo. При приеме внутрь абсорбируется от 82 до 95 % препарата. Максимальные плазменные концентрации А771726 определяются от 1 до 24 часов после однократно принятой дозы. Лефлуномид может приниматься вместе с пищей. Из-за очень длительного периода полувыведения (Т1/2) А771726 (около 2 недель) использовалась нагрузочная доза 100 мг в день в течение 3-х дней. Это позволило быстро достигнуть равновесного состояния плазменной концентрации А771726. Без нагрузочной дозы для достижения равновесной концентрации потребовался бы 2-х месячный прием препарата. В исследованиях с многократным применением препарата фармакокинетические параметры А771726 были дозозависимыми в диапазоне доз от 5 до 25 мг. В этих исследованиях клинический эффект был тесно связан с плазменной концентрацией А771726 и суточной дозой лефлуномида. При дозе 20 мг в сутки средние плазменные концентрации А771726 при равновесном состоянии имели значение 35 мкг/мл. В плазме происходит быстрое связывание А771726 с альбуминами. Несвязанная фракция А771726 составляет примерно 0,62 %. Связывание А771726 более вариабельно и несколько снижается у больных ревматоидным артритом или хронической почечной недостаточностью. Лефлуномид метаболизируется до одного главного (А771726) и нескольких второстепенных метаболитов, включая 4-трифлюорометилаланин. Биотрансформация лефлуномида в А771726 и последующий метаболизм самого А771726 контролируются несколькими ферментами и происходят в микросомальных и других клеточных фракциях. Исследования взаимодействия с циметидином (неспецифическим ингибитором цитохрома Р450) и рифампицином (неспецифическим индуктором цитохрома Р450) показали, что in vivo СYP-энзимы вовлечены в метаболизм лефлуномида только в незначительной степени. Выведение А771726 из организма медленное и характеризуется клиренсом 31 мл/час. Лефлуномид выводится с фекалиями (вероятно, за счет билиарной экскреции) и с мочой. (Т1/2) составляет около 2 недель. Фармакокинетика А771726 у пациентов, находящихся на хроническом амбулаторном перитонеальном диализе (ХАПД), подобна таковой у здоровых добровольцев. Более быстрое выведение А771726 наблюдается у пациентов, находящихся на гемодиализе, что связано не с экстракцией препарата в диализат, а с вытеснением его из связи с белком. Хотя клиренс А771726 увеличивается приблизительно в 2 раза, конечный (Т1/2) является подобным таковому у здоровых лиц, так как одновременно увеличивается объем распределения. Данные о фармакокинетике препарата у больных с печеночной недостаточностью отсутствуют. Фармакокинетические характеристики у больных моложе 18 лет не изучались. У больных пожилого возраста (65 лет и старше) фармакокинетические данные примерно соответствуют средней возрастной группе. Побочное действиеСо стороны сердечно-сосудистой системы. Часто: умеренное повышение артериального давления; редко: выраженное повышение артериального давления; частота неизвестна: стенокардия, мигрень, ощущение сердцебиения, тахикардия, варикозное расширение вен, васкулит, вазодилатация. Со стороны желудочно-кишечного тракта. Часто: диарея, тошнота, рвота, заболевания слизистой ротовой полости (например, афтозный стоматит, изъязвление губ), боли в брюшной полости; нечасто: нарушение вкусовых ощущений; очень редко: панкреатит; частота неизвестна: гингивит, кандидоз ротовой полости, эзофагит, гастрит, гастроэнтерит, диспепсия, колит, запор, метеоризм, мелена. Со стороны гепато-билиарной системы. Часто: повышение активности «печеночных» трансаминаз (аланинаминотрансферазы (АЛТ), гамма-глутамилтранспептидазы (ГГТ), щелочной фосфатазы (ЩФ), гипербилирубинемия; редко: гепатит, холестаз, желтуха, холелитиаз; очень редко: тяжелые поражения печени (включая печеночную недостаточность, острый некроз печени), которые могут быть фатальными. Со стороны органов дыхания. Часто: респираторные инфекции верхних дыхательных путей, кашель; редко: интерстициальный легочный процесс (включая интерстициальную пневмонию и легочный фиброз) с возможным летальным исходом; частота неизвестна: астма, одышка, носовое кровотечение. Нарушения обмена веществ и питания. Часто: повышение креатинфосфокиназы (КФК); нечасто: гипокалиемия, гиперлипидемия, гипофосфатемия; редко: повышение уровня лактатдегидрогеназы; частота неизвестна: гипоурикемия, сахарный диабет, гипертиреоидизм, периферические отеки. Со стороны нервной системы. Часто: головная боль, головокружение, парестезии; нечасто: беспокойство; очень редко: периферическая нейропатия; частота неизвестна: тревожность, депрессия, сухость слизистой оболочки ротовой полости, нарушения сна, невралгия, неврит, повышенное потоотделение. Со стороны опорно-двигательного аппарата. Часто: тендовагинит; нечасто: разрыв сухожилий; частота неизвестна: артралгия, синовит, мышечные спазмы, артроз, некроз кости, бурсит, миалгия. Со стороны кожи и подкожной клетчатки. Часто: усиленное выпадение волос, алопеция, экзема, кожная сыпь (в том числе макулопапулезная), кожный зуд, сухость кожи; нечасто: крапивница; очень редко: токсический эпидермальный некролиз (синдром Лайелла), мультиформная эритема, синдром Стивенса-Джонсона; частота неизвестна: акне, контактный дерматит, грибковый дерматит, изменение цвета волос, простой герпес, опоясывающий лишай, поражение ногтей, нарушение пигментации кожи, изъязвление кожи. Со стороны иммунной системы. Часто: аллергические реакции; очень редко: серьезные анафилактические/анафилактоидные реакции, ангионевротический отек. Инфекции и инвазии. Редко: тяжелые инфекции (включая оппортунистические и сепсис), которые могут быть фатальными. Повышен риск возникновения инфекционных заболеваний, в частности, ринита, бронхита и пневмонии. Система кроветворения и лимфатическая система. Часто: лейкопения (лейкоциты > 2000/мкл); нечасто: анемия, тромбоцитопения легкой степени (тромбоциты > 100 000/мкл); редко: панцитопения (по видимому за счет антипролиферативного действия), эозинофилия, лейкопения (лейкоциты < 2000/мкл); очень редко: агранулоцитоз. Недавнее, сопутствующее или последующее использование потенциально миелотоксичных агентов может быть ассоциировано с большей степенью риска гематологических эффектов. Со стороны репродуктивной системы. Частота неизвестна: незначительное снижение концентрации спермы, общего количества сперматозоидов и их подвижности. Со стороны почек и мочевыводящей системы. Частота неизвестна: инфекции мочевыводящей системы, почечная недостаточность, альбуминурия, цистит, дизурия, гематурия, поражение предстательной железы, учащенное мочеиспускание, вагинальный кандидоз. Со стороны органов чувств. Частота неизвестна: нечеткость зрительного восприятия, катаракта, конъюнктивит, нарушения вкуса. Общие. Часто: анорексия, потеря массы тела (обычно незначительная), астения; Частота неизвестна: лихорадка, слабость. Прочее. Риск возникновения злокачественных, особенно лимфопролиферативных, заболеваний увеличивается при использовании некоторых иммунодепрессивных препаратов. Показания к применениюКак базисное средство для лечения взрослых пациентов с активной формой ревматоидного артрита с целью уменьшения симптомов заболевания и задержки развития структурных повреждений суставов; Активная форма псориатического артрита. Противопоказания Гиперчувствительность к лефлуномиду или любому другому компоненту препарата; нарушения функции печени; тяжелый иммунодефицит (в том числе, синдром приобретенного иммунодефицита); значительные нарушения костномозгового кроветворения или выраженная анемия, лейкопения или тромбоцитопения в результате других причин (кроме ревматоидного артрита); тяжелые, неконтролируемые инфекции; умеренная или тяжелая почечная недостаточность (клиренс креатинина менее 60 мл/мин, ввиду малого опыта клинического наблюдения); тяжелая гипопротеинемия (например, при нефротическом синдроме); у беременных или женщин детородного возраста, не пользующихся методами надежной контрацепции, в период лечения лефлуномидом и до тех пор, пока плазменный уровень активного метаболита остается выше 0,02 мг/л. Беременность должна быть исключена перед началом лечения лефлуномидом; в период грудного вскармливания (см. раздел «Применение во время беременности и в период грудного вскармливания»); детский возраст (младше 18 лет), в связи с отсутствием данных об эффективности и безопасности. Мужчины, получающие лечение лефлуномидом, должны быть предупреждены о возможном фетотоксическом действии препарата (связанном с его возможным влиянием на сперматозоиды отца) и о необходимости применения надежных средств контрацепции. Способ применения и дозировкаЛечение лефлуномидом должно начинаться под наблюдением врача, имеющего опыт лечения ревматоидного артрита и псориатического артрита. Таблетки необходимо принимать вне зависимости от приема пищи, глотать целиком, запивая достаточным количеством жидкости. Лечение лефлуномидом начинают с приема внутрь ударной дозы 100 мг один раз в день, в течение 3 дней. В качестве поддерживающей дозы при ревматоидном артрите рекомендуется прием от 10 мг до 20 мг лефлуномида один раз в день, при псориатическом артрите — 20 мг 1 раз в день. Терапевтический эффект обычно проявляется через 4 — 6 недель и может нарастать в дальнейшем до 4 — 6 месяцев. Не требуется никакой корректировки дозы для пациентов старше 65 лет. Передозировка Симптомы. Имелись сообщения о хронической передозировке у пациентов, получавших лефлуномид в дозе до пяти раз превышающую рекомендуемую суточную дозу, а также сообщения об острой передозировке у взрослых и детей. В большинстве случаев передозировки не сообщалось о развитии побочных реакций. Возникающие побочные реакции были сопоставимы с профилем безопасности лефлуномида. Наиболее часто наблюдавшимися побочными реакциями были диарея, боли в животе, лейкопения, анемия и повышение показателей тестов функционального состояния печени. Лечение. В случае передозировки или токсичности рекомендуется принимать колестирамин или активированный уголь, чтобы ускорить очищение организма. Колестирамин, принимаемый перорально по 8 г 3 раза в день в течение суток, снижает содержание А771726 в плазме примерно на 40 % через 24 часа, и на 49-65 % через 48 часов. Введение активированного угля (в виде суспензии) перорально или через желудочный зонд (50 г каждые 6 часов в течение суток) снижает концентрацию активного метаболита А771726 в плазме на 37 % через 24 часа, и на 48 % через 48 часов. Данные процедуры можно повторить по клиническим показаниям. Исследования с гемодиализом и ХАПД указывают, что А771726, главный метаболит лефлуномида, не способен выводиться путем диализа. Взаимодействие Усиление побочных эффектов может иметь место в случае недавнего или сопутствующего применения гепатотоксичных (включая алкоголь) или гематотоксичных и иммуносупрессивных препаратов или когда прием этих препаратов начинают после лечения лефлуномидом без процедуры «отмывания». У пациентов с ревматоидным артритом не было обнаружено никакого фармакокинетического взаимодействия между лефлуномидом (10 — 20 мг в сутки) и метотрексатом (10 — 25 мг в неделю). Пациентам, принимающим лефлуномид, не рекомендуется одновременный прием колестирамина или активированного угля, поскольку это приводит к быстрому и значительному снижению концентрации А771726 в плазме крови. Считается, что это обусловлено нарушением рециркуляции А771726 в печени и тонкой кишке и/или нарушением его желудочно-кишечного диализа. Если пациент уже принимает нестероидные противовоспалительные препараты (НПВП) и/или кортикостероиды, их можно продолжать принимать после начала лечения лефлуномидом. Ферменты, участвующие в метаболизме лефлуномида и его метаболитов, точно не известны. Исследование in vivo его взаимодействия с циметидином (неспецифическим ингибитором цитохрома Р450) показало отсутствие существенного взаимодействия. После сопутствующего введения однократной дозы лефлуномида субъектам, получавшим многократные дозы рифампицина (неспецифического индуктора цитохрома Р450), пиковые уровни А771726 возросли примерно на 40 %, тогда как площадь под кривой «концентрация-время» существенно не изменилась. Механизм данного эффекта не ясен. Исследования in vitro показали, что А771726 угнетает активность цитохрома Р4502С9 (CYP2C9). В клинических исследованиях не наблюдалось никаких проблем при совместном применении лефлуномида и НПВП, метаболизирующихся CYP2C9. С особой осторожностью следует применять лефлуномид вместе с другими препаратами, не являющимися НПВП, метаболизирующимися с помощью CYP2C9, такими как фенитоин, варфарин и толбутамид. Сообщалось об увеличении показателя протромбинового времени при одновременном применении лефлуномида и варфарина. В исследовании, в котором лефлуномид давали здоровым добровольцам женского пола совместно с трехфазными пероральными противозачаточными средствами, содержащими 30 мкг этинилэстрадиола, никакого снижения контрацептивного эффекта противозачаточных средств обнаружено не было, а фармакокинетика А771726 полностью соответствовала предусмотренному диапазону. В настоящее время нет сведений относительно совместного применения лефлуномида с противомалярийными препаратами, используемыми в ревматологии (например, хлорохина и гидроксихлорохина), препаратами золота (внутримышечно или перорально), D-пеницилламином, азатиоприном и другими иммунодепрессивными лекарственными средствами (за исключением метотрексата). Неизвестен риск, связанный с проведением комбинированной терапии, особенно при длительном лечении. Поскольку такого рода терапия может привести к развитию дополнительной или даже синергичной токсичности (например, гепато- или гематоксичности), комбинации данного препарата с другими базисными препаратами (например, метотрексатом) нежелательны. Недавнее сопутствующее или последующее использование потенциально миелотоксичных агентов может быть связано с большей степенью риска гематологических воздействий. Иммунодепрессанты повышают риск развития инфекций, а также злокачественных, особенно лимфопролиферативных заболеваний. Вакцинация. Нет никаких клинических данных относительно действенности и безопасности вакцинации в условиях лечения лефлуномидом. Тем не менее, не рекомендуется проводить вакцинацию живыми вакцинами. При планировании вакцинации живой вакциной следует учитывать длительный Т1/2 лефлуномида после отмены препарата. Особые указанияПрименение во время беременности и в период грудного вскармливания. Лефлуномид нельзя применять беременным или женщинам детородного возраста, которые не пользуются надежной контрацепцией при лечении лефлуномидом и определенное время после этого лечения. До начала лечения препаратом необходимо убедиться в отсутствии беременности. Пациенток необходимо информировать, что как только наступает задержка месячных или если есть иная причина предполагать наступление беременности, они должны незамедлительно сообщить об этом врачу, чтобы сделать тест на беременность. В случае положительного теста на беременность врач должен обсудить с больной возможный риск, которому подвергается данная беременность. Возможно, что быстрое снижение уровня содержания активного метаболита в крови с помощью описанной ниже процедуры выведения препарата поможет при первой задержке месячных снизить риск, которому подвергается плод со стороны лефлуномида. Женщинам, которые принимают лефлуномид и хотят забеременеть, рекомендуется следовать одной из нижеуказанных процедур, чтобы быть уверенными в том, что плод не будет подвержен воздействию токсичных концентраций А771726 (контрольная концентрация ниже 0,02 мг/л). Период ожидания. Можно ожидать, что концентрация А771726 в плазме крови может быть выше 0,02 мг/л в течение длительного периода. Считается, что его концентрация может стать меньше 0,02 мг/л через 2 года после прекращения лечения лефлуномидом. Первый раз концентрация А771726 в плазме крови измеряется по истечении двухлетнего периода ожидания. После этого необходимо измерить концентрацию А771726 в плазме крови, как минимум, через 14 дней. Если величина обоих измерений ниже 0,02 мг/л, не ожидается никакого тератогенного риска. Процедура «отмывания». Колестирамин 8 г вводится 3 раза в день в течение 11 дней; в качестве альтернативы 50 г активированного угля, измельченного в порошок, вводится 4 раза в день в течение 11 дней. Независимо от выбранной процедуры «отмывания» необходимо провести проверку двумя отдельными тестами с интервалом, как минимум, в 14 дней и подождать полтора месяца с того момента, когда концентрация препарата в плазме впервые будет зафиксирована ниже 0,02 мг/л, до момента оплодотворения. Необходимо проинформировать женщин детородного периода о том, что должно пройти 2 года после прекращения лечения лефлуномидом, прежде чем они могут пытаться забеременеть. Если 2-летний период ожидания при надежной контрацепции кажется необоснованным, можно посоветовать провести процедуру «отмывания» в профилактических целях. И колестирамин и активированный уголь могут влиять на абсорбцию эстрогенов и прогестогенов, поэтому надежные пероральные противозачаточные средства не дают стопроцентной гарантии в период «отмывания» с помощью колестирамина или активированного угля. Рекомендуется использовать альтернативные методы контрацепции. Исследования на животных показали, что лефлуномид или его метаболиты переходят в грудное молоко, поэтому женщины, кормящие грудью, не должны принимать препарат. Лефлуномид может применяться у пациентов только после тщательного медицинского обследования. Процедура «отмывания». Процедура «отмывания» проводится по следующей схеме: -колестирамин 8 г вводится 3 раза в день в течение 11 дней; -в качестве альтернативы — 50 г активированного угля, измельченного в порошок, вводится 4 раза в день в течение 11 дней. Влияние на способность управления транспортными средствами и механизмами. Прием препарата может сопровождаться головной болью, головокружением. В связи с этим пациентам, принимающим лефлуномид, следует проявлять осторожность при управлении опасными механическими средствами, в том числе автомобилем. Условия храненияХранить в сухом, защищенном от света, недоступном для детей месте при температуре не выше 25 С.
Взаимодействия препарата Лефлуномид
В настоящее время нет сведений относительно совместного применения лефлуномида с противомалярийными препаратами, используемыми в ревматологии (например хлорохином и гидроксихлорохином), препаратами золота (в/м или перорально), D-пеницилламином, азатиоприном и другими иммунодепрессивными средствами (за исключением метотрексата). Не известен риск, связанный с назначением комплексной терапии, особенно при длительном лечении. Поскольку такого рода терапия может привести к развитию дополнительной или даже синергичной токсичности (например гепато- или гематотоксичности), комбинации данного препарата с другими базисными препаратами (например метотрексатом) нежелательны. Недавнее, сопутствующее или последующее использование потенциально миелотоксичных агентов может быть связано с большей степенью риска гематологических воздействий. Иммунодепрессанты повышают риск развития инфекций, а также злокачественных, особенно лимфопролиферативных заболеваний. Следует соблюдать осторожность при назначении препаратов, метаболизирующихся под действием CYP 2C9 (фенитоин, варфарин, толбутамид), за исключением НПВП. Увеличение выраженности побочных явлений может иметь место в случае недавнего или сопутствующего применения гепатотоксичных или гематотоксичных препаратов или когда прием этих препаратов начинают после лечения лефлуномидом без периода «отмывания». У больных ревматоидным артритом не было обнаружено никакого фармакокинетического взаимодействия между лефлуномидом (10–20 мг/сут) и метотрексатом (10–25 мг/нед). Колестирамин или активированный уголь быстро и значительно снижают концентрацию А771726 в плазме крови. Возможно совместное применение с НПВП и ГКС. Ферменты, участвующие в метаболизме лефлуномида и его метаболитов, точно не известны. Клинически значимое взаимодействие с циметидином (неспецифическим ингибитором цитохрома Р450) отсутствует. После сопутствующего введения однократной дозы лефлуномида на фоне многократных доз рифампицина (неспецифического индуктора цитохрома Р450) максимальные концентрации А771726 возросли примерно на 40%, тогда как AUC существенно не изменилась. Механизм данного эффекта не ясен. Не наблюдается снижения контрацептивного эффекта при совместном применении с трехфазными пероральными противозачаточными средствами, содержащими 30 мкг этинилэстрадиола, при этом фармакокинетика А771726 не изменялась. Нет данных относительно эффективности и безопасности вакцинации на фоне лечения лефлуномидом (не рекомендуется проводить вакцинацию живыми вакцинами). Следует учитывать длительный период полувыведения препарата при планировании вакцинации живой вакциной после его отмены.
Терифлуномид (Teriflunomide)
Особые указания
Лечение должно проводиться под наблюдением врача, имеющего опыт лечения пациентов с рассеянным склерозом. До начала лечения следует провести следующие исследования: измерение АД, определение активности АЛТ, общий анализ крови, включая лейкоцитарную формулу и определение количества тромбоцитов в крови.
Во время лечения терифлуномидом следует регулярно контролировать следующие параметры: АД, активность АЛТ.
В случае появления новых симптомов и признаков (например, инфекции) во время лечения необходимо выполнить общий анализ крови, включая лейкоцитарную формулу, и определение количества тромбоцитов в крови
Терифлуномид медленно выводится из плазмы: концентрации в плазме достигают значений ниже 0,02 мг/л в среднем за 8 месяцев, хотя из-за индивидуальных отклонений в процессе выведения лекарственных веществ оно может продолжаться до 2-х лет. Выведение препарата можно ускорить посредством процедуры ускоренного выведения. Процедура ускоренного выведения может быть использована в любое время после прекращения приема терифлуномида.
У пациентов, принимавших терифлуномид, наблюдалось повышение активности ферментов печени. Эти нежелательные реакции происходили в основном в первые 6 месяцев лечения.
Пациенты с заболеваниями печени в анамнезе входят в группу риска ухудшения функции печени на фоне приема терифлуномида. В данной группе пациентов симптомы поражения печени следует тщательно мониторировать.
Терифлуномид необходимо назначать с осторожностью пациентам, злоупотребляющим алкоголем.
Поскольку терифлунамид характеризуется высокой степенью связывания с белками плазмы, в основном с альбумином, концентрация несвязанного терифлуномида в плазме может повышаться у пациентов с гипопротеинемией, например, при нефротическом синдроме. Терифлуномид не следует назначать пациентам с выраженной гипопротеинемией.
В случае повышения АД необходимо проводить соответствующую антигипертензивную терапию до и на фоне лечения терифлуномидом.
Начало лечения терифлуномидом необходимо откладывать у пациентов, имеющих серьезные активные инфекции, до полного выздоровления.
С учетом иммуномодулирующего эффекта терифлуномида, в случае развития у пациента серьезной инфекции, необходимо рассмотреть необходимость приостановки лечения препаратом, и перед возобновлением терапии выведения оценить возможные преимущества и риски. В связи с длительным T1/2 необходимо рассмотреть необходимость проведения ускоренной элиминации с помощью колестирамина или активированного угля.
Пациентам, имеющим положительный тест на туберкулез на скрининге, перед началом приема терифлуномида необходимо пройти соответствующее лечение.
На фоне терапии интерстициальные заболевания легких могут развиваться остро.
Легочные симптомы, такие как постоянный кашель и одышка, могут стать причиной прекращения терапии и проведения дальнейшего обследования. У пациентов с существующей анемией, лейкопенией и/или тромбоцитопенией, а также у пациентов с нарушенной функцией костного мозга или имеющих риск супрессии костномозгового кроветворения, риск гематологических заболеваний на фоне терапии терифлуномидом повышен. В случае развития указанных нежелательных реакций необходимо рассмотреть возможность применения процедуры ускоренного выведения для уменьшения концентрации терифлуномида в плазме. В случаях выраженных гематологических реакций, включая панцитопению, прием терифлуномида и любого другого миелосупрессирующего препарата должен быть прекращен. Необходимо рассмотреть целесообразность проведения процедуры ускоренного выведения.
В случае появления язвенного стоматита прием терифлуномида следует прекратить. Если при развитии реакций со стороны кожи и/или слизистых подозреваются серьезные генерализованные кожные реакции (синдром Стивена-Джонсона или токсичный эпидермальный некролиз — синдром Лайелла), прием терифлуномида и любых других препаратов, потенциально вызывающих подобные реакции, необходимо прекратить, а также следует немедленно начать процедуру ускоренного выведения. В таких случаях пациентам не следует вновь назначать терифлуномид. Если у пациента, принимавшего терифлуномид, диагностирована периферическая нейропатия, следует рассмотреть возможность прекращения приема терифлуномида и проведение процедуры ускоренного выведения. Применение живых ослабленных вакцин может быть связано с риском инфицирования и поэтому его следует избегать. Поскольку лефлуномид является исходным соединением для терифлуномида, совместный прием терифлуномида с лефлуномидом не рекомендован.
Переход на или с терифлуномида На основании клинических данных, относящихся к одновременному приему терифлуномида с интерфероном бета или с глатирамера ацетатом, можно сказать, что нет никакой необходимости в периоде ожидания при начале терапии терифлуномидом после интерферона бета или глатирамера ацетата, или при начале терапии интерфероном бета или глатирамера ацетатом после терифлуномида.
В связи с длительным T1/2 натализумаба одновременная экспозиция и, следовательно, одновременное воздействие на иммунную систему может произойти в случае начала терапии терифлуномидом в течение 2-3 месяцев после прекращения приема натализумаба. Поэтому следует соблюдать меры предосторожности при переходе с терапии натализумабом на терифлуномид.
С учетом T1/2 финголимода необходим 6-недельный интервал без терапии для элиминации из организма циркулирующих веществ. От 1 до 2-х месяцев необходимо для возвращения количества лимфоцитов к норме после прекращения приема финголимода. Это может привести к сочетанному воздействию на иммунную систему. Поэтому следует соблюдать меры предосторожности при переходе с терапии финголимодом на терифлуномид.
При рассеянном склерозе медиана T1/2 была приблизительно 19 дней после повторяемых доз в 14 мг. Если принято решение об остановке лечения терифлуномидом в ходе интервала в 5 T1/2 (приблизительно 3.5 месяца, хотя у некоторых пациентов может быть и дольше), начало другой терапии приведет к одновременной экспозиции с терифлуномидом. Это может привести к аддитивному эффекту на иммунную систему, что требует обязательного соблюдения мер предосторожности.
Влияние на способность к управлению транспортными средствами и механизмами
При возникновении нежелательных явлений со стороны нервной системы, например, головокружения, следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности.
Передозировка препарата Лефлуномид, симптомы и лечение
Данных относительно передозировки лефлуномида или вызванной им интоксикации у человека нет. Показано назначение колестирамина или активированного угля. Колестирамин, принимаемый перорально по 8 г 3 раза в день в течение суток, снижает содержание А771726 в плазме крови примерно на 40% через 24 ч и на 49–65% через 48 ч. Введение активированного угля (в виде суспензии) перорально или через желудочный зонд (50 г каждые 6 ч в течение суток) снижает концентрацию активного метаболита А771726 в плазме на 37% через 24 ч и на 48% через 48 ч.
Список аптек, где можно купить Лефлуномид:
- Москва
- Санкт-Петербург