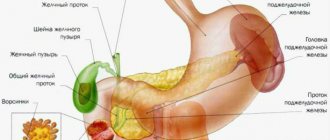
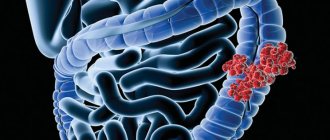
Слепая кишка – начальный отдел толстого кишечника. Она расположена в правой подвздошной области (справа внизу в брюшной полости) и благодаря своему строению сравнивается с вертикальным мешком. В нижней части слепой кишки находится червеобразный отросток.
В Юсуповской больнице созданы все условия для лечения больных раком слепой кишки:
- Палаты оснащены притяжно-вытяжной вентиляцией и кондиционерами, позволяющими обеспечить пациентам комфортный температурный режим;
- Врачи проводят обследование пациентов с помощью новейших аппаратов ведущих европейских и американских производителей;
- Для операций на слепой кишке хирурги используют современный инструментарий и оборудование;
- Онкологи виртуозно выполняют весь спектр известных сегодня оперативных вмешательств;
- Медицинский персонал обеспечивает профессиональный уход до и после операции;
- Врачи проводят противоопухолевую терапию новейшими химиотерапевтическими препаратами, зарегистрированными в РФ.
Пациенты в рамках научных исследований, которые проводятся в клинике, имеют возможность получать новейшие лекарственные средства. Рост злокачественного новообразования может начаться в любом отделе желудочно-кишечного тракта. Рак слепой кишки составляет примерно пятую часть всех онкологических заболеваний толстого кишечника.
Причины
Непосредственная причина рака слепой кишки – не распознанная иммунной системой и вовремя не уничтоженная клеточная мутация, вследствие чего запускается бесконечный цикл деления и роста опухолевых клеток. Злокачественные новообразования слепой кишки, по мнению экспертов Всемирной организации здравоохранения, могут развиваться под воздействием следующих провоцирующих факторов:
- Излишнего употребления красного мяса, прошедшего кулинарную обработку;
- Возрастных изменений в тканях и ослабления кишечной перистальтики;
- Наследственной предрасположенности;
- Хронических заболеваний и патологических состояний желудочно-кишечного тракта (воспалительных, язвенных, дискинетических, доброкачественных неопластических процессов);
- Экологических факторов;
- Присутствия и активности в организме онкогенных вирусов (папилломавируса человека и некоторых подтипов вируса герпеса);
- Курения.
Единой причины, по которой развивается опухоль слепой кишки, учёными до сегодняшнего дня не установлено.
Виды
Для рака слепой кишки применяется TNM классификация. В ней T обозначает размер опухоли, N – наличие поражения лимфатических узлов, M – наличие отдалённых метастазов. Заболевание протекает в 4 стадии:
- Стадия 0 характеризуется очень маленькими размерами опухоли, поражением только верхнего слоя стенки слепой кишки, отсутствием метастазов в регионарных лимфатических узлах;
- При первой стадии рака слепой кишки патологический процесс распространяется на второй и третий слой толстой кишки, однако не прорастает на внешнюю сторону кишечника, отсутствуют метастазы в лимфатических узлах;
- На II стадии злокачественная опухоль прорастает на внешнюю стенку слепой кишки, лимфоузлы не поражаются и метастазов не наблюдается;
- На третьей стадии заболевания опухоль начинает прорастать на близлежащие органы и ткани, поражаются лимфатические узлы, но отдалённых метастазов врачи не выявляют;
- На терминальной, четвёртой, стадии рака слепой кишки злокачественная опухоль начинает прорастать в прилегающие ткани и органы, при этом поражаются лимфатические узлы и выявляются отдалённые метастазы.
Выделяют следующие гистологические типы рака слепой кишки:
- Аденокарцинома развивается из эпителиальных клеток слизистой оболочки кишки;
- Перстневидноклеточный рак имеет вид пузырьков;
- Недифференцированный рак считается наиболее агрессивной формой злокачественного новообразования;
- Неклассифицируемый рак является злокачественной опухолью, которая не относится ни к одной из гистологических форм;
- Плоскоклеточный рак – опухоль слепой кишки, которая состоит из клеток плоского эпителия;
- Железисто-плоскоклеточный рак – новообразование, состоящее их плоского и железистого эпителия.
Аденокарцинома слепой кишки бывает экзофитной или эндофитной опухолью. Она может расти в просвет слепой кишки или прорастать все слои кишечной стенки. Опухоль часто прорастает в мочевой пузырь, матку, придатки, предстательную железу у мужчин, тонкий кишечник, брюшную стенку. Аденокарцинома дает метастазы наиболее часто в печень, редко в легкие, костную систему, мозг. Аденокарцинома бывает высокодифференцированная и низкодифференцированная. Клетки высокодифференцированной опухоли близки к здоровым клеткам, способны выполнять свои функции. Низкодифференцированная опухоль состоит из переродившихся клеток, неспособных выполнять свои функции. Благоприятный прогноз у пациентов с высокодифференцированными опухолями. Онкологи Юсуповской больницы устанавливают диагноз и назначают лечение, учитывая результаты гистологического исследования биологического материала, полученного во время биопсии.
Записаться на приём
ОПУХОЛИ ОБОДОЧНОЙ КИШКИ
12.11.12
Диагностика заболевания
Для диагностики опухолей ободочной кишки применяется рентгенологическое исследование (ирригоскопия), эндоскопическое исследование (колоноскопией), пальцевое и эндоскопическое исследование прямой кишки (ректороманоскопия).
Клинические проявления рака ободочной кишки
Клинические проявления рака ободочной кишки во многом зависят от места расположениязлокачественного новообразования, степени распространения опухолевого процесса и наличия осложнений, отягчающих течение основного заболевания.
Наиболее частые симптомы: боли в животе, нарушение моторно-эвакуаторной функции кишки клинически проявляющиеся чередованием запоров и поносов, патологические выделения с калом, изменение общего состояния больного и, наконец, пальпируемая через переднюю брюшную стенку опухоль.
Боли в животе – наиболее частый симптом рака ободочной кишки и отмечаются практически у 80% пациентов. В клинических наблюдениях при правосторонней локализации опухоли боли, как один из первых симптомов рака, встречались в 2-3 раза чаще, чем при раке левой половины. Этот факт объясняется нарушением двигательной функции: маятникообразное перемещению содержимого кишечника из тонкой кишки в слепую и обратно.
Спастические сокращения кишечника, проталкивающего каловые массы через частично перекрытый опухолью просвет кишки, вызывают болевые ощущения. Внутриопухолевое и перифокальное воспаление кишечной стенки, часто сопутствующее распадающимся инфицированным опухолям, усугубляет боль.
Опухоли ободочной кишки могут длительное время протекать без болевого синдрома и только при распространении новообразования за пределы кишечной стенки, при переходе на брюшину и окружающие органы появляются боли, интенсивность и периодичность которых может быть различной. В зависимости от локализации опухоли болевой синдром может симулировать хронические аппендицит, холецистит, язвенную болезнь желудка и 12-перстной кишки, хронический аднексит.
Для злокачественных новообразований правой половины ободочной кишки характерно сочетание болевого синдрома, гипертермической реакции (повышение температуры), лейкоцитоза и ригидности (напряженность) мышц передней брюшной стенки. Клинические проявления заболевания напоминают деструктивный аппендицит, и правильный диагноз удается установить только во время ревизии органов брюшной полости в процессе хирургического вмешательства. Анализ клинического течения рака правой половины ободочной кишки показал, что почти в 60% случаев наличие опухоли сопровождается болями в правых отделах живота, кишечными расстройствами, гипертермией, наличием симптомов интоксикации и анемией.
Такое сочетание клинических симптомов является характерным для токсико-анемической формы рака ободочной кишки.
Нарушения моторно-эвакуаторной функции толстой кишки приводят к застою кишечного содержимого и обусловливают такие симптомы дискомфорта как чувство тяжести в животе, потерю аппетита, тошноту. Важную роль в развитии кишечного дискомфорта играют рефлекторные функциональные нарушения других органов пищеварительной системы. Всасывание продуктов распада воспаленной слизистой оболочкой, изменение нормального состава кишечной микрофлоры, сопровождающееся появлением патогенных штаммов, выделяющих экзо- и эндотоксинов, приводит к развитию синдрома эндогенной интоксикации. Функциональные расстройства желудочно-кишечного тракта у больных раком ободочной кишки проявляются нарушением пассажа содержимого, запором, вздутием живота, приступообразными болями.
Скопление каловых масс выше опухоли сопровождается усилением процессов гниения и брожения, приводя к вздутию живота с задержкой стула и газов.
В тех случаях, когда течение опухолевого процесса осложняется развитием явлений кишечной непроходимости, в клинической картине больных раком ободочной кишки преобладают такие симптомы как вздутие живота с затрудненным отхождением кала и газов, тошнота, отрыжка, рвота. Боли носят приступообразный характер. По мнению ряда авторов при локализации злокачественной опухоли в левой половине толстой кишки стенозирующий характер опухолевого роста приводит к сужению просвета кишки, вследствие чего каловые массы, скапливаясь выше опухоли могут пальпироваться через брюшную стенку и иногда ошибочно принимаются за опухоль.
Одними из довольно частых и сравнительно ранних клинических проявлений рака ободочной кишки являются патологические выделения из прямой кишки. К таковым относят слизь, кровь, гной, опухолевые массы и др. Наиболее часто патологические примеси в кале отмечены при левосторонней локализации опухоли толстой кишки, нежели при расположении опухоли в правой половине (62,4% и 18,5% соответственно). Значительно реже отмечены выделения гноя, фрагментов опухолевых масс, свидетельствующие о присоединении воспалительного процесса, приводящего к распаду опухоли, инфицированию и образованию перифокальных и внутриопухолевых гнойников. Во всяком случае, наличие таких выделений довольно часто свидетельствует о распространенном опухолевом процессе.
Одним из симптомов, свидетельствующих о далеко зашедшем опухолевом процессе, является пальпируемая через брюшную стенку опухоль. Частота этого симптома колеблется от 40 до 60%.
Любой из перечисленных выше симптомов (боль, кишечные расстройства, наличие патологических примесей в стуле) может присутствовать при любом заболевании кишечника, не только опухоли. Анализ клинического течения рака ободочной кишки свидетельствует о значительном проценте диагностических ошибок (до 35%), приводящих к госпитализации в общетерапевтические и инфекционные клиники для лечения анемии неясной этиологии, дизентерии и др. Высоким остается процент больных, госпитализируемых в общехирургические стационары по экстренным показаниям на высоте обтурационной кишечной непроходимости.
Выделяются следующие клинические формы рака ободочной кишки:
- токсико-анемическая, характеризующаяся различной степенью выраженности анемией, общими симптомами, интоксикацией;
- обтурационная – характеризующаяся появлением признаков нарушения проходимости кишечника и сопровождающаяся приступообразными болями в животе, урчанием и усиленной перистальтикой, задержкой стула и плохим отхождением газов;
- энтероколитическая форма, сопровождающаяся вздутием живота, чередованием поносов с запорами, наличием патологических примесей в кале, тупых, ноющих болей в животе;
- псевдовоспалительная форма, характеризующаяся малой выраженностью кишечных расстройств на фоне признаков воспалительного процесса в брюшной полости;
- опухолевая (атипичная) форма, для которой нехарактерны общие симптомы, нарушение проходимости кишечника, при пальпаторно определяемой опухоли в брюшной полости;
- диспептическая форма, характерными признаками которой являются симптомы желудочного дискомфорта (тошнота, отрыжка, чувство тяжести в эпигастральной области), сопровождающиеся болями, локализующимися преимущественно в верхнем этаже брюшной полости.
Необходимо подчеркнуть, что выделение клинических форм, в известной степени, условно и главным образом характеризует ведущий симптомокомплекс. Тем не менее, знание проявлений рака ободочной кишки позволяет заподозрить наличие опухоли даже в тех случаях, когда заболевание протекает с незначительно выраженными кишечными расстройствами.
Осложненные формы рака ободочной кишки
К осложнениям, довольно часто сопутствующим раку ободочной кишки, оказывающих непосредственное влияние на течение заболевания и прогноз опухолевого процесса относятся кишечная непроходимость различной степени выраженности, перифокальный воспалительный процесс, перфорация опухоли, кишечное кровотечение, а также распространение опухоли на окружающие органы и ткани.
По данным литературы, частота развития кишечной непроходимости у больных раком ободочной кишки составляет от 10 до 60%. Столь выраженные различия в частоте этого осложнения во многом обусловлены тем обстоятельством, что подавляющее большинство больных с осложненным течением опухолевого процесса попадают в скоропомощные хирургические стационары, а не в специализированные лечебные учреждения.
Клиническое течение заболевания во многом зависит от степени выраженности кишечной непроходимости. При декомпенсированной форме кишечной непроходимости (резкое вздутие живота с задержкой стула и газов, рвота, схваткообразные боли по всему животу на фоне выраженных расстройств метаболизма), показано экстренное хирургическое вмешательство, объем и характер которого зависит не только от локализации опухоли, но и от тяжести развившегося осложнения. В случаях компенсированной формы обтурационной кишечной непроходимости, довольно часто эффективными оказываются консервативные мероприятия, позволяющие подготовить больного к плановой операции.
Пассаж жидкого кишечного содержимого сохраняется при сужении просвета кишки до 0,8-1 см, при раке правой половины ободочной кишки явления илеуса (кишечной непроходимости) обычно возникают при больших размерах опухоли. По мере прогрессирования стеноза образуется расширение кишки выше опухоли, приводящее к скоплению каловых масс и появлению ноющих болей в животе, временами носящих схваткообразный и спастический характер.
При локализации опухоли в левых отделах ободочной кишки развитию кишечной непроходимости часто предшествуют запоры, чередующиеся с обильным зловонным жидким стулом. В случаях декомпенсированной кишечной непроходимости к расстройству функции органов желудочно-кишечного тракта довольно быстро присоединяются метаболические расстройства, приводящие к нарушению жизненно важных функций органов и систем.
Большую опасность при раке ободочной кишки представляют внутриопухолевые и перифокальные воспалительные процессы. Частота таких осложнений достаточно велика: от 12 до 35%.
Воспалительные изменения в опухоли, обусловленные наличием в кишечном содержимом большого количества вирулентных микроорганизмов, качественный и количественный состав которой изменяется при распаде опухолевой ткани, приводят к инфицированию и формированию воспалительных инфильтратов и гнойников.
В большинстве клинических наблюдений при гистологическом исследовании удаленных препаратов у больных с перифокальным воспалительным процессом отмечалось изъязвление опухоли и признаки острого гнойного воспаления с формированием абсцессов, некрозов и свищей в толще жировой ткани, строме опухоли или в лимфатических узлах.
Перфорация кишечной стенки и кровотечение из распадающейся опухоли – наиболее грозные осложнения этого заболевания. Длительный стаз кишечного содержимого на фоне хронической кишечной непроходимости в сочетании с трофическими расстройствами стенки кишки приводят к образованию пролежней и перфорации.
Наиболее неблагоприятной для прогноза является перфорация опухоли в свободную брюшную полость, приводящая к разлитому каловому перитониту. При перфорации отрезка кишки, лишенного брюшинного покрова, острый гнойный очаг формируется в забрюшинном пространстве. У ряда больных точечное перфорационное отверстие прикрывается сальником, либо расположенным рядом органом, приводя к образованию перифокального воспалительного процесса, распространяющегося на близлежащие органы и ткани. Перифокальное и внутриопухолевое воспаление, осложняющее течение основного заболевания с одной стороны, и перфорация опухоли ободочной кишки с другой, являются звеньями одного и того же патологического процесса, в основе которого лежит инфицирование пораженного отдела ободочной кишки условно патогенными штаммами микроорганизмов, проникающими через патологически измененную кишечную стенку.
Диагностика
Совершенствование методов клинического обследования больного с применением современной рентгенологической и эндоскопической техники, использование широкого арсенала скрининговых методов диагностики до последнего времени существенно не улучшило раннее выявление рака ободочной кишки. Более 70% больных раком ободочной кишки на момент госпитализации имели III и IV стадии заболевания. Только 15% из них обратились к специалисту в сроки до 2 месяцев с момента появления первых симптомов заболевания. Менее чем у половины из осмотренных больных диагноз был установлен в сроки до 2 месяцев от начала заболевания, а у каждого четвертого для выяснения характера заболевания потребовалось более полугода. Довольно часто встречающиеся диагностические ошибки приводили к выполнению необоснованных хирургических вмешательств, физиотерапевтических процедур, приводящих к диссеминации опухолевого процесса.
Диагноз рака ободочной кишки устанавливают на основании рентгенологического и эндоскопического исследований. Не менее важным методом физикального обследования больного является пальпация живота, позволяющая не только выявить опухоль в брюшной полости, но и оценить ее консистенцию размеры, мобильность.
По данным ряда авторов, в 60-70% случаев опухоль толстой кишки доступна пальпации.
Типы исследований
- Рентгенологическое исследование, наряду с колоноскопией, является ведущим в диагностике рака ободочной кишки.
- Ирригоскопия позволяет получить информацию о локализации новообразования, установить протяженность поражения, определить форму роста опухоли, оценить ее подвижность, а иногда – судить о взаимосвязи с другими органами. При выполнении ирригоскопии возможно также выявить синхронные опухоли толстой кишки. Последнее обстоятельство важно еще и потому, что при стенозирующем характере роста новообразования эндоскопическое исследование не позволяет до операции оценить состояние вышележащих отделов толстой кишки.
- Эндоскопическое исследование, наряду с визуализацией злокачественной опухоли, позволяет получить материал для гистологического исследования, являющегося необходимым атрибутом предоперационной диагностики злокачественного новообразования.
- Наиболее простым и широко распространенным методом эндоскопического исследования толстой кишки является ректороманоскопия, при которой возможно оценить состояние нижнего отдела кишечной трубки. При выполнении ректороманоскопии исследователь оценивает состояние слизистой оболочки толстой кишки, сосудистый рисунок, наличие патологических примесей в просвете кишки, эластичность и подвижность кишечной стенки. При выявлении опухоли толстой кишки изучают ее размеры, внешний вид, консистенцию, подвижность при инструментальной пальпации, производят биопсию.
Определение степени распространения опухолевого процесса
Программа обследования больного до операции, кроме уже перечисленных традиционных методов, включает в себя специальные рентгенологические и радиоизотопные исследования.
В основе гематогенного метастазирования лежит процесс эмболизации раковыми клетками путей венозного оттока из органа, пораженного опухолевым процессом. Проникновение опухолевых клеток в венозные сосуды происходит в результате инвазии и разрушения опухолью стенки сосуда. Основная масса венозной крови у больных колоректальным раком по системе нижней и верхней брыжеечных вен поступает в воротную вену, что объясняет факт основной локализации отдаленных метастазов в печени.
Ультразвуковое исследование нашло широкое распространение для оценки степени распространения опухолевого процесса. Оно основано на принципе регистрации отраженной ультразвуковой волны от границ раздела тканей, отличающихся по плотности и строению. Обладая высокой разрешающей способностью и информативностью, ультразвуковое исследование практически безвредный диагностический метод, позволяющий визуализировать опухолевые узлы размерами 0,5-2,0 см.
Анатомо-топографическое строение печени, хорошее распространение в ней ультразвука обусловливает высокую информативность исследования. Важным является тот факт, что УЗИ помогает определить не только характер патологических изменений в печени, но и установить локализацию и глубину залегания очаговых изменений. При выполнении ультразвуковой томографии получается послойное изображение внутренней структуры печени и выявляются патологические объемные образования или диффузные изменения. УЗИ печени возможно повторять довольно часто без ущерба для организма больного, что позволяет оценивать результаты проводимого лечения.
Применение рентгеновской компьютерной томографии (КТ) в медицине способствовало значительному улучшению диагностики различных патологических состояний.
Компьютерная томография обладает следующими важными преимуществами перед другими методами обследования:
- представляет изображение анатомических структур в виде поперечного среза, исключая совмещение их изображений;
- обусловливает четкое изображение структур, незначительно отличающихся по плотности друг от друга, что является крайне важным для диагностики;
- представляет возможность для количественного определения плотности тканей на каждом участке изображения исследуемого органа для дифференциальной диагностики патологических изменений;
- имеет неинвазивный характер диагностического метода, безопасность и малая лучевая нагрузка на организм больного.
По данным исследователей, при анализе КТ-картины метастатических опухолей колоректального рака в 48% случаев опухолевые узлы содержали кальцинаты, а иногда выявляли тотальное обызвествление метастатических опухолей.
Радионуклеидные (изотопные) методы диагностики и оценки степени распространения колоректального рака в повседневной практической работе лечебных учреждений используются достаточно редко. Одним из таких методов является позитивная сцинтиграфия, основанная на использовании таких специфических препаратов, как галлий в виде цитратного комплекса, а также меченый изотопом индия блеомицин.
ЛЕЧЕНИЕ РАКА ОБОДОЧНОЙ КИШКИ
Выбор вида хирургического вмешательства и обоснование его объема
История хирургического лечения рака ободочной кишки насчитывает более 150 лет. Reybard в 1833 году выполнил первую резекцию ободочной кишки по поводу злокачественной опухоли с формированием межкишечного анастомоза. В России в 1886 году Е.В. Павлов выполнил первую резекцию слепой кишки по поводу ее злокачественной опухоли с анастомозом между восходящей ободочной и подвздошной кишкой. В отличие от манипуляций на тонкой кишке резекция толстой кишки, по мнению В. Шмидена (1910 г.) относится к числу самых ответственных хирургических вмешательств, связанных с существованием таких особенностей, как наличие патогенной микрофлоры в содержимом полого органа, отсутствие брыжейки в фиксированных участках ободочной кишки, более тонким слоем мышечной оболочки. Указанные особенности толстой кишки предопределяют повышенную требовательность к надежности формирования межкишечных анастомозов с учетом анатомических особенностей различных отделов ободочной кишки и адекватности кровоснабжения анастомозируемых сегментов.
Основным недостатком данных хирургических вмешательств является наличие хоть и временной колостомы – вывода кишки на переднюю брюшную стенку. Поэтому в специализированных онкопроктологических клиниках происходит переосмысление показаний к выполнению двухэтапных хирургических вмешательств, считая их оправданными лишь у ослабленных больных с явлениями декомпенсированной кишечной непроходимости.
Объем и характер хирургического вмешательства по поводу рака ободочной кишки зависит от ряда факторов, среди которых важнейшими являются локализация, степень распространения опухоли, наличие осложнений основного заболевания, а также общее состояние больного.
Выбор вида хирургического вмешательства при осложненном течении рака ободочной кишки
Большинство больных колоректальным раком поступают в специализированные лечебные учреждения в III и IV стадии опухолевого процесса. У многих из них отмечаются различные осложнения (обтурационная форма кишечной непроходимости, перфорация опухоли, кровотечение и перифокальный воспалительный процесс), нередко требующие выполнения экстренного хирургического вмешательства.
Результаты оперативных вмешательств у больных с осложненным колоректальным раком в известной мере зависят от квалификации оперирующего хирурга, его способности оценить степень и выраженность патологического процесса, осложняющего течение основного заболевания, и учетом общего состояния больного.
При выборе вида хирургического вмешательства стремятся не только избавить больного от острого хирургического осложнения, но и при возможности выполнить радикальную операцию.
Одним из наиболее опасных осложнений рака ободочной кишки является перифокальное и внутриопухолевое воспаление, часто распространяющееся на окружающие ткани. Частота подобного осложнения достаточно высока и колеблется от 6% до 18%. Это осложнение проявляется клиникой острого воспаления и интоксикацией, а распространение процесса на соседние органы и окружающие ткани способствует образованию инфильтратов, абсцессов, флегмон. Нередко выраженный воспалительный процесс в опухоли и окружающих ее органах трактуют как опухолевую инфильтрацию, что является причиной неадекватного объема хирургического вмешательства.
Наличие перифокального и внутриопухолевого воспаления при раке ободочной кишки оказывает существенное влияние на выбор объема и характера хирургического вмешательства лишь в тех случаях, когда воспалительный процесс распространяется на окружающие органы и ткани, и вынуждает прибегать к выполнению комбинированных хирургических вмешательств.
Комбинированные операции при раке ободочной кишки
Расширение объема хирургического вмешательства, обусловленное распространением злокачественной опухоли на близлежащие органы и ткани увеличивает продолжительность операции, травму и кровопотерю. Выход опухоли за пределы кишечной стенки свидетельствует о далеко зашедшем неопластическом процессе, но отсутствие отдаленных метастазов, позволяет выполнить комбинированную операцию, которая, улучшая качество жизни больных, избавляет от тяжелых осложнений опухолевого процесса и создает реальные предпосылки для применения специфических методов противоопухолевого лечения.
Паллиативные хирургические вмешательства у больных раком ободочной кишки
Почти у 70% больных раком ободочной кишки в момент выполнения хирургического вмешательства устанавливают III и IV стадию заболевания, а у каждого третьего больного, из числа оперированных, диагностируют отдаленные метастазы, преимущественно в печень и легкие. Развитие кишечной непроходимости вынуждает прибегать к симптоматическим хирургическим вмешательствам – колостомии, формированию обходного анастомоза у больных с IV стадией заболевания. Однако, все больше хирургов при распространенном колоректальном раке отдают предпочтение паллиативной резекции или гемиколэктомии.
Паллиативная резекция ободочной кишки или гемиколэктомия существенно улучшает качество жизни, избавляя пациента от таких осложнений опухолевого процесса, как гнойно-септические осложнения, кровотечение, распад опухоли с образованием калового свища.
Сравнительный анализ непосредственных и отдаленных результатов лечения больных раком ободочной кишки, подвергшихся резекции или гемиколэктомии, независимо от того, носила ли операция радикальный или паллиативный характер, показал, что частота и характер послеоперационных осложнений были примерно одинаковымии.
Паллиативные хирургические вмешательства в объеме резекции или гемиколэктомии находят все больше сторонников и все чаще являются операцией выбора при метастатическом раке ободочной кишки. Этому способствовало снижение частоты послеоперационных осложнений и летальности, расширение показаний к резекции пораженных метастазами органов (печень, легкие). Определяя показания к выполнению паллиативных хирургических вмешательств в объеме резекции ободочной кишки или гемиколэктомии, учитывается как общее состояние больного, так и степень диссеминации опухоли.
Одним из важных факторов, оказывающих прогноз на течение заболевания у больных, подвергнутых резекции печени по поводу метастазов, является временной интервал между лечением по поводу первичной опухоли и выявлением метастазов в печень. Установлено, что чем больше продолжительность безрецидивного течения опухолевого процесса, тем благоприятнее прогноз хирургического лечения метастазов в печень.
При определении объема хирургического вмешательства по поводу метастатического колоректального рака важную роль играет изучение функционального состояния печени. Печеночная недостаточность сама по себе является одной из основных причин послеоперационной летальности при обширных резекциях печени. Печень является органом с большими компенсаторными возможностями. Достаточно 10-15% здоровой ее паренхимы для полноценного функционирования органа.
Важным вопросом для определения хирургической тактики является количество метастатических узлов в печени. Множественные узлы значительно ухудшают прогноз и являются одной из основных причин отказа от активной хирургической тактики. Однако, наличие множественных узлов, локализующихся в одной анатомической половине печени не являются противопоказанием к хирургическому лечения, хотя, конечно, прогноз у таких больных значительно хуже, чем при единственном и единичных (2-3 узла) метастазах.
Комбинированное лечение рака ободочной кишки
Причины неудач оперативного лечения больных аденокарциномой ободочной кишки – местные рецидивы и отдаленные метастазы. В отличие от рака прямой кишки, при этом заболевании местные рецидивы встречаются относительно редко, а преобладают метастазы в печень. У больных с III стадией рака ободочной кишки местные рецидивы встречаются в 7% случаев, а отдаленные метастазы – в 20%. Возникновение этих неблагоприятных вторичных опухолевых образований обусловлено диссеменацией опухолевых клеток во время операции. Повысить абластичность оперативных вмешательств позволяет предоперационная лучевая терапия, которая в последнее время стала внедряться в практическую деятельность онкопроктологических клиник.
В зависимости от последовательности применения ионизирующего излучения и оперативного вмешательства различают пред-, после- и интраоперационную лучевую терапию.
Предоперационная лучевая терапия
В зависимости от целей, с которыми назначается предоперационная лучевая терапия можно выделить две основные ее формы:
- облучение операбельных форм рака ободочной кишки;
- облучение неоперабельных (местно-распространенных) или сомнительно операбельных форм опухолей.
Гибель опухолевых клеток в результате лучевого воздействия приводит к уменьшению размера опухоли, отграничению от окружающих нормальных тканей за счет разрастания соединительнотканных элементов (в случаях длительного предоперационного облучения и отсроченных операций). Реализация положительного эффекта предоперационной лучевой терапии определяется величиной дозы излучения.
В клинических исследованиях было показано, что доза 40-45 Гр приводит к гибели 90-95% субклинических очагов роста. Очаговая доза не более 40 Грей, подведенная по 2 Грея ежедневно в течение 4 недель, не вызывает сложностей в выполнении последующей операции и не оказывает заметного влияния на заживление послеоперационной раны.
Послеоперационная лучевая терапия
Определенными достоинствами послеоперационной лучевой терапии являются:
- планирование объема и методики облучения проводится на основе данных, полученных во время операции и после тщательного морфологического изучения удаленных тканей;
- отсутствуют факторы, оказывающие отрицательное влияние на заживление послеоперационных ран;
- оперативное вмешательство выполняется максимально быстро от момента уточняющей диагностики заболевания.
Для достижения лечебного эффекта при послеоперационной лучевой терапии необходимо подведение высоких доз – не менее 50-60 Грей.
Наличие воспалительных явлений в зоне оперативного вмешательства, нарушение крово- и лимфоснабжения приводит к задержке поступления кислорода к опухолевым клеткам и их комплексам, что делает их радиоустойчивыми. Одновременно, нормальные ткани в состоянии регенерации становятся более радиочувствительными, а именно их в большем объеме надо включать в мишень для послеоперационного облучения, т.к. нужно воздействовать на ложе опухоли, весь послеоперационный рубец и зоны регионарного метастазирования.
Симптомы и признаки
Злокачественные опухоли, локализованные в слепой кишке, характеризуются длительным бессимптомным течением. Быстро прогрессирующий субъективный дискомфорт отмечается на поздних этапах заболевания и не обладает патогномоничной спецификой, которая указывала бы именно на локализацию опухоли в слепой кишке. Пациенты предъявляют следующие жалобы:
- Тошнота, плохой аппетит, отрыжка;
- Метеоризм, внешне необъяснимое чередование поносов и запоров;
- Боль в правой части живота.
По мере увеличения опухоли в размерах и её повреждения каловыми массами прогрессирует кровоточивость. Она в течение определённого периода может оставаться скрытой, проявляться нарастающими симптомами анемии и астении:
- Апатией;
- Шаткостью;
- Слабостью, быстрой утомляемостью;
- Бледноземлистым цветом кожи;
- Исхуданием.
Частое или регулярное истечение алой крови при дефекации – один из типичных симптомов колоректального рака любой локализации. В терминальной стадии болезни обычно присоединяются следующие признаки рака слепой кишки:
- Интенсивный болевой синдром, обусловленный прорастанием опухоли в окружающие структуры и давлением на соседние органы;
- Явления частичной кишечной непроходимости или полного перекрытия просвета кишки;
- Желтуха и печеночная недостаточность, поскольку строение кишечной системы циркуляции лимфы и кровоснабжения обусловливает метастазирование опухолевого процесса в печень.
Диагностика
Предварительный диагноз «рак слепой кишки» специалисты клиники онкологии устанавливают в ходе сбора жалоб и анамнеза, клинического осмотра. Опухоль большого размера можно выявить во время пальпации живота. В целях дифференциальной диагностики, для уточнения расположения, формы и размеров опухоли, выявления метастазов проводят дополнительные методы исследования:
- Колоноскопию;
- Ирригоскопию;
- Компьютерную томографию;
- Ультразвуковой скрининг;
- Диагностическую лапароскопию.
В ходе эндоскопического или лапароскопического исследования врачи обязательно отбирают материал для гистологического анализа, который позволяет прийти к однозначным диагностическим выводам. Наиболее информативным методом диагностики рака сигмовидной кишки является ректоскопия. При сигмоидоскопии обследуют до 25 см дистального отдела толстой кишки.
Использование гибкого сигмоидоскопа и колоноскопа позволяет провести более точную предоперационную диагностику рака слепой кишки. Большой чувствительностью обладает рентгенологический метод с использованием двойной контрастной клизмы. Он позволяет выявлять небольшие по размеру опухоли. Злокачественное новообразование проявляется в виде характерного сужения или уплотнения, которое находится в контрастной зоне. В сомнительных случаях врачи Юсуповской больницы повторяют обследование или проводят колоноскопию.
Все более широкое распространение приобретает сканирующая компьютерная томография с контрастированием воздухом. Этот метод используют при принятии окончательного решения о необходимости оперативного вмешательства. В Юсуповской больнице для выявления рака слепой кишки широко используют спиральную компьютерную томографию с малой толщиной среза, так называемую «виртуальную колоноскопию».
Клетками карциномы кишки продуцируется раковоэмбриональный антиген (РЭА) – онкомаркер рака. Однако он недостаточно специфичен для того, чтобы служить надёжным индикатором существования опухоли. Раковоэмбриональный антиген обнаруживают и при панкреатите, воспалительных процессах кишечника, у курильщиков и у лиц, которые злоупотребляют алкоголем. Тест на РЭА используют у больных с исходно высоким уровнем этого онкомаркера после проведения хирургической операции. Его уровень после успешной операции снижается, а увеличение концентрации РЭА в послеоперационном периоде может быть первым признаком рецидива новообразования.
Врачи Юсуповской больницы проводят дифференциальную диагностику рака слепой кишки со следующими заболеваниями:
- Дивертикулезом толстой кишки;
- Язвенным и ишемическим колитом;
- Синдромом раздражённой кишки.
Другие заболевания, проявляющиеся ректальными кровотечениями (геморрой, полипоз) затрудняют постановку диагноза. Боли в области правой половины живота могут свидетельствовать о развитии острого аппендицита. Если у пациента определяются положительные симптомы «острого живота», ему выполняют ургентную операцию, во время которой устанавливают истинную причину болевого синдрома.
Тубулярная аденома слепой кишки относится к доброкачественным новообразованиям. Она может проявляться симптомами, напоминающими признаки раковой опухоли.
Записаться на приём
Симптоматика и диагностика опухолей слепой кишки
Выявить проблему необходимо как можно раньше. Хронические запоры, ощущения вздутия живота, тяжести в желудке и неполной дефекации, слизь, гной или кровь в каловых массах, тошнота и рвота — при этих признаках необходимо обратиться к врачу для установления диагноза. По мере развития рака прямой кишки среди симптомов появляются слабость и утомляемость, резкая потеря аппетита и веса, незначительное повышение температуры, сильные боли, кишечная непроходимость и нарушения в работе других органов.
Для диагностики используют простукивание, пальпацию, пальцевое обследование, анализы мочи, крови, кала, КТ и МРТ, колоноскопию, ирригоскопию, ректороманоскопию, цитоскопию, УЗИ. Это позволяет уточнить локализацию и размеры опухоли, ее особенности, выявить поражение других органов и наличие метастазов.
Наш эксперт в этой сфере:
Иванов Антон Александрович
Медицинский директор, врач онколог-хирург, к.м.н
Позвонить врачу
Позвонить врачу
Лечение
Одной из ключевых особенностей рака слепой кишки является то, что он полностью и безрецидивно излечим почти 93-97% случаев. Это относится лишь к начальным стадиям заболевания. Ранняя диагностика злокачественной опухоли – жизненно важный вопрос. По этой причине врачи Юсуповской больницы при наличии симптомов заболеваний кишечника исключают прежде всего рак.
Лечение опухоли слепой кишки всегда носит интенсивный комбинированный характер. Онкологи Юсуповской больницы задействуют все три основных направления современной онкологии – хирургическое вмешательство, лучевое лечение и химиотерапию.
Приоритетным способом лечения данного вида рака считается хирургическое удаление опухоли. С помощью лапароскопии проводятся операции на начальных стадиях опухолей. Во время эндоскопических операций минимально повреждаются окружающие ткани.
При растущих опухолях выполняется широкая резекция участка пораженной слепой кишки и брыжейки, удаляется лимфатический аппарат. Проводится правосторонняя гемиколэктомия: хирург удаляет до 20 см терминального отдела подвздошной кишки, правую половину толстой кишки, в том числе восходящую, слепую, правую треть поперечно-ободочной кишки и печеночную кривизну.
При множественном поражении органов и тканей метастазами операция по удалению опухолей не проводится, выполняется устранение тяжелых симптомов – непроходимости кишечника, назначается антибактериальная терапия, химиотерапия и паллиативное лечение. Хороший прогноз у больных с отсутствием метастазов в регионарных лимфатических узлах.
Консервативную терапию рака слепой кишки в Юсуповской больнице проводят в случае невозможности проведения оперативного вмешательства. Врачи клиники онкологии применяют новейшее оборудование ведущих мировых производителей для лучевой терапии и противоопухолевые препараты последнего поколения. Они оказывают эффективное действие и обладают минимальным спектром побочных эффектов.
Воздействие цитостатических лекарственных средств позволяет уменьшить размер новообразования, что повышает шансы его успешного удаления. Системная химиотерапия уничтожает малейшие раковые очаги и предотвращает развитие рецидива опухоли после операции. В зависимости от гистологической природы новообразования, реакции пациента на химиотерапевтические лекарства, врачи Юсуповской больницы используют монохимиотерапию (назначают 1 цитостатический препарат, который эффективно поражает данный вид раковых клеток) или полихимиотерапию – комбинацию нескольких различных видов лекарственных средств, деструктивно влияющих на опухоль.
Лучевые методы используются при подготовке к операции в качестве способа уменьшения массы опухоли. В Юсуповской больнице радиотерапия проводится на современном оборудовании. Линейные ускорители генерируют облучение, которое с предельной точностью поражает только мутированные ткани, не задевая здоровых клеток. Мощность оборудования позволяет сократить время проведения сеанса, тем самым, воздействие на весь организм является более щадящим.
Лечение рака слепой кишки включает проведение радиохирургических методов, в частности, использование кибер-ножа (Cyber Knife). Установка позволяет сфокусировать в одной точке 150-300 тонких лучей. Они попадают в нужную цель под разными углами, не оказывая губительного воздействия на здоровые ткани. Там, где лучи пересекаются (в опухоли слепой кишки) создаётся высокий уровень радиации. Благодаря высокодозному точному облучению количество сеансов может быть сокращено до 2-5.
В некоторых случаях врачи применяют специализированные методы лучевой терапии: интраоперационную лучевую терапию или брахитерапию. Эти виды лучевого лечения помогают избавиться от небольших опухолей, которые невозможно удалить оперативным путём. Интраоперационная лучевая терапия выполняется во время операции. В данном случае используют высокую однократную дозу лучевой терапии для уничтожения труднодоступной опухоли слепой кишки.
Брахитерапия проводится крошечными SIR-сферами с радиоактивным веществом под названием иттрий-90. Её используют при вторичном раке печени, возникшем на фоне злокачественной опухоли слепой кишки, когда операция не является вариантом выбора. Метод позволяет замедлить рост раковых клеток.
Если рак слепой кишки находится на первой стадии развития, отсутствует прорастание опухоли в соседние органы и метастазы, в Юсуповской больнице проводят лапароскопическое удаление опухоли. Этот малоинвазивный способ, наиболее щадящий для пациента. Хирургу не требуется делать обширных разрезов. Оперативное вмешательство осуществляется через несколько проколов передней стенки живота.
При более обширных поражениях онкологи иссекают повреждённый участок кишки с прилегающими тканями и накладывают анастомоз – восстанавливают целостность кишечника, создают обходной путь для пищи, сшивая два участка кишки. В некоторых случаях рака слепой кишки, чтобы избежать распространения опухоли на соседние органы, хирурги производят резекцию региональных лимфатических сосудов и узлов вместе с новообразованием, единым блоком. Если сохранить орган не представляется возможным, хирурги удаляют не только слепую кишку, но и участок тонкого или толстого кишечника. Далее формируют колостому – отверстие для вывода содержимого кишечника. Через него каловые массы попадают в калоприёмник, который носит пациент.
В некоторых случаях колостома накладывается на непродолжительное время, чтобы оптимизировать процесс лечения кишечника. Она может быть и постоянной. При современных хирургических методах, которые применяют онкологи Юсуповской больницы, и использовании лучевой терапии, лечении современными химиотерапевтическими препаратами до операции, большинству пациентов с раком слепой кишки, не требуется постоянная колостома. Грамотное применение хирургами клиники онкологии приёмов антибластики, очищения места удаления опухоли от малейших оставшихся атипичных клеток, значительно снижает риски появления рецидива у пациентов Юсуповской больницы.
4.Лечение
Одной из ключевых особенностей рака слепой кишки является то, что он полностью и безрецидивно излечим почти во всех случаях (в разных источниках приводятся оценки на уровне 93-97%). Однако это относится лишь к начальным стадиям, – что и делает раннюю диагностику вопросом витальной важности, – и не касается каких бы то ни было внемедицинских практик, единственным подтвержденным результатом которых является финансовая прибыль для одних лиц и самоубийственная трата времени для других.
Лечение всегда носит интенсивный комбинированный характер и подразумевает задействование всех трех основных направлений современной онкологии – хирургического вмешательства, лучевой терапии и химиотерапии.
Прогноз при раке слепой кишки
Прогноз при злокачественных новообразованиях слепой кишки зависит от глубины прорастания первичной опухоли, наличия регионарных и отдалённых метастазов. Показатель пятилетней выживаемости напрямую зависит от стадии рака слепой кишки. В последние несколько десятилетий этот показатель вырос. Это связано с тщательной диагностикой и современными методами лечения, которые применяют онкологи Юсуповской больницы.
Прогноз у пациента после иссечения опухоли зависит не просто от наличия или отсутствия метастазов в регионарные лимфоузлы, а от числа поражённых лимфатических узлов. К неблагоприятным факторам, ухудшающим прогноз при раке слепой кишки, относится прорастание новообразования в жировую клетчатку, перфорация толстой кишки, низкая степень дифференцировки раковых клеток, переход рака на соседние ткани и органы, переход опухоли в просвет крупных вен.
Пятилетняя выживаемость при II стадии рака слепой кишки составляет 85%. Если установлен диагноз «рак слепой кишки 3 стадия», прогноз для пятилетней выживаемости 74%, а при четвёртой стадии опухолевого процесса до пяти лет доживает 6% пациентов. По этой причине онкологи Юсуповской больницы не рекомендуют откладывать визит к врачу при появлении признаков кишечного дискомфорта. Звоните в любое время суток. Контакт-центр Юсуповской больницы работает без выходных и обеденного перерыва.
Записаться на приём
1.Общие сведения
В толстом кишечнике человека различают несколько основных отделов: ободочная, наиболее протяженная кишка; сигмовидная кишка как нижнее продолжение ободочной и переход в прямую; прямая кишка, заканчивающаяся анальным отверстием. Слепая кишка относится к начальному участку толстого кишечника. Она расположена справа и благодаря своему строению чаще всего сравнивается с вертикальным мешком. В нижней части слепой кишки находится червеобразный аппендикс (досл. «придаток»), который длительное время, – и, как показали более поздние исследования, ошибочно, – считался функционально бесполезным рудиментом.
Рак толстого кишечника на сегодняшний день является острой, глобально значимой проблемой, занимая лидирующие позиции в общем объеме онкопатологии и в перечнях причин летальности; более того, летальность при данной локализации опухолевого процесса обнаруживает тенденцию к нарастанию. Даже наиболее развитые страны мира, вынужденные затрачивать огромные ресурсы и усилия на осуществление национальных скрининг-программ ранней диагностики (имеющей критически важное значение в данном случае), с большим трудом и пока лишь незначительно сдерживают эту тревожную тенденцию, обусловленную рядом факторов современной цивилизации.
Известно, что рост злокачественного новообразования может начаться в любом отделе ЖКТ (как, собственно, и в любой зоне организма вообще), однако в силу анатомических и функциональных особенностей такая вероятность, этиопатогенез и факторы риска для различных локализаций неодинаковы. Рак слепой кишки составляет примерно пятую часть всех онкозаболеваний толстого кишечника.
Обязательно для ознакомления! Помощь в лечении и госпитализации!