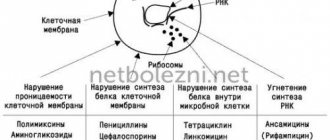
Спектр действия
Активность препаратов из группы цефалоспоринов постепенно меняется при переходе от поколения к поколению:
- Лекарства 1-2 поколений наиболее эффективны при заражении грамположительной флорой (стафило- и стрептококки, коринебактерии).
- Для 3 и 5 поколений цефалоспоринов уже имеет место возросшая активность к грамотрицательным бактериям (энтеробактер, гемофильная палочка, гонококк, менингококк, клебсиелла, моракселла, протей) и анаэробам (пептококк, пептострептококк, клостридии, бактероиды) наряду с высокой эффективностью против грамположительной флоры. В дополнение цефтазидим и цефиксим губительны для синегнойной палочки.
- Цефалоспорины 4 поколения отличаются: их эффект максимален для грамотрицательных бактерий, при этом цефепим так же обладает антисинегнойным эффектом.
Антибиотики из ряда цефалоспоринов относятся к β-лактамным антибиотикам. Каждый из их представителей имеет в своей структуре 7-АЦК (7-аминоцефалоспорановую кислоту) и отличается более высокой устойчивостью к особому ферменту бактерий β-лактамазе. Путем предотвращения синтеза компонентов клеточной стенки бактериальных клеток, цефалоспорины реализуют свое бактерицидное действие, т.е. полностью разрушают микробные клетки.
Миф. Современные антибиотики настолько «сильные», что перед ними не устоит ни одна бактерия
Правда.
На самом деле одной из самых актуальных проблем современной фармакологии и здравоохранения в целом является стремительное развитие резистентных штаммов бактерий, устойчивых в том числе и к современным антибиотикам последних поколений. Возникновение устойчивости зарегистрировано к каждому без исключения классу антимикробных препаратов. Она может развиваться на любом этапе достижения терапевтического эффекта (и даже на нескольких сразу). Основные механизмы развития устойчивости [1, 2]:
- Изначально устойчивые штаммы. Например, некоторые грамотрицательные бактерии имеют наружные клеточные мембраны, защищающие их клетки от действия ряда пенициллинов и цефалоспоринов.
- Спонтанные мутации, приводящие к появлению организмов, устойчивых к антибиотикам.
- Передача генов устойчивости к антимикробным препаратам — самый распространенный и важный механизм развития антибиотикорезистентности.
Устойчивость к антибиотикам — глобальная проблема, которая может иметь непредсказуемые последствия для каждого из нас. Увы, но огромный вклад в ее существование вносят сами потребители. Об этом уместно напомнить покупателям с рецептами на антибиотики, подчеркнув, что существенно снизить риски развития устойчивых штаммов позволяет прием антимикробных препаратов только по назначению врача и четкое соблюдение дозы и режима антибиотикотерапии.
Распространенные представители
Из многочисленного списка цефалоспоринов наиболее часто применяющимися в настоящий момент являются представители 3 поколения, а именно цефтриаксон, цефтибутен, цефдиторен. Это объясняется широким спектром их действия и относительно невысокой стоимостью. Кроме того, последние два препарата выпускаются в пероральной форме, что очень удобно для приема пациентами.
Может создаться впечатление, что цефалоспорины, выпускаемые в таблетках, — редко используемые лекарства. Это не так: такие препараты применимы даже при тяжелых инфекциях различных органов, когда иные антибиотики не оказывают должного эффекта.
Целесообразно сравнить самых распространенных представителей по ряду важнейших критериев:
Скорость эффекта (время максимальной концентрации в крови):
| Цефтриаксон | Цефтибутен | Цефдиторен |
|
|
|
Микробный спектр действия:
| Цефтриаксон | Цефтибутен | Цефдиторен |
| ||
|
|
|
Устойчивые штаммы бактерий:
| Цефтриаксон | Цефтибутен | Цефдиторен |
|
|
|
Побочные эффекты:
| Цефтриаксон | Цефтибутен | Цефдиторен |
| Нервная система | ||
|
|
|
| Сердечно-сосудистая система, кроветворение | ||
|
|
|
| Желудочно-кишечный тракт | ||
| ||
| Мочеполовая система | ||
|
|
|
| Аллергические реакции | ||
|
|
|
Применение у беременных и кормящих пациенток:
| Цефтриаксон | Цефтибутен | Цефдиторен |
|
|
|
См. Как отличить коронавирус от ОРВИ, гриппа, простуды. Пневмония при коронавирусе: симптомы, лечение Нобазит при ковиде Ингавирин при коронавирусе Симптомы и лечение коронавируса
Стратегические подходы к выбору цефалоспориновых антибиотиков при инфекциях дыхательных путей
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказывается недостаточно. Фактор удобства приема препарата и, что особенно непривычно для нашего понимания, вопросы цены и стоимости лечения в условиях серьезного ограничения финансирования здравоохранения часто могут оказаться определяющими. На приобретение лекарственных средств лечебные учреждения тратят 15–20% своего бюджета, причем 50–60% этих расходов приходится на долю антибактериальных препаратов, что заставляет пересмотреть существующие и искать новые подходы к их применению.
Путаница, возникающая при использовании различных антибактериальных препаратов, в том числе и цефалоспориновых антибиотиков (ЦА), связана с недопониманием или просто незнанием основных принципов клинической химиотерапии. В связи с этим мы хотели бы остановиться на некоторых ошибках и «заблуждениях» практикующих врачей, возникающих при назначении антибактериальных препаратов, на примере ЦА, а также определить их место в лечении инфекции дыхательных путей.
Часто от практикующих врачей приходится слышать о безусловных преимуществах IV поколения препаратов перед III, III поколения перед II и т. д. Это абсолютно неверно. Такая точка зрения приводит к использованию «резервных» и мощных препаратов при лечении банальной инфекции, способствует развитию резистентности, а значит, лишает возможности применять препараты первых поколений и, наконец, вызывает значительное и неоправданное увеличение стоимости курса лечения.
ЦА занимают одно из важных мест в лечении инфекций верхних и нижних дыхательных путей. Наиболее ответственным этапом в антибактериальной терапии данной категории пациентов является выбор первоначального препарата. От адекватности выбора зависит эффективность и безопасность лечения, а также его комфортность, переносимость, стоимость, эпидемиологическая ситуация.
Анализ имеющихся данных об использовании ЦА в России за 1997–1998 гг. позволяет выявить предпочтения врачами того или иного препарата (группы препаратов) и определенных методов его введения. Как видно из рис. 1, при назначении цефалоспориновых антибиотиков подавляющее большинство врачей выбирают парентеральные препараты.
Данный факт лишь подтверждает, что в нашей стране пероральные лекарственные средства, и особенно пероральные цефалоспорины, очень мало популярны и практически не используются. Такое отношение к таблетированным формам отражает некоторый консерватизм практических врачей, связанный с тем, что еще 15-20 лет назад существовавшие тогда пероральные средства не выдерживали сравнения с парентеральными препаратами ни по эффективности терапии, ни по ее переносимости. Лишь последние десятилетия с момента создания первого перорального цефалоспорина — цефалексина и появления новых пероральных бактерицидных препаратов эта лекарственная форма несколько укрепила свои позиции не только в амбулаторной, но и в стационарной практике. Однако радикально на положении дел это не сказалось.
Очевидно, что такая форма назначения препаратов имеет безусловные преимущества. Это проявляется и в возможности амбулаторного ведения больного, и в удобстве приема препарата, и в снижении риска постинъекционных осложнений и длительности пребывания в стационаре, и даже в избавлении от психологического дискомфорта, связанного с инъекциями.
Наличие антибактериальных препаратов в двух формах — для парентерального и перорального применения — делает возможным их использование для проведения так называемой ступенчатой терапии. Суть такого лечения состоит в назначении внутривенного или внутримышечного препарата и в последующем, через двое-трое суток после достижения клинического эффекта, переводе на пероральный прием. Возможность проведения ступенчатой терапии одним и тем же препаратом является существенным преимуществом данного лекарственного средства перед его аналогами. Ступенчатая терапия предоставляет клинические и экономические преимущества как пациенту, так и лечебному учреждению.
На основании приведенных данных трудно понять логику выбора цефалоспоринового антибиотика того или иного поколения и принципы, которыми руководствуется врач при назначении препарата. Анализ использования цефалоспориновых антибиотиков по поколениям (см. рис. 2 и 3) свидетельствует о предпочтительном назначении препаратов I и III поколений, причем из препаратов III поколения (61%) половина приходится на цефотаксим, а из препаратов I поколения большая часть приходится на цефазолин.
В клинической практике врач начинает проводить антибактериальную терапию, в большинстве случаев не имея результатов микробиологической верификации инфекционного агента, а зачастую и без перспектив получения такого рода данных. Поэтому при выборе антибактериального препарата по-прежнему приходится ориентироваться на сведения, полученные из литературы, данные микробиологического мониторинга, а также на особенности клинической ситуации. Все это позволяет с большей или меньшей долей вероятности определить этиологический инфекционный агент с учетом клинической формы инфекции дыхательных путей (пневмония, хронический бронхит, синусит и т. д.), возраста (дети, старики), сопутствующих заболеваний (сахарный диабет, хроническая алкогольная интоксикация, лечение глюкокортикоидами и цитостатиками). Необходимо также иметь в виду особенности развития инфекции в амбулаторных условиях или в стационаре (лечение по поводу другого заболевания, пребывание в реанимации) при соответствующей эпидемиологической ситуации. Следует отметить, что при выборе препарата важно отличать «госпитальную», или нозокомиальную инфекцию, возникшую спустя двое суток после поступления в стационар, от «амбулаторной» инфекции, долечиваемой в стационаре. В последнем случае тактика антибактериальной терапии должна существенно отличаться.
Таким образом, ориентировочная этиология бронхолегочной инфекции служит основанием для выбора среди ЦА конкретного препарата (или поколения препаратов) с соответствующей антимикробной активностью.
У больных с амбулаторной инфекцией верхних и нижних дыхательных путей, основными возбудителями которых являются стрептококки, Н. influenzae, Moraxella catarrhalis, — препаратами выбора могут быть ЦА I или II поколения. В амбулаторных условиях предпочтение следует отдавать оральным цефалоспоринам (цефаклор, цефуроксим аксетил, цефтибутен). В то же время необходимо иметь в виду недостаточную активность ЦА в целом в отношении атипических бактерий (8–35% в этиологии «домашней» пневмонии) и некоторых анаэробных микроорганизмов, вероятность влияния которых увеличивается у больных с хроническими синуситами и отитами.
При обострениях хронического бронхита особое значение приобретают препараты, высокоустойчивые к действию b-лактамаз, продуцируемых как грамотрицательными, так и грамположительными микроорганизмами (цефуроксим аксетил), и обладающие высокой активностью против Н.influenzae (цефтибутен).
При выявлении показаний для госпитализации больных с «домашней» инфекцией, подразумевающих более тяжелое течение, чаще обнаруживаются Streptococcus pneumonia, Staphylococcus aureus, Н.influenzae и Еntеrobacteriacea. В этом случае более обосновано назначение парентеральных цефалоспоринов II поколения (цефуроксим, цефамандол). Однако именно в таких ситуациях чаще всего и допускаются ошибки: при госпитализации больного в стационар с «домашней» пневмонией нередко назначают бензилпенициллин, аминопенициллины и ЦА I поколения (малоэффективные ввиду высокой резистентности патогенной флоры), либо, для «перестраховки» и при наличии в стационаре, ЦА III поколения (цефотаксим, реже цефтриаксон). Однако более обосновано — и это определяется спектром активности препарата — назначение ЦА II. Среди больных, получающих терапию в стационаре по поводу инфекций нижних дыхательных путей, преобладают нетяжелые случаи. Поэтому идеология назначения ЦА II поколения в качестве «стартовых» препаратов должна доминировать как с позиции адекватной клинической эффективности, экономической целесообразности, так и с позиции сохранения резерва в более тяжелых ситуациях.
Выбор ЦА в качестве первоначального антибиотика при внебольничной пневмонии у больных моложе 60 лет без сопутствующей патологии следует считать, по-видимому, не всегда оправданным. Это обусловлено этиологически широким спектром пневмоний в данной ситуации, который может включать не только пневмококки и Н.influenzae, но и так называемые атипичные возбудители — Мусорlаzma pneumоniaе, Legionella, Chlamidia pneumоniaе, которые не чувствительны к цефалоспоринам всех генераций. Между тем рациональная эмпирическая антибактериальная терапия бронхолегочных инфекций, в том числе пневмоний, должна предусматривать выбор препарата, по возможности активного против всех вероятных в данной ситуации возбудителей. К сожалению, сегодня трудно назвать препарат, полностью удовлетворяющий этим требованиям, за исключением нового поколения фторхинолонов или «респираторных» фторхинолонов. Некоторые из них — например, грепафлоксацин — проходят сейчас в нашей стране регистрацию. В случаях назначения ЦА при данном варианте пневмоний предпочтение следует отдавать ЦА I и II поколения. Применение в подобных ситуациях ЦА III поколения нерационально ввиду высокого риска развития резистентности. Выбор конкретного препарата среди ЦА I–II поколения должен осуществляться исходя из преимущества лекарственных форм, фармакокинетических свойств, стоимости и др. При нетяжелых пневмониях возможно назначение оральных цефалоспоринов. При этом необходимо иметь в виду их различную противомикробную активность по отношению к различным микроорганизмам. Так, например, цефтибутен обладает наибольшей активностью в отношении Н.influenzae, а цефуроксим аксетил — в отношении S.аureus.
Общие принципы выбора первоначального ЦА сохраняются и у больных пневмонией на фоне тяжелых сопутствующих заболеваний (ХОЗЛ, сердечная недостаточность, сахарный диабет, алкогольная интоксикация и др.) и в возрасте старше 60 лет. Этиологическое значение в данной клинической ситуации приобретают Н.influenzae, S.аureus, некоторые грамотрицательные микроорганизмы (Е.соli, Сlebsiella), возрастает частота бета-лактамазопродуцирующих бактерий. В связи с этим возрастает значение препаратов, активных в отношении названных возбудителей. Известно, что противомикробное действие ЦА при переходе активности от первого поколения к последующим характеризуется снижением противостафилококковой активности и преобладанием активности против некоторых грамотрицательных микроорганизмов. Ценным свойством является устойчивость ЦА II поколения к b-лактамазам. В связи с этим врач должен ориентиро-ваться в данной ситуации на цефалоспорины II или по крайней мере III поколения.
Иной подход, определяющий выбор ЦА для лечения бронхолегочной инфекции, наблюдается у больных с «госпитальной» инфекцией. Госпитальные пневмонии занимают особое место среди всех внутрибольничных инфекций из-за тяжести течения и трудностей терапии. Основными возбудителями госпитальных пневмоний являются грамотрицательные микроорганизмы семейства Еntеrobacteriacea — Сlebsiella, Protei, Enterobacter, Providencia, Serracia, а также Staphylococcus аureus, как чувствительный, так и устойчивый к метициллину. Вероятность этиологической роли того или иного инфекционного агента при госпитальных пневмониях определяется особенностями клинической ситуации (послеоперационный период, пребывание в реанимации, искусственная вентиляция легких и т. д.). У больных реанимационных и ожоговых отделений, с иммунодефицитами и муковисцидозом основным микроорганизмом бактериальных осложнений является синегнойная палочка, выявляемая в 70–95% случаев. Наряду с ней у таких больных высевается золотистый стафилококк или гемофильная палочка, устойчивая к ЦА II–III поколения. Основное место в лечении госпитальных пневмоний среди ЦА занимают препараты III (цефтазидим, цефоперазон) и IV поколений (цефпиром, цефепим). С учетом вероятности этиологической роли Pseudomonas aeruginoza в соответствующих ситуациях (ИВЛ, наличие трахеостомы, предшествующая глюкокортикоидная терапия) назначаемые ЦА должны обладать антисинегнойной активностью. Среди имеющихся в распоряжении врача ЦА наибольшей активностью в отношении Pseudomonas aeruginoza обладают цефалоспорины III поколения (цефтазидим, цефоперазон) и IV поколения (цефпиром), которые, однако, не имеют серьезных преимуществ в отношении синегнойной палочки перед цефтазидимом. Появление в терапевтическом арсенале ЦА IV поколения расширяет возможности антибактериальной терапии госпитальных пневмоний с высокой вероятностью грамотрицательной флоры, в том числе золотистого стафилококка, и могут рассматриваться как препараты ургентных ситуаций.
| Цефалоспорины, открытые более 50 лет тому назад, продолжают занимать прочные позиции в лечении различных бактериальных заболеваний, несмотря на появление новых антимикробных средств. Цефалоспориновые антибиотики подразделяются на четыре поколения, отличающиеся по спектру действия, антибактериальной активности, стабильности в присутствии b-лактамаз, фармакокинетическому профилю. Все это наряду с многообразием лекарственных форм и стоимостью определяет их различные показания. Очевидно, что по мере появления новых поколений цефалоспориновых антибиотиков в клинической практике возникает немаловажная проблема дифференцированного назначения препарата с учетом свойств как самого антибиотика, так и особенностей инфекционно- воспалительного процесса у конкретного больного |
Таким образом, рациональный выбор первоначального ЦА для лечения инфекций верхних и нижних дыхательных путей определяется в первую очередь вероятностью этиологической роли того или иного микроорганизма в конкретной клинической ситуации. Такой подход требует от практического врача (а именно от него зависит адекватный выбор препарата) умения выявлять особенности каждого случая пневмонии (эпидемиологическую обстановку, фоновую патологию, факторы риска и др.) и ориентировки в антимикробном спектре назначаемого антибиотика. Однако в клинической практике при выборе ЦА, как, впрочем, и других антибиотиков, приходится наряду с ориентировочной этиологией бронхолегочной инфекции учитывать и другие факторы. Среди последних имеет значение фармакокинетика препарата, наличие разнообразных лекарственных форм, риск развития побочных эффектов, стоимость и др.
В настоящее время не окончательно определено место пероральных препаратов III поколения в клинической практике, так как их сравнительная клиническая и бактериологическая эффективность мало отличается от препаратов II поколения. Более того, как было сказано выше, преимущество цефалоспоринов III поколения состоит в их высокой активности в отношении b-лактамазопродуцирующих бактерий, наиболее часто вызывающих серьезные стационарные инфекции. Но поскольку в этом случае больные находятся в стационаре, то уже более обоснованно получают парентеральную терапию. В то же время ввиду сниженной активности в отношении грамположительных бактерий, часто являющихся причиной именно амбулаторной инфекции, назначение препаратов III поколения имеет меньше преимуществ перед препаратами II поколения.
Цель антибактериальной терапии состоит не только в достижении клинического эффекта, но и в полной эрадикации возбудителя, т. е. бактериологической эффективности. Это в основном определяется адекватным дозированием препарата для достижения необходимой концентрации в очаге инфекции. Высокая степень накопления препарата в тканях является необходимым требованием к лекарственному веществу.
ЦА первого поколения хуже проникают в ткани, что уменьшает степень бактериальной эрадикации.
Данные о биодоступности оральных ЦА следует иметь в виду при дифференцированном назначении их больным с сопутствующей патологией кишечника, связанной с нарушением всасывания, а также при одновременном приеме антисекреторных препаратов, антацидов, с учетом влияния пищи на всасывание ЦА.
Знание путей элиминации ЦА наряду с оценкой функционального состояния печени и почек (возраст, сопутствующая патология) также может определять выбор более адекватного для данной ситуации препарата. Выбирая ЦА для лечения тяжелых госпитальных пневмоний, например, у новорожденных и стариков или у больных с патологией почек, при наличии почечной недостаточности предпочтение следует отдать цефоперазону с учетом его преимущественно билиарной экскреции.
При дифференцированном выборе ЦА необходимо учитывать риск развития побочных эффектов. Наиболее типичны реакции гиперчувствительности (лихорадка, кожная сыпь), гематологические синдромы (цитопения, эозинофилия), нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея), печени (повышение активности трансаминаз), почек (повышение уровня креатинина), ЦНС (головная боль), флебиты при внутривенном введении. Поэтому анамнестические и клинико-лабораторные данные о наличии у больных какой-либо патологии должны влиять на выбор соответствующего препарата.
Флебиты часто возникают при введении цефалотина, цефотаксима, цефепима. Цефуроксим, цефоперазон, цефтибутен могут вызывать анемию (чаще гемолитическую), а при назначении цефалотина, цефамандола, цефотаксима, цефтазидима иногда выявляются фиксированные на эритроцитах антитела. Повышение активности печеночных ферментов возможно на фоне лечения цефоперазоном, цефтриаксоном, цефтазидимом, цефуроксимом. Уровень креатинина может повышаться при лечении цефалексином и цефподоксимом. Оральные цефалоспорины чаще всего вызывают нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея). При лечении парентеральными ЦА отмечено увеличение протромбинового времени, за исключением цефтазидима, не влияющего на синтез факторов протромбинового комплекса и показатели свертываемости крови. Возможны реакции гиперчувствительности (кожная сыпь, лихорадка, эозинофилия) на фоне применения почти всех ЦА III поколения.
Таким образом, дифференцированный выбор ЦА для лечения инфекций верхних и нижних дыхательных путей должен базироваться на учете и адекватной оценке многих факторов, включающих как особенности клинической ситуации, так и антимикробную активность и фармакокинетические характеристики назначаемого препарата.
Классификация цефалоспоринов
В ряд цефалоспоринов входят лекарственные препараты пяти поколений. Разделение их на группы происходило постепенно, параллельно открытию новых веществ и их свойств. Внутри каждого поколения выделяют пероральные (принимаемые «через рот») и парентеральные (поступающие в организм через инъекции) формы.
1 поколение:
| Представители | Торговое название | Способ применения, цена |
| Цефазолин (парентеральный) | Цефазолин | Порошок для изготовления инъекционного раствора: 0,5 гр. (разведя в 2 мл стерильной воды) – 2,0 гр. (разведя в 4 мл стерильной воды) в сутки в 3-4 приема, вводить внутривенно. 20-910 руб. |
| Цефазолин-АКОС | Порошок для изготовления инъекционного раствора: по 0,5 гр. х 2 раза в день внутривенно (разведя в 5 мл стерильной воды) или внутримышечно (разведя в 2 мл стерильной воды).30-50 руб. | |
| Цефалотин (парентеральный) | Цефалотин | Порошок для изготовления инъекционного раствора: 0,5-1,0 гр. каждые 6 часов внутривенно или внутримышечно. 800-1000 руб. |
| Цефалексин (парентеральный, пероральный) | Цефалексин | Капсулы: 0,25-0,5 гр. каждые 6 часов, запивая водой, за 30-60 минут до приема пищи. 80-120 руб. |
| Гранулы для приготовления суспензии внутрь во флаконе: добавить 80 мл дистиллированной воды, встряхнуть, полученную смесь пить в соответствии с мерной ложкой (флакон содержит 0,25 гр. вещества). 1,0-2,0 гр. в сутки, при этом в 1 мл готовой смеси находится 25 мг цефалексина. 80-100 руб. | ||
| Экоцефрон | Капсулы: 0,25-0,5 гр. каждые 6 часов, запивая водой, за 30-60 минут до приема пищи. 80-100 руб. | |
| Цефадроксил (пероральный) | Дурацеф | Капсулы, таблетки, гранулы для суспензии – исключены из реестра применяемых лекарств в РФ. |
| Биодроксил |
2 поколение:
| Представители | Торговое название | Способ применения, цена |
| Цефуроксим (парентеральный, пероральный) | Зинацеф | Порошок для изготовления инъекционного раствора: 0,75-1,5 гр. внутривенно х 3 раза в день. 130-250 руб. |
| Зиннат | Капсулы: по 0,25-0,5 х 2 раза в день после еды. 220-400 руб. | |
| Гранулы для приготовления суспензии внутрь во флаконе: 0,125-0,25 гр. в сутки во время приема пищи. 250-330 руб. | ||
| Аксосеф | Таблетки: 0,25-0,5 гр. х 2 раза в день. 400-600 руб. | |
| Порошок для изготовления инъекционного раствора: 0,75-1,5 гр. внутривенно х 3 раза в день. Максимально 6,0 гр. в сутки. 120-250 руб. | ||
| Цефамандол (парентеральный) | Цефат | Порошок для изготовления инъекционного раствора: 0,5-1,0 гр. каждые 6 часов внутримышечно (растворив в 3 мл стерильной воды) или внутривенно (растворив в 10 мл изотонического хлорида натрия). 120-360 руб. |
| Цефаклор (пероральный) | Цеклор | Капсулы, таблетки, гранулы для суспензии – исключены из реестра применяемых лекарств в РФ. |
| Цефаклор Штада | ||
| Альфацет |
3 поколение:
| Представители | Торговое название | Способ применения, цена |
| Цефотаксим (парентеральный) | Клафоран | Порошок для изготовления инъекционного раствора: 0,5-2,0 гр. (в зависимости от инфекции) х 1 раз в сутки внутримышечно (прежде растворив 1,0 гр. – в 4 мл, 2,0 гр. – в 10 мл стерильной воды) или внутривенно (прежде растворив в 40-100 мл стерильной воды) медленно. 130-150 руб. |
| Цефосин | Порошок для изготовления инъекционного раствора: 1,0 гр. каждые 8-12 часов внутримышечно (растворив 1,0 гр. в 4 мл стерильной воды), внутривенно медленно (прежде растворив 1,0 гр. – в 4 мл, 2,0 гр. – в 10 мл стерильной воды) или капельно (50-100 мл изотонического раствора хлорида натрия на 1,0-2,0 гр. вещества). 50-70 руб. | |
| Цефтазидим (парентеральный) | Фортум | Порошок для изготовления инъекционного раствора: 1,0-6,0 гр. х 1 раз в сутки в 2-3 внутривенные или внутримышечные инфузии. 450-520 руб. |
| Цефтидин | Порошок для изготовления инъекционного раствора: 1,0-6,0 гр. х 1 раз в день (обычно по 1,0 гр. каждые 8 часов) внутривенно или внутримышечно. 150-200 руб. | |
| Цефтриаксон (парентеральный) | Цефтриаксон | Порошок для изготовления инъекционного раствора: 1,0-2,0 гр. х 1 раз в день внутримышечно/внутривенно. 30-900 руб. |
| Азаран | Порошок для изготовления инъекционного раствора: 1,0 гр. растворить в 3,5 мл 1% раствора лидокаина гидрохлорида, применять 1 раз в день внутримышечно. 2300-2700 руб. | |
| Цефоперазон (парентеральный) | Цефобид | Порошок для изготовления инъекционного раствора: 2,0-4,0 гр. в сутки внутримышечно, разделив общую суточную дозу на 2 приема. 250-300 руб. |
| Цефпар | Порошок для изготовления инъекционного раствора: 2,0-4,0 гр. в сутки внутривенно или внутримышечно, дозу разделить на прием равными частями каждые 12 часов. 30-100 руб. | |
| Цефиксим (капсулы, суспезия) | Супракс | Капсулы: 0,4 гр. одиножды в сутки. 700-780 руб. |
| Панцеф | Таблетки: 0,4 гр. х 1 раз в день или 0,2 гр. х 2 раза в день. 380-590 руб. | |
| Гранулы для приготовления суспензии внутрь во флаконе: флакон хорошо встряхнуть, добивать 66 мл кипяченой воды комнатной температуры, еще раз встряхнуть, принимать по 0,4 гр. х 1 раз в день или 0,2 гр. х 2 раза в день (используя мерный колпачок). 390-700 руб. | ||
| Супракс Солютаб | Шипучие таблетки: 0,4 гр. х 1 раз в день или 0,2 гр. х 2 раза в день, растворив в стакане с водой. 800-1000 руб. | |
| Цефтибутен (капсулы) | Цедекс | Капсулы: 0,4 гр. х 1 раз в сутки. 800-1100 руб. |
| Цефдиторен (в таблетках) | Спектрацеф | Таблетки: 0,2/0,4 гр. дважды в день. 1300-1400 руб. |
4 поколение:
| Представители | Торговое название | Способ применения, цена |
| Цефепим (парентеральный) | Максипим | Порошок для изготовления инъекционного раствора: 0,5-2,0 гр. каждые 12 часов, вводить внутривенно медленно (развести 5/10 мл стерильной воды) или внутримышечно (развести в 1,3/2, мл стерильной воды). 350-400 руб. |
| Цефепим | Порошок для изготовления инъекционного раствора: 0,5-1,0 гр. каждые 12 часов, введение внутривенное или внутримышечное (объемы разведения аналогичны). 120-150 руб. | |
| Цефпиром (парентеральный) | Цефанорм | Порошок для изготовления инъекционного раствора: 1,0-2,0 гр. внутривенно каждые 12 часов. 1300-1500 руб. |
| Изодепом | Порошок для изготовления инъекционного раствора: 0,25/0,5/1,0/2,0 гр., разделив введение пополам на каждые 12 часов. Вводить внутривенно медленно/капельно или внутримышечно (разводить дозу в 25/50/100/200 мл стерильной воды или изотонического раствора хлорида натрия соответственно). 600-900 руб. |
5 поколение:
| Представители | Торговое название | Способ применения, цена |
| Цефтобипрол (парентеральный) | Зефтера | Лиофилизат для изготовления инъекционного раствора – исключен из реестра применяемых лекарств в РФ. |
| Цефтаролин (парентеральный) | Зинфоро | Порошок для изготовления инъекционного раствора: по 0,6 гр. каждые 12 часов в виде внутривенной инфузии в течение 60 минут (после добавления в порошок 20 мл стерильной воды, полученную смесь встряхнуть и перенести во флакон, куда добавить 50/100/250 мл изотонического раствора хлорида натрия). 25000-27000 руб. |
Специально для защиты от разрушительного действия ферментов бактерий β-лактамаз создана комбинация цефоперазон + сульбактам в парентеральных препаратах:
- Сульперазон (порошок для изготовления инъекционного раствора: 1,0-2,0 гр. цефоперазона + 1,0-2,0 гр. сульбактама в соотношении 1:1, поделив дозу на 2 приема, вводить внутривенно, внутримышечно). 480-550 руб.
- Сульперацеф (порошок для изготовления инъекционного раствора: 0,5-1,0 гр. цефоперазона + 0,5-1,0 гр. сульбактама в отношении 1:1, вводить внутримышечно или внутривенно каждые 12 часов). 2400-3000 руб.
Все препараты из списка цефалоспоринов абсолютно запрещены к употреблению совместно с алкогольными напитками любой крепости. В обратном случае развивается антабусный эффект – острое смертельно опасное токсическое воздействие на организм в виде расстройств дыхания, сердечной деятельности и бронхоспазма.
Применение в детском возрасте
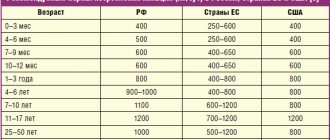
Антибиотики группы цефалоспоринов в своем большинстве не противопоказаны к применению у пациентов детского возраста. Средние суточные дозировки для детей составляют:
| Цефалоспорин | Доза |
| Цефазолин |
|
| Цефалотин | 0,02-0,04 гр/кг в сутки, разделив введение на каждые 6 часов. |
| Цефалексин |
|
| Цефуроксим |
|
| Цефамандол |
|
| Цефотаксим |
|
| Цефтазидим |
|
| Цефтриаксон |
|
| Цефоперазон | 0,05-0,2 гр/кг в сутки (вводить за 2 раза). |
| Цефиксим |
|
| Цефтибутен |
|
| Цефдиторен |
|
| Цефепим |
|
| Цефпиром |
|
| Цефтаролин | Нет полноценной информации о безопасности и эффективности препарата у детей до 18 лет. |
Цефалоспорины всех поколений не теряют актуальности на современном этапе развития медицины. Благодаря большому спектру действия этих препаратов представляется возможным излечение от широкого круга инфекционных заболеваний. К сожалению, микроорганизмы постоянно изменяют свою структуру, пытаясь стать невосприимчивыми к губительному действию антибиотиков. Во избежание этого не принимайте антибактериальные препараты без назначения врача.
Автор:
Селезнева Валентина Анатольевна врач-терапевт