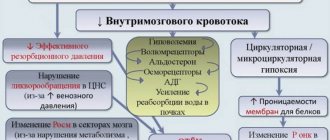
В настоящее время острые нарушения мозгового кровообращения являются наиболее частым жизнеугрожающим заболеванием и одной из главных причин инвалидизации не только в России, но и в мире. По данным Всемирной федерации неврологических обществ, ежегодно в мире регистрируется около 15 млн инсультов. В России заболеваемость инсультом составляет 3,4 на 1000 человек в год, при этом около 30% инсультов приводят к летальному исходу в остром периоде [1, 2]. В течение последующего года умирают еще 10—15% больных. У 80% выживших после инсульта развивается та или иная степень ограничений в повседневной жизни [3]. В нашей стране инвалидизация вследствие инсульта (3,2 на 10 000 населения в год) опережает другие заболевания [4].
Существенный негативный вклад в инвалидизацию больных после инсульта вносят когнитивные нарушения, поскольку зачастую при отсутствии четкой очаговой симптоматики именно расстройства когнитивной сферы определяют тяжесть состояния больного и трудности в процессе его бытовой и профессиональной адаптации. В течение первого года после ишемического инсульта деменция развивается в 25—30% случаев [5]. Приблизительно в 1/3 случаев она является результатом декомпенсации или активизации предшествующего нейродегенеративного процесса, в остальных случаях постинсультная деменция обусловлена сосудистой мозговой недостаточностью [6—8]. У больных с постинсультной деменцией увеличивается риск развития повторного инсульта, что может быть связано с трудностями проведения вторичной профилактики у этой группы пациентов. Есть данные о том, что наличие выраженного когнитивного дефицита негативно влияет и на восстановление двигательных функций [9—12].
Особой формой когнитивных расстройств является афазия, которая представляет собой нарушение сформировавшейся речи, возникающее при очаговых поражениях коры и прилежащей подкорковой области доминантного полушария головного мозга и являющееся системным расстройством различных форм речевой деятельности при сохранности элементарных форм слуха и движений речевого аппарата [13]. Тотальная и сенсорная афазии в остром периоде отмечаются у 84% больных с кровоизлияниями и у 50% — с ишемическим инсультом в случае поражения доминантного полушария, спустя несколько месяцев сенсомоторная афазия сохраняется у 12—13% больных [6]. Любая форма когнитивных нарушений в целом и речи, в частности, ведет к изменению личности, к нарушению общей и вербальной коммуникации. Меняется поведение больного, его эмоциональное состояние, качество жизни.
Длительное время широко обсуждается вопрос о применении препаратов нейропротективного действия в остром периоде инсульта. Большинство исследователей склоняются к мнению, что раннее назначение нейропротекторов позволяет улучшить прогноз восстановления нарушенных функций, увеличить период «терапевтического окна», уменьшить размеры очага повреждения головного мозга [14—16]. В настоящее время активно ведется поиск эффективных лекарственных средств для первичной и вторичной нейропротекции, проводятся исследования, доказывающие необходимость назначения данных препаратов в остром периоде инсульта.
В настоящее время разработан новый оригинальный нейропротективный препарат для парентерального введения — целлекс (ЗАО «Фарм-Синтез», Россия). Он представляет собой белково-пептидный комплекс из эмбрионального головного мозга свиней, который способен обеспечивать регенерацию нервной ткани человека. Целлекс обладает прямым нейрорепаративным действием, что принципиально отличает его от нейротропных средств из других групп. Прямое репаративное действие целлекса на нейрональный и глиальный клеточные пулы нервной ткани доказано доклиническими исследованиями: в экспериментах с лабораторными животными на моделях острого ишемического повреждения мозга методом фотоиндуцированного тромбоза, на клеточных культурах нейронов мозжечка в модели глутаматной токсичности, а также на моделях глобальной преходящей и неполной гипоксиях мозга.
Полученные результаты явились основанием для проведения клинического исследования «Многоцентровое рандомизированное сравнительное открытое клиническое исследование эффективности и безопасности препарата целлекс в лечении больных с острым нарушением мозгового кровообращения», в котором было предусмотрено изучение влияния целекса на когнитивные и речевые нарушения.
Цель исследования — изучение действия целлекса на восстановление когнитивных и речевых функций в остром периоде инсульта.
Материал и методы
Многоцентровое сравнительное открытое клиническое исследование эффективности и безопасности препарата целлекс в лечении больных с острым инсультом проводилось на 6 клинических базах. В исследование были включены 180 пациентов с инсультом. Диагноз острого нарушения мозгового кровообращения, характер и локализация инсульта устанавливались согласно критериям регистра инсульта Национальной ассоциации по борьбе с инсультом (НАБИ) [5], на основании данных анамнеза (предшествующие заболевания сердечно-сосудистой системы, показатели артериального давления, характер развития неврологических симптомов), клинических данных (неврологический осмотр с оценкой выраженности общемозговых, оболочечных и очаговых симптомов) и данных дополнительных исследований (лабораторные исследования крови и цереброспинальной жидкости, осмотр глазного дна, компьютерная или магнитно-резонансная томография головного мозга, транскраниальная допплерография и дуплексное сканирование сосудов головного мозга с эмболодетекцией).
Критерии включения больных в настоящее исследование: мужчины в возрасте от 35 до 80 лет включительно; женщины в возрасте от 55 до 80 лет включительно, находящиеся в постменопаузальном периоде не менее 2 лет; больные, подписавшие письменное информированное согласие или их ближайшие родственники (при крайней тяжести пациента); больные с острым ишемическим или геморрагическим инсультом в соответствии с критериями МКБ-10, подтвержденными при рентгеновской компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) головного мозга, госпитализированные в течение 1-х суток от развития заболевания.
Критериями исключения являлись: крайняя тяжесть пациента с уровнем сознания ниже 5 баллов по шкале комы Глазго (кома III cт. по отечественной классификации); регресс неврологической симптоматики в течение первых 24 ч от начала заболевания (транзиторная ишемическая атака); наличие у пациента заболеваний или состояний, указанных в противопоказаниях к назначению препарата целлекс: эпилепсия, маниакальный психоз, продуктивный бред, делирий; наличие в анамнезе анафилактических реакций на препараты белковой природы (альбумин, плазма крови, иммуноглобулины, сыворотки); наличие злокачественного новообразования; острые и/или хронические бактериальные и вирусные заболевания в стадии обострения; аутоиммунные заболевания в стадии декомпенсации, сопровождающиеся системным васкулитом; хроническая печеночная или почечная недостаточность в стадии обострения; выраженная или неконтролируемая патология сердца; предшествующая нейротропная метаболическая терапия в течение 14 дней перед госпитализацией пациента.
Среди включенных в исследование больных 147 (81,7%) перенесли ишемический инсульт и 33 (18,3%) — геморрагический инсульт.
К характеристике выборки можно также добавить, что у 148 (82%) больных были выявлены признаки атеросклероза. В 135 (75%) случаях отмечалось сочетание атеросклероза с артериальной гипертензией. В 158 (87,8%) наблюдениях имелась гипертоническая болезнь. Сахарный диабет, сочетающийся с атеросклерозом и артериальной гипертензией, выявлялся у 14 (7,8%) больных. В 78 (43,3%) наблюдениях определялись признаки ишемической болезни сердца, 15 (8,3%) больных ранее перенесли инфаркт миокарда. У 37 (20,5%) больных отмечалась постоянная форма мерцательной аритмии: на фоне коронарокардиосклероза — у 29, на фоне ревматизма — у 8; 8 (4,4%) пациентов ранее перенесли инсульт в том же сосудистом бассейне, из них у 3 этому предшествовали транзиторные ишемические атаки. Все больные были доставлены в стационар в течение первых суток заболевания.
Целлекс применялся на фоне стандартной базисной терапии в виде раствора для подкожного введения по 0,1 мг 1 раз в сутки первые 10 дней и с 21-х по 27-е сутки заболевания. Все препараты, не входящие в стандартную базисную терапию, обладающие нейротропным, антигипоксантным действием, были запрещены к применению на протяжении всего срока исследования. В случае, когда прием данных препаратов на фоне базисной терапии был неизбежен, пациент из исследования исключался.
В зависимости от особенностей терапии больные были разделены на две группы — основную и группу сравнения.
В основную группу из 180 вошли 90 (50%) больных, которым на фоне базисной терапии был назначен целлекс. Их средний возраст был 61,4±9,5 года. Группу сравнения также составили 90 (50%) пациентов, получавших только базисную терапию. Их средний возраст был 62,2±8,9 года.
Кроме того, в зависимости от тяжести состояния больные основной группы и группы сравнения были дополнительно разделены на три подгруппы. При определении тяжести состояния учитывались выраженность изменений сознания и других общемозговых симптомов, оболочечной симптоматики, вегетотрофических расстройств, очаговых неврологических нарушений на момент поступления в клинику. Разделение по тяжести состояния проводилось в соответствии со шкалой инсульта (NIHSS). Легкой степени соответствовали 0—6 баллов, средней — 7—14 баллов, тяжелой — 15 и выше баллов.
В основной группе легкая степень тяжести состояния была определена у 21 (23,3%) больного, средняя — у 49 (54,4%) пациентов и тяжелая — у 20 (22,2%). В группе сравнения легкая степень — в 36 (40%) случаях, средняя — в 44 (49%) и тяжелая — в 10 (11%).
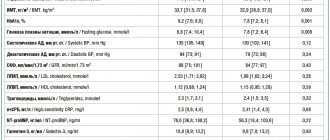
Распределение больных в выделенных группах и подгруппах по возрасту, полу, степени тяжести, характеру и бассейну поражения представлено в табл. 1 и 2.
Таблица 1. Распределение больных основной группы и группы сравнения по полу, типу инсульта, тяжести состояния и бассейну поражения в группе целлекс Примечание. ЛСМА — левая средняя мозговая артерия; ПСМА — правая средняя мозговая артерия; ВББ — вертебрально-базилярная система; ЛП — левое полушарие; ПП — правое полушарие; САК — субарахноидальное кровоизлияние.
Таблица 2. Распределение больных в изученных группах по показателям состояния высших психических функций
Всем больным проводился мониторинг основных физиологических показателей (артериальное давление, частота сердечных сокращений, электрокардиография, частота дыхания, температура тела, гликемия) в первые 48 ч от начала развития инсульта 4—6 раз в сутки в зависимости от тяжести состояния больного. Осуществлялись также коррекция и поддержание показателей гемодинамики, дыхания, водно-электролитного обмена и обмена глюкозы, коррекция отека мозга и повышенного внутричерепного давления, адекватная нутритивная поддержка, профилактика и борьба с осложнениями.
Оценка динамики нарушения высших корковых функций проводилась по тесту ТИПК (Информация—Память—Концентрация внимания) и ОР — опросник речи). Уровень сохранности сознания больных в остром периоде инсульта оценивали также в соответствии со шкалой комы Глазго: значения 8 баллов и ниже свидетельствовали о наличии комы, 9—12 баллов — от сопора до оглушения, 13—15 баллов — от легкой заторможенности до ясного сознания.
Статистическая обработка полученных результатов проводилась с использованием пакета программ Microsoft Exсel 2003 и Statistica 6.0 с использованием пакетов ANOVA и DENOVA. При нормальном распределении признака применялись t
-критерий Стьюдента и дисперсионный анализ с повторными измерениями, при распределении, признака, отличного от нормального, — ранговый дисперсионный анализ, критерии знаков и парных сравнений Вилкоксона, для тестирования зависимости — точный критерий Фишера. Различия считались статистически достоверными при
p
<0,05.
Полное 4-недельное исследование закончили 168 больных; 4 больных выведены по объективным причинам: выявление метастатического поражения мозга, развитие алкогольного делирия, перевод в нейрохирургическое отделение для оперативного лечения внутримозговой гематомы, перевод в стационар другой больницы по настоянию родственников. Из 3 умерших больных группы сравнения у 1 пациентки смерть наступила в результате тромбоэмболии легочной артерии, у 1 пациента развился острый инфаркт миокарда на фоне пароксизма мерцательной аритмии, у 1 пациентки к 3-м суткам отмечалось нарастание общемозговой и очаговой неврологической симптоматики с отеком мозга. Из 5 умерших больных, получавших целлекс, у 1 пациента поставлен патологоанатомический диагноз — опухоль головного мозга, у 1 пациента, поступившего в крайне тяжелом состоянии, отмечалось нарастание отека с вклинением ствола мозга к 3-м суткам, у 3 пациентов, поступивших в тяжелом состоянии, отмечалось прогрессивное нарастание очагового неврологического дефицита и общемозговой симптоматики с декомпенсацией сопутствующей патологии (у 1 пациентки — сахарного диабета 2-го типа и мерцательной аритмии, у 1 пациента — печеночной недостаточности на фоне хронического алкоголизма, у 1 пациента — выраженное прогрессирование сердечно-сосудистой недостаточности на фоне несостоятельности кардиостимулятора).
При анализе состояния высших психических функций по клиническим шкалам (средний балл NIHSS; средний балл расстройств сознания, средние значения по ОР) сравниваемые группы исходно достоверно различались: состояние этих функций у больных, лечившихся целлексом, изначально было достоверно тяжелее, чем в группе сравнения (см. табл. 2).
Оценка динамики неврологического дефицита по клиническим шкалам от 1-х суток к 3, 6, 10, 21-м и 28-м суткам проводилась методом сравнения средних изменений клинического балла в исследуемых группах с применением t-критерия Стьюдента для независимых выборок. Исследование значимости различий между показателями в контрольных точках проводилось методом дисперсионного анализа.
Целлекс® (Cellex)
Фирма-производитель: ФАРМ-СИНТЕЗ ЗАО (Россия)
р-р д/п/к введения 0.1 мг/1 мл: амп. 1 мл или 2 мл 1, 2, 4, 5 или 10 шт. Рег. №: ЛП-001393
Клинико-фармакологическая группа:
Ноотропный препарат
Форма выпуска, состав и упаковка
Раствор для п/к введения
прозрачный, бесцветный или светло-желтый, без запаха или со специфическим запахом; допускается опалесценция.
| 1 мл | |
| целлекс® субстанция-раствор (замороженный, в пересчете на белок*) | 0.1 мг |
Вспомогательные вещества:
глицин — 3.75 мг, натрия гидрофосфата дигидрат — 2.99 мг, натрия дигидрофосфата моногидрат — 0.47 мг, натрия хлорид — 5.85 мг, вода д/и — до 1 мл.
* Состав на 1 мл. Активное вещество:
полипептиды из головного мозга эмбрионов свиней активное вещество в пересчете на общий белок 0.9-2.4 мг (номинальное содержание общего белка 1.65 мг на 1 мл субстанции).
Вспомогательные вещества:
глицин — 3.75 мг, 0.1М раствора динатрия гидрофосфата — до pH 7.8 (около 0.8 мг сухого вещества), натрия хлорид — 5.85 мг, полисорбат 80 — 0.005 мг, вода очищенная — до 1 мл.
1 мл — ампулы темного стекла (1) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные. 1 мл — ампулы темного стекла (1) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные. 1 мл — ампулы темного стекла (2) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные 1 мл — ампулы темного стекла (2) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные. 1 мл — ампулы темного стекла (5) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные. 1 мл — ампулы темного стекла (5) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные. 2 мл — ампулы темного стекла (1) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные. 2 мл — ампулы темного стекла (1) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные. 2 мл — ампулы темного стекла (2) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные. 2 мл — ампулы темного стекла (2) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные. 2 мл — ампулы темного стекла (5) — упаковки ячейковые контурные из пленки поливинилхлоридной (1) — пачки картонные. 2 мл — ампулы темного стекла (5) — упаковки ячейковые контурные из пленки поливинилхлоридной (2) — пачки картонные.
Описание активных компонентов препарата «Целлекс®»
Фармакологическое действие
Ноотропный препарат. Наличие тканеспецифических сигнальных белков и полипептидов — факторов роста, факторов дифференцировки нервных клеток в препарате обуславливает его прямое нейрорепаративное действие, за счет регуляции концентраций пула нейротрансмиттеров, с торможением спиловера возбуждающих аминокислот.
Препарат активирует вторичную нейропротекцию за счет стимуляции процессов синаптогенеза, восстановления сигналов аутофагии, улучшения тканевой иммунорегуля ции с торможением иммуногенной цитотоксичности макрофагов. При этом отмечается тканеспецифическое и системное репаративное действие препарата с восстановлением регенеративного и репаративного потенциала клеток мозга, уменьшение числа поврежденных клеток и выраженности перифокального отека в зоне пенумбры (позволяет добиться значительного ограничения очага некроза мозговой ткани) с восстановлением микроциркуляции и общей перфузии.
Восстановление и регуляторная стимуляция различных компартментов ЦНС с системным воздействием факторов роста, дифференцировки и сигнальных молекул обеспечивает снижение сроков восстановления и реабилитации пациентов с повреждениями центральной и периферической нервной системы сосудистого генеза и восстановлением двигательной, чувствительной и когнитивной функций.
Терапевтический эффект обычно развивается через 3-5 дней после начала введения препарата.
Показания
Цереброваскулярные болезни:
—
острые нарушения мозгового кровообращения в остром и раннем реабилитационном периоде течения заболевания в составе комплексной терапии.
Режим дозирования
Взрослым
препарат назначают в дозе 0.1-0.2 мг 1 раз/сут п/к в течение 10 дней в зависимости от тяжести состояния больного. При необходимости проводят повторный курс через 10 дней.
Исследования по применению препарата у детей
не проводились.
Побочное действие
Возможно:
аллергические реакции в виде невыраженной гиперемии в месте введения, реакции гиперчувствительности (кожная сыпь, зуд, ангионевротический отек), субфебрилитет, нарушение сна, головная боль.
Противопоказания
— эпилепсия;
— маниакальный психоз;
— продуктивный бред;
— делирий;
— возраст до 18 лет (в связи с недостаточностью клинических данных).
С осторожностью
следует назначать препарат при наличии в анамнезе аллергических реакций на препараты белково-пептидной природы.
Беременность и лактация
При беременности действие препарата не изучено. Отсутствие соответствующих исследований не позволяет применять препарат у данного контингента больных.
Применение для детей
Исследования по применению препарата в детской практике не проводились.
Особые указания
С особой осторожностью следует назначать препарат при артериальной гипертензии злокачественного течения в стадии декомпенсации, симпато-адреналовых кризах по типу панических атак, выраженных тревожно-депрессивных расстройствах.
Препарат не содержит прионовых инфекций и вирусов.
Влияние на способность к вождению автотранспорта и управлению механизмами
В настоящее время не имеется данных о влиянии препарата Целлекс® на способность к управлению автомобилем и работе с механизмами, требующей повышенного внимания и скорости психических и двигательных реакций.
Передозировка
В настоящее время случаев передозировки препарата Целлекс® не отмечено.
Лекарственное взаимодействие
При совместном применении с психостимулирующими препаратами и алкоголем возможно психомоторное возбуждение, нарушения сна.
Возможно уменьшение активности средств для наркоза, транквилизаторов, нейролептиков.
Условия отпуска из аптек
Препарат отпускается по рецепту.
Условия и сроки хранения
Препарат следует хранить в защищенном от света, недоступном для детей месте при температуре от 2° до 8°С. Срок годности — 1 год.
Лекарственное взаимодействие
При совместном применении с психостимулирующими препаратами и алкоголем возможно психомоторное возбуждение, нарушения сна.
Возможно уменьшение активности средств для наркоза, транквилизаторов, нейролептиков.
Целлекс р-р п/к введ 0 ,1 мг/мл 1 мл амп N 5
Действующее вещество:
Полипептиды из головного мозга эмбрионов свиней
АТХ
N06BX Психостимуляторы и ноотропные препараты другие
Фармакологические группы
- Ноотропные средства, прочие средства, влияющие на нервную систему [Ноотропы]
- Ноотропные средства, прочие средства, влияющие на нервную систему [Другие нейротропные средства]
Состав
| Раствор для подкожного введения | 1 мл |
| активное вещество: | |
| Целлекс® субстанция-раствор (замороженный в пересчете на белок1) | 0,1 мг |
| вспомогательные вещества: глицин — 3,75 мг; натрия гидрофосфата дигидрат — 2,99 мг; натрия дигидрофосфата моногидрат — 0,47 мг; натрия хлорид — 5,85 мг; вода для инъекций — до 1 мл | |
| 1 состав на 1 мл: активное вещество — полипептиды из головного мозга эмбрионов свиней, в пересчете на общий белок — 0,9–2,4 мг (номинальное содержание общего белка — 1,65 мг на 1 мл субстанции); вспомогательные вещества — глицин — 3,75 мг, 0,1М раствор динатрия гидрофосфата — до рН 7,8 (около 0,8 мг сухого вещества), натрия хлорид — 5,85 мг, полисорбат 80 — 0,005 мг, вода очищенная — до 1 мл |
Описание лекарственной формы
Раствор: прозрачная бесцветная или светло-желтая жидкость, без запаха или со специфическим запахом. Допускается опалесценция. Допускается наличие отдельных нитей коагулята.
Фармакологическое действие
Фармакологическое действие — нейропротективное.
Фармакодинамика
Наличие тканеспецифических сигнальных белков и полипептидов — факторов роста, дифференцировки нервных клеток в препарате — обусловливает его прямое нейрорепаративное действие за счет регуляции концентраций пула нейротрансмиттеров с торможением спиловера возбуждающих аминокислот.
Препарат активирует вторичную нейропротекцию за счет стимуляции процессов синаптогенеза, восстановления сигналов аутофагии, улучшения тканевой иммунорегуляции с торможением иммуногенной цитотоксичности макрофагов. При этом отмечается тканеспецифическое и системное репаративное действие препарата с восстановлением регенеративного и репаративного потенциала клеток мозга, уменьшением числа поврежденных клеток и выраженности перифокального отека в зоне пенумбры (позволяет добиться значительного ограничения очага некроза мозговой ткани) с восстановлением микроциркуляции и общей перфузии.
Восстановление и регуляторная стимуляция различных компартментов ЦНС с системным воздействием факторов роста, дифференцировки и сигнальных молекул обеспечивает снижение сроков восстановления и реабилитации пациентов с повреждениями ЦНС и периферической нервной системы сосудистого генеза и восстановление двигательной, чувствительной и когнитивной функций. Терапевтический эффект обычно развивается через 3–5 дней после начала введения препарата.
Фармакокинетика
Сложный состав препарата Целлекс®, активная фракция которого состоит из сбалансированной и стабильной смеси биологически активных белков и полипептидов, обладающих суммарным полифункциональным действием, не позволяет провести обычный фармакокинетический анализ отдельных компонентов.
Показания препарата Целлекс®
Цереброваскулярные болезни — острые нарушения мозгового кровообращения в остром и раннем реабилитационном периоде течения заболевания, в составе комплексной терапии.
Противопоказания
эпилепсия;
маниакальный психоз;
продуктивный бред;
делирий;
возраст до 18 лет (в связи с недостаточностью клинических данных).
С осторожностью: аллергические реакции на препараты белково-пептидной природы в анамнезе.
Применение при беременности и кормлении грудью
Отсутствие соответствующих исследований не позволяет применять препарат у данного контингента больных.
Побочные действия
Могут отмечаться аллергические реакции в виде невыраженной гиперемии в месте введения, реакции гиперчувствительности (кожная сыпь, зуд, ангионевротический отек), субфебрилитет, нарушение сна, головная боль.
Взаимодействие
При совместном применении с психостимулирующими препаратами и алкоголем возможно психомоторное возбуждение, нарушения сна.
Возможно уменьшение активности средств для наркоза, транквилизаторов, нейролептиков.
Способ применения и дозы
П/к.
Взрослые: 0,1–0,2 мг 1 раз в сутки п/к в течение 10 дней, в зависимости от тяжести состояния больного. При необходимости проводят повторный курс через 10 дней. Исследования по применению препарата в детской практике не проводились.
Правила введения раствора
Препарат вводится п/к через стерильный шприцевый фильтр, входящий в комплект.
Для введения набирают необходимое количество препарата Целлекс® в шприц, снимают иглу, затем надевают на шприц стерильный шприцевый фильтр с диаметром пор 0,22 мкм. Берут новую иглу и надевают ее на стерильный шприцевый фильтр. Препарат готов к применению.
Передозировка
В настоящее время случаи передозировки препарата Целлекс® не отмечены.
Особые указания
С особой осторожностью назначается при артериальной гипертензии злокачественного течения в стадии декомпенсации, симпатоадреналовых кризах по типу панических атак, выраженных тревожно-депрессивных расстройствах.
При беременности действие препарата не изучено.
Препарат не содержит прионовые инфекции и вирусы.
Влияние на способность управлять транспортными средствами и работать с механизмами. В настоящее время не имеется данных о влиянии препарата Целлекс® на способность к управлению автомобилем и работу с механизмами, требующими повышенного внимания и скорости психических и двигательных реакций.
Форма выпуска
Раствор для подкожного введения, 0,1 мг/мл. В ампулах темного стекла вместимостью 1 или 2 мл импортных, имеющих кольцо натяжения для вскрытия, или ампулах, имеющих точку разлома, 1 или 2 мл. Допускается цветовая маркировка ампул в виде двух зеленых полосок. 1, 2, 5 амп. по 1 или 2 мл в контурной ячейковой упаковке из пленки ПВХ. 1 или 2 контурные ячейковые упаковки в пачке картонной. В каждой пачке стерильные шприцевые фильтры с диаметром пор 0,22 мкм в количестве, равном количеству ампул.
Условия отпуска из аптек
По рецепту.
Целлекс
Целлекс – лекарственное средство группы ноотропов. Включает в свой состав тканеспецифичные белки, передающие сигналы между клетками, полипептидные факторы роста, факторы дифференциации нейронов. Обладает нейрорепаративным эффектом. Регулирует содержание и соотношение нейромедиаторов с подавлением диффузии возбуждающих аминокислот. Стимулирует процессы зарождения и развития синапсов. Восстанавливает сигналы, инициирующие аутофагию. Улучшает иммунорегуляцию на уровне клеток и тканей. Подавляет токсичность гистофагоцитов по отношению к клеткам. Способствует регенерации и репарации клеток головного мозга, защищает их от повреждения. Уменьшает перифокальный отек в зоне ишемической полутени. Ограничивает очаг омертвения тканей головного мозга. Восстанавливает микроциркуляцию в коре головного мозга, способствует насыщению кровью церебральных тканей. Терапевтический эффект от приема препарата развивается, как правило, на 3-5 сутки после начала медикаментозного курса. Кратность применения – 1 раз в день. Продолжительность лечения составляет в среднем 10 суток в зависимости от клинической ситуации и выраженности терапевтического ответа. Допускается возможность проведения повторного курса, который проводят после 10-дневного перерыва. В педиатрической практике препарат не используется в связи с отсутствием клинических данных о его эффективности и безопасности у данной категории пациентов. Целлекс вводится подкожно с помощью специального шприца, который поставляется с препаратом. При введении используют стерильную фильтр-насадку на шприц. Забор необходимого количества раствора и его введение осуществляется разными иглами. При применении Целлекса возможны локальные аллергические реакции, выражающиеся в притоке крови к месту инъекции, кожной сыпи, ощущении болезненно-щекочущего раздражения кожных покровов, вызывающем потребность чесать раздражённое место, ангионевротическом отеке, повышении температуры тела до субфебрильных значений, снижении качества сна, головных болях.
Целлекс не применяют при эпилепсии, маниакально-депрессивном психозе, бредовых состояниях, белой горячке, а также в период беременности и грудного вскармливания (в связи с отсутствием данных). Лица со злокачественной декомпенсированной артериальной гипертензией, паническими атаками, тяжело протекающими смешанными тревожно-депрессивными расстройствами должны принимать Целлекс с особой осторожностью. Лекарственное средство не содержит инфекционных агентов, размножение которых происходит без участия нуклеиновых кислот. При наличии у пациента в анамнезе аллергии на лекарственные средства на основе белков следует обеспечить ему регулярное медицинское наблюдение. При сочетании Целлекса с лекарственными средствами, стимулирующими ЦНС, и с этанолсодержащими продуктами возможно возникновение двигательного беспокойства, речевого возбуждения, расстройств сна. Целлекс может снижать эффект транквилизаторов, антипсихотических средств. Эффективность препарата при цереброваскулярных заболеваниях подтверждена клинически. В нашей стране подобные заболевания являются острейшей проблемой, причем не только медицинской, но и социальной. Каждый год «прирастает» 450 тысячами случаев инсультов, половина из которых летальны уже в первый год. Целлекс позволяет предупредить острые нарушения кровообращения в тканях головного мозга, а также ускоряет сроки восстановления после ишемических эпизодов.