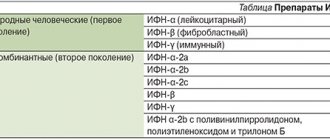
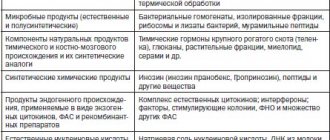
Фармакодинамика и фармакокинетика
Вещество обладает способностью ингибировать процесс выработки фосфокиназы, останавливать процессы фосфорилирования белков в зараженных вирусом клетках. Средство полностью и необратимо инактивирует вирус опоясывающего лишая и герпеса, когда они находятся вне клеток. Происходит блокировка внедрения активных частиц вируса внутрь здоровых клеток, вредоносный агент утрачивает способность синтезировать новые структурные компоненты.
При местном использовании соединение обладает способностью накапливаться в пораженных клетках, при этом, практически не подвергаясь системной абсорбции.
Эффективное применение глицирризиновой кислоты при вирусных инфекциях половых органов
Вирусные инфекции половых органов продолжают привлекать пристальное внимание исследователей и клиницистов вследствие роста заболеваемости, значительной контагиозности и потенциальной онкогенности.
Рисунок 1. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при генитальном герпесе
Рисунок 2. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при генитальном герпесе
Рисунок 3. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при папилломавирусной инфекции
Рисунок 4. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при папилломавирусной инфекции
Рисунок 5. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при цитомегаловирусной инфекции
Рисунок 6. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при цитомегаловирусной инфекции
Исследования последних лет показали, что вирусы способны поддерживать воспалительный процесс в зоне поражения с изменением структурно-функциональных характеристик ткани, вызывать изменения антигенной структуры инфицированных клеток, индуцируя появление аутоантител, могут быть индукторами неопластических трансформаций. Локальные изменения слизистых оболочек и кожи при вирусной инвазии проявляются появлением в ткани воспалительных инфильтратов, активацией клеток иммунной системы, изменением уровня цитокинов, факторов роста и протеолитических ферментов, активацией ангиогенеза, изменением экспрессии генов.
Корень солодки Glycyrrhiza glabra –
одно из наиболее известных лекарств в мире, которое было известно еще шумерам и является классическим средством в китайской и тибетской медицине. О нем в своих работах упоминал Гиппократ, Феофраст описывал его как «скифский корень с Азовского моря». В целом солодка используется в качестве лечебного средства более 5000 лет. В конце 70-х годов прошлого столетия впервые было показано, что вещество, выделенное из корня солодки, подавляет активность вирусов. Наиболее активным веществом солодкового корня можно назвать глицирризиновую кислоту, которая сходна по строению со стероидными гормонами, в частности с фенантреновой частью стероидов.
Препараты солодки обладают многосторонней биологической активностью и оказывают противовоспалительное, противовирусное и иммуномодулирующее действие. Противовоспалительное действие заключается в купировании воспалительных реакций, вызываемых гистамином, серотонином и брадикинином. Кислота ингибирует активность фосфолипазы А и образование простагландина Е2 в активированных макрофагах, ускоряет миграцию лейкоцитов в зону воспаления. При этом угнетается как экссудативная, так и пролиферативная фаза воспалительного процесса. Как показали исследования, глицирризиновая кислота обладает также выраженным противовирусным действием. Первое исследование антивирусных свойств глицирризиновой кислоты было проведено в 1979 году, а в 90-е годы было установлено, что она прерывает репликацию вирусов на ранних стадиях за счет ингибирования киназы Р.
В ряде исследований было показано, что мутантные штаммы вирусов, резистентные к ацикловиру, сохраняют чувствительность к глицирризиновой кислоте. При взаимодействии кислоты с вирионами изменяются различные фазы вирусного цикла, что сопровождается необратимой инактивацией вирусных частиц, находящихся в свободном состоянии вне клеток; блокируется внедрение активных вирусных частиц внутрь клетки, нарушается способность вируса к индукции синтеза новых вирусных частиц.
Глицирризиновая кислота обладает также выраженным иммуномодулирующим действием. Показана способность глицирризиновой кислоты индуцировать образование ИФН и активировать неспецифические факторы клеточного иммунитета.
С целью исследования локального действия глицирризиновой кислоты (экстракт Glicyrriza
glabra,
препарат Эпиген-интим, «Cheminova») при вирусных инфекциях половых органов в исследование были включены 100 женщин в возрасте от 17 до 40 лет, наличие инфицирования у которых доказано путем детекции в половом тракте вирусной ДНК методом полимеразной цепной реакции.
Все пациентки были разделены на группы:
- I группа – 30 женщин с папилломавирусной инфекцией половых органов;
- II группа – 30 женщин с типичной формой генитального герпеса (легкой и средней степени тяжести);
- III группа – 30 женщин с цитомегаловирусной инфекцией половых органов;
- контрольная группа – 10 здоровых женщин репродуктивного возраста.
В исследовании с целью оценки механизма действия исследуемого препарата использовалась модель моноинфекции и монотерапии. В каждой группе пациенткам проводили местную терапию глицирризиновой кислотой (n = 20) или препаратом плацебо (n = 10) в течение 1 мес., препарат наносили ежедневно по 2-3 раза на слизистые оболочки половых органов путем распыления, при локализации поражений на шейке матки препарат применяли интравагинально с помощью специальной насадки. Назначение препарата или плацебо в группах проводили слепым методом. Во время исследования лечение другими противовирусными препаратами не проводилось. Клиническую эффективность терапии оценивали в ходе лечения, период последующего наблюдения составил 6 мес.
С целью оценки локального действия глицирризиновой кислоты (до лечения и сразу после его окончания) исследовали слизь цервикального канала на содержание провоспалительных Th1-цитокинов –
IL-1b, IL-6, TNF-α и IFN-γ, противовоспалительных Th2-цитокинов – IL-4, IL-10, а также матриксных металлопротеиназ ММР-1 и тканевых ингибиторов матриксных металлопротеиназ ТIМР-1.
Слизь из цервикального канала брали универсальным зондом, встряхиванием на вортексе в течение 1 минуты, смывали в 1 мл фосфатно-солевого раствора. Далее центрифугировали в течение 3 мин. при 3000 об./мин. Надосадок немедленно замораживали и хранили до выполнения реакций при температуре 80ºС. В образцах слизи из цервикального канала с помощью иммуноферментного анализа определяли содержание IL-1b, IL-6, IL-10, IFN-g, TNF-a, IL-4 («Цитокин», Россия), а также тканевых MMP-1 и TIMP-1 («Chemicon», США). Уровни факторов в цервикальной слизи нормировали по содержанию белка в пробах, который определяли колориметрическим методом с помощью бицинхониновой кислоты («Sigma», США).
Анализ динамики клинических симптомов инфекции после применения глицирризиновой кислоты свидетельствует о высокой клинической эффективности препарата. При типичной форме генитального герпеса на фоне лечения длительность и клиническая выраженность рецидивов герпеса по субъективной оценке больных значительно уменьшилась, что позитивно повлияло на качество жизни пациенток. По сравнению с плацебо на фоне применения глицирризиновой кислоты отмечалось быстрое купирование симптомов вульводинии (зуда, жжения, дискомфорта в области герпетических высыпаний вульвы и влагалища); более быстрое заживление поражений (в среднем на 2 ± 0,78 дня по сравнению с плацебо); ускорение процессов эпителизации зон поражения; значительное сокращение зоны гиперемии вокруг герпетических элементов и реакции регионарных лимфатических узлов. Значительное снижение на фоне лечения местной воспалительной реакции, окружающей герпетические элементы, и ускорение процессов репарации ткани способствовало снижению риска присоединения вторичной бактериальной инфекции и развитию осложнений.
На фоне терапии глицирризиновой кислотой у пациенток с экзофитными формами папилломавирусной инфекции гениталий отмечалось купирование симптомов стойкого дискомфорта, зуда и жжения в области наружных половых органов через 4-6 дней от начала применения препарата. При наличии небольших и множественных кондилом вульвы и влагалища отмечено значительное уменьшение экзофитных образований в размере и общей площади поражения. При цитомегаловирусной инфекции исходно только у 6 пациенток отмечались симптомы вульводинии, которые были быстро купированы на фоне терапии глицирризиновой кислотой.
Основной задачей исследования была оценка влияния глицирризиновой кислоты на локальные молекулярно-биологические процессы в половом тракте при вирусных инфекциях. При анализе содержания провоспалительных цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале до лечения во всех группах было выявлено, что персистенция вирусной инфекции сопровождалась значительным увеличением уровня Th1-цитокинов, что отражало интенсивность воспалительных реакций в ткани и являлось важным маркером фазы активации вирусной инфекции. При всех типах вирусной инфекции локальные уровни Th1-цитокинов достоверно превышали контрольные значения:
- при генитальном герпесе в I группе уровень IL-1b был повышен в 33,2 раза, IL-6 – в 3,5 раза, TNF-α – в 4,6 раза и IFN-γ – в 3,6 раза;
- при папилломавирусной инфекции во II группе уровень IL-1b был повышен в 62,4 раза, IL-6 – в 2,4 раза, TNF-α – в 13,6 раза и IFN-γ – в 3 раза;
- при цитомегаловирусной инфекции в III группе уровень IL-1b был повышен в 18,6 раза, IL-6 – в 1,3 раза, TNF-α – в 3,7 раза и IFN-γ – в 2,8 раз (во всех случаях p
Уровни регуляторных противовоспалительных Th2-цитокинов IL-4 и IL-10 во всех группах до лечения были ниже контрольных значений, что свидетельствует об индуцированном вирусами угнетении системы противовоспалительной защиты ткани, однако эти изменения были достоверно не значимы – p > 0,05 (рисунки: 1, 3, 5).
При анализе системы тканевых протеолитических ферментов матриксных металлопротеиназ и их ингибиторов как ключевых эффекторов тканевого ремоделирования и важных маркеров воспалительного процесса во всех группах выявлено повышение локальной активности ММР-1 (рисунки: 2, 4, 6).
После курса терапии глицирризиновой кислотой локальные уровни Th1-цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале достоверно снизились до контрольных значений, при этом динамика изменений была особенно показательна в I группе пациенток с генитальным герпесом, где исходная интенсивность воспалительных реакций была максимальной (рисунки 1, 3 и 5).
Терапия глицирризиновой кислотой привела к усилению защитного потенциала слизистой оболочки – к активации противовоспалительных Th2-цитокинов, при этом уровни IL-4 и IL-10 повысились, в ряде случаев превысив контрольные значения. При применении плацебо уровни провоспалительных Th1-цитокинов и регуляторных Th2-цитокинов незначительно колебались за счет волнообразности самого вирусного инфекционного процесса, но достоверно не изменились (p > 0,05 во всех группах по сравнению с исходными значениями и контролем).
При анализе действия глицирризиновой кислоты на уровень тканевых матриксных металлопротеиназ выявлено достоверное снижение после лечения активности протеолитических ферментов до контрольных значений:
- в I группе уровень ММР-1 снизился в 2,25 раза (p
- во II группе – в 1,9 раза (p
- в III группе – уровень ММР-1 снизился незначительно (p > 0,05).
Терапия препаратом привела к повышению протективных свойств слизистой оболочки – выявлено повышение до контрольных значений уровня тканевых ингибиторов металлопротеиназ: уровень ТIМР-1 достоверно повысился в I и II группах (p
На фоне применения плацебо во всех группах отмечено дальнейшее прогрессирование нарушений в системе ММР-1/ТIМР-1 с активацией матриксных металлопротеиназ и снижением содержания тканевых ингибиторов матриксных металлопротеиназ.
Обсуждение
Хроническая персистенция вирусных агентов в слизистых оболочках приводит к нарушению медиаторных взаимодействий, изменению ангиоархитектоники ткани, активации факторов роста, которые, в свою очередь, активируют процессы пролиферации клеток и ангиогенез. При нарушении медиаторных взаимодействий и клеточного ансамбля иммунный барьер слизистых оболочек и кожи неполноценен, что приводит к активации условно-патогенной флоры, присоединению вторичной инфекции и в конечном итоге к усилению воспалительного процесса.
Применение глицирризиновой кислоты при вирусной инвазии привело к нормализации локального соотношения цитокинов Th1 и Th2 типов: уровни ключевых провоспалительных цитокинов IL-1, IL-6, TNF-α и IFN-γ снизились до контрольных значений, уровни противовоспалительных цитокинов IL-4, IL-10 повысились, что доказывает выраженный противовоспалительный и иммуномодулирующий эффект препарата. Одновременно было выявлено нормализующее влияние глицирризиновой кислоты на систему матриксных металлопротеиназ и их ингибиторов со снижением патологического литического потенциала инфекционных агентов. Таким образом, показано антидеструктивное и протективное действие препарата.
В целом глицирризиновая кислота может быть успешно использована в комплексной терапии вирусных инфекций гениталий. Применение препарата разрешено в период беременности и кормления грудью.
Глицирризиновая кислота, инструкция по применению (Способ и дозировка)
Режим дозирования определяется индивидуально.
Спрей используют для наружного применения. Препарат распыляют в течение некоторого времени (нескольких секунд) на пораженную поверхность на расстоянии 5 см. Кратность применения – до 6 раз в день.
Продолжительность лечения – от 5 до 10 дней.
Вагинально средство назначают по 3-4 раза в день, в течение одной недели – 10 дней. Через 10 дней рекомендуется заново повторить курс.
Крем наносится на пораженный вирусом участок 3-5 раз в день в течение недели или 10 дней.
Клинические исследования глицирризиновой кислоты
Глицирризиновая кислота (ГК) является основным активным компонентом корня солодки, которая успешно применяется в медицине уже более 3000 лет.
На сегодняшний день эффективность и безопасность ГК при заболеваниях печени хорошо изучены. Тем не менее, научный интерес к данному веществу сохраняется и продолжается поиск новых перспективных областей его применения в медицине. Так, в наиболее крупной базе медицинской информации – PubMed – размещено более 1400 публикаций, посвященных ГК. Среди них – результаты 54 клинических исследований, 31 из которых является рандомизированным, то есть, представляет «золотой стандарт» исследований лекарственных препаратов.
Результаты клинических исследований
Рандомизированное клиническое исследование ГК при неалкогольной жировой болезни печени (НАЖБП), включавшее 66 пациентов, продемонстрировало, что она достоверно уменьшает выраженность воспаления в печени, снижая уровень аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ).
Аналогичные результаты были получены в 12 рандомизированных клинических исследованиях ГК при алкогольной болезни печени с общей численностью участников 838 человек.
В 2-х рандомизированных клинических исследованиях у 436 пациентов с ХГС после неэффективной противовирусной терапии (ПВТ) было показано положительное влияние ГК на воспаление (достоверное снижение уровня АЛТ). А в одном из них также было продемонстрировано уменьшение степени фиброза.
Кроме того, в ретроспективном исследовании 1249 пациентов, было выявлено, что длительное введение ГК (в течениеи нескольких лет) при ХГС, в случае невозможности излечения противовирусными препаратами, достоверно уменьшает частоту развития наиболее грозного осложнения данного заболевания – первичного рака печени.
Во всех этих исследованиях профиль безопасности ГК был оценен, как благоприятный.
Имеющаяся доказательная база позволила включить ГК в рекомендации Азиатско-Тихоокеанской Ассоциации по изучению печени (APASL) и разрешить ГК для медицинского применения у человека Европейским медицинским агентством (EMA).
Фосфоглив* – лекарственный препарат на основе глицирризиновой кислоты и эссенциальных фосфолипидов
Фосфоглив* является средством патогенетической терапии. Его действие направлено на коррекцию нарушений функций печени. В состав препарата входят эссенциальные фосфолипиды и описанная выше глицирризиновая кислота.
Эссенциальные фосфолипиды обладают мембраностабилизирующим действием, способствуя восстановлению поврежденных клеток печени.
Глицирризиновая кислота в составе препарата оказывает противовоспалительное, антиоксидантное и антифибротическое действие. Благодаря ей средство показывает высокую степень эффективности не только при лечении воспаления, но и в целях профилактики.
Ипатова О.М. Фосфоглив: механизм действия и применение в клинике. Под ред. академика РАМН Арчакова А.И. М.: Изд. ГУ НИИ биомедицинской химии РАМН, 2005. с. 318.1
Ali Akbar Hajiaghamohammadi, Amir Ziaee, Rasoul Samimi. The Efficacy of Licorice Root Extract in Decreasing Transaminase Activities in Non-alcoholic Fatty Liver Disease: A Randomized Controlled Clinical Trial // Phytotherapy Research. 2012; 26 (9): 1381–1384.2
Community herbal monograph on Glycyrrhiza glabra L. and/or Glycyrrhiza inflata Bat. and/or Glycyrrhiza uralensis Fisch., radix. Committee on Herbal Medicinal Products (HMPC). 22 May 2012. EMA/HMPC/571119/2010.3
Kenji Ikeda, Yasuji Arase, Masahiro Kobayashi et al. A Long-Term Glycyrrhizin Injection Therapy Reduces Hepatocellular Carcinogenesis Rate in Patients with Interferon-Resistant Active Chronic Hepatitis C: A Cohort Study of 1249 Patients // Digestive Diseases and Sciences. 2006; 51 (3): 603–609.4
M. P. Manns, H. Wedemeyer, A. Singer et al. Glycyrrhizin in patients who failed previous interferon alpha-based therapies: biochemical and histological effects after 52 weeks // Journal of Viral Hepatitis. 2012; 19: 537–546.5
Masao Omata, Tatsuo Kanda, Ming-Lung Yu et al. APASL consensus statements and management algorithms for hepatitis C virus infection // Hepatol Int. DOI 10.1007/s12072-012-9342-y.6
Meng Wei,Yu Liang-zhu,Wang Li. Effects of Compound Glycyrrhizin on Liver Function in Patients with Alcoholic Liver Diseases: a Meta-analysis // China Pharmacy. 2013; 24 (12): 1116-1118.7
Tekla GJ Van Rossum, Arnold G Vulto, Wim CJ Hop et al. Intravenous glycyrrhizin for the treatment of chronic hepatitis C: a double blind, randomized, placebo-controlled phase I/II trial // Journal of gastroenterology and hepatology. 1999; 14: 1093-1099.8
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня: Гепатосан
Сирепар
Гепатомакс
Фосфоглив
Фосфоглив форте
Тиотриазолин
Карсил Форте
Дарсил
Силибор
Карсил
Эрбисол
Силимар
Метионин
Ремаксол
Энерлив
Лаеннек
Прогепар
Антраль
Калия оротат
Легалон
Торговое название Глицирризиновой кислоты: Тринатриевая соль глицирризиновой кислоты, Эпиген Интим, Глицирризин.
Сочетание Глицирризиновая кислота + Фосфолипиды находится в препаратах: Хепабос, Фосфоглив, Фосфоглив Форте.
Купить Фосфоглив капсулы №50 в аптеках
Торговое наименование:
Фосфоглив®
Международное непатентованное или группировочное наименование:
Глицирризиновая кислота +Фосфолипиды
Лекарственная форма:
капсулы.
Состав
на одну капсулу:
Действующие вещества: фосфолипиды (Липоид С 80) (в пересчете на 100 % вещество) (основной компонент фосфатидилхолин 73-79 %) – 65,0 мг, натрия глицирризинат (тринатриевая соль глицирризиновой кислоты) – 35,0 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая — 141,2 мг, кальция карбонат — 204,7 мг, кальция стеарат — 0,9 мг, тальк — 7,7 мг, кремния диоксид коллоидный (аэросил) — 5,5 мг
Капсулы твердые желатиновые – 96,0 мг [Состав капсулы: корпус: краситель солнечный закат желтый (Е110) — 1,0000%, титана диоксид (Е171) — 1,0000 %, желатин — до 100,0%; крышечка: титана диоксид (Е171) — 0,2000 %, краситель железа оксид черный (Е172) — 3,5000 %, желатин — до 100,0 %].
Описание:
капсулы твердые желатиновые № 0, корпус капсулы – оранжевого цвета, крышка – черного цвета. Содержимое капсулы – гранулированный порошок от белого со слегка желтоватым оттенком до светло-желтого цвета, со слабым специфическим запахом.
Фармакотерапевтическая группа:
гепатопротекторное средство
Фармакологические свойства
Фармакодинамика
Комбинированное средство. Оказывает гепатопротекторное, мембраностабилизирующее и противовирусное действие.
Глицирризиновая кислота оказывает гепатопротекторное действие за счет антиоксидантного, противовоспалительного эффектов, а также влияния на фиброгенез.
Антиоксидантное действие. Глицирризиновая кислота связывает свободные кислородные радикалы и ингибирует ферменты, инициирующие перекисное окисление липидов (ПОЛ) в гепатоцитах.
Противовоспалительное действие. Глицирризиновая кислота уменьшает воспаление за счет ингибирующего влияния на NF-kB- и TLR4-сигнальные пути; угнетения продукции провоспалительных цитокинов (ФНО α, ИЛ-1, ИЛ-6, ИЛ-8); стимулирования продукции противовоспалительных цитокинов (ИЛ-2, ИЛ- 10, ИЛ-12).
Глицирризиновая кислота ингибирует 11β-оксистероиддегидрогеназу, что способствует повышению эндогенного кортизола в крови (псевдокортикостероидный эффект).
Влияние на фиброгенез связано с уменьшением экспрессии гена коллагена 1-го типа и снижением продукции коллагена звездчатыми клетками печени (клетками Ито), а также разрушением активированных клеток Ито через систему натуральных киллеров, что способствует замедлению прогрессирования фиброза.
Подавляет репродукцию вирусов в печени и других органах за счет стимуляции продукции интерферонов, повышения фагоцитоза, увеличения активности естественных клеток-киллеров.
При поражениях кожи за счет противовоспалительного действия ограничивает распространение процесса и способствует регрессу заболевания.
Фосфатидилхолин (действующее вещество фосфолипидов) является основным структурным элементом клеточных и внутриклеточных мембран, восстанавливает их структуру и функции при повреждении, оказывая мембраностабилизирующее действие. Нормализует белковый и липидный обмены, предотвращает потерю гепатоцитами ферментов и других активных веществ, способствует восстановлению функций печени.
Фармакокинетика
Глицирризиновая кислота
После перорального приема в кишечнике под влиянием фермента β-глюкуронидазы, продуцируемого бактериями нормальной микрофлоры, из глицирризиновой кислоты образуется активный метаболит — β-глицирретовая кислота, которая всасывается в системный кровоток. В крови β-глицирретовая кислота связывается с альбумином и практически полностью транспортируется в печень. Выделение β -глицирретовой кислоты происходит преимущественно с желчью, в остаточном количестве — с мочой.
По экспериментальным данным, фосфолипиды улучшают липофильные свойства глицирризиновой кислоты, увеличивая интенсивность и скорость ее всасывания более чем в 2 раза.
Фосфатидилхолин
Более 90% принятых внутрь фосфолипидов всасывается в тонкой кишке. Большая часть их расщепляется фосфолипазой А до 1 -ацетил-лизофосфатидилхолина, 50% которого подвергается обратному ацетилированию в полиненасыщенный фосфатидилхолин в процессе всасывания в слизистой оболочке кишечника. Полиненасыщенный фосфатидилхолин с током лимфы попадает в кровь, откуда, главным образом, в связанном с липопротеинами высокой плотности виде поступает в печень. Фармакокинетика у людей изучалась с помощью диленолеил фосфатидилхолина с радиоактивной меткой –3Н (холиновая часть) и 14C (остаток линолевой кислоты). Максимальная концентрация 3Н достигается через 6-24 часа, составляя 19,9% от назначенной дозы; 14С – через 4-12 часов, составляя 27,9%. Период полувыведения холинового компонента равен 66 часам, остатка линолевой кислоты – 32 часам. В кале обнаруживается 2% 3Н и 4,5% — 14С; в моче – 6% 3Н и минимальное количество 14С. Оба изотопа всасываются в кишечнике более, чем на 90%.
Показания к применению
— Жировая дегенерация печени (гепатоз), алкогольные, токсические, в том числе лекарственные, поражения печени. — В составе комплексной терапии вирусных гепатитов, цирроза печени и псориаза.
Противопоказания
— Повышенная чувствительность к глицирризиновой кислоте, фосфатидилхолину или другим компонентам препарата; — Антифосфолипидный синдром; — Беременность (данных по эффективности и безопасности недостаточно); — Период грудного вскармливания (данных по эффективности и безопасности недостаточно); — Детский возраст младше 12 лет (данных по эффективности и безопасности недостаточно).
С осторожностью
Применять с осторожность у больных с портальной гипертензией и артериальной гипертонией. У больных с артериальной гипертензией. При наличии данных заболеваний, перед началом приема препарата необходимо проконсультироваться с врачом.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания (данных по эффективности и безопасности недостаточно).
Способ применения и дозы
Принимают внутрь, во время еды, не разжевывая, запивая небольшим количеством жидкости.
Рекомендуемый режим дозирования у взрослых и детей старше 12 лет — по 2 капсулы 3 раза в сутки. Длительность применения может составлять до 6 месяцев, в среднем – 3 месяца.
Побочное действие
Обычно препарат Фосфоглив переносится хорошо, побочные действия развиваются очень редко, по данным пострегистрационного наблюдения — частота
Аллергические реакции: кожная сыпь, затруднение носового дыхания, конъюнктивит, кашель.
Со стороны сердечно-сосудистой системы: транзиторное (преходящее) повышение артериального давления, периферические отеки.
Со стороны пищеварения: диспепсия (отрыжка, тошнота, вздутие живота), дискомфорт в животе.
При возникновении перечисленных симптомов следует прекратить прием препарата и проконсультироваться с врачом.
Передозировка
Случаев передозировки не зарегистрировано.
Взаимодействие с другими лекарственными препаратами
Не описано.
Особые указания
В случае повышения артериального давления следует прекратить прием препарата и обратиться к врачу.
Влияние на способность управлять транспортными средствами и работать с механизмами
Препарата не оказывает негативного влияния на способность управлять транспортными средствами и выполнять другую работу, требующую повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Капсулы.
По 30, 50, 100, 200 или 300 капсул в пластиковые контейнеры с крышками из полиэтилена высокого давления или пропилена.
По 10 капсул в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой.
1 контейнер или 2, 3, 5 контурных ячейковых упаковок вместе с инструкцией по применению помещают в пачку из картона.
Условия хранения.
Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Срок годности.
3 года. По окончанию срока годности препарат не использовать.
Условия отпуска.
Без рецепта.