Роль ренин–ангиотензин–альдостероновой системы в патогенезе фибрилляции предсердий
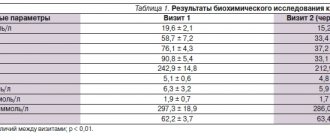
В настоящее время ФП признается в качестве неоднородной клинической и электрофизиологической единицы с различными механизмами, триггерами, субстратами возникновения и поддержания аритмии, что требует различных подходов к ее лечению и профилактике. Вместе с тем, в большинстве случаев лечение ФП остается симптоматическим, включая в себя профилактическую антикоагулянтную и фармакологическую терапию. Протекторная антиаритмическая терапия имеет низкую эффективность и связана с высоким риском побочных явлений. Эти ограничения в применении антиаритмических препаратов привели к использованию нефармакологических методов лечения и разработке специфических терапевтических стратегий, направленных на предотвращение развития электрофизиологической среды, поддерживающей аритмию. В последние годы были получены данные о влиянии на частоту возникновения и рецидивирования ФП лекарственных препаратов, не обладающих непосредственными антиаритмическими свойствами. Данное направление лечения получило название «upstream–терапия», в дословном переводе – «терапия, направленная против течения» или, точнее, «не лежащая в рамках привычной антиаритмической терапии». К данной группе препаратов относятся средства, которое могут воздействовать на патогенетические механизмы ФП: воспаление, фиброз, окислительный стресс и ремоделирование миокарда предсердий. Поэтому в отличие от антиаритмической терапии, которая носит исключительно симптоматический характер, «upstream–терапия» может называться патогенетической. Одним из перспективных и многообещающих направлений в лечении ФП является использование препаратов, блокирующих ренин–ангиотензин–альдостероновую систему (РААС). Соответствующий раздел впервые появился в новых рекомендациях по диагностике и лечению ФП [1]. Роль РААС в патогенезе различных заболеваний сердечно–сосудистой системы давно и хорошо известна, однако исследования последних лет доказывают прямое влияние компонентов РААС на электрофизиологические свойства кардиомиоцитов предсердий. Существуют несколько основных патогенетических механизмов прямого воздействия РААС на структурное и электрофизиологическое ремоделирование предсердий: увеличение фиброза предсердной ткани, растяжение и дилатация предсердий, прямое влияние на функцию ионных каналов и межклеточного взаимодействия кардиомиоцитов предсердий [3]. Ведущим звеном в патогенезе развития и поддержания ФП являются изменения анатомических свойств предсердий, к которым относят: дилатацию предсердий, расширение устьев легочных вен, апоптоз кардиомиоцитов предсердий, интерстициальный фиброз, увеличение массы миокарда предсердий, экспрессию генов ионных каналов [4], изменение распределения уязвимых участков [5]. Гипертрофия и дилатация предсердий отражают процессы «аритмогенного ремоделирования» [6]. Значительно реже выявляют неоднородные участки фиброза и жировой инфильтрации миокарда предсердий, что может быть исходом воспалительных или дегенеративных процессов в сердечной мышце. ФП наиболее часто возникает у пациентов с ХСН, что ведет к обширному интерстициальному фиброзу предсердий и повышенной выработке коллагена I типа [7]. Kostin S. и соавт. (2002) при электронно–микроскопическом исследовании биопсийного материала предсердия больных с ФП обнаружили нарушение межклеточных контактов и апоптоз кардиомиоцитов предсердий. Описанные изменения, по мнению авторов, обеспечивают возникновение и увеличивают продолжительность существования эпизода ФП [8]. Экспериментальные работы последних лет обнаружили увеличение I типа рецепторов ангиотензина II и уровня ангиотензинпревращающего фермента в ткани левого предсердия у пациентов с ФП [9,10]. Стимуляция рецепторов ангиотензина II первого типа инициирует каскад процессов фосфорилирования и активирует различные митоген–активируемые протеинкиназы, что приводит к гипертрофии и апоптозу кардиомиоцитов предсердий, аккумуляции фибробластов и индукции коллагена [11]. Повышенная готовность к возникновению ФП связана с прогрессирующим уменьшением эффективного рефрактерного периода предсердий. Эти изменения получили название феномена электрофизиологического ремоделирования предсердий [1]. Компоненты РААС напрямую влияют на изменение транспорта ионов кальция и натрия через мембрану кардиомиоцита. Ангиотензин II инициирует активацию кальциевых каналов L–типа, аналогичные изменения транспорта ионов кальция происходят при увеличении концентрации альдостерона [12,13]. Изменение потока ионов по кальциевым каналам L–типа приводит к укорочению потенциала действия, уменьшению эффективного рефрактерного периода предсердий и появлению ФП. Доказано влияние тканевого компонента РААС на проницаемость мембраны кардиомиоцита для ионов натрия. Повышение концентрации ангиотензина II уменьшает транспорт ионов натрия внутрь клетки, тем самым изменяя порог возбудимости кардиомиоцитов предсердий [14]. Кроме того, в исследованиях in vitro было доказано, что увеличение ангиотензина II способствует фосфорилированию белка мембраны СX43 и изменению межклеточных связей кардиомиоцитов [15]. Нарушение межклеточного взаимодействия снижает скорость распространения волны возбуждения по предсердиям и инициирует появление ФП. Таким образом, активация РААС играет ведущую роль в развитии структурного ремоделирования предсердий, что приводит к изменению электрофизиологических свойств предсердной ткани и возникновению ФП. Есть основание полагать, что блокада РААС может уменьшить число впервые выявленных эпизодов ФП и предотвратить повторные пароксизмы аритмии. На сегодняшний день проведено 23 крупных рандомизированных клинических исследования по изучению влияния терапии ингибиторами АПФ (иАПФ) и блокаторами рецепторов к ангиотензину (БРА) на частоту возникновения новых эпизодов ФП или ее вторичную профилактику (табл. 1). Общее количество пациентов, включенных в мета–анализ, составило 87 048 человек. С целью первичной профилактики ФП иАПФ или БРА применялись у больных с артериальной гипертензией (АГ), ХСН и после перенесенного инфаркта миокарда (ИМ). Вторичная профилактика ФП проводилась при совместном приеме иАПФ или БРА с антиаритмическими препаратами после кардиоверсии или для удержания синусового ритма у больных с персистирующей формой ФП [16]. Первичная профилактика ФП с использованием иАПФ или БРА Артериальная гипертензия. Всего было проведено 6 исследований, оценивавших первичную профилактику ФП при приеме иАПФ или БРА у больных АГ. Из них только в двух исследованиях – LIFE (Losartan Intervention For Endpoint Reduction in Hypertension) и VALUE (Valsartan Antihypertensive Long–Term Use Evaluation) – было обнаружено статистически значимое снижение возникновения новых случаев ФП при назначении БРА [17,18]. В остальных исследованиях – CAPP (Captopril Prevention Project), STOP–2 (Swedish Trial in Old Patients With Hypertension–2), HOPE (Heart Outcomes Prevention Evaluation) и TRANSCEND (Telmisartan Randomized Assessment Study in ACE Intolerant Subjects With Cardiovascular Disease) – достоверных отличий в частоте появления новых случаев ФП при приеме иАПФ или БРА выявлено не было [19–22]. Несмотря на противоречивые результаты выполненных исследований, различия в эффективности проводимого лечения можно объяснить существенными изменениями в выборке пациентов и препаратов сравнения. Так, в исследованиях LIFE и VALUE использовались БРА, исследования CAPP и STOP–2 оценивали эффективность иАПФ. В исследовании LIFE были включены больные с АГ и гипертрофией левого желудочка (ГЛЖ), а исследования CAPP, STOP–2, HOPE и TRANSCEND проводились на общей популяции больных. По всей видимости, низкий протекторный эффект иАПФ при проведении первичной профилактики ФП в исследованиях CAPP и STOP–2 мог быть связан с отсутствием субстрата лечения у больных без ГЛЖ, т. к. структурное ремоделирование предсердий наиболее значимо при выраженной ГЛЖ. Таким образом, назначение иАПФ и БРА для первичной профилактики ФП наиболее оправдано у больных АГ с ГЛЖ. Антиаритмический эффект этих препаратов зависит от выраженности органических изменений миокарда и опосредован их органопротективными свойствами. Сердечная недостаточность. Эффективность иАПФ и БРА при проведении вторичной профилактики ФП у больных ХСН была продемонстрирована в трех рандомизированных клинических исследованиях: SOLVD (Studies оf Left Ventricular Dysfunction), CHARM (Candesartan in Heart Failure: Assessment of Reduction in Mortality and Morbidity) и Val–HeFT (Valsartan Heart Failure Trial) [23–25]. В исследовании SOLVD оценивалась эффективность лечения эналаприлом больных с низкой фракцией выброса левого желудочка (ФВ ЛЖ). Через 3 года наблюдения число новых случаев ФП у больных, получавших эналаприл, было более чем в 4 раза ниже по сравнению с группой плацебо. Кроме того, была выявлена взаимосвязь между снижением относительного риска ФП и ФВ ЛЖ [23]. Результаты исследований CHARM и Val–HeFT доказали значительное уменьшение новых случаев ФП при лечении кандесартаном и валсартаном. Во всех трех исследованиях с использованием иАПФ или БРА у пациентов с ХСН было показано снижение относительного риска новых случаев ФП примерно на 44%, что позволяет рекомендовать использование этих препаратов как превентивное лечение для первичной профилактики ФП [23–25]. Перенесенный инфаркт миокарда. Проводилось только 2 исследования с применением иАПФ у больных, перенесших острый ИМ. Результаты наблюдений оказались диаметрально противоположными. Исследование GISSI–3 (Gruppo Italiano per lo Studio Della Sopravvivenza Nell’Infarto Miocardico–3) не выявило статистически достоверного уменьшения вероятности ФП в течение 6 нед. после острого ИМ при использовании терапии лизиноприлом [26]. Исследование TRACE (Trandolapril Cardiac Evaluation) показало значительное уменьшение вероятности появления ФП в течение 4 лет при лечении трандолаприлом больных с первой недели после ИМ [27]. Необходимо отметить, что в исследование TRACE были включены пациенты со сниженной ФВ ЛЖ, в то время как в исследовании GISSI–3 83% больных не имели сердечной недостаточности. Вероятно, применение иАПФ и БРА для профилактики ФП в первую очередь оправдано у больных с ХСН, т. к. появление инотропной дисфункции миокарда ЛЖ значительно увеличивает риск развития аритмии. Вторичная профилактика ФП Эффективность иАПФ и БРА при проведении вторичной профилактики ФП оценивалась у больных с персистирующей формой ФП после проведения кардиоверсии. В результате в семи работах (из восьми) было показано статистически достоверное уменьшение риска пароксизмов ФП на фоне лечения иАПФ или БРА, и эти эффекты сохранялись недели после проведения кардиоверсии. Большинство больных, включенных в исследования, имели АГ или ХСН. Madrid A.H. et al. (2002, 2004) изучали эффективность назначения ирбесартана в дополнение к амиодарону. Больные, получавшие ирбесартан, имели достоверно меньшее число пароксизмов ФП при сравнении с контрольной группой [28,29]. Ueng et al. (2003) показали, что назначение эналаприла к стандартной антиаритмической терапии амиодароном существенно снижает частоту пароксизмов ФП у больных после электрической кардиоверсии [30]. В работе Van den Berg et al. (1995) было доказано, что назначение лизиноприла совместно с амиодароном существенно снижает риск повторных пароксизмов ФП у пациентов с ХСН [31]. Эффективность назначения иАПФ при проведении вторичной профилактики ФП была также продемонстрирована в исследованиях Grecu et al. (2007) и Belluzzi et al. (2009) [32,33]. Проведенные исследования показали, что назначение иАПФ к стандартной антиаритмической терапии позволяет значительно дольше сохранять синусовый ритм у больных с персистирующей формой ФП после кардиоверсии. Tveit et al. (2007) исследовали эффективность вторичной профилактики ФП при приеме кандесартана. Пациенты, получавшие БРА, имели значительно меньшее число пароксизмов ФП при сравнении с группой плацебо [34]. Результаты рандомизированного клинического исследования GISSI–AF (Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto Miocardico – Atrial Fibrillation) показали, что прием валсартана в дозе 320 мг/сут. в дополнение к стандартной антиаритмической терапии не предотвращает рецидивов ФП в течение 1 года наблюдения [35]. Результаты исследования можно назвать противоречивыми, так как в контрольной группе больных допускался прием иАПФ, что могло уменьшить частоту пароксизмов ФП в данной группе. Таким образом, исследование GISSI–AF не обнаружило достоверной разницы в частоте приступов ФП при приеме иАПФ и БРА. В исследовании Yin et al. (2006) [36] и трех работах Fogari et al. (2006, 2008) был продемонстрирован антиаритмический эффект иАПФ и БРА у больных с пароксизмальной ФП [37–39]. Авторы показали, что применение препаратов, блокирующих РААС, значительно уменьшает частоту рецидивов ФП и необходимость в приеме нагрузочных доз антиаритмических препаратов. В настоящее время имеется недостаточно данных, позволяющих однозначно рекомендовать использование иАПФ и БРА исключительно для профилактики ФП. Антиаритмические эффекты препаратов этих групп наиболее очевидны у пациентов, имеющих факторы риска ФП: АГ, ГЛЖ или ХСН. Результаты клинических исследований продемонстрировали эффективность иАПФ и БРА при проведении как первичной, так и вторичной профилактики ФП, что обусловлено их способностью предупреждать развитие структурного и электрофизиологического ремоделирования предсердий. Исследование роли РААС в патогенезе ФП является наиболее актуальным вопросом современной кардиологии.
Литература 1. Fuster V., Ryden L.E. et al. ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation – executive summary // Eur. Heart. J. 2006, Vol. 27, Р. 1979–2030. 2. Stevenson W.G., Stevenson L.W. Atrial fibrillation and heart failure–five more years. // N. Engl. J. Med. 2004, Dec 2, Vol. 351(23). Р. 2437–2440. 3. Iravanian S., Dudley S.C. The Renin–Angiotensin–Aldosterone System (RAAS) and Cardiac Arrhythmias // Heart Rhythm. 2008 June; 5(6 Suppl. 1): S.12–17. 4. Cha T.J., Ehrlich J.R., Zhang L., Nattel S. Atrial ionic remodeling induced by atrial tachycardia in the presence of congestive heart failure. // Circulation. 2004, Sep 21, Vol. 110(12). Р. 1520–1526. 5. Yue L., Feng J., Gaspo R., Li G.R., Wang Z., Nattel S. Ionic remodeling underlying action potential changes in a canine model of atrial fibrillation. // Circ. Res., 1997, Vol. 815. P. 12–25. 6. Li D., Karen S., Leung T.K., Nattel S. Promotion of atrial fibrillation by heart failure in dogs: atrial remodeling of a different sort. // Circulation. 1999, Vol. 100. Р. 87–95. 7. Gronefeld G.C., Hohnloser S.H. Heart failure complicated by atrial fibrillation: mechanistic, prognostic, and therapeutic implications. // J. Cardiovasc. Pharmacol. Ther., 2003, Jun; Vol. 8(2). Р. 107–113. 8. Kostin S., Klein G., Szalay Z., Hein S., Bauer E.P., Schaper J. Structural correlate of atrial fibrillation in human patients. // Cardiovasc Res. 2002 May; Vol. 54(2). Р. 361–379. 9. Boldt A., Wetzel U., Weigl J. et al. Expression of angiotensin II receptors in human left and right atrial tissue in atrial fibrillation with and without underlying mitral valve disease. // J Am Coll Cardiol. 2003;42:1785–1792. 10. Goette A., Arndt M., Rocken C. et al. Regulation of angiotensin II receptor subtypes during atrial fibrillation in humans. // Circulation. 2000;101:2678–2681. 11. Oudot A., Vergely C., Ecarnot–Laubriet A. et al. Angiotensin II activates NADPH oxidase in isolated rat hearts subjected to ischaemia–reperfusion. // Eur J Pharmacol. 2003;462:145–154. 12. Kaibara M., Mitarai S., Yano K. et al. Involvement of Na+–H+ antiporter in regulation of L–type Ca2+ channel current by angiotensin II in rabbit ventricular myocytes. // Circ Res. 1994;75:1121–1125. 13. Benitah J.P., Vassort G. Aldosterone upregulates Ca2+ current in adult rat cardiomyocytes. // Circ Res. 1999;85:1139–1145. 14. Shang L.L., Sanyal S., Pfahnl A.E. et al. NF– B–dependent transcriptional regulation of the cardiac scn5a sodium channel by angiotensin II. Am J Physiol Cell Physiol. 2008;294:C372–92007. 15. Kasi V.S., Xiao H.D., Shang L.L. et al. Cardiac–restricted angiotensin–converting enzyme overexpression causes conduction defects and connexin dysregulation. // Am J Physiol Heart Circ Physiol. 2007;293:H182–H192. 16. Schneider M.P., Tsushung A., Bohm М. et al. Prevention of Atrial Fibrillation by Renin–Angiotensin System Inhibition // Journal of the American College of Cardiology. 2010; 55: 2299–307. 17. Wachtell K., Lehto M., Gerdts E. et al. Angiotensin II receptor blockade reduces new–onset atrial fibrillation and subsequent stroke compared to atenolol: the Losartan Intervention for End Point Reduction in Hypertension (LIFE) study. // J Am Coll Cardiol. 2005, 45:712–9. 18. Schmieder R.E., Kjeldsen S.E., Julius S., McInnes G.T., Zanchetti A., Hua T.A. Reduced incidence of new–onset atrial fibrillation with angiotensin II receptor blockade: the VALUE trial. // J Hypertens. 2008;26:403–11. 19. Hansson L., Lindholm L.H., Niskanen L. et al. Effect of angiotensinconverting–enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomised trial. // Lancet. 1999;353:611–6. 20. Hansson L., Lindholm L.H., Ekbom T. et al. Randomised trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients With Hypertension–2 study. // Lancet. 1999;354:1751–6. 21. Salehian O., Healey J., Stambler B. et al. Impact of ramipril on the incidence of atrial fibrillation: results of the Heart Outcomes Prevention Evaluation study. // Am Heart J. 2007;154:448–53. 22. Yusuf S., Teo K., Anderson C. et al. Effects of the angiotensin–receptor blocker telmisartan on cardiovascular events in high–risk patients intolerant to angiotensin–converting enzyme inhibitors: a randomized controlled trial. // Lancet. 2008;372:1174–83. 23. Vermes E., Tardif J.C., Bourassa M.G. et al. Enalapril decreases the incidence of atrial fibrillation in patients with left ventricular dysfunction: insight from the Studies of Left Ventricular Dysfunction (SOLVD) trials. // Circulation 2003;107:2926–31. 24. Ducharme A., Swedberg K., Pfeffer M.A. et al. Prevention of atrial fibrillation in patients with symptomatic chronic heart failure by candesartan in the Candesartan in Heart Failure: Assessment of Reduction in Mortality and Morbidity (CHARM) program. // Am Heart J. 2006;152:86–92. 25. Maggioni A.P., Latini R., Carson P.E. et al. Valsartan reduces the incidence of atrial fibrillation in patients with heart failure: results from the Valsartan Heart Failure Trial (Val–HeFT). // Am Heart J. 2005;149:548–57. 26. Pizzetti F., Turazza F.M., Franzosi M.G. et al. Incidence and prognostic significance of atrial fibrillation in acute myocardial infarction: the GISSI–3 data. // Heart. 2001;86:527–32. 27. Pedersen O.D., Bagger H., Kober L., Torp–Pedersen C. Trandolapril reduces the incidence of atrial fibrillation after acute myocardial infarction in patients with left ventricular dysfunction. // Circulation. 1999;100:376–80. 28. Madrid A.H., Bueno M.G., Rebollo J.M. et al. Use of irbesartan to maintain sinus rhythm in patients with long–lasting persistent atrial fibrillation: a prospective and randomized study. // Circulation. 2002;106:331–6. 29. Madrid A.H., Marin I.M., Cervantes C.E. et al. Prevention of recurrences in patients with lone atrial fibrillation. The dose–dependent effect of angiotensin II receptor blockers. // J Renin Angiotensin Aldosterone Syst. 2004;5:114–20. 30. Ueng K.C., Tsai T.P., Yu W.C. et al. Use of enalapril to facilitate sinus rhythm maintenance after external cardioversion of long–standing persistent atrial fibrillation. Results of a prospective and controlled study. // Eur Heart J. 2003;24:2090–8. 31. Van den Berg M.P., Crijns H.J., Van Veldhuisen D.J., Griep N., De Kam P.J., Lie K.I. Effects of lisinopril in patients with heart failure and chronic atrial fibrillation. // J Card Fail 1995;1:355–63. 32. Grecu M., Olteanu R.O., Olteanu S.S., Georgescu C.A. Does treatment with ACE inhibitors prevent the long term recurrences of lone atrial fibrillation after cardioversion? // Rom J Intern Med. 2007;45:29–33. 33. Belluzzi F., Sernesi L., Preti P., Salinaro F., Fonte M.L., Perlini S. Prevention of recurrent lone atrial fibrillation by the angiotensin–II converting enzyme inhibitor ramipril in normotensive patients. // J Am Coll Cardiol. 2009;53:24–9. 34. Tveit A., Grundvold I., Olufsen M. et al. Candesartan in the prevention of relapsing atrial fibrillation. // Int J Cardiol. 2007;120:85–91. 35. Disertori M., Latini R., Barlera S. et al. Valsartan for prevention of recurrent atrial fibrillation. // N Engl J Med. 2009;360:1606–17. 36. Yin Y., Dalal D., Liu Z. et al. Prospective randomized study comparing amiodarone vs. amiodarone plus losartan vs. amiodarone plus perindopril for the prevention of atrial fibrillation recurrence in patients with lone paroxysmal atrial fibrillation. // Eur Heart J 2006;27:1841–6. 37. Fogari R., Derosa G., Ferrari I. et al. Effect of valsartan and ramipril on atrial fibrillation recurrence and P–wave dispersion in hypertensive patients with recurrent symptomatic lone atrial fibrillation. // Am J Hypertens. 2008;21:1034–9. 38. Fogari R., Mugellini A., Destro M. et al. Losartan and prevention of atrial fibrillation recurrence in hypertensive patients. // J Cardiovasc Pharmacol. 2006;47:46–50. 39. Fogari R., Zoppi A., Mugellini A. et al. Comparative evaluation of effect of valsartan/amlodipine and atenolol/amlodipine combinations on atrial fibrillation recurrence in hypertensive patients with type 2 diabetes mellitus. // J Cardiovasc Pharmacol. 2008;51:217–22.
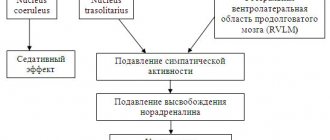
Механизм функционирования
Вследствие уменьшения АД в юкстагломерулярных клетках нефрона, начинает выделяться протеолитический фермент ренин, является гормоноподобных веществ. Под действием ренина из белка α 2 -глобулиновой фракции крови — ангиотензиногена, путем ограниченного протеолиза отщепляется декапептид ангиотензин I, который под действием ангиотензинпревращающего фактора (АПФ) превращается в ангиотензин II. Ангиотензин II в свою очередь проявляет вазокнстрикторну действие и стимулирует выделение корой надпочечников альдостерона, под действием которого увеличивается реабсорбция ионов натрия и воды в дистальном отделе нефрона, что приводит к увеличению объема циркулирующей крови (ОЦК).
Вследствие увеличения ОЦК и непосредственной сосудосуживающего действия ангиотензина II возрастает артериальное давление крови.