Противодиабетические препараты – это лекарственные средства, которые снижают уровень глюкозы в крови и используются для лечения сахарного диабета 1-го или 2-го типа.
Сахарный диабет – это заболевание, обусловленное недостаточностью образования инсулина в поджелудочной железе или же снижением его функции. К основным симптомам сахарного диабета относят гипергликемию (повышение уровня глюкозы в крови), глюкозурию (появление глюкозы в моче), полиурию (увеличение диуреза), полидипсию (повышенную жажду), кетоацидоз (появление в крови токсичных кетоновых тел).
Недостаточность инсулина может быть абсолютной и относительной.
Абсолютная недостаточность инсулина развивается в результате гибели β-клеток островков поджелудочной железы, которые вырабатывают инсулин. В таком случае говорят о сахарном диабете 1-го типа (инсулинозависимый диабет).
Сахарный диабет 1-го типа возникает обычно в молодом возрасте у генетически предрасположенных людей под влиянием вирусов, токсинов, стресса и т.д. Такой диабет требует постоянного лечения препаратами инсулина.
При относительной недостаточности самого инсулина вырабатывается достаточное количество, периферические ткани к нему практически не чувствительны. Это характеризует инсулиннезависимый диабет или сахарный диабет 2-го типа. Мощным провоцирующим фактором развития сахарного диабета 2-го типа является ожирение. Применение препаратов инсулина практически не дает лечебного эффекта. В этом случае используют синтетические противодиабетические средства.
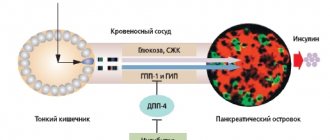
Глюкоза является основным источником энергии для человека. Поступает в организм с пищей в составе сложных углеводов – полисахаридов (крахмала, гликогена) и дисахаридов (сахарозы, лактозы), которые, расщепляясь в пищеварительном тракте, образуют глюкозу. Из тонкого кишечника глюкоза с помощью особых транспортных белков всасывается в кровь и распространяется по организму.
В крови глюкоза, однако, долго не задерживается, достаточно быстро проникая в клетки головного мозга, мышц, печени и т.д., где и включается в биохимические процессы, которые приводят к образованию необходимой клеткам энергии. Транспорт глюкозы из крови в клетки тканей организма также осуществляется с помощью особых белков-переносчиков, которые активирует гормон β-клеток островков поджелудочной железы инсулин.
Если поджелудочная железа вырабатывает мало инсулина или же он неактивен в отношении переносчиков, глюкоза не может попасть в клетки, накапливаясь в крови (гипергликемия). При этом страдает сама клетка, которая, не получая необходимого источника энергии, вынуждена искать другие источники энергии, например, жирные кислоты. Однако превращение жирных кислот происходит с образованием токсичных промежуточных продуктов – кетоновых тел, которые выделяются в кровь (кетонемия).
В крови кетоновые тела вызывают повреждение стенки сосудов и клеток крови – эритроцитов, тромбоцитов. Попадая в головной мозг, кетоновые тела угнетают сознание, нарушают дыхание, а в больших дозах даже вызывают кому.
Глюкоза в крови, в свою очередь, тоже не является безопасным веществом. Не попав в клетку, где она моментально преобразуется в энергию или откладывается про запас, глюкоза начинает окислять белки крови (альбумины, гемоглобин) и поверхностные белки мембран клеток сосудистой стенки. Это также приводит к повреждению сосудов и нарушению кровообращения.
Наиболее чувствительны к негативному действию гипергликемии и кетонемии сосуды мелкого калибра – сосуды сетчатки глаза, капилляры клубочков почек, капилляры стопы.
Фармакологическое действие
Препараты инсулинов понижают уровень глюкозы в крови путем усиления ее утилизации периферическими тканями.
Кроме того, инсулины оказывают анаболическое действие – повышают синтез белка, стимулируют рост мышц.
Синтетические противодиабетические препараты снижают уровень глюкозы в крови за счет увеличения секреции собственного инсулина (производные сульфонилмочевины, меглитиниды, ингибиторы дипептидилпептидазы-4, аналоги глюкагоноподобного пептида 1-го типа); повышения чувствительности периферических тканей к инсулину (бигуаниды, тиазолидиндионы); уменьшения всасывания глюкозы в кишечнике (ингибиторы α-глюкозидазы, смолы); усилении выведения глюкозы с мочой (ингибиторы натрий-глюкозного котранспортера 2-го типа).
Препараты сульфонилмочевины в современной клинической практике
Сахарный диабет (СД) является величайшей в истории человечества неинфекционной эпидемией. Около 85-97% СД составляют больные с СД типа 2 (СД 2) (5). В Российской Федерации, как и во всех странах мира, повсеместно отмечается рост заболеваемости СД 2 (1, 2).
Таблица 1. Терапевтические цели при СД 2
Таблица 2. Клиническая эффективность ПССП
Рисунок 1. Химическая структура глибенкламида
Рисунок 2. Влияние глибенкламида на массу тела по сравнению с другими ПССП
Масштабность проблемы тем более значительна, ведь наряду с официально зарегистрированными случаями СД 2, у значительной части населения диагноз не установлен, и наблюдается нарушенная толерантность к глюкозе (НТГ) или нарушение гликемии натощак. Ежегодно примерно у 1,5-7,3% лиц с НТГ развивается СД 2 (14). Следовательно, фактическая распространенность СД 2 в несколько раз превышает официально зарегистрированную распространенность. Необходимо особо подчеркнуть, что наибольшее количество пациентов с НТГ или с СД 2 – это люди активного трудоспособного возраста.
Медицинская и социальная значимость СД 2 определяется прежде всего его тяжелыми осложнениями, которые приводят к ранней инвалидизации и высокой смертности, сокращению продолжительности и ухудшению качества жизни пациентов. Развитие осложнений связывают в первую очередь с хронической гипергликемией, что было убедительно доказано в ходе длительных крупномасштабных исследований (7, 12).
СД 2 – это хроническое заболевание, развивающееся в результате сочетанного воздействия генетических и средовых факторов (5). Для СД 2 к настоящему времени принята концепция полигенного наследования. В развитии заболевания имеют значение два фундаментальных патофизиологических механизма: прогрессирующее нарушение функции β-клеток поджелудочной железы и различной степени выраженности инсулинорезистентность (ИР). При манифестации СД 2 секреция инсулина в среднем снижается на 50%, а чувствительность к инсулину – на 70% (5). В дальнейшем функция β-клеток ухудшается примерно со скоростью 4-5% в год от момента установления диагноза.
ИР, как наиболее раннее нарушение, намного опережает клиническую манифестацию СД 2. Это состояние, характеризующееся недостаточным биологическим ответом организма на физиологические концентрации инсулина. Основными внешними факторами, способствующими реализации ИР, является увеличение потребления высококалорийной пищи, недостаточная физическая активность и избыточная масса тела. В условиях ИР, которая во многом обусловлена нарушением действия инсулина на пострецепторном уровне, происходит снижение утилизации глюкозы мышечной и жировой тканью. ИР печени сопровождается снижением синтеза гликогена, активизацией глюконеогенеза и гликогенолиза. Длительное время ИР компенсируется нефизиологической гиперинсулинемией, способствующей поддержанию нормогликемии на этом этапе заболевания.
У здоровых людей секреция инсулина в ответ на прием пищи имеет 2 фазы. Одним из ранних патофизиологических дефектов секреторной функции β-клеток при СД 2 является именно нарушение ранней фазы секреции инсулина, в норме ограничивающей нефизиологический подъем гликемии в постпрандиальный период (5). Ранняя фаза прандиального ответа, составляющая около 10% от всего за сутки секретируемого инсулина, вызывает подавление эндогенной продукции глюкозы печенью, подавляет секрецию глюкагона и липолиз, повышает чувствительность периферических тканей к действию инсулина, способствуя утилизации ими глюкозы. Другими особенностями нарушенной секреторной функции β-клеток являются сниженный и отсроченный во времени ответ на прием смешанной пищи, повышение концентрации проинсулина, нарушение пульсативной секреции инсулина.
В дальнейшем механизм компенсаторной гиперинсулинемии утрачивается и секреция инсулина становится недостаточной по отношению к нарастающей гипергликемии. В этих условиях печень избыточно продуцирует глюкозу, что приводит к гипергликемии натощак. Кроме того, гепатическая продукция глюкозы продолжается несмотря на пищевую нагрузку и в сочетании с относительной недостаточностью выброса инсулина также приводит к постпрандиальной гипергликемии. При СД 2 наибольшая диспропорция между секрецией инсулина и потребностью в нем возникает именно после приема пищи.
По результатам крупных эпидемиологических и обсервационных исследований в области диабета были получены убедительные доказательства наличия тесной связи между эволюцией СД 2, нарушениями углеводного обмена и возрастающим риском микро- и макрососудистых осложнений заболевания (4, 12). Так, в исследовании UKPDS были продемонстрированы достоверные преимущества интенсивного контроля гликемии СД 2 (11): снижение уровня HbA1c на 0,9% при длительности наблюдения до 10 лет уменьшает риск смерти на 21%, острого инфаркта миокарда на 14%, микрососудистых осложнений на 37% и заболеваний периферических сосудов на 43%. Важно отметить, что при впервые диагностированном СД 2 осложнения наблюдаются практически у 50% больных (8). Так, согласно данным исследования CODE-2 (Cost of Diabetes in Europe – Type 2), изучавшего распространенность различных хронических осложнений у больных СД, различные осложнения имели 59% обследованных, причем у 23% было два, а у 3% – три осложнения и более (7).
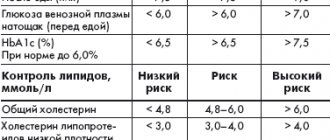
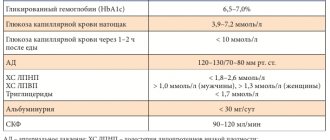
В связи с вышесказанным оптимизация подходов к терапии у пациентов с СД 2 является приоритетной проблемой современной медицины, а лечебная стратегия должна прежде всего предупреждать и сводить к минимуму риск развития хронических осложнений заболевания. Очевидно, что в настоящий момент требуется изменение подходов к лечению СД 2 для достижения более эффективного контроля над этим заболеванием. Это интенсивная стратегия лечения, направленная против хронической гипергликемии на стойкое достижение компенсации углеводного обмена сразу с момента диагностики СД 2. С этой целью многие национальные и международные диабетологические ассоциации четко определили целевой показатель важнейшего параметра метаболического контроля – гликированного гемоглобина (HbA1c): ADA/EASD:
Прежде чем переходить к вопросам фармакотерапии СД 2, следует отметить важность немедикаментозных подходов к лечению заболевания и обязательного проведения самоконтроля гликемии, без которых любая фармакотерапия будет недостаточна. Современные рекомендации по диетотерапии СД 2 включают в себя следующие принципы: энергетическая ценность пищи, поддерживающая массу тела близкой к идеальной, а в случае избыточного веса – низкокалорийное питание.
Большинству больных СД 2 следует придерживаться дробного питания (5-6 раз в день небольшими порциями), что позволяет не только избежать сильного чувства голода при уменьшении суточной калорийности объема порций, но и препятствует постпищевой гипергликемии. Рекомендуемое содержание углеводов – 50-60%, белков не более 15% от общей калорийности суточного рациона; предусматривается максимальное ограничение или исключение легкоусвояемых и преимущественное потребление сложных углеводов. Доля жиров в суточном рационе не должна превышать 30%, насыщенные жиры должны составлять не более 10% от всего потребляемого жира. Предусматривается включение полиненасыщенных жиров в качестве противоатерогенного средства, необходимо снижение потребления холестерина (менее 300 мг в день) и повышение употребление продуктов с высоким содержанием пищевых волокон, сокращение приема алкоголя (менее 30 г в день).
Одновременно с изменением питания должны проводиться мероприятия, направленные на повышение двигательной активности. Хороший эффект оказывает рациональная физическая нагрузка, безопасная и эффективная с учетом индивидуальных особенностей каждого пациента: например, пешие прогулки, плавание продолжительностью 30-45 мин. 3-5 раз в неделю или любой посильный комплекс физических упражнений. Физические нагрузки как уменьшают выраженность ИР, так и стимулируют утилизацию глюкозы инсулиннезависимыми тканями, в которых индуцированное упражнениями увеличение потребления глюкозы не зависит от действия инсулина. Во время физических нагрузок происходит уменьшение выраженности гиперинсулинемии, а потребление глюкозы мышцами увеличивается несмотря на снижение уровня инсулина. Необходимо добиваться снижения веса при его избытке и предупреждения дальнейшего накопления; наиболее безопасным и надежным является темп похудения на 0,5-1 кг в неделю. Процесс снижения массы тела должен контролироваться врачом, что особенно актуально для пожилых пациентов.
Пероральные сахароснижающие средства включают несколько основных групп: препараты сульфонилмочевины (ПСМ), бигуаниды, тиазолидиндионы, ингибиторы α-глюкозидазы, но в последнее время появились и новые группы этих средств (инкретиномиметики, ингибиторы дипептидилпептидазы IV типа). Исходный выбор препаратов остается важной задачей, в решении которой помогает анализ сравнительной эффективности пероральных сахароснижающих препаратов (ПССП) (таблица 2).
Одним из наиболее известных и широко применяемых препаратов в терапии СД 2 являются ПСМ. Интересна история их создания: ПСМ были разработаны после того, как в 1940-х при изучении антибактериальной активности сульфаниламидов было случайно обнаружено их побочное действие в виде гипогликемии у лабораторных животных (1). Широкое клиническое применение данного класса лекарственных средств началось еще в 50-х годах прошлого столетия.
Механизм действия этих препаратов – класса секретогогов – связан главным образом со стимуляцией β-клеток поджелудочной железы, сопровождающейся мобилизацией и усилением эндогенной секреции инсулина, особенно в присутствии глюкозы (1, 4, 6). Наличие в островках Лангерганса функционально-активных β-клеток является основой для проявления эффекта этих сахароснижающих препаратов. Периферическое (экстрапанкреатическое) действие, по-видимому, вторично и обусловлено повышением инсулинемии и снижением глюкозотоксичности, что вызывает угнетение гепатической продукции глюкозы и улучшение ее утилизации периферическими тканями; собственные экстрапанкретические эффекты убедительно не доказаны (1).
Инсулин секретируется β-клетками в ответ на различные стимулы, каждый из которых вносит свой вклад в функционирование этих клеток. ПСМ связываются со специфическими белками-рецепторами на клеточной мембране β-клеток – SUR-1, представляющими собой белки АТФ-зависимых К+-каналов клеточной мембраны (9). В настоящее время роль АТФ-зависимых К+-каналов в процессе регуляции секреции инсулина считается ключевой (3, 10). После взаимодействия ПСМ с рецептором развивается цепь последовательных событий: закрытие АТФ-зависимых К+-каналов транспорта ионов калия, прекращение трансмембранного потока ионов калия и деполяризация мембраны. В дальнейшем деполяризация мембраны активирует кальциевые каналы, и значительно увеличивается приток кальция внутрь β-клеток. Повышение концентрации ионов кальция внутри β-клеток способствует движению гранул, содержащих инсулин, через их мембрану и секреции инсулина в кровоток. При низком уровне глюкозы в крови и при низкой концентрации АТФ внутри β-клеток канал транспорта ионов калия открыт, и за счет его функционирования создается мембранный потенциал, который препятствует проникновению внутрь β-клеток ионов кальция, необходимых для движения гранул, содержащих инсулин, через мембрану β-клеток и секреции гормона в кровоток. Следовательно, ПСМ активируют физиологический механизм, посредством которого глюкоза стимулирует продукцию инсулина.
Принципиальный подход к выбору того или иного ПСМ основывается на оценке баланса эффективности, безопасности и доступности для пациента. Неодинаковая аффинность ПСМ к специфическим рецепторам β-клеток поджелудочной железы обусловливает их различную сахароснижающую активность (6, 4). Чем выше сродство препарата к рецептору, тем будет дольше его подавляющее влияние на АТФ-зависимые К+-каналы, а значит, тем сильнее будет стимулироваться эндогенная секреция инсулина за счет поступления в β-клетки ионов кальция. Среди ПСМ наиболее выраженным сахароснижающим эффектом обладает глибенкламид, поскольку препарат характеризуется максимальным сродством к АТФ-зависимым K+-каналам β-клеток. Более того, высокая сахароснижающая активность препарата объясняется и особенностями химической структуры – наличием не только сульфонилмочевинной, но и бензамидной группировки (рисунок 1). Итак, взаимодействуя с двумя связывающими местами рецепторов β-клеток поджелудочной железы, глибенкламид наиболее быстро и сильно способствует закрытию АТФ-зависимых К+-каналов, стимулирует деполяризацию мембраны, повышение внутриклеточного Са2+ и, следовательно, секрецию эндогенного инсулина.
В настоящее время глибенкламид – это единственный ПСМ, терапия которым доказано снижает риск развития хронических осложнений СД 2. Существенным является, что по данным исследования URPDS лечение глибенкламидом позволило снизить риск развития микрососудистых осложнений на 30% (р = 0,015), включая ретинопатию, требующую фотокоагуляции – на 33% (р = 0,008). Проблема макрососудистых осложнений СД 2 представляется еще более серьезной: глибенкламид значительно уменьшал частоту инфаркта – на 22% (р = 0,056). Благодаря столь выраженному сахароснижающему действию, задокументированному в URPDS длительному опыту применения, отличающему глибенкламид от всех других ПСМ, этот препарат по-прежнему остается золотым стандартом пероральной сахароснижающей терапии и наиболее часто используемым ПСМ (13).
В Российской Федерации применяется как традиционная форма глибенкламида (немикронизированная, 5 мг), так и микронизированные формы препарата. Ввиду особенностей фармакокинетики и фармакодинамики микронизированные формы глибенкламида (препарат Манинил®, , Германия) (1,75/3,5 мг) назначаются в настоящее время шире, чем немикронизированная. Большим достоинством микронизированной формы глибенкламида является быстрая абсорбция (полное высвобождение действующего вещества в течение 5 мин. после растворения) и соответственно полная биодоступность (100%), благодаря чему суточная доза глибенкламида снижается на 30-40% в отличие от традиционной формы глибенкламида 5 мг. Терапевтическая концентрация препарата Манинил® в крови достигается быстро, в течение 15-30 мин. Период полувыведения микронизированной формы глибенкламида составляет 1,5-3,5 ч; длительность сахароснижающего действия, однако, не соответствует этому периоду и составляет сутки. Благодаря этим фармакокинетическим характеристикам микронизированные формы глибенкламида можно принимать 1-2 раза в сутки, что удобно для пациентов, а плавное достижение максимальной концентрации через 2,5 часа – на подъеме постпрандиальной гипергликемии – позволяет избежать риска гипогликемий между приемами пищи, что, без сомнения, важно для пожилых пациентов.
Начальная доза микронизированной формы глибенкламида обычно составляет 1,75-3,5 мг в день, Манинил® необходимо принимать непосредственно перед приемом пищи. Доза препарата постепенно титруется до достижения необходимого терапевтического эффекта – целевых показателей гликемии – не быстрее чем каждые 5-7 дней; если суточная доза составляет 50% от максимальной терапевтической дозы (14 мг/сут.), то рекомендуется 2-кратный прием Манинила.
Глибенкламид метаболизируется с образованием неактивных и активных оксиметаболитов и характеризуется двойным путем выведения: 50% через почки, столько же с желчью. При хронической почечной недостаточности выведение глибенкламида не меняется, однако снижается связывание с белками, вследствие чего возрастает свободная фракция Манинила и риск развития гипогликемии (1).
Всегда следует помнить о возможном риске развития гипогликемических состояний, особенно опасных в пожилом возрасте, на фоне сахароснижающей терапии. Одной из частых причин гипогликемий является быстрое увеличение суточной дозы или неправильно подобранные дозы Манинила, а также нарушение режима питания (резкое ограничение сложных углеводов, пропуск очередного приема пищи) и нерациональная физическая нагрузка.
Пациенты с СД 2 часто имеют различную сопутствующую патологию, поэтому в клинической практике необходимо принимать во внимание и проблему лекарственного взаимодействия. Так, при назначении целого ряда препаратов за счет различных механизмов может наблюдаться как усиление, так и ослабление действия глибенкламида, как и других ПСМ: снижают сахароснижающую активность глюкокортикоиды, барбитураты, фенотиазины, тиазидные диуретики, тиреоидные гормоны (супрессивная терапия), эстрогены, гестагены, адреномиметики, производные никотиновой кислоты, рифампицин. Напротив, следующие препараты усиливают сахароснижающее действие: салицилаты, сульфаниламиды, анаболические стероиды, пентоксифиллин, аллопуринол, хлорамфеникол, пиразолоновые производные, клофибрат, безафибрат, ингибиторы моноаминоксидазы, непрямые антикоагулянты, противогрибковые средства системного действия, спиртсодержащие лекарственные средства.
Известно, что 85-90% больных с СД 2 имеют избыточную массу тела или ожирение. Нежелательным побочным эффектом глибенкламида, как и других ПСМ, в ряде случаев может быть прогрессирование ожирения (рисунок 2), что можно уменьшить или предотвратить соблюдением врачебных рекомендаций по питанию и физическим нагрузкам, что часто не претворяется активно на практике пациентами.
Не возможно обойти вниманием такой важный вопрос, как доступность терапии, в связи как с хроническим характером течения заболевания и необходимостью длительной сахароснижающей терапии, так и с огромным, постоянно растущим количеством больных СД 2 и непростой экономической ситуацией, сложившейся в нашей стране. В этом плане наиболее выгодным является применение Манинила с учетом высокой эффективности, длительного опыта применения и наличия современной микронизированной формы препарата. Высокую социальную значимость глибенкламида подчеркивают и эксперты ВОЗ, включив его в очередной раз в перечень Основных лекарственных средств – наиболее эффективных, безопасных и выгодных с фармако-экономической точки зрения средств для лечения социально значимых заболеваний; глибенкламид является единственным представителем ПСМ в данном списке (15).
Противопоказаниями к назначению Манинила являются: СД типа 1, диабет после панкреатэктомии, кетоацидоз, хирургические вмешательства (большие операции), тяжелые инфекции и травмы, аллергии на ПСМ или сходные с ними препараты в анамнезе, тяжелые нарушения функции почек и печени. Следует воздержаться от назначения препарата в период беременности и лактации.
У большинства больных СД 2 монотерапия ПССП не обеспечивает долгосрочного эффективного гликемического контроля: по результатам исследования UKPDS монотерапия одним из пероральных сахароснижающих препаратов через 3 года от начала лечения была эффективной только у половины пациентов, а через 9 лет – лишь у 25%; это приводит к необходимости назначения комбинированной терапии (11). Дальнейшее поддержание компенсации углеводного обмена может быть достигнуто при использовании комбинации из двух-трех ПССП с разным механизмом действия или при добавлении к лечению базального инсулина. Манинил® может эффективно использоваться в комбинированной терапии как с метформином, тиазолидиндионами, миметиками инкретина, так и с инсулином (4, 6).
В заключение следует отметить, что при назначении сахароснижающей терапии не нужно пренебрегать ПСМ – основой фармакотерапии заболевания – Манинилом с длительным опытом клинического применения и доказанной эффективностью, что позволит задержать или отсрочить время появления осложнений заболевания, улучшить прогноз и повысить качество жизни пациентов.
Классификация противодиабетических препаратов
Препараты инсулинов классифицируют по происхождению на бычий (говяжий), свиной и человеческий инсулин.
Бычий и свиной инсулины получают из поджелудочной железы крупного рогатого скота и свиней соответственно.
Человеческий (рекомбинантный, генно-инженерный) инсулин получают с помощью биотехнологий – ген человеческого инсулина внедряют в клетку пекарских дрожжей или кишечной палочки, которые затем начинают вырабатывать гормон, полностью аналогичный инсулину человека.
Кроме того, препараты инсулинов классифицируют по продолжительности действия:
- препараты инсулинов быстрого действия (начало действия – 15-30 мин, продолжительность – 4-6 ч): инсулин лизпро, инсулин аспарт, инсулин глулизин;
- препараты инсулинов средней продолжительности действия (начало действия – 1-1,5 ч, продолжительность – 8-12 ч): инсулин человеческий, инсулин свиной;
- препараты инсулинов длительного действия (начало действия – 4-8 ч мин, продолжительность – 20-30 ч): инсулин гларгин, инсулин детемир, инсулин деглудек.
Кроме того, существуют комбинированные препараты инсулинов длительного действия с инсулинами быстрого действия (инсулин деглудек + инсулин аспарт), а также комбинация инсулина длительного действия с агонистом глюкагоноподобного пептида-1 (инсулин гларгин + ликсисенатид).
Синтетические противодиабетические препараты классифицируют по химическому строению, механизму действия и происхождению:
- производные сульфонилмочевины: глибенкламид, гликлазид, глимепирид, гликвидон;
- бигуаниды: метформин;
- тиазолидиндионы: пиоглитазон, розиглитазон;
- ингибиторы α-глюкозидазы: акарбоза, воглибоза;
- ингибиторы дипептидилпептидазы-4: ситаглиптин, вилдаглиптин, саксаглиптин, алоглиптин, линаглиптин, гемиглиптин;
- аналоги глюкагоноподобного пептида 1-го типа: эксенатид, лираглутид, ликсисенатид, дулаглутид;
- ингибиторы натрий-глюкозного котранспортера 2-го типа: дапаглифлозин, канаглифлозин, эмпаглифлозин;
- меглитиниды: натеглинид, репаглинид;
- ингибиторы альдозоредуктазы: изодибут;
- смолы: гуаровая камедь;
- препараты растительного происхождения: побеги черники, створки плодов фасоли.
Кроме того, в случаях, когда для достижения выраженного сахароснижающего действия недостаточно одного препарата, разработаны эффективные комбинации: бигуаниды + производные сульфонилмочевины; бигуаниды + ингибиторы дипептидилпептидазы-4; тиазолидиндионы + ингибиторы дипептидилпептидазы-4; ингибиторы натрий-глюкозного котранспортера 2-го типа + ингибиторы дипептидилпептидазы-4; бигуаниды + производные сульфонилмочевины + тиазолидиндионы.
Изменение и интенсификация терапии
На первом или последующих визитах пациента нужно предупреждать о возможной необходимости интенсификации терапии:
“Со временем заболевание обычно прогрессирует и эффект от препарата ослабевает. При недостаточной эффективности одного таблетированного препарата может возникнуть необходимость увеличения дозы и/или добавления второго и иногда третьего препарата. Время снижения эффекта от терапии очень индивидуально. В будущем для контроля уровня сахара крови может потребоваться инсулинотерапия. Она может носить временный характер (например, при хирургическом вмешательстве) или назначаться постоянно. Если это произойдет, это не будет являться Вашей виной”.
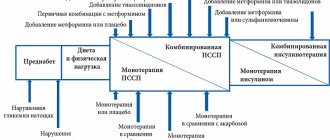
Можно отметить, что в некоторых случаях пероральная терапия может быть временно приостановлена при достижении показателей хорошего контроля — чаще всего при значительном снижении массы тела. Но в большинстве случаев от приема одного препарата переходят к приему еще одного таблетированного препарата (комбинации). При интенсификации терапии можно использовать более удобный вариант приема сразу двух препаратов в одной таблетке (фиксированные комбинации). Возможность применения фиксированных комбинаций важна для пациентов с СД2, поскольку заболевание зачастую сопровождается сопутствующей патологией и, соответственно, приемом других препаратов. Пациент должен быть достаточно осведомлен о преимуществах фиксированных комбинаций, т. к. это может повышать его приверженность лечению. Стоит остановиться на самых распространенных видах комбинированной терапии:
- метформин + ПСМ — комбинация, позволяющая повышать выработку инсулина и чувствительность к нему в организме. Быстро снижает уровень сахара крови, но имеет недостатки в отношении риска развития гипогликемии и набора массы тела;
- метформин + ингибиторы ДПП-4 — комбинация, позволяющая повышать выработку инсулина глюкозозависимым путем и чувствительность к инсулину. Не приводит к развитию гипогликемий и набору массы тела.
Основы лечения сахарного диабета
Противодиабетические препараты подбираются индивидуально опытным врачом-эндокринологом с учетом массы тела пациента, типа и тяжести сахарного диабета, сопутствующих заболеваний.
Препараты инсулинов пациенты с сахарным диабетом 1-го типа используют пожизненно.
В лечении сахарного диабета 1-го типа, помимо препаратов инсулина, важное значение имеет низкоуглеводная диета. Для контроля потребления углеводов, а также расчета индивидуальной дозы инсулина, используют систему хлебных единиц – ХЕ, где 1 ХЕ равна 1 куску белого или ржаного хлеба.
Применение препаратов инсулина должно имитировать ритм естественной секреции инсулина, для чего используют препараты инсулина разной продолжительности действия. Обычно утром используют препарат инсулина длительного действия, а препараты короткого действия три раза в день – за 15-20 мин до еды. Пропускать прием пищи при этом категорически не рекомендуется.
Препараты инсулинов вводят подкожно, с помощью одноразового пластикового шприца или шприц-ручки со сменными картриджами. Пациентам необходимо иметь 2 шприц-ручки – одну для инсулина короткого действия, другую – для препарата длительного действия.
В неотложных случаях (гипергликемическая кома) допустимо введение инсулинов короткого действия внутривенно.
В лечении сахарного диабета 2-го типа, помимо лекарственных препаратов, важное значение имеет диета и регулярные умеренные физические нагрузки.
Эффект препаратов этой фармакологической группы сохраняется только при регулярном приеме, потому синтетические противодиабетические средства принимают постоянно длительно (чаще всего – пожизненно).
Практически все синтетические противодиабетические препараты используют внутрь (перорально). Исключением являются аналоги глюкагоноподобного пептида 1-го типа – их вводят подкожно.
Вопросы контроля
Пациентов молодого возраста нужно предупреждать о том, что хороший метаболический контроль помогает предотвращать долгосрочные осложнения. Для контроля течения заболевания необходимо проводить регулярный медицинский осмотр, включающий оценку состояния глазного дна, оценку пульсации на артериях стоп, чувствительности стоп, определение ряда лабораторных показателей (уровней гликированного гемоглобина, липидов, креатинина, скорости клубочковой фильтрации и т. д.).
Самоконтроль — это хороший способ активно вовлекать пациента в процесс лечения. Он включает самостоятельное измерение уровня глюкозы крови, контроль массы тела, самостоятельное измерение артериального давления, ежедневный осмотр стоп. Частота самостоятельного измерения глюкозы крови при лечении ПССП определяется индивидуально, зависит от исходного уровня контроля гликемии, но не реже 1-2 раз в неделю до и через 2 часа после еды. Необходимо уведомлять пациента, при каких показателях гликемии ему необходимо обратиться к врачу.
Для пожилых пациентов самоконтроль должен быть сфокусирован на отсутствии симптомов высокого уровня сахара крови. Самостоятельное использование тестов может быть применимо при появлении недомогания.
Важно отметить, что уровни сахара крови и гликированного гемоглобина будут регулярно оцениваться во время посещения врача и отражать результаты усилий самого больного.