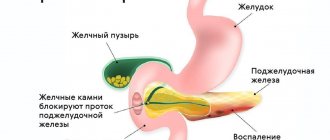
Каждые весну и осень я мучаюсь от обострения гастрита и панкреатита, поэтому минимум раз в год я ложусь в больницу, где мне делают уколы, дают таблетки и иногда ставят капельницы. Это нарушает весь режим жизни – проблемы на работе (я главный менеджер строительной компании, поэтому не могу долго отсутствовать), в семье (дети скучают), да и очень много денег уходит на такую кучу лекарств. Решение купить Даларгин пришло неожиданно и из неоткуда. На очередном приеме у врача сидя в ожидании своей очереди я познакомилась с женщиной, которая рассказала, что она дважды в год перед сезоном обострения проходит курс терапии при помощи Даларгина и обострение не наступает. Спросила у гастроэнтеролога об этом лекарстве – она сказала, что да, действительно, можно воспользоваться этим советом.
Когда я пришла домой, то нашла описание Даларгина и как же удивилась, что он эффективен и при панкреатите, а я ведь была у врача по поводу хронического гастрита.
Купила препарат, врачи дали назначение (дозировку, продолжительность курса, как вводить и т. д.) и как раз в конце февраля начала колоть уколы. В сентябре сделала то же самое и так теперь постоянно. Если честно, то забыла, когда в больнице лежала, года два точно нет.
PS: Стоят ампулы недешево, но по сравнению с той суммой, которую я обычно выкладывала при лечении в клинике, это сущие пустяки.
Даларгин – избегайте подделок
Отзыв оставил(а) Dgchuss
Оценка: 3
(из 5-ти)
Достоинства:
Реальная вещь, а если учитывать, что курс лечения максимум месяц, то еще и недорого выходит
Недостатки:
Если покупать через интернет, можно нарваться на подделку
Иногда прохожу курс терапии при помощи инъекций Даларгином. У меня язва двенадцатиперстной кишки. Вводят препарат внутривенно. Я обычно колюсь дома, так как жена ветеринар, поэтому имеет опыт ставить уколы. Обычно реакция была нормальная и всегда покупал через интернет (дешевле, чем в аптеке). А тут после первого же укола у меня сильно начало урчать в желудке и появился понос. Но самое странное – мне не стало легче.
После этого я поговорил с врачом и мы пришли к выводу, что скорее всего, я наткнулся на фальсификат. Не стал жалеть деньги и время на поиски того сайта, где покупал раньше и заказал необходимое количество ампул. В этот раз побочных реакций не было, а эффект присутствовал. Вот такая печальная история, так что ищите официальный сайт, где продает оригинальный Даларгин.
УДК 616.3-089-06:616.37-002-08:615.243
Изучена эффективность даларгина в комплексной терапии хронического панкреатита, развившегося после резекции желудка у больных язвенной болезнью. Показано положительное влияние даларгина на клиническое течение заболевания и функциональное состояние поджелудочной железы. Авторы связывают это с восстановлением микроциркуляции и антиоксидантным действием препарата. Согласно данным отдаленных наблюдений, эффект терапии сохранялся в течение года.
Evaluation of dalargin effectiveness in the treatment of postgastroresectional pancreatitis
The efficacy of dalargin in the treatment of chronic pancreatitis, which developed after stomach resection in patients with peptic ulcer disease, was investigated. The positive effect of dalargin on the clinical course of disease and the functional state of the pancreas was found. The authors attribute this to the restoration of microcirculation and antioxidant action of the drug. According to long-term observations the effect of therapy was maintained throughout the year.
Резекция желудка остается в числе основных оперативных вмешательств при осложненной язвенной болезни желудка и двенадцатиперстной кишки [1]. Однако после резекции желудка у 14,3-24,1% больных развивается постгастрорезекционный панкреатит (ПП) [2, 3]. Это может быть следствием выключения антральной гормональной зоны и двенадцатиперстной кишки, играющих важную роль в координации деятельности пищеварительной системы [4, 5], а также результатом высокой нагрузки на поджелудочную железу (ПЖ) в связи с ее компенсаторно-приспособительной функцией после резекции желудка. Длительный болевой синдром и развитие внешнесекреторной панкреатической недостаточности существенно снижают качество жизни пациентов, требуют серьезной медикаментозной терапии.
В последние годы в коррекции различных патологических процессов, в том числе в ПЖ, рекомендуются природные пептиды и их синтетические аналоги. Одним из таких регуляторных пептидов является аналог лей-энкефалина даларгин [6, 7]. Проведенные в стационарных условиях клинические испытания даларгина продемонстрировали его высокую активность в лечении обострений язвенной болезни желудка и двенадцатиперстной кишки [8]. Положительный терапевтический эффект препарата отмечен у больных острым панкреатитом [6, 7].
Цель нашей работы — изучение особенностей изменений функционального состояния ПЖ после резекции желудка и обоснование использования даларгина в лечении больных ХП.
Материалы и методы. Под наблюдением находилось 50 больных язвенной болезнью желудка и двенадцатиперстной кишки после резекции желудка с развившимся впоследствии ПП, из них у 27 больных проведена резекция — по Бильроту-1 и у 23 — по Бильрот-2. Исследование больных проводилось в сроки от 1 до 31 года после оперативного вмешательства. Больные были в возрасте от 26 до 71 года. Мужчин было 45 (90%), женщин — 5 (10%). Длительность заболевания язвенной болезнью до операции составила от 1 до 39 лет.
Пациенты были разделены на 2 группы, сопоставимые по возрасту, тяжести течения, выраженности болевого синдрома, длительности течения панкреатита, по частоте сопутствующей патологии: 25 больных группы наблюдения получали в комплексной терапии даларгин ежедневно в дозе 1 мг внутримышечно 2 раза в день, курсовая доза даларгина составляла 20-30 мг; 25 больных группы сравнения получали традиционную терапию, включающую спазмолитики, М-холинолитики, ингибиторы протонной помпы, ферментные препараты.
Диагноз ставился на основании анамнестических, объективных и лабораторных данных, данных ультрасонографии, фиброгастродуоденоскопии, интрагастральной рН-метрии и компьютерной томографии. Экзокринную функцию ПЖ оценивали по уровню амилазы, липазы и трипсина в сыворотке крови, диастазы мочи; эндокринную функцию — по уровню инсулина и С-пептида в сыворотке крови. Амилазу в сыворотке крови и диастазу в моче определяли методом Каравея, липаза определялась унифицированным методом. Трипсин, инсулин и С-пептид, а также ТТГ, Т3, Т4, кортизол и гастрин в сыворотке крови определялись радиоиммунологическим методом. Активность процессов перекисного окисления липидов определяли по уровню малонового диальдегида (МДА) в сыворотке крови. Состояние микроциркуляции оценивали с помощью конъюнктивальной биомикроскопии на щелевой лампе ЩЛ 2Б БП по методу В.С. Волкова (1977).
Результаты лабораторно-инструментальных исследований больных сравнивали с данными 15 практически здоровых лиц. Данные обрабатывались методом вариационной статистики, для оценки межгрупповых различий применяли t-критерий Стьюдента, для выявления зависимости между показателями — метод корреляционного анализа.
Результаты и их обсуждение
В процессе комплексной терапии с применением даларгина полностью удалось снять болевые ощущения у 21 (84%) из 25 больных. Уменьшение болевого синдрома отмечено в основном к 3–4-му дню терапии, а исчезновение — на 5–6-й день. При традиционной терапии удалось снять полностью болевой синдром у 72% больных, уменьшение болевого синдрома происходило в основном к 5–7-му дню лечения.
Комплексная терапия с применением даларгина способствовала уменьшению или устранению диспепсических жалоб. Наиболее быстро в группе наблюдения исчезали тошнота, чувство тяжести и распирания в подложечной области. Несколько медленнее проходила отрыжка. Улучшение аппетита отмечено у 80% обследуемых группы наблюдения. Даларгин способствовал нормализации стула у больных: запоры прошли у всех больных, кашицеобразный стул стал оформленным. В группе сравнения тошнота, вздутие живота проходили или уменьшались медленнее.
Применение даларгина отчетливо снимало болезненность при пальпации брюшной стенки у 84% больных, в частности, в области проекции ПЖ, в зоне Шоффара, Губергрица — Скульского, но несколько позже обратного развития спонтанного болевого синдрома.
У больных группы наблюдения базальный уровень амилазы крови был повышенным в 17,85% случаев, пониженным — в 21,4% случаев. В группе сравнения повышенный уровень амилазы в сыворотке крови выявлен в 37,5% случаев, пониженный — в 37,5%. У всех больных с недостаточной секреторной функцией ПЖ при ультразвуковом исследовании выявлено повышение эхогенности структуры органа, что указывает на развитие склеротических процессов в ткани железы как результат ранее перенесенных обострений заболевания.
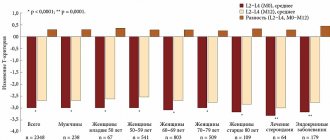
В процессе лечения мы наблюдали разнонаправленную динамику уровней ферментов крови (рис. 1, 2).
Рисунок 1. Динамика содержания амилазы с исходно повышенным уровнем в процессе терапии даларгином (I) и традиционным лечением (II)
Примечание: * — достоверность по отношению к исходному уровню;
**— достоверность по отношению к здоровым (p<0,05)
Рисунок 2. Динамика амилазы с исходно пониженным уровнем в процессе терапии даларгином (I) и традиционным лечением (II)
Примечание: * — достоверность по отношению к исходному уровню;
**— достоверность по отношению к здоровым (p<0,05)
У больных с повышенным содержанием амилазы в крови уровень ее достоверно снизился в процессе лечения в обеих группах, у больных с пониженным базальным уровнем амилазы крови отмечено его повышение в процессе курсового лечения даларгином, изменение уровня амилазы в группе сравнения было несущественным (рис. 2).
Повышение уровня амилазы можно объяснить стимулирующим действием даларгина на клетки ПЖ. Даларгин стимулирует процессы клеточного деления и синтеза ДНК, устраняет развитие эритростазов и микротромбозов, улучшает микроциркуляцию в ПЖ, предупреждает развитие межацинарного и внутриклеточного отека в неповрежденном сегменте железы [9-11].
При исследовании трипсина в сыворотке крови выявлено повышение его у всех обследованных больных ПП. В ходе терапии концентрация трипсина в крови в обеих группах достоверно снижалась (табл.1). Активность липазы у обследованных больных исходно была повышена и в процессе лечения уменьшилась в обеих группах пациентов.
Таблица 1.
Динамика уровня липазы и трипсина в крови больных ПП в процессе терапии
| Обследованные группы | Период исследования | Липаза (ед.) | Трипсин (нг/мл) |
| Группа сравнения | до лечения | 1,24±0,11* (n=11) | 620,2±9,8* (n=10) |
| после лечения | 0,64±0,09** (n=10) | 510,9±11,6** (n=11) | |
| Группа наблюдения | до лечения | 1,27±0,12* (n=9) | 840,6±9,8* (n=10) |
| после лечения | 0,5±0,07** (n=8) | 380,8±11,1** (n=9) | |
| Здоровые | 0,78±0,14 (n=10) | 225,6±17,2 (n=10) | |
Примечание: n — количество обследованных;
* — достоверность по отношению к здоровым (p<0,05),
** — достоверность по отношению к исходному уровню
По данным копрологических исследований, у 23 больных (46%) отмечена амилорея, у 12 (24%) — креаторея и у 7 (14%) — стеаторея. В процессе терапии отмечается положительная динамика копрограммы: в группе сравнения количество больных с креатореей уменьшилось на 50%, с амилореей — с 13 до 7 человек, со стеатореей — с 4 до 2 человек; в группе наблюдения количество больных с креатореей уменьшилось с 6 до 2 человек, с амилореей с 10 до 4 человек и со стеатореей — с 3 до 1 человека.
Как показывают данные табл. 2, у 55,8% больных содержание инсулина в крови было повышено в сравнении со здоровыми лицами, а у 33,2% больных отмечено снижение его уровня. Снижение базального уровня инсулина было отмечено у больных со склеротическими изменениями ПЖ, установленными при эхографии. Секреция инсулина как с исходным низким, так и с исходно повышенным его уровнем незначительно увеличивалась в обеих группах больных в ходе лечения.
Таблица 2.
Динамика уровня инсулина в крови больных ПП в процессе терапии (мкед/мл)
| Группа обследованных | Уровень инсулина | До лечения | После лечения |
| Группа сравнения | Исходно снижен | 6,02±0,86 (n=8) | 6,92±0,41 (n=9) |
| Исходно повышен | 16,25±1,25* (n=12) | 17,73±1,0 (n=10) | |
| Группа наблюдения | Исходно снижен | 5,93±0,56* (n=7) | 6,46±0,41 (n=8) |
| Исходно повышен | 12,88±1,06* (n=13) | 14,52±0,96 (n=11) | |
| Здоровые | 8,83±0,96 (n=10) | ||
Примечание: n — количество обследованных;
* — достоверность по отношению к здоровым (p<0,05)
Способность ПЖ вырабатывать инсулин в полной мере отражает определение концентрации С-пептида в сыворотке крови [12]. Нами не выявлено существенных отличий уровня С-пептида у обследованных больных от здоровых лиц: в контрольной группе он составил 0,3±0,09 пмоль/мл, в группах наблюдения и сравнения — 0,37±0,06 пмоль/мл и 0,34±0,03 пмоль/мл соответственно. В ходе терапии в обеих группах отмечена тенденция к росту концентрации С-пептида в сыворотке крови. Повышение уровней инсулина и С-пептида можно связать со стимулирующим действием терапии на островковую ткань, улучшением метаболизма ткани ПЖ, восстановлением микроциркуляции. Так, по данным биомикроскопии конъюнктивы, в группе наблюдения конъюнктивальный индекс достоверно уменьшился с 6,23±0,68 до 4,21±0,28 (у здоровых он был 1,88±0,23) и в группе сравнения имел тенденцию к снижению (с 6,26±0,66 до 5,33±0,44).
Уровень гастрина у обследованных нами больных был достоверно выше в сравнении со здоровыми лицами (табл. 3). Повышение содержания гастрина в крови возможно обусловлено не только атрофическими поражениями слизистой культи желудка, сопровождающимися низкой концентрацией соляной кислоты, но и высоким содержанием трипсина в крови, способствующего образованию активного гастрина [13]. Установлена зависимость изменений уровня гастрина от вида проводимой терапии. Так, в группе сравнения отмечалась тенденция к повышению его уровня, а в ходе лечения даларгином — тенденция к его снижению.
Таблица 3.
Динамика уровня гормонов в крови больных постгастрорезекционным панкреатитом в процессе терапии
| Группа обследованных | Период исследования | Кортизол (нмоль/л) | Гастрин (нг/л) | Т3 (нмоль/л) | Т4 нмоль/л) | ТТГ (мед/л) |
| Группа сравнения | до лечения | 483,6±19,7* (n=12) | 66,86±7,5 (n=9) | 1,58±0,13 (n=11) | 118,2±9,8 (n=10) | 1,81±0,32 (n=8) |
| после лечения | 398,9±23,8 (n=9) | 71,95±4,9 * (n=10) | 1,81±0,17 (n=10) | 99,9±11,6 (n=11) | 1,7±0,29 (n=7) | |
| Группа наблюдения | до лечения | 480,3±21,7* (n=10) | 76,3±3,8* (n=7) | 1,8±0,09 (n=9) | 120,6±9,8 (n=10) | 2,31±0,41 (n=7) |
| после лечения | 461,2±18,0* (n=11) | 61,2±5,7 (n=13) | 2,01±0,2 (n=8) | 118,8±11,1 (n=9) | 2,1±0,34 (n=6) | |
| Здоровые | 364,75±22,3 (n=15) | 52,8±3,91 (n=15) | 1,82 ±0,14 (n=10) | 124,68±17,2 (n=10) | 2,19±0,47 (n=10) | |
Примечание: n — число наблюдений;
* — достоверность по отношению к здоровым (р<0,05)
По нашим данным, базальный уровень кортизола у больных был выше, чем у здоровых (табл. 3). В процессе лечения в обеих группах больных наблюдалась тенденция к снижению уровня кортизола в крови. Учитывая, что кортизол является одним из стрессовых гормонов [12, 14, 15], мы склонны считать, что гиперкортизолемия у больных в большей мере имела стрессовое происхождение и уменьшалась с купированием болевого синдрома.
У больных базальный уровень Т3 был ниже, а в содержании Т4 существенных изменений не отмечено (табл. 3). В процессе лечения в обеих группах больных наблюдалось увеличение уровня Т3. Уровень ТТГ у больных ПП практически не отличался от здоровых лиц. Проводимая терапия в обеих группах больных приводила к снижению его концентрации в крови.
Содержание МДА в крови, указывающего на активность процессов перекисного окисления липидов, в обеих группах больных было повышено по сравнению со здоровыми. После проведенного курса терапии даларгином количество его в крови уменьшилось с 9,05±0,51 до 6,48±0,44 ммоль/л (р<0,05), в то время как в группе больных, получавших традиционную терапию оно изменялось несущественно. Это мы связываем с выраженным антиоксидантным действием даларгина.
Для оценки эффективности терапии, по данным отдаленных результатов, нами проведено наблюдение за 31 больным в течение двух лет после курса терапии, при этом 15 больных были из группы наблюдения, а 16 пациентов — из группы сравнения. После стационарного лечения больные находились на диспансерном учете. Рецидивы заболевания наступили в течение двух лет в группе сравнения у 9 (56,3%), а у больных группы наблюдения обострение заболевания отмечено у 6 (40%). При этом рецидивы заболевания в группе сравнения чаще наступали в первые месяцы после выписки из стационара и в целом в течение года частота их составила 43,8%. В группе наблюдения рецидивы заболевания возникали на 2-м году после стационарного лечения.
Причиной наступления рецидива заболевания большинство больных (39,5%) отметило нарушение режима питания, физические нагрузки и нервно-психическое перенапряжение. В группе сравнения из 9 больных с обострением ПП 7 больным (77,8%) было проведено стационарное лечение, тогда как в группе наблюдения стационарно пролечено 3 (50%) из 6 больных.
Выводы
1. При включении даларгина в состав комплексной терапии у больных ПП ликвидируются или уменьшаются болевой синдром и диспепсические явления, одновременно отмечается ряд положительных изменений и со стороны функционального состояния ПЖ.
2. В ходе терапии происходит снижение повышенного уровня гастрина и кортизола в периферической крови.
3. Выявлена выраженная антиоксидантная активность даларгина, что может являться одним из патогенетических механизмов его лечебного действия.
4. Применение даларгина при ПП по данным ближайших и отдаленных наблюдений превосходило по эффективности традиционную терапию.
Я.И. Григус, О.Д. Михайлова, В.Ф. Булычев, А.Ю. Горбунов
Ижевская государственная медицинская академия
Григус Ян Ильич — кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней с курсом сестринского дела
Литература:
1. Жижин Ф.С., Капустин Б.Б. Однорядный антирефлюксный анастомоз при трубчатой резекции желудка // Материалы конфер. «Актуальные аспекты госпитальной хирургии». — Ижевск, 2000. — С. 21-24.
2. Помелов В.С., Барамидзе Г.Г. Диагностика, профилактика и лечение постгастрорезекционного рефлюкс-гастрита // Хирургия. — 1994.— № 5. — С. 32-35.
3. Вахрушев Я.М., Иванов Л.А. Постгастрорезекционные синдромы. — Ижевск, «Экспертиза», 1998. — 139 с.
4. Уголев А.М. Энтериновая (кишечная гормональная) система. — Наука, Л., 1978, 315 с.
5. Вахрушев Я.М. Новые подходы к изучению функциональных связей желудочно-кишечного тракта с железами внутренней секреции // Тер. архив. — 1985. — № 9. — С. 98-102.
6. Георгадзе А.К., Бузенков С.В., Джакия А.К. и др. Особенности диагностики и лечения жирового панкреонекроза // Хирургия. — 1991. — № 4. — С. 11-14.
7. Пенин В.А., Титов М.И., Титов В.Н. и др. Механизм действия и перспективы применения нового отечественного аналога энкефалина — даларгина в комплексном лечении острого панкреатита // Сб. науч. трудов «Острый панкреатит». — Москва, ММСИ, 1986. — С. 20-25.
8. Алексеенко С.А., Тимошин С.С. Влияние блокаторов Н2-рецепторов гистамина и даларгина на репаративные процессы слизистой оболочки гастродуоденальной системы у больных язвенной болезнью двенадцатиперстной кишки // Клин. мед. — 1996. — № 9. — С. 52-54.
9. Титов М.И., Виноградов В.А., Беспалов Т.Д. и др. Даларгин — пептидный препарат с цитопротективным действием // Бюлл. ВКНЦ АМН СССР. — 1985. — № 2 — С. 72-76.
10. Виноградов В.А., Полонский В.М. Даларгин — наиболее активный синтетический аналог эндогенных опиоидов для лечения язвенной болезни (итоги пятилетнего поиска) // Бюлл. ВКНЦ АМН СССР. — 1986. — № 2. — С. 62-63.
11. Иваников И.О., Виноградов В.А. Результаты применения даларгина при панкреатите // Матер. конф. ВНОГ. — Смоленск, 1991. — С. 224-226.
12. Вахрушев Я.М., Трусов В.В., Виноградов Н.А. Печень и гормоны. — Ижевск, 1992. — 112 с.
13. Trefflot M.J., Laugier R., Brethols A. et al. Increased gastrin release in chronic calcifying pancreatitis and in chronic alcoholism // Horm. Metab. Res. — 1980. — № 12. — Р. 240.
14. Клиническая эндокринология (Руководство для врачей) / под ред. Н.Т. Старковой. — М.: Медицина, 1991. — 512 с.
15. Михайлова О.Д. Эндогенная интоксикация при хроническом панкреатите // Рос. журнал гастроэнтерологии, гепатологии и колопроктологии. — 2010. — № 5. — С. 65.
Даларгин в качестве вспомогательного лекарства
Отзыв оставил(а) Кирилл
Оценка: 4
(из 5-ти)
Достоинства:
Работает быстро и эффективно
Недостатки:
Цена
У меня проблемы с тройничным нервом, поэтому принимаю одновременно много препаратов разных групп. К сожалению, некоторые из них очень негативно сказываются на органах желудочно-кишечного тракта, особенно кислый Карнитон. В связи с этим врач порекомендовал мне дополнительно делать инъекции раствором Даларгин, так как он снижает кислотность, нейтрализует протеолиз и секрецию в поджелудочной железе. А еще ускоряет обменные процессы и вообще положительно влияет на организм.
Для снижения кислотности, что было самой важной моей проблемой мне предлагали и другие альтернативные варианты в виде таблеток, что было бы гораздо дешевле. Но по эффективности с Даларгином ни один препарат не сравнится.
Антисекреторные препараты в комплексном лечении острого панкреатита
Острый панкреатит – острое асептическое воспаление ткани поджелудочной железы демаркационного типа, в основе которого лежат острая дистрофия, ферментная аутоагрессия с некробиозом панкреатоцитов и последующим исходом в некроз ткани железы и окружающих структур с присоединением эндогенной вторичной гнойной инфекции или в склероз поджелудочной железы с атрофией ее железистого аппарата.
В современной клинике ургентной хирургии острый панкреатит занимает третье место по числу экстренно госпитализированных больных, уступая лишь острому аппендициту и острому холециститу. Несмотря на постоянное совершенствование лечебной тактики и внедрение новых диагностических и лечебных технологий, на протяжении последнего десятилетия летальность при остром панкреатите колеблется в пределах 7-15%, а при деструктивных формах панкреатита достигает 40-80%.
На сегодняшний день опубликовано колоссальное количество работ, посвященных проблеме острого панкреатита. Однако до сих пор большинство положений относительно этиологии, патогенеза, классификации и лечебной тактики при данной патологии остаются весьма дискутабельными. Принято считать, что острый панкреатит является полиэтиологическим заболеванием. При этом американские авторы основной его причиной считают злоупотребление алкоголем, немецкие – желчнокаменную болезнь, китайские и вьетнамские авторы – аскаридоз. Тем не менее, традиционно выделяют две группы этиологических факторов данного заболевания. К первой группе относятся факторы, определяющие нарушение оттока панкреатического секрета из ацинусов по внутридольковым протокам в главный панкреатический проток и далее в ДПК, что приводит к резкому повышению давления в протоковой системе поджелудочной железы (гипертензионно-протоковые факторы). Внутрипротоковая гипертензия возникает при спазме, воспалительных, рубцовых и неопластических стенозах большого дуоденального сосочка, том числе и сфинктера Одди, холедохолитиазе. Спазм сфинктера Одди может быть следствием как различных нервно-рефлекторных влияний с рецепторов гепатогастродуоденальной зоны, так и непосредственного раздражения симпатического и парасимпатического отделов нервной системы. Возбуждение блуждающего нерва обуславливает гиперсекрецию панкреатического сока, спазм сфинктера Одди, возникновение стаза и гипертензии в системе панкреатических протоков. Установлено, что длительный прием алкоголя в относительно больших дозах непосредственно вызывает повышение давления в мелких протоках поджелудочной железы. Этиологические факторы, относящиеся ко второй группе, приводят к первичному поражению ацинарных клеток в условиях нормального внутрипротокового давления (первично ацинарные факторы). Известно, что первичное поражение ацинарных клеток поджелудочной железы может возникать при локальных расстройствах гемоперфузии, аллергических реакциях, метаболических нарушениях, гормональном дисбалансе, токсических воздействиях, инфекциях, травме поджелудочной железы. Роль алиментарного этиологического фактора острого панкреатита может быть сведена к следующему. Пища, богатая белками и жирами, алкоголь вызывают выраженную секрецию панкреатического сока, богатого белком и бедного бикарбонатами, что при неадекватном оттоке может служить причиной развития алиментарного панкреатита.. Усиленная секреторная деятельность ацинарных клеток при чрезмерных пищевых раздражениях или при употреблении бедной белком пищи сопровождается необратимыми внутриклеточными повреждениями ацинарного аппарата и развитием метаболического панкреатита. Отмечено, что чрезмерное употребление богатой белками пищи может приводить к сенсибилизации организма белковыми метаболитами, что приводит к развитию аллергического панкреатита.. Таким образом, основными этиологическими факторами острого панкреатита можно назвать следующие: желчнокаменная болезнь, патология терминального отдела общего желчного протока и БДС, злоупотребление алкоголем, травмы (в т. ч. и операционные) поджелудочной железы, сосудистые заболевания, нарушения обмена веществ, инфекции, интоксикации, аутоаллергические состояния. Экспериментально показано и подтверждено клинически, что наиболее тяжелые формы острого панкреатита развиваются при сочетании трех этиологических факторов:
панкреатической гиперсекреции;
острой внутрипротоковой гипертензии;
внутриканальцевой активации панкреатических ферментов.
Патогенез острого панкреатита в настоящее время также остается предметом острых дискуссий. Считается, что к развитию острого панкреатита приводит нарушение внутриклеточного образования и транспорта ферментов поджелудочной железы, а также интраацинарная активация проферментов гидролазами. Пусковым механизмом патологических реакций, являющихся основой воспалительно-некротического поражения поджелудочной железы, служит высвобождение из ацинарных клеток активированных панкреатических ферментов, в норме присутствующих в виде неактивных проферментов. При этом сегодня принято считать, что процессы аутолиза первично обусловлены действием именно липолитических ферментов. Активация липаз происходит при контакте проферментов последних с желчными кислотами и энтерокиназами. Данная ситуация возникает при гидравлической деструкции ацинусов вследствие внутрипротоковой гипертензии, которая является, в основном, следствием гиперсекреции поджелудочной железы и билиарно-панкреатического или дуодено-панкреатического рефлюкса при стенозе или недостаточности сфинктера Одди и дуоденальной гипертензии. Предполагается, что алкоголь оказывает не только непосредственный токсический эффект на панкреатоциты, но также вызывает образование белковых микроконгломератов, окклюзирующих мелкие панкреатические протоки. Заметим, что липаза поджелудочной железы не повреждает здоровую клетку. Повреждение обусловлено действием фосфолипазы А, приводящим к деструкции клеточных мембран, что делает возможным проникновение в клетку липазы. При реализации данного механизма формируются локусы жирового панкреонекробиоза с перифокальным демаркационным валом. Если патобиохимический процесс ограничивается этим, то формируется жировой панкреонекроз. В том случае, если при чрезмерном накоплении в ткани железы жирных кислот рН достигает 3, 4-4, 3, происходит трансформация внутриклеточного трипсиногена в трипсин. При этом трипсин активирует проферменты лизосом, а также другие протеиназы, вызывающие протеолиз панкреатоцитов. Активированная эластаза лизирует стенки сосудов, междольковые соединительнотканные перемычки, что способствует быстрому распространению ферментного аутолиза в поджелудочной железе и в окружающих структурах. Под действием трипсина активизируются все проферменты поджелудочной железы (эластазы, карбоксипептидазы, профермент химотрипсина), проферменты калликреин-кининовой системы, фибринолитические ферменты и профакторы гемокоагуляции, что, в конечном счете, приводит к местным и общим патобиохимическим расстройствам с возможным финалом в виде синдрома полиорганной недостаточности. Принято выделять доинфекционную стадию заболевания, при которой формируются асептические воспалительные и некротические очаги, и фазу инфекционных осложнений – инфицированный панкреонекроз, инфицированный панкреонекроз с панкреатогенным абсцессом, забрюшинная флегмона.
Таким образом, одним из основополагающих моментов комплекса патологических реакций, объединяемых понятием «острый панкреатит», служит внутрипротоковая гипертензия в поджелудочной железе. При этом основной составляющей повышения внутрипротокового давления является секреция (в ряде ситуаций – гиперсекреция) панкреатического сока.
Традиционной классификацией острого панкреатита, принятой практическими хирургами, является клинико-морфологическая классификация, выделяющая острый отечный панкреатит и деструктивные формы панкреатита – жировой панкреонекроз, геморрагический панкреонекроз, а также предусматривающая возможное развитие ранних и поздних осложнений. С. Ф. Багненко, А. Д. Толстой, А. А. Курыгин (2004) выделяют следующие клинические формы острого панкреатита, соответствующие патофизиологической фазности его течения:
I фаза – ферментативная, составляет первые пять суток заболевания. В этот период происходит формирование панкреонекроза различной протяжённости, развитие эндотоксикоза (средняя длительность гиперферментемии составляет 5 суток), а у части пациентов – полиорганной недостаточности и эндотоксинового шока. Максимальный срок формирования панкреонекроза составляет трое суток, после этого срока он в дальнейшем не прогрессирует. Однако при тяжёлом панкреатите период формирования панкреонекроза гораздо меньше (24-36 часов). Целесообразно выделять две клинические формы: тяжёлый и нетяжёлый острый панкреатит.
- Тяжёлый острый панкреатит. Частота встречаемости 5%, летальность – 50-60%. Морфологическим субстратом тяжёлого острого панкреатита является распространённый панкреонекроз (крупноочаговый и тотально-субтотальный), которому соответствует эндотоксикоз тяжёлой степени.
- Нетяжёлый острый панкреатит. Частота встречаемости 95%, летальность – 2-3%. Панкреонекроз при данной форме острого панкреатита либо не образуется (отёк поджелудочной железы), либо носит ограниченный характер и широко не распространяется (очаговый панкреонекроз – до 1, 0 см). Нетяжёлый острый панкреатит сопровождается эндотоксикозом, выраженность которого не достигает тяжёлой степени.
II фаза – реактивная (2-я неделя заболевания), характеризуется реакцией организма на сформировавшиеся очаги некроза (как в поджелудочной железе, так и в парапанкреальной клетчатке). Клинической формой данной фазы является перипанкреатический инфильтрат.
III фаза – расплавления и секвестрации (начинается с 3-ей недели заболевания, может длиться несколько месяцев). Секвестры в поджелудочной железе и в забрюшинной клетчатке начинают формироваться с 14-х суток от начала заболевания. Возможно два варианта течения этой фазы:
- асептические расплавление и секвестрация – стерильный панкреонекроз; характеризуется образованием постнекротических кист и свищей;
- септические расплавление и секвестрация – инфицированный панкреонекроз и некроз парапанкреальной клетчатки с дальнейшим развитием гнойных осложнений. Клинической формой данной фазы заболевания являются гнойно-некротический парапанкреатит и его собственные осложнения (гнойно-некротические затёки, абсцессы забрюшинного пространства и брюшной полости, гнойный оментобурсит, гнойный перитонит, аррозионные и желудочно-кишечные кровотечения, дигестивные свищи, сепсис и т. д. ).
Следует заметить, что далеко не все авторы разделяют точку зрения об эволюции патоморфологических изменений при остром панкреатите и предполагают возможность возникновения первично-деструктивного процесса (геморрагический панкреонекроз) без предшествующего острого отечного панкреатита и жирового панкреонекроза. Возможно, это связано с тем, что пациенты вследствие известной социальной подоплеки госпитализируются уже на стадии геморрагического панкреонекроза или при наличии гнойных осложнений. Тем не менее, большинством исследователей поддерживается мнение о преемственности морфологических фаз острого панкреатита. Так, M. Schein (2004) называет панкреатит «болезнью четырех недель». И это вполне объяснимо, как с точки зрения патоморфологии, так и с прагматичной точки зрения практикующего американского хирурга. Действительно, первые две недели – настойчивое комплексное консервативное лечение, в последующем периоде – оперативные вмешательства от малоинвазивных (лапароскопия, транспариетальные пункции) до весьма агрессивных (некрсеквестрэктомия, оментопанкреатобурсостомия, вскрытие панкреатогенных абсцессов и флегмоны забрюшинного пространства). Поскольку в рамках настоящего раздела автор не ставил своей целью продолжение дискуссии о лечебной тактике при остром панкреатите (прежде всего – о показаниях, сроках и объеме оперативного пособия), основное внимание уделено вопросу консервативного лечения пациентов с данной патологией. Следует отметить, что, по мнению целого ряда авторов (А. Д. Толстой, 2003, M. Schein, 2004), именно патогенетически обоснованная комплексная консервативная терапия при остром панкреатите имеет решающее значение для исхода заболевания. Это особенно актуально при остром отечном панкреатите, поскольку предотвращает переход данной формы панкреатита в панкреонекроз. Не менее актуальной является интенсивная консервативная терапия при уже сформировавшихся очагах жировой или геморрагической деструкции, предупреждающая в данном случае распространение воспалительно-некротических очагов на ранее интактную ткань. Кроме того, учитывая первичную асептичность процесса при остром панкреатите в начальный период заболевания с позиций здравого смысла целесообразно именно активное терапевтическое лечение, направленное на купирование патологических процессов в самой поджелудочной железе, предупреждение и лечение синдрома панкреатогенной токсемии, профилактику гнойно-септических осложнений.
В настоящее время принципиальные положения консервативного лечения острого панкреатита изложены во всех руководствах по неотложной абдоминальной хирургии. Позволим напомнить их читателю с некоторыми комментариями. Итак, при остром панкреатите показаны:
- Мероприятия, направленные на угнетение экзокринной функции поджелудочной железы: А) «Холод, голод и покой» (локальная гипотермия, строгая диета, постельный режим) ; Б) Медикаментозное подавление панкреатической секреции: цитостатики (5-фторурацил, тегафур), ингибиторы желудочной секреции (антисекреторные препараты – Н2-блокаторы, ИПП), агонисты опиоидных рецепторов (даларгин), панкреатическая рибонуклеаза, соматостатин и его синтетические аналоги (октреотид).
- Спазмолитическая терапия: миотропные спазмолитики (дротаверин, папаверин), холинолитики (платифиллин, атропин), инфузии глюкозо-новокаиновой смеси.
- Мероприятия, направленные на инактивацию циркулирующих в крови панкреатических ферментов и торможение каскада реакций калликреин-кининовой системы: ингибиторы протеаз – апротинин, ε- аминокапроновая кислота.
- Купирование болевого синдрома: нестероидные противовоспалительные препараты, опиоидные (разумеется, за исключением морфина) анальгетики, регионарные новокаиновые блокады.
- Коррекция гиповолемических и водно-электролитных расстройств, улучшение микроциркуляции, ингибирование свободно-радикального окисления: инфузии кристаллоидов, коллоидов (препараты гидроксикрахмала, желатины), перфторорганические эмульсии, альбумин, свежезамороженная плазма, специфические и неспецифические антиоксиданты.
- Дезинтоксикационная терапия и методы афферентной детоксикации: инфузии декстранов, форсированный диурез, экстракорапоральная детоксикация (гемо-, лимфо- и энтеросорбция, плазмаферез, ультрагемофильтрация).
- Восполнение энергетических затрат (не менее 3500 ккал/сут): парентеральное питание, сбалансированное энтеральное зондовое питание.
- Коррекция синдрома энтеральной недостаточности: профилактика или купирование пареза кишечника, декомпрессия тонкой и толстой кишки, энтеральный лаваж, применение энтеросорбентов, антигипоксантов.
- Превентивное назначение антибактериальных препаратов: цефалоспорины III поколения, фторхинолоны, метронидазол, при развившемся панкреонекрозе – карбапенемы (меропенем).
- Посиндромная терапия.
В работах различных авторов за последние пять-десять лет отчетливо прослеживается эволюция лечебной тактики у больных с острым панкреатитом от агрессивной хирургической до консервативной выжидательной. Современный подход к лечению больных острым панкреатитом диктует необходимость выбора конкретного варианта проводимой терапии с учетом стадийности течения панкреатита, принимая во внимание динамику лабораторных показателей и данных инструментальных исследований – ультразвуковое исследование, компьютерная томография, магнитно-резонансная томография.
Следует отметить, что непременным условием лечения пациентов с любой клинико-морфологической формой острого панкреатита является соблюдение главного условия – создания покоя для поджелудочной железы. Это достигается путем подавления продукции ферментов панкреатоцитами, вследствие чего значительно уменьшается выделение ферментов, лизирующих белки (трипсин, химотрипсин, эластаза) и фосфолипидные мембраны клеток (фосфолипазы, холестеролэстераза). Таким образом, состояние покоя панкреатоцита способствует регрессу аутолиза и предупреждает некротические изменения тканей. В этой связи в комплексной терапии острого панкреатита ведущее место занимают препараты, прямо или косвенно угнетающие экзокринную функцию поджелудочной железы. Максимальный лечебный эффект достигается при синергичном подавлении синтеза ферментов на уровне поджелудочной железы, выведении и инактивации уже циркулирующих в крови энзимов.
Исторически первым классом соединений, используемым с этой целью при остром панкреатите, явились цитостатики – 5-фторурацил, тегафур. Недостатком этих препаратов является угнетение лейкопоэза, нарушение иммуногенеза, возникновение гипо- и диспротеинемии. Применение данных препаратов оправдано при верифицированном панкреонекрозе с целью максимального подавления секреторной функции поджелудочной железы и тем самым снижения уровня панкреатических ферментов в плазме. Ранее для ингибирования секреции поджелудочной железы широко применялись препараты класса ингибиторов протеаз, но в настоящее время установлено, что препараты ингибиторов протеаз активны лишь в крови. Ингибиторы протеаз в ткань поджелудочной железы, как правило, не попадают в достаточных концентрациях и не могут эффективно осуществлять свою функцию по отношению к ферментам поджелудочного сока. Кроме того, ингибиторы протеаз обладают аутоиммунизирующим действием. Для угнетения экзокринной функции поджелудочной железы оправдано применение агонистов опиоидных рецепторов (даларгин), избирательно накапливающихся в панкреатоцитах и угнетающих синтез панкреатических проферментов. Близким по механизму действием обладает панкреатическая рибонуклеаза, разрушающая матричную РНК клеток, за счет чего ингибируется синтез белков панкреатоцитами. К препаратам выбора при остром панкреатите относится синтетический аналог гормона соматостатина – октреотид, оказывающий выраженное ингибирующее действие на экзокринную функцию поджелудочной железы за счет активации специфических D-рецепторов панкреатоцитов. Основными направлениями его действия являются ингибирование базальной и стимулированной секреции поджелудочной железы, желудка, тонкой кишки, регуляция активности иммунной системы, выработки цитокинов, цитопротективный эффект. Кроме того, октреотид таким же образом действует на париетальные и главные клетки желудка, способствуя снижению кислотообразования. Обычный режим дозирования октреотида 300-600 мкг/сут. при трехкратном внутривенном или подкожном введении.
Патогенетически обоснованным методом ингибирования секреции поджелудочной железы является применение средств, снижающих желудочную секрецию – антисекреторных препаратов. Для понимания механизма действия антисекреторных препаратов при остром панкреатите следует коротко остановиться на регуляции секреции поджелудочной железы. Регуляция секреции сока поджелудочной железы осуществляется нейрогуморальными механизмами, причем основное значение отводится гуморальным факторам – гастроинтестинальным гормонам (секретин, холецистокинин-панкреозимин), активизирующихся с участием рилизинг-пептидов, секретируемых в слизистой оболочке двенадцатиперстной кишки. Секретин усиливает продукцию жидкой части сока, а холецистокинин-панкреозимин стимулирует ферментативную активность поджелудочной железы. Инсулин, гастрин, бомбензин, соли желчных кислот, серотонин также усиливают секреторную активность железы. Выделение панкреатического сока тормозят: глюкагон, кальцитонин, соматостатин. Процесс панкреатической секреции включает в себя три фазы. Цефалическая (сложнорефлекторная) фаза обусловлена преимущественно рефлекторным возбуждением блуждающего нерва. Желудочная фаза связана с эффектами блуждающего нерва и гастрина, секретируемого антральными железами при поступлении пищи в желудок. Во время кишечной (интестинальной) фазы, когда кислый химус начинает поступать в тонкий кишечник, скорость панкреатической секреции становится максимальной, что, в первую очередь, связано с выделением клетками слизистой кишечника секретина и холецистокинина. Таким образом, имеется прямая связь между секрецией соляной кислоты париетальными клетками желудка, снижением интрадуоденального рН, выработкой секретина слизистой двенадцатиперстной кишки и увеличением секреции панкреатического сока. Именно поэтому для ингибирования секреции панкреатического сока, снижения внутрипротокового давления в поджелудочной железе и, в конечном счете, для уменьшения внутрипанкреатической активации ферментов используют меры, направление на подавление секреции соляной кислоты в желудке – физиологического стимулятора секреции поджелудочной железы. Снижение кислотности желудочного сока обусловливает менее выраженное закисление двенадцатиперстной кишки, вследствие чего уменьшается выделение секретина – основного гормона, стимулирующего экскреторную функцию поджелудочной железы.
Следует отметить, что, несмотря на широкое (а в ряде клиник – облигатное) использование антисекреторных препаратов для терапии больных с острым панкреатитом, систематические исследования по данному вопросу ни в России, ни за рубежом не проводились. Из отдельных сообщений известно, что:
— применение омепразола в комплексном лечении пациентов с острым панкреатитом и обострением хронического панкреатита способствует более быстрому купированию абдоминального болевого синдрома, нормализации клинической картины, соответствующих инструментальных и лабораторных показателей (Звягинцева Т. Д. и соавт. , 2003; Минушкин О. Н. и соавт. , 2004) ;
— клиническая эффективность омепразола при остром панкреатите – самая высокая среди противоязвенных средств. Омепразол обладает высокой липофильностью, легко проникает в париетальные клетки слизистой оболочки желудка, где накапливается и активируется при кислом значении pH. У рабепразола, по сравнению с омепразолом, более короткая продолжительность действия. При остром панкреатите суточная доза омепразола составляля 40 мг (М. Buchler et al. , 2000) ;
— на день сегодняшний, основываясь на принципах доказательной медицины, можно со всей уверенностью утверждать, что эффективность ИПП при остром панкреатите достоверно выше по сравнению с блокаторами Н2-гистаминовых рецепторов (K. Bardhan et al. , 2001, данные метаанализа N. Chiba et al. , 1999).
Учитывая тот факт, что для исключения ацидификации двенадцатиперстной кишки интрагастральный рН должен быть не ниже 4, оптимальным режимом применения парентеральной формы омепразола (Лосек) при остром панкреатите следует считать болюсное введение 80 мг препарата с последующей непрерывной инфузией со скоростью 4 мг/ч.
Необходимость применения антисекреторных препаратов при остром панкреатите обусловлена еще двумя обстоятельствами. Очень часто (не менее чем в 20% случаев) острые панкреатиты сочетаются с язвенной болезнью. При этом очевидно наличие как минимум одной причинно-следственной связи: язвообразование – острый панкреатит. Во-первых, возможно развитие воспалительно-некротического процесса в поджелудочной железе вследствие пенетрации язв в головку и тело железы. Во-вторых, язвенная болезнь, как правило, сочетается с выраженными нарушениями моторики двенадцатиперстной кишки, что, реализуясь посредством дуоденальной гипертензии, приводит к формированию дуоденально-панкреатического рефлюкса. В этих сложных клинических ситуациях контроль над кислотообразованием в желудке является одной из основных задач лечения. Поэтому в данном случае применение антисекреторных препаратов, в том числе и длительное, имеет абсолютные показания. Наконец, еще одним показанием для назначения антисекреторных препаратов при остром панкреатите является профилактика стрессового эрозивно-язвенного повреждения, необходимость которой особенно актуальна при тяжелом течении острого панкреатита с развитием крупноочагового панкреонекроза, гнойно-септических осложнений и синдрома полиорганной недостаточности.
В заключение хотим еще раз подчеркнуть, что применение комплекса современных мероприятий интенсивной терапии (антисекреторная терапия, другие ингибиторы секреции поджелудочной железы и протеолитических ферментов, средства детоксикации) у пациентов с острым панкреатитом, с учетом стадийности и индивидуальной динамики заболевания, как и своевременная профилактика гнойных осложнений панкреонекрозов несомненно позволят улучшить результаты лечения больных с острым панкреатитом, сократить пребывание больных в стационаре, уменьшить потребность в проведении инвазивных методов лечения и, самое главное, снизить летальность.
Необычное применение Даларгина
Отзыв оставил(а) Fatina
Оценка: 5
(из 5-ти)
Достоинства:
Многогранность препарата, скорость проявления эффекта
Недостатки:
Особых не нашла
У меня был гранулезный фарингит, поэтому я очень удивилась, когда моя лечащая врач в больнице предложила проколоть курс при помощи уколов Даларгин. Я этот препарат знаю не понаслышке, так как у мужа язва желудка и периодически мы покупаем ампулы. И точно знаю, что он от панкреатита и язв. Но врачу доверилась, так как у нее хорошая репутация, да и работает она уже больше 30 лет.
Так вот кололи уколы мне в заднюю стенку глотки, но как-то подслизисто. Удивил результат – при фарингите мучает очень-очень сильный кашель, а один укол мгновенно его нейтрализовал. После курса в 5 дней кашель как рукой сняло. Не ожидала такого вот удивительного эффекта. Ставлю 5+
Оценка эффективности даларгина в лечении постгастрорезекционного панкреатита
УДК 616.3-089-06:616.37-002-08:615.243
Изучена эффективность даларгина в комплексной терапии хронического панкреатита, развившегося после резекции желудка у больных язвенной болезнью. Показано положительное влияние даларгина на клиническое течение заболевания и функциональное состояние поджелудочной железы. Авторы связывают это с восстановлением микроциркуляции и антиоксидантным действием препарата. Согласно данным отдаленных наблюдений, эффект терапии сохранялся в течение года.
Evaluation of dalargin effectiveness in the treatment of postgastroresectional pancreatitis
The efficacy of dalargin in the treatment of chronic pancreatitis, which developed after stomach resection in patients with peptic ulcer disease, was investigated. The positive effect of dalargin on the clinical course of disease and the functional state of the pancreas was found. The authors attribute this to the restoration of microcirculation and antioxidant action of the drug. According to long-term observations the effect of therapy was maintained throughout the year.
Резекция желудка остается в числе основных оперативных вмешательств при осложненной язвенной болезни желудка и двенадцатиперстной кишки [1]. Однако после резекции желудка у 14,3-24,1% больных развивается постгастрорезекционный панкреатит (ПП) [2, 3]. Это может быть следствием выключения антральной гормональной зоны и двенадцатиперстной кишки, играющих важную роль в координации деятельности пищеварительной системы [4, 5], а также результатом высокой нагрузки на поджелудочную железу (ПЖ) в связи с ее компенсаторно-приспособительной функцией после резекции желудка. Длительный болевой синдром и развитие внешнесекреторной панкреатической недостаточности существенно снижают качество жизни пациентов, требуют серьезной медикаментозной терапии.
В последние годы в коррекции различных патологических процессов, в том числе в ПЖ, рекомендуются природные пептиды и их синтетические аналоги. Одним из таких регуляторных пептидов является аналог лей-энкефалина даларгин [6, 7]. Проведенные в стационарных условиях клинические испытания даларгина продемонстрировали его высокую активность в лечении обострений язвенной болезни желудка и двенадцатиперстной кишки [8]. Положительный терапевтический эффект препарата отмечен у больных острым панкреатитом [6, 7].
Цель нашей работы — изучение особенностей изменений функционального состояния ПЖ после резекции желудка и обоснование использования даларгина в лечении больных ХП.
Материалы и методы. Под наблюдением находилось 50 больных язвенной болезнью желудка и двенадцатиперстной кишки после резекции желудка с развившимся впоследствии ПП, из них у 27 больных проведена резекция — по Бильроту-1 и у 23 — по Бильрот-2. Исследование больных проводилось в сроки от 1 до 31 года после оперативного вмешательства. Больные были в возрасте от 26 до 71 года. Мужчин было 45 (90%), женщин — 5 (10%). Длительность заболевания язвенной болезнью до операции составила от 1 до 39 лет.
Пациенты были разделены на 2 группы, сопоставимые по возрасту, тяжести течения, выраженности болевого синдрома, длительности течения панкреатита, по частоте сопутствующей патологии: 25 больных группы наблюдения получали в комплексной терапии даларгин ежедневно в дозе 1 мг внутримышечно 2 раза в день, курсовая доза даларгина составляла 20-30 мг; 25 больных группы сравнения получали традиционную терапию, включающую спазмолитики, М-холинолитики, ингибиторы протонной помпы, ферментные препараты.
Диагноз ставился на основании анамнестических, объективных и лабораторных данных, данных ультрасонографии, фиброгастродуоденоскопии, интрагастральной рН-метрии и компьютерной томографии. Экзокринную функцию ПЖ оценивали по уровню амилазы, липазы и трипсина в сыворотке крови, диастазы мочи; эндокринную функцию — по уровню инсулина и С-пептида в сыворотке крови. Амилазу в сыворотке крови и диастазу в моче определяли методом Каравея, липаза определялась унифицированным методом. Трипсин, инсулин и С-пептид, а также ТТГ, Т3, Т4, кортизол и гастрин в сыворотке крови определялись радиоиммунологическим методом. Активность процессов перекисного окисления липидов определяли по уровню малонового диальдегида (МДА) в сыворотке крови. Состояние микроциркуляции оценивали с помощью конъюнктивальной биомикроскопии на щелевой лампе ЩЛ 2Б БП по методу В.С. Волкова (1977).
Результаты лабораторно-инструментальных исследований больных сравнивали с данными 15 практически здоровых лиц. Данные обрабатывались методом вариационной статистики, для оценки межгрупповых различий применяли t-критерий Стьюдента, для выявления зависимости между показателями — метод корреляционного анализа.
Результаты и их обсуждение
В процессе комплексной терапии с применением даларгина полностью удалось снять болевые ощущения у 21 (84%) из 25 больных. Уменьшение болевого синдрома отмечено в основном к 3–4-му дню терапии, а исчезновение — на 5–6-й день. При традиционной терапии удалось снять полностью болевой синдром у 72% больных, уменьшение болевого синдрома происходило в основном к 5–7-му дню лечения.
Комплексная терапия с применением даларгина способствовала уменьшению или устранению диспепсических жалоб. Наиболее быстро в группе наблюдения исчезали тошнота, чувство тяжести и распирания в подложечной области. Несколько медленнее проходила отрыжка. Улучшение аппетита отмечено у 80% обследуемых группы наблюдения. Даларгин способствовал нормализации стула у больных: запоры прошли у всех больных, кашицеобразный стул стал оформленным. В группе сравнения тошнота, вздутие живота проходили или уменьшались медленнее.
Применение даларгина отчетливо снимало болезненность при пальпации брюшной стенки у 84% больных, в частности, в области проекции ПЖ, в зоне Шоффара, Губергрица — Скульского, но несколько позже обратного развития спонтанного болевого синдрома.
У больных группы наблюдения базальный уровень амилазы крови был повышенным в 17,85% случаев, пониженным — в 21,4% случаев. В группе сравнения повышенный уровень амилазы в сыворотке крови выявлен в 37,5% случаев, пониженный — в 37,5%. У всех больных с недостаточной секреторной функцией ПЖ при ультразвуковом исследовании выявлено повышение эхогенности структуры органа, что указывает на развитие склеротических процессов в ткани железы как результат ранее перенесенных обострений заболевания.
В процессе лечения мы наблюдали разнонаправленную динамику уровней ферментов крови (рис. 1, 2).
Рисунок 1. Динамика содержания амилазы с исходно повышенным уровнем в процессе терапии даларгином (I) и традиционным лечением (II)
Примечание: * — достоверность по отношению к исходному уровню;
**— достоверность по отношению к здоровым (p<0,05)
Рисунок 2. Динамика амилазы с исходно пониженным уровнем в процессе терапии даларгином (I) и традиционным лечением (II)
Примечание: * — достоверность по отношению к исходному уровню;
**— достоверность по отношению к здоровым (p<0,05)
У больных с повышенным содержанием амилазы в крови уровень ее достоверно снизился в процессе лечения в обеих группах, у больных с пониженным базальным уровнем амилазы крови отмечено его повышение в процессе курсового лечения даларгином, изменение уровня амилазы в группе сравнения было несущественным (рис. 2).
Повышение уровня амилазы можно объяснить стимулирующим действием даларгина на клетки ПЖ. Даларгин стимулирует процессы клеточного деления и синтеза ДНК, устраняет развитие эритростазов и микротромбозов, улучшает микроциркуляцию в ПЖ, предупреждает развитие межацинарного и внутриклеточного отека в неповрежденном сегменте железы [9-11].
При исследовании трипсина в сыворотке крови выявлено повышение его у всех обследованных больных ПП. В ходе терапии концентрация трипсина в крови в обеих группах достоверно снижалась (табл.1). Активность липазы у обследованных больных исходно была повышена и в процессе лечения уменьшилась в обеих группах пациентов.
Таблица 1.
Динамика уровня липазы и трипсина в крови больных ПП в процессе терапии
| Обследованные группы | Период исследования | Липаза (ед.) | Трипсин (нг/мл) |
| Группа сравнения | до лечения | 1,24±0,11* (n=11) | 620,2±9,8* (n=10) |
| после лечения | 0,64±0,09** (n=10) | 510,9±11,6** (n=11) | |
| Группа наблюдения | до лечения | 1,27±0,12* (n=9) | 840,6±9,8* (n=10) |
| после лечения | 0,5±0,07** (n=8) | 380,8±11,1** (n=9) | |
| Здоровые | 0,78±0,14 (n=10) | 225,6±17,2 (n=10) | |
Примечание: n — количество обследованных;
* — достоверность по отношению к здоровым (p<0,05),
** — достоверность по отношению к исходному уровню
По данным копрологических исследований, у 23 больных (46%) отмечена амилорея, у 12 (24%) — креаторея и у 7 (14%) — стеаторея. В процессе терапии отмечается положительная динамика копрограммы: в группе сравнения количество больных с креатореей уменьшилось на 50%, с амилореей — с 13 до 7 человек, со стеатореей — с 4 до 2 человек; в группе наблюдения количество больных с креатореей уменьшилось с 6 до 2 человек, с амилореей с 10 до 4 человек и со стеатореей — с 3 до 1 человека.
Как показывают данные табл. 2, у 55,8% больных содержание инсулина в крови было повышено в сравнении со здоровыми лицами, а у 33,2% больных отмечено снижение его уровня. Снижение базального уровня инсулина было отмечено у больных со склеротическими изменениями ПЖ, установленными при эхографии. Секреция инсулина как с исходным низким, так и с исходно повышенным его уровнем незначительно увеличивалась в обеих группах больных в ходе лечения.
Таблица 2.
Динамика уровня инсулина в крови больных ПП в процессе терапии (мкед/мл)
| Группа обследованных | Уровень инсулина | До лечения | После лечения |
| Группа сравнения | Исходно снижен | 6,02±0,86 (n=8) | 6,92±0,41 (n=9) |
| Исходно повышен | 16,25±1,25* (n=12) | 17,73±1,0 (n=10) | |
| Группа наблюдения | Исходно снижен | 5,93±0,56* (n=7) | 6,46±0,41 (n=8) |
| Исходно повышен | 12,88±1,06* (n=13) | 14,52±0,96 (n=11) | |
| Здоровые | 8,83±0,96 (n=10) | ||
Примечание: n — количество обследованных;
* — достоверность по отношению к здоровым (p<0,05)
Способность ПЖ вырабатывать инсулин в полной мере отражает определение концентрации С-пептида в сыворотке крови [12]. Нами не выявлено существенных отличий уровня С-пептида у обследованных больных от здоровых лиц: в контрольной группе он составил 0,3±0,09 пмоль/мл, в группах наблюдения и сравнения — 0,37±0,06 пмоль/мл и 0,34±0,03 пмоль/мл соответственно. В ходе терапии в обеих группах отмечена тенденция к росту концентрации С-пептида в сыворотке крови. Повышение уровней инсулина и С-пептида можно связать со стимулирующим действием терапии на островковую ткань, улучшением метаболизма ткани ПЖ, восстановлением микроциркуляции. Так, по данным биомикроскопии конъюнктивы, в группе наблюдения конъюнктивальный индекс достоверно уменьшился с 6,23±0,68 до 4,21±0,28 (у здоровых он был 1,88±0,23) и в группе сравнения имел тенденцию к снижению (с 6,26±0,66 до 5,33±0,44).
Уровень гастрина у обследованных нами больных был достоверно выше в сравнении со здоровыми лицами (табл. 3). Повышение содержания гастрина в крови возможно обусловлено не только атрофическими поражениями слизистой культи желудка, сопровождающимися низкой концентрацией соляной кислоты, но и высоким содержанием трипсина в крови, способствующего образованию активного гастрина [13]. Установлена зависимость изменений уровня гастрина от вида проводимой терапии. Так, в группе сравнения отмечалась тенденция к повышению его уровня, а в ходе лечения даларгином — тенденция к его снижению.
Таблица 3.
Динамика уровня гормонов в крови больных постгастрорезекционным панкреатитом в процессе терапии
| Группа обследованных | Период исследования | Кортизол (нмоль/л) | Гастрин (нг/л) | Т3 (нмоль/л) | Т4 нмоль/л) | ТТГ (мед/л) |
| Группа сравнения | до лечения | 483,6±19,7* (n=12) | 66,86±7,5 (n=9) | 1,58±0,13 (n=11) | 118,2±9,8 (n=10) | 1,81±0,32 (n=8) |
| после лечения | 398,9±23,8 (n=9) | 71,95±4,9 * (n=10) | 1,81±0,17 (n=10) | 99,9±11,6 (n=11) | 1,7±0,29 (n=7) | |
| Группа наблюдения | до лечения | 480,3±21,7* (n=10) | 76,3±3,8* (n=7) | 1,8±0,09 (n=9) | 120,6±9,8 (n=10) | 2,31±0,41 (n=7) |
| после лечения | 461,2±18,0* (n=11) | 61,2±5,7 (n=13) | 2,01±0,2 (n=8) | 118,8±11,1 (n=9) | 2,1±0,34 (n=6) | |
| Здоровые | 364,75±22,3 (n=15) | 52,8±3,91 (n=15) | 1,82 ±0,14 (n=10) | 124,68±17,2 (n=10) | 2,19±0,47 (n=10) | |
Примечание: n — число наблюдений;
* — достоверность по отношению к здоровым (р<0,05)
По нашим данным, базальный уровень кортизола у больных был выше, чем у здоровых (табл. 3). В процессе лечения в обеих группах больных наблюдалась тенденция к снижению уровня кортизола в крови. Учитывая, что кортизол является одним из стрессовых гормонов [12, 14, 15], мы склонны считать, что гиперкортизолемия у больных в большей мере имела стрессовое происхождение и уменьшалась с купированием болевого синдрома.
У больных базальный уровень Т3 был ниже, а в содержании Т4 существенных изменений не отмечено (табл. 3). В процессе лечения в обеих группах больных наблюдалось увеличение уровня Т3. Уровень ТТГ у больных ПП практически не отличался от здоровых лиц. Проводимая терапия в обеих группах больных приводила к снижению его концентрации в крови.
Содержание МДА в крови, указывающего на активность процессов перекисного окисления липидов, в обеих группах больных было повышено по сравнению со здоровыми. После проведенного курса терапии даларгином количество его в крови уменьшилось с 9,05±0,51 до 6,48±0,44 ммоль/л (р<0,05), в то время как в группе больных, получавших традиционную терапию оно изменялось несущественно. Это мы связываем с выраженным антиоксидантным действием даларгина.
Для оценки эффективности терапии, по данным отдаленных результатов, нами проведено наблюдение за 31 больным в течение двух лет после курса терапии, при этом 15 больных были из группы наблюдения, а 16 пациентов — из группы сравнения. После стационарного лечения больные находились на диспансерном учете. Рецидивы заболевания наступили в течение двух лет в группе сравнения у 9 (56,3%), а у больных группы наблюдения обострение заболевания отмечено у 6 (40%). При этом рецидивы заболевания в группе сравнения чаще наступали в первые месяцы после выписки из стационара и в целом в течение года частота их составила 43,8%. В группе наблюдения рецидивы заболевания возникали на 2-м году после стационарного лечения.
Причиной наступления рецидива заболевания большинство больных (39,5%) отметило нарушение режима питания, физические нагрузки и нервно-психическое перенапряжение. В группе сравнения из 9 больных с обострением ПП 7 больным (77,8%) было проведено стационарное лечение, тогда как в группе наблюдения стационарно пролечено 3 (50%) из 6 больных.
Выводы
1. При включении даларгина в состав комплексной терапии у больных ПП ликвидируются или уменьшаются болевой синдром и диспепсические явления, одновременно отмечается ряд положительных изменений и со стороны функционального состояния ПЖ.
2. В ходе терапии происходит снижение повышенного уровня гастрина и кортизола в периферической крови.
3. Выявлена выраженная антиоксидантная активность даларгина, что может являться одним из патогенетических механизмов его лечебного действия.
4. Применение даларгина при ПП по данным ближайших и отдаленных наблюдений превосходило по эффективности традиционную терапию.
Я.И. Григус, О.Д. Михайлова, В.Ф. Булычев, А.Ю. Горбунов
Ижевская государственная медицинская академия
Григус Ян Ильич — кандидат медицинских наук, ассистент кафедры пропедевтики внутренних болезней с курсом сестринского дела
Литература:
1. Жижин Ф.С., Капустин Б.Б. Однорядный антирефлюксный анастомоз при трубчатой резекции желудка // Материалы конфер. «Актуальные аспекты госпитальной хирургии». — Ижевск, 2000. — С. 21-24.
2. Помелов В.С., Барамидзе Г.Г. Диагностика, профилактика и лечение постгастрорезекционного рефлюкс-гастрита // Хирургия. — 1994.— № 5. — С. 32-35.
3. Вахрушев Я.М., Иванов Л.А. Постгастрорезекционные синдромы. — Ижевск, «Экспертиза», 1998. — 139 с.
4. Уголев А.М. Энтериновая (кишечная гормональная) система. — Наука, Л., 1978, 315 с.
5. Вахрушев Я.М. Новые подходы к изучению функциональных связей желудочно-кишечного тракта с железами внутренней секреции // Тер. архив. — 1985. — № 9. — С. 98-102.
6. Георгадзе А.К., Бузенков С.В., Джакия А.К. и др. Особенности диагностики и лечения жирового панкреонекроза // Хирургия. — 1991. — № 4. — С. 11-14.
7. Пенин В.А., Титов М.И., Титов В.Н. и др. Механизм действия и перспективы применения нового отечественного аналога энкефалина — даларгина в комплексном лечении острого панкреатита // Сб. науч. трудов «Острый панкреатит». — Москва, ММСИ, 1986. — С. 20-25.
8. Алексеенко С.А., Тимошин С.С. Влияние блокаторов Н2-рецепторов гистамина и даларгина на репаративные процессы слизистой оболочки гастродуоденальной системы у больных язвенной болезнью двенадцатиперстной кишки // Клин. мед. — 1996. — № 9. — С. 52-54.
9. Титов М.И., Виноградов В.А., Беспалов Т.Д. и др. Даларгин — пептидный препарат с цитопротективным действием // Бюлл. ВКНЦ АМН СССР. — 1985. — № 2 — С. 72-76.
10. Виноградов В.А., Полонский В.М. Даларгин — наиболее активный синтетический аналог эндогенных опиоидов для лечения язвенной болезни (итоги пятилетнего поиска) // Бюлл. ВКНЦ АМН СССР. — 1986. — № 2. — С. 62-63.
11. Иваников И.О., Виноградов В.А. Результаты применения даларгина при панкреатите // Матер. конф. ВНОГ. — Смоленск, 1991. — С. 224-226.
12. Вахрушев Я.М., Трусов В.В., Виноградов Н.А. Печень и гормоны. — Ижевск, 1992. — 112 с.
13. Trefflot M.J., Laugier R., Brethols A. et al. Increased gastrin release in chronic calcifying pancreatitis and in chronic alcoholism // Horm. Metab. Res. — 1980. — № 12. — Р. 240.
14. Клиническая эндокринология (Руководство для врачей) / под ред. Н.Т. Старковой. — М.: Медицина, 1991. — 512 с.
15. Михайлова О.Д. Эндогенная интоксикация при хроническом панкреатите // Рос. журнал гастроэнтерологии, гепатологии и колопроктологии. — 2010. — № 5. — С. 65.
Что мне нравится в Даларгине
Отзыв оставил(а) Джин
Оценка: 4
(из 5-ти)
Достоинства:
Наш производитель, которому можно доверять
Недостатки:
Почему-то резко подскочил в цене
Отличный препарат с безупречным качеством, быстрым и всесторонним действием. Но таких в принципе много, особенно в этой ценовой категории. Поэтому лично я обращаю особое внимание на тот факт, что Даларгин имеет минимум противопоказаний – эт беременность, аллергия на компоненты, гипертония и некоторые болезни в инфекционных формах. Что касается побочных реакций, то они отсутствуют. Если, конечно, придерживаться противопоказаний. То есть,если не страдаешь от повышенного артериального давления, то оно критически не повысится или если нет аллергии, то она и не появится.
Даларгин на всех действует по-разному
Отзыв оставил(а) Litvinyacha
Оценка: 3
(из 5-ти)
Достоинства:
Неплохой итоговый результат
Недостатки:
Напишу ниже
Даларгин частенько колят отцу (у него язва) и ему почему-то всегда помогает быстро, особенно при приступах. когда у меня обнаружился панкреатит, то вполне естественно. что я решила использовать тоже Даларгин (после консультации с доктором). В больницу ложиться отказалась,поэтому колола дома по схеме, указанной мне доктором. Если честно, то удивилась, что облегчение пришло только на третий день, а до этого ни малейшей реакции. Хотела уже забросить это дело, да папа настоял, чтоб продолжила курс. в итоге пролечилась нормально и даже результаты анализов намного стали лучше. Только непонятно, почему на всех действует по-разному? Дума., это огромный минус. Ну и цена….