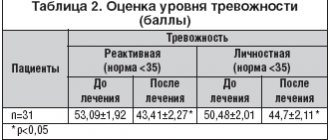
Велаксин
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период лактации (грудного вскармливания).
Женщины детородного возраста должны применять надежные методы контрацепции в период лечения и немедленно обратиться к врачу в случае наступления беременности или планирования беременности.
Венлафаксин и метаболит ОДВ выделяются с грудным молоком. Безопасность этих веществ для новорожденных детей не доказана, поэтому при необходимости приема венлафаксина в период лактации следует решить вопрос о прекращении грудного вскармливания. Если лечение матери было завершено незадолго до родов, у новорожденного могут возникнуть симптомы отмены.
Применение при нарушениях функции печени
Противопоказан при тяжелых нарушениях функции печени.
При умеренной печеночной недостаточности (протромбиновое время от 14 до 18 сек) дозу следует снизить на 50%.
Применение при нарушениях функции почек
Противопоказан при почечной недостаточности тяжелой степени (КК < 10 мл/мин).
Пациентам с почечной недостаточностью при КК 10-30 мл/мин дозу следует снизить на 25-50%. В связи с удлинением T1/2 венлафаксина и его активного метаболита (ОДВ) таким пациентам следует принимать всю дозу 1 раз/сут.
Пациенты, находящиеся на гемодиализе, могут получать 50% обычной суточной дозы венлафаксина после завершения сеанса гемодиализа.
Применение у детей
Противопоказан в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
У пациентов пожилого возраста венлафаксин следует применять в наименьшей эффективной дозе. При повышении дозы пациент должен находиться под тщательным медицинским наблюдением
Пациентов пожилого возраста следует предупредить о возможности возникновения головокружения и нарушения чувства равновесия. Во время приема венлафаксина, особенно в условиях дегидратации или снижения ОЦК, у пожилых пациентов может наблюдаться гипонатриемия и/или синдром недостаточной секреции АДГ
Особые указания
С осторожностью следует применять венлафаксин после недавно перенесенного инфаркта миокарда, при сердечной недостаточности в стадии декомпенсации, при нестабильной стенокардии, артериальной гипертензии, тахикардии, тахиаритмии, судорогах в анамнезе, внутриглазной гипертензии, закрытоугольной глаукоме, маниакальных состояниях в анамнезе, предрасположенности к кровотечениям со стороны кожных покровов и слизистых оболочек, исходно сниженной массе тела.
У больных с депрессивными расстройствами перед началом любой лекарственной терапии следует учитывать вероятность суицидальных попыток. Поэтому для снижения риска передозировки в начале лечения следует по возможности применять венлафаксин в минимальной эффективной дозе, а пациент должен находиться под тщательным медицинским наблюдением.
У пациентов с аффективными расстройствами при лечении антидепрессантами (в т.ч. венлафаксином), могут возникать гипоманиакальные или маниакальные состояния. Как и другие антидепрессанты, венлафаксин следует назначать с осторожностью пациентам с манией в анамнезе. Такие пациенты нуждаются в медицинском наблюдении.
При возникновении эпилептических припадков лечение следует прервать.
Риск тахикардии повышается при применении венлафаксина в высоких дозах.
Во время лечения рекомендуется регулярный контроль АД, особенно в период уточнения или повышения дозы.
Пациентов, особенно пожилого возраста, следует предупредить о возможности возникновения головокружения и нарушения чувства равновесия.
Во время приема венлафаксина, особенно в условиях дегидратации или снижения ОЦК (в т.ч. у пожилых пациентов и больных, принимающих диуретики), может наблюдаться гипонатриемия и/или синдром недостаточной секреции АДГ.
Во время приема препарата может наблюдаться мидриаз, в связи с чем рекомендуется контроль внутриглазного давления у больных, склонных к его повышению или страдающих закрытоугольной глаукомой.
Как и при лечении другими препаратами, действующими на ЦНС, врач должен установить тщательное наблюдение за пациентами для выявления признаков злоупотребления венлафаксином. Тщательный контроль и наблюдение необходимы пациентам, имеющим в анамнезе указания на такие симптомы.
На фоне приема венлафаксина следует соблюдать особую осторожность при проведении электросудорожной терапии, т.к. опыт применения венлафаксина в этих условиях отсутствует.
В период лечения следует избегать приема алкоголя.
Влияние на способность к вождению автотранспорта и управлению механизмами
Несмотря на то, что венлафаксин не влияет на психомоторные и когнитивные функции, следует учитывать, что любая лекарственная терапия психоактивными препаратами может ухудшать мыслительные процессы и снижать способность к выполнению двигательных функций. Об этом следует предупредить пациента перед началом лечения. При возникновении такого рода нарушений степень и длительность ограничений должны быть установлены врачом.
Применение велафакса у пациентов с коморбидными депрессией и тревогой
Депрессивные и тревожные расстройства являются двумя наиболее распространёнными группами психических нарушений. Так, около 19 % населения обнаруживает признаки, достаточные для диагностики депрессивного эпизода, а у 17 % общей популяции выявляются критерии тревожного расстройства (Kessler R.C. и соавт., 1994). Подобного же рода закономерность наблюдается и среди амбулаторных пациентов как психиатрических (Bradley N. соавт., 2007), так и общемедицинских учреждений (Zing W. соавт., 1990). Около 2/3 пациентов с установленным диагнозом большой депрессии обнаруживают признаки, достаточные для диагностики текущего тревожного расстройства (Zimmerman M. соавт., 2000).
Сосуществование симптомов тревоги и депрессии имеет важное терапевтическое и прогностическое значение, поскольку у данной группы пациентов чаще наблюдается хроническое течение заболевания, более выражены нарушения социального и бытового функционирования (Liebowitz M.R., 1993, Lyddiard R.B., 1991). Наличие тревоги у лиц с большой депрессией увеличивает риск совершения суицидных попыток (Placidi G.P. соавт., 2000; Scocco P. соавт., 2000, Schaffer A. соавт., 2000). Распознавание сосуществования депрессии и тревоги является важным фактором, детерминирующим выбор оптимальной терапии. Однако до недавнего времени дизайн клинических исследований зачастую предусматривал исключение пациентов с коморбидными состояниями. Это привело к тому, что на практике выбор препарата для терапии у лиц с коморбидной патологией продолжает представлять большие сложности, поскольку основывается на данных исследований спектра действия препаратов у лиц с так называемыми «чистыми расстройствами». Именно этот факт придаёт изучению эффективности и безопасности антидепрессантов, в особенности препаратов последних поколений, у пациентов с сосуществующими тревогой и депрессией бесспорную актуальность.
В эпоху классических антидепрессантов лишь 20–30 % пациентов с симптоматикой, соответствующей критериям большой депрессии DSM-IY, обращались за медицинской помощью. Отчасти это объяснялось бытовавшим среди пациентов мнением, что доступные методы лечения депрессии являются «субъективно неприятными» ввиду развития побочных эффектов (Angst J., 1990). Потребность в снижении побочных эффектов и увеличении эффективности терапии привела к появлению селективных ингибиторов обратного захвата серотонина (СИОЗС), доказавших свою эффективность как в отношении большой депрессии, дистимии, так и большинства вариантов тревожных расстройств. Вместе с тем, ингибиторы реаптейка серотонина оказались менее эффективными, чем трициклические антидепрессанты, в отношении тяжёлых форм витальной депрессии (Danish University Antidepressant Group, 1990, Anderson I.M., 1998), что привело к поиску химических соединений, обладающих множественными, но специфическими механизмами действия. Клинический и экспериментальный опыт инициировал создание препарата венлафаксин (велафакс, производство компании Pliva), являющегося смешанным ингибитором обратного захвата норадреналина и серотонина, лишенным влияния на другие нейротрасмиттерные системы. По данным клинических исследований, венлафаксин оказался не только более эффективным в купировании симптомов умеренной депрессии по сравнению с имипрамином (Lecrubier Y. и соавт., 1997), но и в отношении выраженной депрессивной симптоматики по сравнению с флюоксетином (Сlerc G.E. и соавт., 1994). Велафакс показал свою эффективность в терапии депрессивных расстройств лёгкой и средней степени тяжести, в том числе с выраженным тревожным компонентом (Волель Б.А., Романов Д.В., 2007). Среди антидепрессантов последних поколений венлафаксин продемонстрировал наилучшее соотношение доза–ответ, что, очевидно, связано с тем, что в малых терапевтических дозах (75–125 мг) венлафаксин выступает как ингибитор реаптейка серотонина с одновременным минимальным эффектом обратного захвата норадреналина, но однако норэпинефриновый эффект возрастает при повышении доз до 150–375 мг. Вместе с тем, профиль побочных эффектов венлафаксина приблизительно эквивалентен СИОЗС.
Высокая эффективность и безопасность венлафаксина привели к тому, что данный препарат во многих сравнительных исследованиях используется в качестве эталонного либо референтного. Вместе с тем, в России препараты, действующим веществом которых является венлафаксин (в их числе препарат велафакс, производство компании Плива), появились лишь несколько лет назад, что придаёт исследованиям их терапевтических характеристик несомненный интерес и актуальность.
ПРОЦЕДУРА ИССЛЕДОВАНИЯ
12-недельное открытое постмаркетинговое исследование было направлено на исследование эффективности велафакса в отношении депрессивной и тревожной симптоматики, общего клинического впечатления, а также показателей переносимости и безопасности у пациентов, переносящих «депрессивный эпизод» (F32), «рекуррентное депрессивное расстройство» (F33) либо «смешанное тревожное и депрессивное расстройство» (F41.2) в соответствии с критериями МКБ-10. При этом необходимым условием для включения в группу испытуемых являлась степень выраженности депрессивной симптоматики, соответствовавшая 20 баллам и более шкалы депрессии Гамильтона (HAM-D21), а уровень тревоги в соответствии со шкалой тревоги Гамильтона (HAM-А) должен был составлять ≥ 20 баллов. В исследование включались лишь те пациенты, оценка тяжести клинического состояния которых по CGI-S составляла ≥ 4.
Дизайн исследования предполагал 4 визита (визит включения, третья, шестая и 12-я недели терапии). В рамках визитов проводили оценку степени выраженности депрессии посредством 21 Item Hamilton Depression Rating Scale (HAM-D21) и Montgomery Asberg Depression Rating Scale (MADRS), оценку степени выраженности тревоги посредством Hamilton Anxiety Rating Scale (HAM-А), а также определение общего клинического впечатления с использованием Clinical Global Impression Severity of Illness (CGI-S) and Improvement (CGI-I). Переносимость исследуемых препаратов оценивалась на 3- и 4-м визите. В исследование не включались лица, имеющие установленную гиперчувствительность к исследуемому препарату, злоупотребляющие спиртными напитками, страдающие умеренной и тяжёлой формами почечной и печёночной недостаточности, некомпенсированными формами сахарного диабета. Критериями исключения служили также употребление опиоидов, беременность и лактация, наличие коморбидных психотических заболеваний, актуальная суицидопасность пациента, а также возраст моложе 18 лет.
Подбор оптимальной дозы проводился индивидуально в соответствии с клиническими данными. Стартовая доза велафакса составляла от 75 до 150 мг в сутки, распределённых на два приёма. Повышение дозировок на 37,5–75 мг допускалось каждые два–три дня до достижения ответа на терапию. Максимальная суточная доза составляла 375 мг. Дизайн исследования допускал при необходимости применение бензодиазепиновых анксиолитиков в течение первых трёх недель приёма велафакса с последующим постепенным снижением дозировок к четвертой неделе приёма, а также применение бензодиазепинов, имидазопириновых анксиолитиков и гипнотиков при нарушениях сна в течение всего периода исследования.
До начала исследования у пациентов было получено письменное информированное согласие на участие в исследовании.
Статистическую обработку полученных данных проводили с помощью программы Statistika 6,0 (компания StatSoft, США).
МАТЕРИАЛЫ
В исследование, проводившееся в отделении гериатрической психиатрии Санкт-Петербургского научно-исследовательского психоневрологического института им. В.М. Бехтерева, были включены 30 пациентов (11 стационарных и 19 амбулаторных): 10 мужчин и 20 женщин в возрасте от 21 до 72 лет. Средний возраст больных составил 54,1 ± 6,32 года. Состояние 6 пациентов, вошедших в группу исследования, соответствовало критериям депрессивного эпизода (F32), 25 пациентов страдали рекуррентным депрессивным расстройством (F33) МКБ-10. Уровень депрессивной симптоматики в момент включения в исследование у пациентов составил 25,54 ± 3,85 балла HAM-D21, 30,10 ± 6,70 балла MADRS, что соответствует тяжёлому депрессивному эпизоду. В нашу выборку не вошли лица, имевшие установленный диагноз «смешанное тревожное и депрессивное расстройство», вместе с тем, выраженность тревоги, измеренная посредством HAM-А, составила 21,06 ± 3,28 балла, что является достаточным для диагностики тревожного состояния. Средняя тяжесть заболевания равнялась 4,32 ± 0,77 баллам по CGI-S.
11 (33 %) пациентов имели подтверждённую сопутствующую соматическую патологию, при этом из 10 больных, страдавших ишемической болезнью сердца и гипертонической болезнью, 8 постоянно принимали β-блокаторы, блокаторы кальциевых каналов либо антигипертензивные средства. У двух больных, включённых в исследование, имелась патология желудочно-кишечного тракта, однако состояние пациентов применения сопутствующей терапии не требовало.
Начальная доза велафакса у 12 больных составила 75 мг, у 18 пациентов – 150 мг, дозировка определялась степенью выраженности депрессивной симптоматики. Эффективную дозу сохраняли до конца наблюдения (12 недель терапии). Средняя доза препарата в момент окончания исследования составила 256,9 ± 81,0 мг в сутки.
РЕЗУЛЬТАТЫ
Из 30 пациентов, включённых в исследование, 27 больных (90,0 %) полностью завершили 12-недельный курс приёма велафакса. Два пациента (10,0 %) выбыли из исследования в течение первых трёх недель приёма препарата по следующим причинам: 1 пациент (3,2 %) ввиду выраженной тошноты при хорошем терапевтическом ответе, 1 больной отказался от продолжения участия по причине увеличения цифр артериального давления и опасений развития декомпенсации гипертонической болезни при повышении дозировок. Один (3,2 %) пациент был выведен из исследования на шестой неделе приёма велафакса ввиду неэффективности терапии высокими дозами.
В ходе исследования оснований для коррекции доз препаратов для терапии сопутствующей соматической патологии не отмечалось, каких-либо признаков лекарственного взаимодействия и осложнений течения имевшихся соматических заболеваний не было констатировано. У 2 пациентов с патологией ЖКТ (хронический гастрит) нежелательных явлений не отмечалось. Среди побочных эффектов, отмеченных в период приёма велафакса, у 2 (6,4 %) молодых пациентов мужского пола при хорошем терапевтическом эффекте отмечалась умеренно выраженная сексуальная дисфункция, что, тем не менее, не привело к отказу от приёма терапии. Оценивавшаяся на третьем и четвёртом визите переносимость препарата была определена как «хорошая», «очень хорошая» либо «отличная» у всех пациентов.
Пять пациентов при включении в исследование принимали бензодиазепиновые транквилизаторы либо гипнотики ввиду выраженных расстройств сна, потребность в применении которых исчезла по мере стабилизации состояния (конец 3-й недели приёма велафакса).
Анализ полученных в ходе исследования данных позволяет констатировать редукцию симптомов депрессии и тревоги у пациентов, вошедших в исследование. Результаты статистической обработки данных психометрических шкал HAM-D21, HAM-А, MADRS представлены на рис. 1 (представлены параметры, имеющие достоверные отличия, р < 0,0001).
Как следует из данных, представленных на рис. 1, уровень тревоги и депрессии у пациентов, включённых в исследование, измеряемый посредством шкал HAM-D21, HAM-А, MADRS снижался, при этом наблюдались достоверные различия в степени выраженности симптоматики между первым и вторым, вторым и третьим, третьим и четвёртым визитами по всем вышеперечисленным шкалам. В то же время, к 12-й неделе приёма велафакса средний уровень депрессии к моменту окончания исследования в нашей выборке средний балл по HAM-D21 составил 5,7 ± 3,45, по MADRS – 6,89 ± 4,80, что соответствует отсутствию депрессивной симптоматики. Следует отметить, что динамика показателей шкалы депрессии Гамильтона в нашей выборке разнилась у пациентов различных возрастных подгрупп. Так, у пациентов моложе 50 лет наблюдалась быстрая редукция депрессивной симптоматики: 10 из 12 пациентов (83 %) этой возрастной категории к 3-й неделе приёма могли быть отнесены к респондерам, поскольку уровень депрессивной симптоматики в соответствии с HAMD уменьшился более, чем на 50 %. К 12-й неделе приёма велафакса 93 % пациентов моложе 50 лет достигли ремиссии. В то же время, у пациентов старше 50 лет было отмечено более медленное уменьшение степени выраженности симптоматики, к 6-й неделе приёма лишь 65 % пациентов данной возрастной подгруппы могли быть отнесены к респондерам, однако к моменту окончания исследования ремиссии достигли 83 % пациентов старше 50 лет.
Особый интерес представляет динамика параметров, выделяемых как т. н. «ключевой фактор» и «фактор тревоги/соматизации», так и отражение собственного депрессивного и собственно тревожного компонентов депрессивного состояния. Динамика параметров, составляющих ключевой фактор, представлена на рис. 2.
Как следует из данных, представленных на рис. 2, значения параметров «депрессивное настроение», «чувство вины», «нарушения работоспособности», «заторможенность» достоверно различались между визитом включения и 6-й неделей приёма (второй визит), достоверно снижались между 3-й и 6-й, 6-й и 12-й неделями терапии (первый, второй и третий визиты соответственно). Значение переменной «суицидные мысли» достоверно уменьшилось между визитом включения и 3-й неделей приёма велафакса (первый визит) а в дальнейшем достоверно значимых различий не имело.
Динамика параметров фактора «тревога/соматизация» представлена на рис. 3.
Как следует из данных, представленных на рис. 3, уровень психической и соматической тревоги, степень выраженности гастроинтестинальных и соматических симптомов достоверно различались между визитом включения и 3-й неделей приёма (первый визит), 3-й и 6-й, 6-й и 12-й неделями приема велафакса (первым, вторым и третьим визитом соответственно). Достоверные различия значений параметра «ипохондрия» и «отношение к заболеванию» обнаружены между третьей и шестой, шестой и двенадцатой неделями приёма велафакса.
У пациентов нашей выборки констатировано постепенное уменьшение степени тяжести заболевания, о чем свидетельствуют достоверные различия показателей шкалы CGI-S между началом лечения и третьей неделей приёма велафакса, третьей и шестой, шестой и двенадцатой неделями приёма велафакса при одновременном изменении параметров общего улучшения с наиболее выраженным достоверным изменением показателей по шкале CGI-I между 3-й и 6-й неделями приёма (первый и второй визит соответственно).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Терапия пациентов с наличием симптомов депрессии и тревоги в клинической картине продолжает представлять значительные трудности, несмотря на значительный арсенал препаратов, имеющихся в настоящий момент в распоряжении практического врача. Нередко в клинической практике эффективность антидепрессантов в отношении тревожно-депрессивной симптоматики оказывается более низкой, чем это демонстрируют клинические исследования, в силу того, что простая экстраполяция данных, полученных при исследовании эффективности и безопасности препаратов, у пациентов с «чистыми состояниями», привносит определённые трудности в вопросы выбора оптимального препарата для терапии больных с коморбидными депрессией и тревогой. Именно поэтому исследования эффективности и безопасности антидепрессивных средств, в особенности, препаратов последних поколений у данной категории больных не теряют своей актуальности.
Целью нашего исследования было изучение терапевтической активности и переносимости велафакса у пациентов, состояние которых укладывалось в рамки депрессивного эпизода либо рекуррентного депрессивного расстройства МКБ-10. Нашу выборку составили лица, степень выраженности депрессивной симптоматики у которых в момент включения в исследование, оцениваемая посредством 21 Item Hamilton Depression Rating Scale (HAM-D21) и Montgomery Asberg Depression Rating Scale (MADRS), соответствовала критериям тяжёлого депрессивного эпизода. В то же время, степень выраженности тревоги, оценивавшаяся по Hamilton Anxiety Rating Scale (HAM-А), была достаточной для диагностики тревожного состояния, что позволяет отнести пациентов, вошедших в нашу выборку, к лицам с коморбидными депрессией и тревогой.
Полученные нами данные позволяют констатировать тот факт, что велафакс обладает достаточной эффективностью не только в отношении собственно депрессивной симптоматики, но и сосуществующей с депрессией тревоги, о чем свидетельствует изменения параметров психометрических шкал, оценивающих степень выраженности тревоги. Обращает на себя внимание синхронность и гармоничность снижения уровня депрессивной и тревожной симптоматики при приёме велафакса у пациентов нашей выборки. Динамика показателей использованных нами психометрических шкал свидетельствует о наличии достоверной разницы в уровне выраженности тревоги и депрессии уже к третьей неделе приёма велафакса по сравнению с началом исследования, что свидетельствовует о быстроте наступления терапевтического эффекта.
Следует отметить некоторые особенности влияния велафакса на психопатологическую симптоматику в различных возрастных группах. Так, число респондеров среди молодых пациентов к третьей неделе приёма препарата составило более 80 %, что согласуется с имеющимися в литературе данными о высокой скорости наступления эффекта велафакса (Волель Б.А., Романов Д.В., 2007). В то же время у пациентов старше 50 лет терапевтический эффект наступал медленнее, лишь к 6-й неделе приёма число респондеров составило около 65 %. Вместе с тем, к моменту завершения исследования средний уровень выраженности депрессивной симптоматики и тревоги в нашей выборке соответствовал состоянию ремиссии в обеих возрастных подгруппах. Подобного рода динамика наступления терапевтического эффекта не является неожиданной, поскольку свойственна пациентам пожилого возраста, особенно, при применении селективных ингибиторов обратного захвата серотонина и тианептина, в меньшей степени амитриптилина (Андрусенко М.П., 2003).
В то же время, следует подчеркнуть, что значительная степень выраженности психопатологической симптоматики обусловила относительно высокие средние эффективные дозировки препарата, более 50 % пациентов получали максимальные или субмаксимальные дозы велафакса, при этом у всех пациентов, полностью завершивших исследование, переносимость характеризовалась как «хорошая», «очень хорошая» и «отличная». Низкий процент выбывших из исследования пациентов свидетельствует о высокой эффективности и хорошей переносимости велафакса.
Таким образом, результаты нашего исследования показали высокую терапевтическую эффективность велафакса в отношении выраженной депрессии и тревоги, что наряду с благоприятным профилем переносимости и высоким уровнем безопасности, может служить основанием для применения велафакса у пациентов с коморбидными тревожными и депрессивными расстройствами.
Список литературы
1. Андрусенко М.П. Особенности развития терапевтического эффекта антидепрессантов в позднем возрасте // Психиатрия. 2003; 1: 46–51. 2. Волель Б.А., Романов Д.В. Опыт применения венлафаксина (велафакса) у пациентов в амбулаторной и клинической практике // Терапия психических расстройств. 2007; 2: 48–52. 3. Anderson I.M. SSRIs versus tricyclic antidepressants in depressed inpatientsa: a meta-analysis of efficacy and tolerability // Depress Anxiety. 1998; 7: 11–18. 4. Angst J. Natural History and epidemiology of depression. In: Gobb J., Goeting N., eds. Current approaches, Southampton: Duphar Medical Relations, 1990; 1–11. 5. Bradley N., Rush J., Trivedi M., Wisniewski S., Balasubramani G.K., Spencer D., Petersen T., Klinkman M., Warden D., Nicholas L., Fava M. Major Depression Symptoms in Primary Care and Psychiatric Care Settings: A Cross-Sectional Analysis // Ann Fam Med. 2007; 5: (2: 126–134. 6. Сlerc G.E., Ruimy P., Verdeau-Pailles. And on behalf of the Venlafaxine French Inpatient Study Grupp. A double-blind comparison of venlafaxine and fluoxetine in patients hospitalized for major depression and melancholia // Int. Clin. Psychopharmacol. 1994; 9: 139–143. 7. Danish University Antidepressant Group. Paroxetine: a selective serotonin reuptake inhibitor showing better tolerance, but weaker antidepressant effect than clomipramine in controlled multicenter study // J. Affective Disorders. 1990; 18: 289–299. 8. Kessler, R.C., Blazer, D.G., McGonagle, K.A. The prevalence and distribution of major depression in a national community sample: the National Comorbidity Survey // American Journal of Psychiatry. 1994; 151; 979–986. 9. Lecrubier Y, Bourin M., Moon C. Efficacy of venlafaxine in depressive illness in general practice // Acta Psychiatr. Scand. 1997; 95: 485–493. 10. Liebowitz M.R. Depression with anxiety and atypical depression // J. Clin. Psychiatry. 1993; 54: Suppl. 2: 10–14. 11. Lyddiard R.B. Co-exiting depression and anxiety: special diagnostic and treatment issues // J. Clin. Psychiatry. 1991; 52: Suppl. 6: 48–54. 12. Placidi G.P., Oquendo M.A., Malone K.M. Anxiety in major depression: relationship to suicide attempts // Am. J. Psychiatry. 2000; 157: 1614–1622. 13. Scocco P., Marietta P., Tonietto M. The role of psychopathology and suicidal intention in predicting suicide risk: a longitudinal study // Psychopathol. 2000; 33: 143–150. 14. Schaffer A., Levitt A.J., Bagby R.M., Suicidal ideation in major depression: sex differences and impact of comorbid anxiety // Can. J. Psychiatry. 2000; 45: 822–828. 15. Zimmerman M., McDermut W., Mattia J.I. Frequency of anxiety disorders in psychiatric outpatients with major depressive disorder (Brief report) // Am. J. Psychiatry. 2000; 157: 1337–1340. 16. Zing W.W., Magruder-Habib K., Velez R. The comorbidity of anxiety and depression in general medical outpatients: a longitudinal study // J. Clin. Psychiatry. 1990; 51: Suppl. 6: 77–80.
Венлафаксин
Применение при беременности и кормлении грудью
Не следует назначать венлафаксин беременным и кормящим грудью женщинам, т.к. безопасность препарата в период беременности и лактации у женщины не установлена в достаточной степени, ввиду того, что отсутствуют адекватно проведенные контролируемые клинические исследования на достаточно большой выборке таких пациенток. Это касается здоровья, как матери, так и, в большей степени, плода/ребенка.
Женщины детородного возраста должны быть предупреждены об этом до начала лечения, следует немедленно обратиться к врачу в случае наступления беременности или планирования беременности в период лечения препаратом. Венлафаксин и его метаболит (ОДВ) выделяются в грудное молоко. При необходимости приема препарата в период лактации необходимо прекращение грудного вскармливания.
На практике встречаются случаи назначения венлафаксина матерям во время беременности и незадолго до родов, когда в конкретной ситуации ожидаемая польза для матери превышает потенциальный риск для плода. В этих случаях у новорожденных часто наблюдались осложнения, которые требовали: увеличение сроков госпитализации, поддержания дыхания и кормления через зонд. Данные осложнения могут развиваться сразу после родов и характерны также в случае приема других антидепрессантов из группы ИОЗСН или СИОЗС (не содержащих венлафаксина). В подобных случаях сообщалось о следующих клинических симптомах у новорожденных: расстройства внешнего дыхания, цианоз, апноэ, судороги, нестабильность температуры, трудности кормления, рвота, гипогликемия, мышечная гипертония или гипотония, гиперрефлексия, тремор, дрожание, раздражительность, вялость, постоянный плач, сонливость или бессонница. Подобные нарушения могут свидетельствовать о серотонинергических эффектах препарата Венлафаксин.
Если венлафаксин применялся во время беременности, и лечение матери было завершено незадолго до родов, у новорожденного может возникнуть синдром отмены. У такого новорожденного следует исключить наличие серотонинового синдрома или злокачественного нейролептического синдрома. Эпидемиологические данные свидетельствуют о том, что применение СИОЗС во время беременности, особенно на поздних сроках беременности, может увеличить риск персистирующей легочной гипертензии новорожденных.
Особые указания
Суицид и суицидальное поведение
Депрессия связана с повышенным риском возникновения суицидальных мыслей, нанесения себе телесных повреждений и суицида (суицидальное поведение). Этот риск сохраняется вплоть до наступления выраженной ремиссии. Поскольку в течение первых нескольких недель терапии или даже большего промежутка времени улучшения может не наблюдаться, до наступления такого улучшения необходимо осуществлять тщательное наблюдение за пациентами. Согласно накопленному клиническому опыту риск суицида может увеличиваться на ранних этапах выздоровления.
Пациенты с суицидальными попытками в анамнезе или с высоким уровнем размышления на суицидальные темы до начала лечения в большей степени подвержены риску суицидальных мыслей или попыток суицида, за такими пациентами необходимо осуществлять тщательное наблюдение. Мета-анализ плацебо-контролируемых клинических исследований антидепрессантов с участием взрослых пациентов с психическими нарушениями показал, что при приеме антидепрессантов по сравнению с приемом плацебо у пациентов моложе 25 лет повышен риск суицидального поведения. Медикаментозное лечение этих пациентов и, в частности, пациентов с высокой степенью риска суицида, должно сопровождаться тщательным наблюдением, особенно на раннем этапе терапии и при коррекции дозы. Пациентов (и лиц, ухаживающих за такими пациентами) следует предупредить о необходимости контролировать любые проявления клинического ухудшения, суицидального поведения или мыслей, а также необычных изменений в поведении, и немедленно обращаться за медицинской помощью при появлении этих симптомов.
У небольшого количества пациентов, принимающих антидепрессанты, в т.ч. венлафаксин, во время начала лечения, изменения дозы или прекращения лечения может наблюдаться агрессия.
Проведенные до настоящего времени клинические исследования не выявили толерантности к венлафаксину или зависимости от него. Несмотря на это, как и при лечении другими препаратами, действующими на ЦНС, врач должен установить тщательное наблюдение за пациентами для выявления признаков злоупотребления препаратом, а также за пациентами, имеющими в анамнезе такие симптомы.
Особые группы пациентов
Венлафаксин не разрешен к применению у детей.
У пациентов с наблюдавшейся ранее агрессией венлафаксин следует применять с осторожностью.
У больных с аффективными расстройствами, биполярным расстройством при лечении антидепрессантами, в т.ч. венлафаксином, могут возникать гипоманиакальные и маниакальные состояния. Как и другие антидепрессанты, венлафаксин должен назначаться с осторожностью больным с манией в анамнезе. Такие пациенты нуждаются в медицинском наблюдении.
При терапии венлафаксином могут возникнуть судорожные расстройства. Как и все антидепрессанты, венлафаксин следует применять с осторожностью у пациентов с судорожными расстройствами в анамнезе, за такими пациентами необходимо установить тщательный контроль. Лечение должно быть прекращено при развитии судорог.
Акатизия
Применение венлафаксина было связано с развитием акатизии, которая характеризуется неприятным для пациента чувством внутреннего двигательного беспокойства и проявляющийся в неспособности больного долго сидеть спокойно в одной позе или долго оставаться без движения. Это состояние может наблюдаться в начале лечения и в течение первых недель лечения. У пациентов, которые появились такие симптомы, увеличение дозы не рекомендуется.
Биполярное расстройство
До начала лечения, необходимо определить тех пациентов, которые находятся в группе риска биполярного расстройства. Такая проверка должна включать подробное изучение анамнеза, в т.ч. семейного, для выявления случаев самоубийства, биполярного расстройства. Следует отметить, что венлафаксин не рекомендован для использования при лечении биполярной депрессии.
Применение у пациентов с сопутствующими заболеваниями
Клинический опыт применения венлафаксина у больных с сопутствующими заболеваниями ограничен.
Следует с осторожностью применять у пациентов с теми заболеваниями, у которых действие венлафаксина на гемодинамические показатели и/или метаболизм может быть значимым.
Пациентов следует предупредить о немедленном обращении к врачу при появлении сыпи, уртикарных элементов или других аллергических реакций.
У некоторых больных во время приема венлафаксина отмечено дозозависимое повышение АД и/или повышение ЧСС, поэтому рекомендуется регулярный контроль артериального давления и ЭКГ, особенно в период уточнения или повышения дозировки венлафаксина. В опыте постмаркетингового применения венлафаксина (при передозировке) были зарегистрированы летальные сердечные аритмии. Перед назначением венлафаксина пациентам с высоким риском развития серьезных нарушений сердечного ритма следует оценить соотношение вероятной пользы к возможному риску при применении.
Пациенты, особенно пожилые, должны быть предупреждены о возможности возникновения головокружения и нарушения чувства равновесия с целью профилактики травматизма.
Во время приема венлафаксина, особенно в условиях дегидратации или снижения ОЦК (в т.ч. у пожилых пациентов и больных, принимающих диуретики), может наблюдаться гипонатриемия и/или синдром недостаточной секреции антидиуретического гормона.
Венлафаксин не исследован на пациентах, перенесших недавно инфаркт миокарда и страдающих декомпенсированной сердечной недостаточностью. Таким пациентам препарат следует назначать с осторожностью.
Прием СИОЗС или венлафаксина пациентами с сахарным диабетом может вызвать изменение уровня глюкозы в плазме крови. Может потребоваться коррекция дозы инсулина и/или противодиабетических лекарственных средств.
Во время лечения рекомендуется воздерживаться от приема любых алкогольсодержащих напитков.
Безопасность и эффективность применения венлафаксина в сочетании с лекарственными средствами, снижающими вес тела (включая фентермин) установлены не были. Не рекомендуется одновременный прием венлафаксина и лекарственных средств, снижающих вес тела.
Женщины детородного возраста должны применять соответствующие методы контрацепции во время приема венлафаксина.
Разъяснения особых симптомов и состояний, возникновение которых возможно при лечении препаратом
Сухость во рту отмечается у 10% пациентов, получавших венлафаксин. Это может увеличить риск развития кариеса. Пациенты должны тщательно соблюдать гигиену полости рта.
Применение венлафаксина может вызвать развитие акатизии, характеризующейся субъективными неприятными ощущениями или двигательным беспокойством и необходимостью часто двигаться, что часто сопровождается неспособностью сидеть или стоять на месте. В основном это происходит в течение первых нескольких недель лечения. Повышение дозы у пациентов, у которых развиваются указанные симптомы, может вызвать нежелательные последствия.
В плацебо-контролируемых клинических испытаниях у 5.3% пациентов было зарегистрировано клинически значимое увеличение содержания холестерина в сыворотке крови. Необходим контроль уровня холестерина при длительном лечении.
Синдром отмены
Во время прекращения лечения распространен синдром отмены, особенно, если это резкое прекращение. Риск синдрома отмены может зависеть от нескольких факторов, включая продолжительность лечения, величину терапевтических доз и скорость их снижения. Очень редко сообщается о данных симптомах у пациентов, которые случайно пропустили прием препарата.
Симптомы синдрома отмены обычно наступают в течение первых нескольких дней после прекращения лечения. Обычно эти симптомы проходят в течение 2 недель, хотя у некоторых людей они могут быть 2-3 месяца и более. Рекомендуется постепенно снижать дозу венлафаксина при прекращении приема препарата — в течение нескольких недель или месяцев, в зависимости от выраженности клинических симптомов заболевания.
Серотониновый синдром
Прием венлафаксина, как и других серотонинергических препаратов, может вызвать серотониновый синдром, потенциально опасное для жизни состояние, в особенности при одновременном применении других лекарственных средств, которые могут повлиять на серотонинергические нейромедиаторные системы, таких как, ингибиторы МАО.
Симптомы серотонинового синдрома могут включать в себя изменения психического статуса (возбуждение, галлюцинации, кома), вегетативную неустойчивость (тахикардия, лабильность АД, гипертермия), нервно-мышечные расстройства (гиперрефлексия, нарушение координации) и/или желудочно-кишечные симптомы (тошнота, рвота, диарея).
Влияние на способность к вождению автотранспорта и управлению механизмами
В период лечения следует соблюдать осторожность при выполнении потенциально опасных видов работ, требующих повышенной концентрации внимания и быстроты психомоторной реакции (в т.ч. вождение автомобиля и управление механизмами).
Материал и методы
Обследованы 32 больных, 15 женщин и 17 мужчин, в возрасте от 18 до 57 лет (средний возраст 31,75 года) с эндогенной депрессией, проходивших стационарное лечение в клинических отделениях отдела по изучению эндогенных психических расстройств и аффективных состояний ФГБНУ «Научный центр психического здоровья» РАН.
По дизайну исследование было открытым натуралистическим. Средняя длительность заболевания от его первой манифестации равнялась 7,9 года, среднее число перенесенных до включения в исследование депрессивных эпизодов было 3,3. Продолжительность текущего депрессивного эпизода до начала приема велаксина в среднем составляла 4,5 мес.
По нозологической принадлежности больные распределились следующим образом: у 22 (68,6%) пациентов были диагностированы эндогенные аффективные заболевания — маниакально-депрессивный психоз (МДП), циклотимия; у 5 (15,6%) депрессия развилась в динамике малопрогредиентной шизофрении, и у 5 (15,6%) отмечалась постпсихотическая депрессия в рамках приступообразной шизофрении. По МКБ-10 депрессивное состояние больных было диагностировано соответственно следующим рубрикам: F31.3—F31.4; F32.0—F32.2; F33.0—F33.2; F21; F20.4. Типологически депрессивные состояния определялись как тоскливые (3 больных, 9,4%), тревожные (11 случаев; 34,4%) и апато-адинамические (18 больных; 56,2%). Таким образом, в соответствии с двухуровневой психопатологической моделью депрессии [24], первые 2 ее типа определялись как типичные представляли позитивную аффективность (тоскливые и тревожные депрессии), апато-адинамические депрессии как атипичные и относились к негативной аффективности.
По сумме баллов по шкале депрессии Гамильтона (HAM-D) до начала лечения: легкая степень выраженности депрессивных расстройств была зарегистрирована только у 2 (6,25%) человек, средняя — у 13 (40,6%), тяжелая депрессия была у 17 (53,15%), т. е. у подавляющего большинства пациентов депрессия была средней и тяжелой степени.
В исследовании использовался венлафаксин, выпускаемый под названием велаксин в таблетках по 75 мг (Венгрия). Препарат назначался внутрь, начиная с 37,5—75 мг в день. В дальнейшем, исходя из состояния больных, в течение последующих дней суточную дозу увеличивали, доводя до максимальной для данного больного, но не более чем до 300 мг. В среднем наибольшая используемая средняя доза велаксина составила 182,1—198,2 мг в день. Прием препарата был двукратным, утром и вечером. Согласно протоколу исследования, курс терапии велаксином составил 56 дней (8 нед).
Для оценки выраженности депрессивной симптоматики и определения терапевтического эффекта помимо метода клинического наблюдения применялась шкала HAM-D-24, содержащая 24 признака. Выраженность депрессивной симптоматики оценивали до начала курсового лечения (0-й день), затем в 1, 3, 5-й дни терапии и далее в конце каждой из 8 нед курсового лечения. Эффективность антидепрессивного действия велаксина оценивалась по степени редукции баллов по HAM-D в % по отношению к оценке до лечения в следующих градациях: редукция баллов до 20% — как «незначительный», на 21—50% — как «умеренный», на 51—80% — как «хороший» и на 81—100% — как «значительный» эффект (включая «практическое выздоровление»). Снижение суммарного балла по HAM-D до 6 и менее означало полный «выход» в ремиссию. Сохранение балльной оценки тяжести депрессии по HAM-D на прежнем уровне или увеличение суммарного балла расценивались как отсутствие эффекта или «ухудшение» состояния. Для оценки спектра антидепрессивного действия велаксина определялась степень редукции среднего суммарного балла отдельных признаков, выделяемых в HAM-D, условно характеризующих меланхолические или тоскливые (пункты 1—3, 22—24), апато-адинамические (пункты 7 и  и тревожные (пункты 9 и 10) проявления в структуре депрессивного состояния.
и тревожные (пункты 9 и 10) проявления в структуре депрессивного состояния.
Кроме того, в указанные выше сроки производилась оценка тяжести депрессивного состояния и степени его улучшения в динамике с использованием шкалы общего клинического впечатления CGI и ее подшкал CGI-S и CGI-I. Для регистрации побочных эффектов применялась шкала-интервью UKU, которая состоит из 4 подшкал, позволяющих выделить психические, неврологические, вегетативные и так называемые другие побочные эффекты.
Результаты
В ходе назначенного 56-дневного курса лечения велаксином 31 (96,9%) человек был признан респондерами, из них «незначительный» эффект от лечения отмечался у 1 (3,1%) больного, «умеренный» — у 3 (9,4%), «хороший» — у 2 (6,25%), а у 25 (78,1%) пациентов проявился «значительный» терапевтический эффект. Таким образом, снижение интенсивности депрессивных расстройств на 50% и более при лечении велаксином обнаруживалось в подавляющем большинстве случаев — у 27 (84,4%) больных, что отражено на рис. 1.
Рис. 1. Степень выраженности терапевтического эффекта велаксина при эндогенной депрессии. По оси абсцисс — степень редукции по HAM-D,%; по оси ординат — % больных.
В целом эффективность велаксина, оцененная на 56-й день терапии, была достаточно высока: средний суммарный балл выраженности депрессии по HAM-D подвергся редукции на 85,9%. Уже к концу 1-й недели терапии велаксином наблюдался положительный терапевтический ответ на прием препарата: уменьшение депрессии было на уровне «незначительного» эффекта, но приближалось к 20% уровню редукции расстройств, граничащему с «умеренным» улучшением. Отчетливое же «умеренное» улучшение (редукция оценки по HAM-D на 33,2%) наблюдалось к 14-му дню лечения; между 21-м и 28-м днями лечения терапевтический эффект достигал диапазона «хорошего» со снижением балльных значений по HAM-D на 50% и больше, а к 6-й неделе эффект от лечения велаксином уже приближался к границе «значительного» (до 76,7% редукции тяжести симптомов депрессии). В последующие 7—8-ю нед терапии обнаруживалось бесспорное «значительное» улучшение состояния больных (редукция расстройств более чем на 80%), вплоть до «выздоровления» (рис. 2). У 20 из 31 больных (в 64,5% случаев), закончивших курс лечения велаксином, депрессия полностью редуцировалась и наблюдался «выход» в ремиссию (общий балл по HAM-D у них стал равен 6 и ниже).
Рис. 2. Спектр терапевтического действия велаксина при эндогенных депрессиях (балл по HAM-D). Здесь и на рис 3, 4 и 5 (на последнем — правая ось): по оси ординат — средний балл в % к баллу до начала терапии, по оси абсцисс — день терапии.
Тяжесть состояния, оцененная по подшкале CGI-S, в среднем снижалась при лечении велаксином с 4,7 до 1,6 балла к концу исследования (от «значительно выраженной» до менее чем «слабо выраженной», т. е. до практического отсутствия расстройства). Причем заметное снижение тяжести симптоматики отмечалось в период между 7-м и 21-м днями лечения, когда интенсивность проявлений депрессии последовательно снижалась в среднем до «умеренно» и «слабо» выраженной. С 5-й недели терапии выраженность депрессивных расстройств становилась «очень слабой», а на 7—8-й неделе курсовой терапии отмечался практический «выход» из депрессии с «отсутствием» депрессивных признаков (средний уровень их тяжести составлял 1,6 балла). За время 56-дневного курса терапии оценка степени улучшения депрессивного состояния по подшкале CGI-I показала «ухудшение» психического состояния (5-й уровень оценки) только у 1 (3,1%) человека, осталась «без изменений» (4-й уровень оценки) тоже у 1 (3,1%) больного, «незначительное улучшение» (3-й уровень) — также у 1 (3,1%), «выраженное» улучшение (2-й уровень) наблюдалось у 4 (12,6%), у остальных 25 (78,1%) пациентов регистрировалось «значительное» улучшение (1-й уровень оценки).
Было установлено, что в спектре антидепрессивного действия велаксина все 3 компонента его психотропной активности в соответствии с конечными результатами лечения представлены практически в одинаковой степени с незначительным перевесом в показателях противотоскливого действия (см. рис. 2). Так, степень редукции среднего суммарного балла расстройств по пунктам 1—3 и 22—24 HAM-D (отражающим собственно тимолептическое действие препарата) составила 88,2%, по пунктам 7 и 8 (стимулирующий эффект) — 83,7%, а по пунктам 9 и 10 (антитревожное действие) — 85,1%. Однако реализация всех 3 компонентов действия велаксина по времени была различной и имела свои особенности. Так, наиболее быстро в ходе лечения выявлялись тимолептический и особенно анксиолитический эффекты. Они развивались практически параллельно, достигая уровня снижения тяжести расстройств по HAM-D соответственно на 32,8 и 37,1% уже к 14-му дню терапии («умеренный» эффект). В то же время стимулирующий эффект велаксина несколько «запаздывал» по сравнению с антитревожным и антитоскливым действием, достигая сходных значений («умеренный» эффект — редукция расстройств на 36,9%) лишь к 21-му дню исследования.
В дальнейшем, в период с 21-го по 28-й дни лечения, тимолептический и противотревожный компоненты действия в спектре антидепрессивной активности велаксина по темпу развития выравнивались и нарастали до диапазона отчетливого «хорошего» эффекта (редукции балльной оценки на 60,2 и 59,2%). Но уже с 5-й недели лечения собственно тимолептический эффект начинал превосходить анксиолитический в показателях глубины редукции расстройств по соответствующим пунктам HAM-D: тимолептическое действие проявлялось на уровне «значительного» уже на 6-й неделе, а антитревожное — только после 7-й недели курсовой терапии. Формирование стимулирующего эффекта «запаздывало» по степени проявлений по сравнению с двумя другими компонентами действия велаксина на 1 неделе, и «значительная» его выраженность определялась только на 8-й неделе лечения. И только на этом этапе лечения, как уже говорилось, глубина стимулирующего эффекта велаксина примерно совпадала с выраженностью тимолептического и анксиолитического эффектов.
В соответствии с установленными данными об особенностях реализации отдельных компонентов антидепрессивного действия в спектре психотропной активности велаксина была проанализирована его терапевтическая эффективность в зависимости от синдромального типа депрессии, т. е. от доминирующего аффекта, определяющего картину депрессивного состояния (рис. 3). Обнаружено, что при ведущем тревожном аффекте редукция среднего суммарного балла по HAM-D составила к 56-му дню лечения 85,5%; при преобладании апато-адинамического аффекта эффективность велаксина была сходной — средний суммарный балл по HAM-D снизился на 85,9%. Наиболее же высокая эффективность велаксина наблюдалась при лечении пациентов с ведущим тоскливым аффектом в картине депрессии — редукция среднего суммарного балла по HAM-D составила 91,1%. Но при относительно сходной степени уменьшения депрессивной симптоматики также были отмечены различия в особенностях динамики реализации антидепрессивного эффекта препарата. Так, при ведущих тревожном и тоскливом аффектах, т. е. у пациентов с позитивной аффективностью и наиболее типичными проявлениями депрессии, редукция депрессивной симптоматики шла равными темпами, достигая 21,1% (при тревожной) и 22,5% (при тоскливой депрессии) уже к 7-му дню терапии. В дальнейшем уменьшение среднего суммарного балла по HAM-D происходило более интенсивно и достигало более чем 50% редукции симптомов депрессии к 28-му дню лечения. При терапии велаксином пациентов с негативной аффективностью (атипичная апато-адинамическая депрессия) улучшение наступало более медленно. Редукция среднего суммарного балла по HAM-D на 20% и более («умеренный» эффект) происходила у них лишь на 2—3-й неделе терапии; и только к 4-й неделе регистрировался «хороший» эффект велаксина (редукции расстройств на 61,3%). К 7—8-й неделе лечения улучшение в состоянии было уже «значительным» (более чем 80% редукция расстройств), оно совпадало по выраженности с терапевтическим эффектом велаксина при тревожных депрессиях и несколько «отставало» от эффекта при тоскливой депрессии.
Рис. 3. Динамика эффективности велаксина при разных типах эндогенной депрессии (балл по HAM-D).
Анализ эффективности велаксина в зависимости от нозологической принадлежности депрессии выявил также некоторые особенности (рис. 4): наименьшим показатель уменьшения среднего суммарного балла по HAM-D к концу курсового лечения был у больных малопрогредиентной шизофренией, он был равен 82,3%. У этих же больных отмечался и самый медленный темп редукции депрессивных расстройств — к 7-му дню он составлял лишь 15,2%, а редукция на 50% и более (граница «хорошего» эффекта) достигалась только к 28-му дню; «значительный» эффект обнаруживался у больных малопрогредиентной шизофренией только после 7-й недели лечения велаксином. У больных с аффективным заболеванием (МДП, циклотимия) редукция среднего суммарного балла по HAM-D в конце курсовой терапии была близкой по значению (86,6%), сходной была и скорость уменьшения депрессивных симптомов: к 7-му дню этот показатель достигал 18,2%, а к 4-й неделе терапии уже составлял 59,4% («хороший» эффект). Наилучший результат терапии был достигнут у больных постпсихотическими депрессиями при приступообразной шизофрении — 90,4% редукции расстройств на 56-й день лечения. Несмотря на то что к концу 1-й недели исследования показатель редукции депрессивных проявлений достигал градаций «незначительного» улучшения (19,2%), в дальнейшем уменьшение симптомов депрессии происходило более интенсивно, чем при МДП, демонстрируя «хороший» эффект уже на 14-й день лечения (показатель редукции симптомов —53,9%), а к 28-му дню оно составляло уже 76,5%, т. е. было почти на границе «значительного». Однако следует заметить, что у данных больных изначально степень выраженности депрессивных расстройств была значительно ниже, на уровне «средней» тяжести, чем при других, более «тяжелых», депрессиях (23 балла по HAM-D против 31,3 балла при аффективном заболевании и 31,6 при малопрогредиентной шизофрении).
Рис. 4. Антидепрессивный эффект велаксина в разных нозологических группах больных (балл по HAM-D).
Все указанные закономерности развития терапевтического эффекта велаксина свидетельствуют об отсутствии прямой зависимости от величины его суточной дозы. Как видно из рис. 5, терапевтический эффект начинал проявляться и нарастать с 3—4-й недели лечения (редукция симптомов депрессии на 50% и больше по HAM-D), при увеличении средней суточной дозы до максимальной (182,1—198,2 мг в день). Но в дальнейшем, несмотря на стабилизацию и даже некоторое снижение достигнутой максимальной средней суточной дозы велаксина (до 190,3 мг в день), ответ на терапию продолжал усиливаться более быстрыми темпами, до уровня «значительного» улучшения,
Рис. 5. Соотношение терапевтического эффекта (балл по HAM-D) и суточной дозы велаксина. По левой оси ординат — средняя суточная доза препарата (мг).
В процессе курсовой терапии велаксином у 21 (65,6%) пациента были зарегистрированы 45 нежелательных явлений разного вида; у 5 они были единичными, а у 16 носили сочетанный характер. Наиболее частыми были психические и вегетативные нежелательные явления, отмеченные по шкале UKU, они встречались у 40% больных. Досрочно выбыл из исследования 1 пациент (после 2 нед лечения) из-за развития у него острого аффективно-бредового психоза, требующего изменения терапии. Неврологические и другие побочные эффекты встречались всего у 8,9 и 11,1% больных. Наиболее часто среди отдельных побочных эффектов наблюдались такие, как «взбудораженность/тревога» (у 15,5% больных), уменьшение продолжительности сна и тошнота (у 11,1%), тахикардия и гипергидроз (у 6,6%), седация и запоры (у 4,4%). Все остальные побочные явления встречались в единичных случаях. Частота побочных эффектов в ходе курсового лечения велаксином была наибольшей на 2-й нед лечения, когда средняя суточная доза препарата была незначительной (157,7 мг в день). Наиболее частыми в этот период были психические и автономные нежелательные явления. Но в дальнейшем, несмотря на повышение средней суточной дозы, частота возникновения побочных эффектов постепенно снижалась. Исключение составили «другие» побочные явления, частота которых практически сохранялась на одном уровне до конца лечения. Главным образом это были нарушения сексуальных функций, которые развивались соответственно увеличению суточной дозы велаксина.
Следует отметить, что в целом все нежелательные явления были легкой степени или приближались к умеренно выраженным в первые 2 нед лечения, а затем средняя степень их выраженности при оценке по UKU снижалась до «легкого» уровня, несмотря на постепенное увеличение средних суточных доз велаксина. При этом наиболее тяжелыми изначально были психические побочные явления: средний балл их выраженности по UKU на 1—2-й неделе лечения был равен 1,9—2,0. Однако в ходе дальнейшего курсового лечения тяжесть побочных психических симптомов уже с 3-й неделе уменьшалась. Выраженность некоторых других нежелательных явлений несколько увеличивалась по сравнению с первоначальной: если на 2-й неделе лечения их тяжесть в среднем соответствовала по UKU «легкой» степени (1 балл), то в дальнейшем они достигали 1,5 балла, и при этом степень их тяжести увеличивалась соответственно повышению средней дозы велаксина.
Велаксин® (Velaxin®)
При депрессии возрастает риск суицидальных мыслей и суицидальных попыток. Этот риск сохраняется до наступления стойкой ремиссии. Поэтому пациенты должны находиться под постоянным медицинским наблюдением и им следует выдавать лишь небольшое количество капсул препарата, чтобы снизить риск возможного злоупотребления и/или передозировки. Велаксин® не следует применять при лечении детей и подростков моложе 18 лет. Повышение вероятности суицидального поведения (попытка суицида и суицидальные мысли), а также враждебности, в клинических испытаниях чаще наблюдается среди детей и подростков, получающих антидепрессанты, по сравнению с группами, получающими плацебо.
Сообщалось об агрессивном поведении во время приема венлафаксина (особенно в начале курса лечения и после отмены препарата).
Применение венлафаксина может вызвать психомоторное возбуждение, которое клинически напоминает акатизию, характеризуется беспокойством с потребностью двигаться, часто в сочетании с неспособностью сидеть или стоять на месте. Это чаще всего наблюдается на протяжении первых нескольких недель лечения. При возникновении этих симптомов повышение дозы может оказать неблагоприятный эффект и следует рассмотреть вопрос о целесообразности продолжения приема препарата.
Как и все антидепрессанты, венлафаксин должен назначаться с осторожностью больным с манией и/или гипоманией в анамнезе, так как препарат может вызвать усиление их признаков. В этих случаях необходимо медицинское наблюдение.
Следует соблюдать осторожность при лечении пациентов с судорожными припадками в анамнезе. При возникновении судорожных припадков или повышении их частоты лечение венлафаксином следует прервать.
Подобно избирательным ингибиторам обратного захвата серотонина, венлафаксин следует применять с осторожностью при одновременном применении с антипсихотическими препаратами, так как могут развиться симптомы, напоминающие нейролептический злокачественный синдром.
Пациентов следует предупредить о необходимости немедленно обратиться к врачу при возникновении сыпи, крапивницы или других аллергических реакций.
У некоторых больных во время приема венлафаксина отмечено дозозависимое повышение артериального давления, в связи с чем, рекомендуется регулярный контроль артериального давления, особенно в начале курса лечения или при повышении дозы.
Во время приема венлафаксина описаны отдельные случаи ортостатической гипотензии. Пациенты, особенно пожилые, должны быть предупреждены о возможности возникновения головокружения и нарушения чувства равновесия.
Венлафаксин может вызвать повышение частоты сердечного ритма, особенно во время приема высоких доз. Следует соблюдать особую осторожность при назначении препарата пациентам с состояниями, которые могут усиливаться при повышении частоты сердечного ритма.
Не проведено достаточных исследований применения венлафаксина у пациентов, недавно перенесших инфаркт миокарда или страдающих декомпенсированной сердечной недостаточностью, поэтому применять данный препарат этим пациентам следует с осторожностью.
Как и другие ингибиторы обратного захвата серотонина, венлафаксин может повысить риск кровоизлияний в кожу и слизистые оболочки, поэтому при лечении больных, предрасположенных к кровотечениям, необходима осторожность.
Во время приема венлафаксина, особенно в условиях дегидратации или снижения объема крови (в том числе у пожилых пациентов и больных, принимающих диуретики), может наблюдаться гипонатриемия и/или синдром недостаточной секреции антидиуретического гормона (SIADH).
Во время приема венлафаксина отмечены случаи мидриаза, поэтому пациенты с предрасположенностью к повышению внутриглазного давления или имеющие риск закрытоугольной глаукомы, нуждаются в тщательном медицинском наблюдении.
При почечной и печеночной недостаточности необходима особая осторожность. В некоторых случаях требуется снижение дозы (см. раздел «Способ применения и дозы»).
Безопасность и эффективность применения венлафаксина со средствами, снижающими вес тела, в том числе фентермином, не установлены, поэтому их одновременное применение (как и применение венлафаксина в качестве монотерапии для снижения веса тела) не рекомендуется. Клинически значимое повышение уровня холестерина сыворотки крови отмечено у некоторых пациентов, получающих венлафаксин на протяжении не менее 4 месяцев. Поэтому при длительном приеме препарата целесообразно проводить контроль уровня холестерина сыворотки крови.
После прекращения приема препарата, особенно внезапного, часто возникают симптомы отмены (см. раздел «Побочное действие»). Риск возникновения симптомов отмены может зависеть от нескольких факторов, в том числе длительности курса и дозы, а также скорости снижения дозы.
Симптомы отмены такие как: головокружение, сенсорные нарушения (в том числе парестезии и ощущения прохождения электрического тока), нарушения сна (в том числе бессонница и необычные сновидения), возбуждение или тревога, тошнота и/или рвота, тремор, потливость, головная боль, диарея, учащенное и усиленное сердцебиение и эмоциональная неустойчивость, обычно имеют небольшую или среднюю выраженность, однако у некоторых пациентов они могут быть тяжелыми. Они обычно наблюдаются в первые дни после отмены препарата, хотя были отдельные сообщения о возникновении таких симптомов у пациентов, случайно пропустивших одну дозу. Обычно эти явления проходят самостоятельно в течение 2 недель; однако у некоторых пациентов они могут быть более продолжительными (2-3 месяца или больше). Поэтому перед отменой венлафаксина рекомендуется постепенно снизить его дозу в течение нескольких недель или месяцев в зависимости от состояния пациента (см. разделы «Способ применения и дозы»).